29/11/2022
En el vasto universo de las partículas subatómicas, el electrón se erige como una de las entidades más fundamentales y estudiadas. Sus propiedades, como la carga y la masa, son bien conocidas, pero hay otras características más sutiles que continúan desafiando a los científicos. Una de estas propiedades es el momento dipolar, una medida de la separación de cargas positivas y negativas dentro de un sistema. Si bien la idea de un momento dipolar es sencilla para un par de cargas separadas, cuando se aplica al electrón, una partícula que se considera puntual, el concepto se vuelve sorprendentemente complejo y profundo.
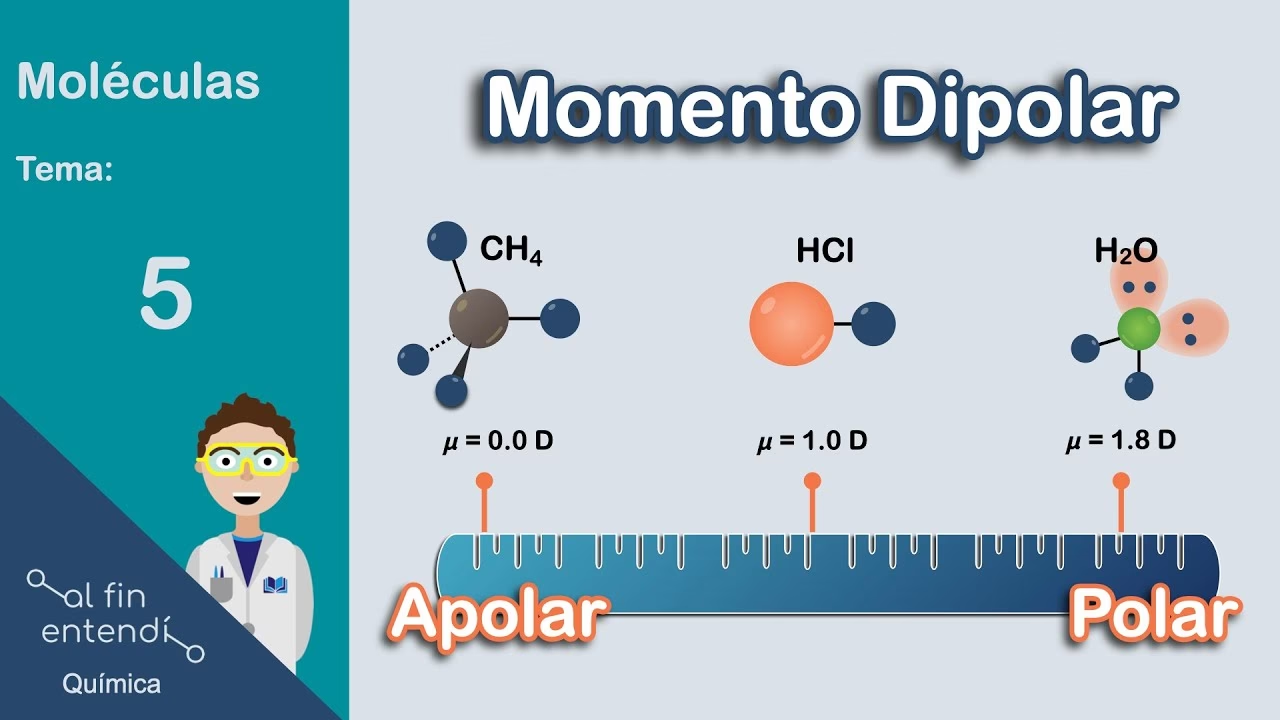
Este artículo explorará qué es un momento dipolar, cómo se aplica a nivel molecular y, crucialmente, la naturaleza intrigante del momento dipolar del electrón, distinguiendo entre su momento dipolar magnético bien establecido y su escurridizo momento dipolar eléctrico, cuya búsqueda es una frontera clave en la física fundamental.
¿Qué es un Momento Dipolar? La Base de la Interacción Eléctrica
En su forma más fundamental, un momento dipolar eléctrico (p) surge de la existencia de dos cargas eléctricas de igual magnitud pero signo opuesto, separadas por una cierta distancia. La fórmula que describe su magnitud es simple y elegante: p = qd. Aquí, 'q' representa la magnitud de una de las cargas y 'd' es la distancia que las separa. Es importante destacar que el momento dipolar no es solo una magnitud; es una cantidad vectorial, lo que significa que tiene una dirección, que convencionalmente se define desde la carga negativa hacia la carga positiva.
Este concepto es omnipresente en la física y la química. Desde la interacción de moléculas de agua hasta el comportamiento de materiales dieléctricos en un campo eléctrico, el momento dipolar juega un papel crucial. Un dipolo genera un campo eléctrico a su alrededor y, a su vez, experimenta una fuerza o un par de torsión cuando se encuentra en un campo eléctrico externo. Cuanto mayor sea el momento dipolar, mayor será la separación de carga o la distancia entre ellas, lo que resulta en interacciones eléctricas más fuertes.
El Momento Dipolar Resultante: Suma de Contribuciones
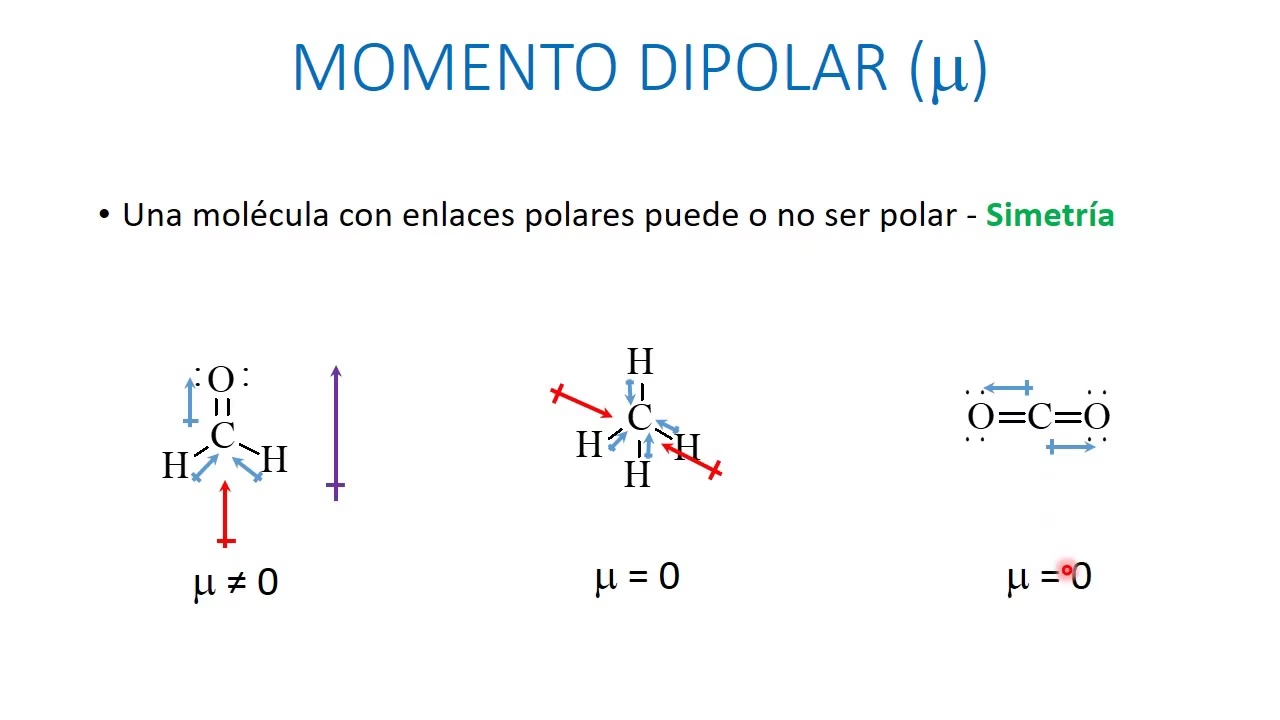
Cuando hablamos de sistemas más complejos, como las moléculas, el concepto de momento dipolar se extiende al de un momento dipolar resultante. En una molécula multiatómica, la polaridad no solo depende de la polaridad de los enlaces químicos individuales, sino también de su disposición geométrica en el espacio. A un nivel simplificado, el momento dipolar eléctrico de una molécula puede considerarse como la suma geométrica (vectorial) de los momentos dipolares de cada enlace individual.
Esta aproximación se basa en la propiedad aditiva del momento dipolar total: cada enlace químico se considera un dipolo, y el momento total se obtiene como la suma vectorial de los momentos de cada enlace particular. La transferibilidad de la polaridad de los enlaces químicos también se utiliza aquí: se acepta que el momento dipolar es una propiedad específica independientemente de la molécula particular en la que participen estos enlaces.
Sin embargo, hay consideraciones importantes. Si una molécula posee un centro de simetría (por ejemplo, el benceno C₆H₆ o el dióxido de carbono CO₂), su momento dipolar es a priori igual a cero. Esto se debe a que el vector del momento dipolar polar es incompatible con un centro de simetría, ya que cualquier vector por sí mismo no posee ese centro.
En segundo lugar, el momento dipolar molecular depende fuertemente de la transferencia de carga de un átomo a otro. Así, las moléculas diatómicas compuestas por átomos idénticos, debido a la simetría de la disposición del par de electrones, no poseen polaridad en absoluto; su momento dipolar eléctrico es igual a cero (por ejemplo, O₂ o N₂). Las moléculas diatómicas compuestas por átomos diferentes son, en la mayoría de los casos, polares. La polaridad del enlace está determinada por la electronegatividad de los átomos constituyentes. Cuanto mayor sea la diferencia en la densidad electrónica, más polar será el enlace. La polaridad alcanza su valor más alto en un enlace puramente iónico. Por lo tanto, el momento dipolar eléctrico caracteriza el grado de ionicidad de un enlace químico.
Por ejemplo, el momento dipolar de los enlaces halógeno-hidrógeno aumenta de HI a HF según el aumento de la electronegatividad de los átomos de halógeno:
| Molécula | Momento Dipolar (D) | Momento Dipolar (C·m) |
|---|---|---|
| HF | 1.91 | 6.37 x 10⁻³⁰ |
| HCl | 1.03 | 3.43 x 10⁻³⁰ |
| HBr | 0.79 | 2.63 x 10⁻³⁰ |
| HI | 0.39 | 1.30 x 10⁻³⁰ |
Los momentos dipolares moleculares pueden calcularse mediante métodos modernos de química cuántica a partir de primeros principios (para moléculas pequeñas). Experimentalmente, los momentos dipolares pueden derivarse de experimentos de difracción de rayos X utilizando una función de distribución de densidad electrónica ρ(r).
Dipolos Inducidos y Polarizabilidad
Cuando un material dieléctrico no polar e isotrópico se coloca en un campo eléctrico externo, este campo local actuará sobre cada molécula. Se producirá un desplazamiento de cargas de diferentes signos, creando un dipolo. Este tipo de dipolo se conoce como dipolo inducido, y su valor es proporcional a la fuerza del campo local. En unidades del Sistema Internacional (SI), esta dependencia se expresa como: p = α ε₀ E_loc.
Aquí, 'p' es el momento dipolar inducido, 'α' es la polarizabilidad, una propiedad que caracteriza la capacidad de una molécula para ser polarizada en un campo eléctrico, 'ε₀' es la permitividad del vacío, y 'E_loc' es la fuerza del campo eléctrico local que actúa sobre la molécula.

El Momento Dipolar del Electrón: Un Desafío para la Física
Ahora, volvamos a la pregunta central: ¿cómo se calcula el momento dipolar del electrón? Aquí es donde el concepto se vuelve más sutil. El electrón, a diferencia de una molécula, no es una combinación de cargas separadas. Se considera una partícula elemental y puntual. Por lo tanto, la fórmula p = qd no se aplica directamente para calcular un momento dipolar intrínseco de un electrón.
Un electrón posee dos tipos de momentos dipolares intrínsecos:
Momento Dipolar Magnético del Electrón:
Este es una propiedad fundamental del electrón, estrechamente ligada a su espín. El electrón se comporta como un pequeño imán, y este momento magnético es bien conocido y ha sido medido con una precisión asombrosa. Es el responsable de fenómenos como el magnetismo y la interacción del electrón con campos magnéticos.
Momento Dipolar Eléctrico Intrínsico del Electrón (eEDM):
Esta es la propiedad que más intriga a los físicos. Un momento dipolar eléctrico intrínseco del electrón (eEDM, por sus siglas en inglés) implicaría que el electrón tiene una ligera separación entre su carga positiva y negativa, o más precisamente, que su distribución de carga no es perfectamente esférica. Según el Modelo Estándar de la física de partículas (nuestra teoría actual más exitosa), el eEDM del electrón debería ser extremadamente pequeño, de hecho, prácticamente cero (se predice que es del orden de 10⁻⁴⁰ e·cm, un valor inmensurablemente pequeño).
Sin embargo, muchas teorías que van más allá del Modelo Estándar (como la supersimetría) predicen un eEDM no nulo, aunque aún muy pequeño, pero considerablemente mayor que la predicción del Modelo Estándar (del orden de 10⁻²⁷ a 10⁻³⁰ e·cm). La existencia de un eEDM medible sería una evidencia directa de nueva física más allá del Modelo Estándar y podría ayudar a explicar uno de los mayores misterios del universo: la asimetría entre materia y antimateria.
¿Cómo se 'Calcula' o Determina el eEDM?
Dado que el eEDM no se calcula con una fórmula simple como p = qd, su determinación se basa en dos enfoques principales:
- Predicciones Teóricas: Los físicos teóricos utilizan modelos avanzados de la física de partículas para predecir el valor del eEDM. Estas predicciones varían enormemente según la extensión del Modelo Estándar que se esté considerando.
- Mediciones Experimentales de Alta Precisión: Aquí es donde reside el verdadero desafío. Los científicos no 'calculan' el eEDM de un electrón individual en el sentido de una operación matemática; más bien, lo buscan y miden experimentalmente. Esto se hace utilizando técnicas extremadamente sofisticadas, a menudo involucrando átomos o moléculas que pueden amplificar el efecto de un eEDM minúsculo. Los experimentos actuales han establecido límites superiores muy estrictos para el eEDM, lo que significa que si existe, es aún más pequeño de lo que muchas teorías de nueva física predicen. La búsqueda del eEDM es uno de los esfuerzos experimentales más sensibles en la física de partículas hoy en día.
La Importancia de los Momentos Dipolares
La comprensión de los momentos dipolares, tanto a nivel molecular como fundamental, es crucial para diversas ramas de la ciencia:
- En Química: Los momentos dipolares moleculares determinan la polaridad de las moléculas, lo que a su vez influye en sus propiedades físicas (puntos de ebullición, solubilidad), su reactividad química y cómo interactúan con otras moléculas. Son esenciales para entender la estructura y función de biomoléculas y el diseño de nuevos materiales.
- En Física de Materiales: Son clave para comprender el comportamiento de los dieléctricos, materiales que pueden almacenar energía eléctrica cuando se exponen a un campo eléctrico.
- En Física Fundamental: La búsqueda del eEDM del electrón es una ventana hacia la física más allá del Modelo Estándar. Un descubrimiento de un eEDM no nulo tendría implicaciones revolucionarias, sugiriendo la existencia de nuevas partículas o interacciones fundamentales que podrían resolver enigmas cosmológicos.
Preguntas Frecuentes (FAQ)
¿El electrón tiene un momento dipolar eléctrico?
Según el Modelo Estándar de la física de partículas, el momento dipolar eléctrico intrínseco del electrón (eEDM) es extremadamente pequeño, teóricamente casi cero. Sin embargo, muchas teorías de nueva física predicen un valor no nulo, aunque minúsculo. Los experimentos actuales buscan activamente un eEDM para encontrar evidencia de esta nueva física, y hasta ahora solo han podido establecer límites superiores muy estrictos, lo que significa que, si existe, es increíblemente pequeño.
¿Por qué es tan difícil medir el eEDM del electrón?
Es extremadamente difícil por varias razones: primero, se predice que es un valor minúsculo, requiriendo una sensibilidad experimental sin precedentes. Segundo, el electrón es una partícula puntual, lo que hace que su momento dipolar intrínseco sea un concepto puramente cuántico, no una separación física de cargas. Los experimentos deben aislar y medir efectos sutiles en sistemas atómicos o moleculares que se amplifican por la presencia de un eEDM, mientras se eliminan todas las demás interacciones y ruidos que puedan enmascarar la señal.
¿Cuál es la diferencia entre un dipolo permanente y un dipolo inducido?
Un dipolo permanente es una característica intrínseca de una molécula debido a la distribución asimétrica de sus cargas, incluso en ausencia de un campo eléctrico externo (ejemplo: agua, H₂O). Un dipolo inducido, por otro lado, se forma en una molécula o átomo que normalmente no es polar, cuando se somete a un campo eléctrico externo. El campo distorsiona la nube electrónica, creando una separación temporal de cargas (ejemplo: átomos de helio en un campo eléctrico).
¿Qué indica un momento dipolar molecular alto?
Un momento dipolar molecular alto indica una mayor separación de carga dentro de la molécula o una mayor distancia entre las cargas parciales. Esto generalmente se traduce en una mayor polaridad de la molécula, lo que afecta sus propiedades físicas como un punto de ebullición más alto, mayor solubilidad en solventes polares, y una mayor capacidad para interactuar con campos eléctricos externos o con otras moléculas polares.
Conclusión
El concepto de momento dipolar, aunque simple en su definición básica para un par de cargas, se revela como una herramienta poderosa y compleja en el estudio de la materia, desde las interacciones moleculares hasta las propiedades fundamentales de las partículas elementales. Mientras que los momentos dipolares moleculares son esenciales para entender la química y las propiedades de los materiales, el momento dipolar eléctrico del electrón representa una de las fronteras más emocionantes de la física moderna.
La búsqueda incansable de un eEDM no nulo no es solo un ejercicio de precisión experimental; es una ventana potencial a un universo de nueva física más allá de lo que actualmente conocemos, prometiendo desvelar secretos sobre la materia oscura, la energía oscura y la propia evolución del cosmos. En este sentido, el aparente 'cero' del eEDM es, paradójicamente, una de las cifras más significativas en la física actual, impulsando a los científicos a buscar respuestas en los rincones más profundos de la naturaleza.
Si quieres conocer otros artículos parecidos a El Momento Dipolar del Electrón: Un Enigma Cuántico puedes visitar la categoría Física.