02/10/2025
En el vasto y fascinante mundo de la química, comprender las cantidades de las sustancias es fundamental. Desde la preparación de soluciones hasta la predicción de los productos de una reacción, todo se basa en la capacidad de cuantificar la materia. Uno de los conceptos más importantes en este sentido es la masa molecular, una medida que nos dice cuánto "pesa" una molécula. Sin embargo, este concepto a menudo genera confusión, especialmente cuando se trata de expresarlo en diferentes unidades: unidades de masa atómica (uma) o gramos. Esta guía exhaustiva está diseñada para desmitificar la masa molecular, explicar cómo se calcula y, crucialmente, cómo se convierte de uma a gramos, un paso esencial para cualquier químico o estudiante de química.

La masa molecular es mucho más que un simple número; es la clave para conectar el mundo submicroscópico de los átomos y moléculas individuales con las cantidades macroscópicas que podemos medir en el laboratorio. Acompáñanos en este viaje para dominar este concepto vital y transformar tu comprensión de la química cuantitativa.
- ¿Qué es Exactamente la Masa Molecular?
- ¿Cómo se Calcula la Masa Molecular (en uma)?
- El Puente Crucial: De UMA a Gramos – El Concepto de Mol y la Masa Molar
- La Importancia Práctica: ¿Por Qué es Crucial esta Conversión?
- Errores Comunes y Cómo Evitarlos
- Tabla Comparativa: Masa Molecular vs. Masa Molar
- Preguntas Frecuentes (FAQ)
- ¿Cuál es la diferencia entre masa atómica y masa molecular?
- ¿La masa molecular y la masa molar son lo mismo?
- ¿Por qué usamos el concepto de mol en química?
- ¿Dónde puedo encontrar las masas atómicas de los elementos para mis cálculos?
- ¿Siempre es el mismo número en uma que en gramos?
- ¿La masa molecular se aplica solo a compuestos moleculares?
- Conclusión
¿Qué es Exactamente la Masa Molecular?
La masa molecular, también conocida como peso molecular, es la suma de las masas atómicas de todos los átomos que componen una molécula. Es una medida de la masa promedio de una molécula de una sustancia. Para entenderla mejor, primero debemos recordar que cada elemento químico tiene una masa atómica característica, que generalmente se encuentra en la tabla periódica. Esta masa atómica es, en esencia, la masa promedio ponderada de los isótopos de un elemento, expresada en unidades de masa atómica (uma).
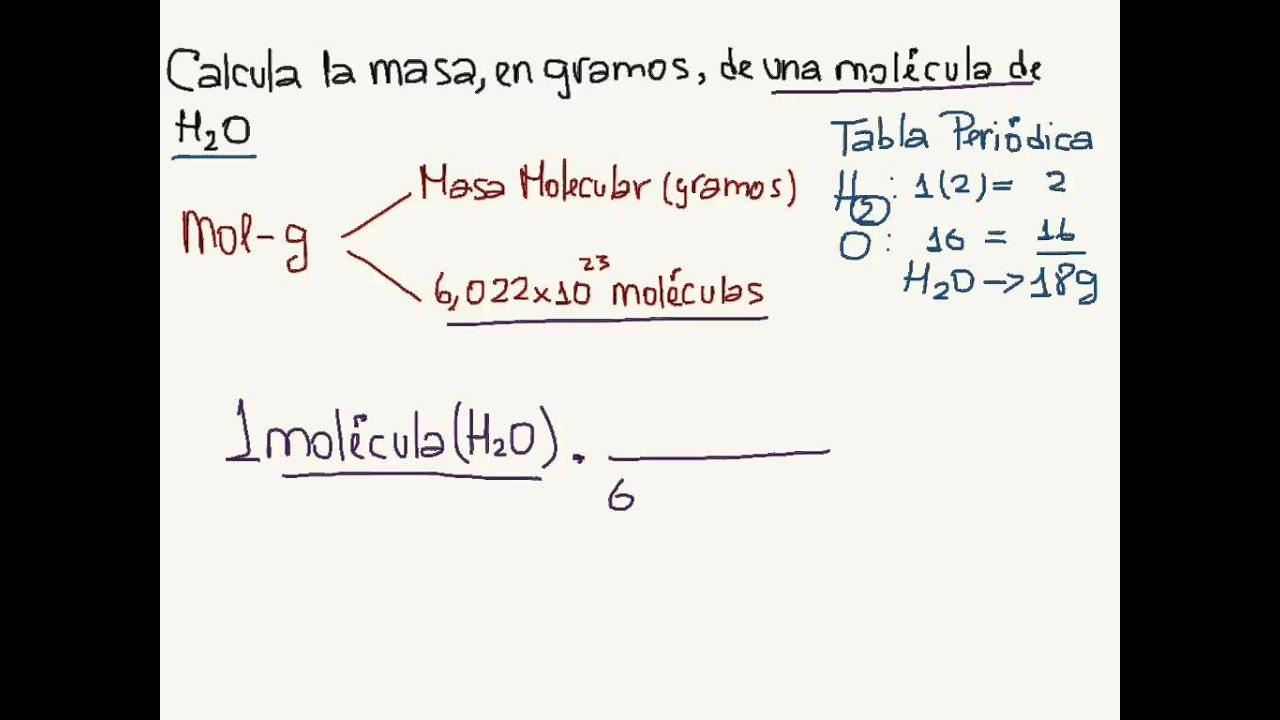
Cuando hablamos de la masa molecular en uma, nos referimos a la masa de una única molécula. Por ejemplo, si consideramos una molécula de agua (H₂O), su masa molecular en uma sería la suma de la masa de dos átomos de hidrógeno y un átomo de oxígeno. Las unidades de masa atómica son increíblemente pequeñas y se utilizan para cuantificar la masa a nivel atómico y molecular, un nivel donde los gramos serían una unidad demasiado grande e impráctica.
La Unidad de Masa Atómica (UMA)
La uma es una unidad de masa utilizada para expresar masas atómicas y moleculares. Se define como 1/12 de la masa de un átomo de carbono-12 (¹²C). Esta definición estándar proporciona una base consistente para comparar las masas de todos los átomos y moléculas. Así, cuando decimos que un átomo de hidrógeno tiene aproximadamente 1.008 uma, estamos indicando que su masa es aproximadamente 1/12 de la masa de un átomo de carbono-12.
¿Cómo se Calcula la Masa Molecular (en uma)?
Calcular la masa molecular es un proceso directo que implica tres pasos principales:
- Identificar la fórmula química: Necesitas saber la fórmula exacta de la molécula para determinar qué átomos la componen y en qué cantidad.
- Obtener las masas atómicas: Consulta una tabla periódica para encontrar las masas atómicas de cada elemento presente en la molécula. Utiliza los valores promedio de masa atómica, que suelen ser los que se muestran debajo del símbolo del elemento.
- Sumar las masas atómicas: Multiplica la masa atómica de cada elemento por el número de veces que aparece en la fórmula y luego suma todos esos valores.
Ejemplos Detallados de Cálculo de Masa Molecular
Ejemplo 1: Agua (H₂O)
- Elementos y cantidad: 2 átomos de Hidrógeno (H), 1 átomo de Oxígeno (O).
- Masas atómicas (aproximadas): H ≈ 1.01 uma, O ≈ 16.00 uma.
- Cálculo:
(2 × 1.01 uma) + (1 × 16.00 uma)
2.02 uma + 16.00 uma = 18.02 uma
La masa molecular del agua es 18.02 uma.
Ejemplo 2: Dióxido de Carbono (CO₂)
- Elementos y cantidad: 1 átomo de Carbono (C), 2 átomos de Oxígeno (O).
- Masas atómicas (aproximadas): C ≈ 12.01 uma, O ≈ 16.00 uma.
- Cálculo:
(1 × 12.01 uma) + (2 × 16.00 uma)
12.01 uma + 32.00 uma = 44.01 uma
La masa molecular del dióxido de carbono es 44.01 uma.
Ejemplo 3: Glucosa (C₆H₁₂O₆)
- Elementos y cantidad: 6 átomos de Carbono (C), 12 átomos de Hidrógeno (H), 6 átomos de Oxígeno (O).
- Masas atómicas (aproximadas): C ≈ 12.01 uma, H ≈ 1.01 uma, O ≈ 16.00 uma.
- Cálculo:
(6 × 12.01 uma) + (12 × 1.01 uma) + (6 × 16.00 uma)
72.06 uma + 12.12 uma + 96.00 uma = 180.18 uma
La masa molecular de la glucosa es 180.18 uma.
El Puente Crucial: De UMA a Gramos – El Concepto de Mol y la Masa Molar
Aquí es donde la confusión a menudo surge, pero también donde reside la belleza de la química cuantitativa. Cuando la masa molecular se expresa en gramos, ya no nos referimos a la masa de una sola molécula, sino a la masa de un mol de moléculas. Este concepto es tan fundamental que tiene su propio nombre: masa molar.
Un mol es una cantidad de sustancia que contiene exactamente 6.022 x 10²³ entidades elementales (átomos, moléculas, iones, etc.). Este número, conocido como el número de Avogadro (NA), es la clave que vincula el mundo microscópico (uma) con el mundo macroscópico (gramos).
La magia de la química radica en una notable coincidencia numérica: la masa molecular de una sustancia en uma es numéricamente igual a la masa de un mol de esa sustancia en gramos. Es decir:
Si la masa molecular de una sustancia es X uma, entonces la masa molar de esa sustancia es X gramos por mol (g/mol).
Esta equivalencia numérica directa simplifica enormemente los cálculos en química. No necesitas realizar una conversión compleja con el número de Avogadro en cada paso; la definición de mol ya incorpora esta relación.
¿Por qué esta Equivalencia Numérica?
Esta equivalencia se deriva de la definición del mol y de la uma. Un mol se define de tal manera que, si la masa de un átomo es X uma, entonces la masa de un mol de esos átomos es X gramos. Es una definición cuidadosamente construida para hacer que los cálculos de laboratorio sean prácticos. Los químicos no pueden pesar una sola molécula en una balanza, pero sí pueden pesar un mol de moléculas.
Ejemplos de Conversión de Masa Molecular (uma) a Gramos (Masa Molar)
Basándonos en los ejemplos anteriores:
- Agua (H₂O):
Masa molecular = 18.02 uma
Masa molar = 18.02 g/mol - Dióxido de Carbono (CO₂):
Masa molecular = 44.01 uma
Masa molar = 44.01 g/mol - Glucosa (C₆H₁₂O₆):
Masa molecular = 180.18 uma
Masa molar = 180.18 g/mol
Como puedes ver, el número es idéntico; solo cambian las unidades, lo que representa un cambio en la escala de la cantidad de sustancia a la que nos referimos.
La Importancia Práctica: ¿Por Qué es Crucial esta Conversión?
La capacidad de convertir la masa molecular de uma a gramos (es decir, entender la masa molar) es fundamental para la estequiometría, la rama de la química que se ocupa de las relaciones cuantitativas entre los reactivos y productos en las reacciones químicas. Sin este concepto, sería imposible:
- Pesar cantidades precisas de reactivos: En el laboratorio, no medimos moléculas individuales, sino gramos de sustancias. La masa molar nos dice cuántos gramos de una sustancia necesitamos para tener un mol de ella, lo que a su vez nos permite relacionar las cantidades de diferentes sustancias en una reacción.
- Calcular rendimientos de reacción: Si sabes cuántos gramos de reactivos usas, puedes predecir cuántos gramos de productos deberías obtener.
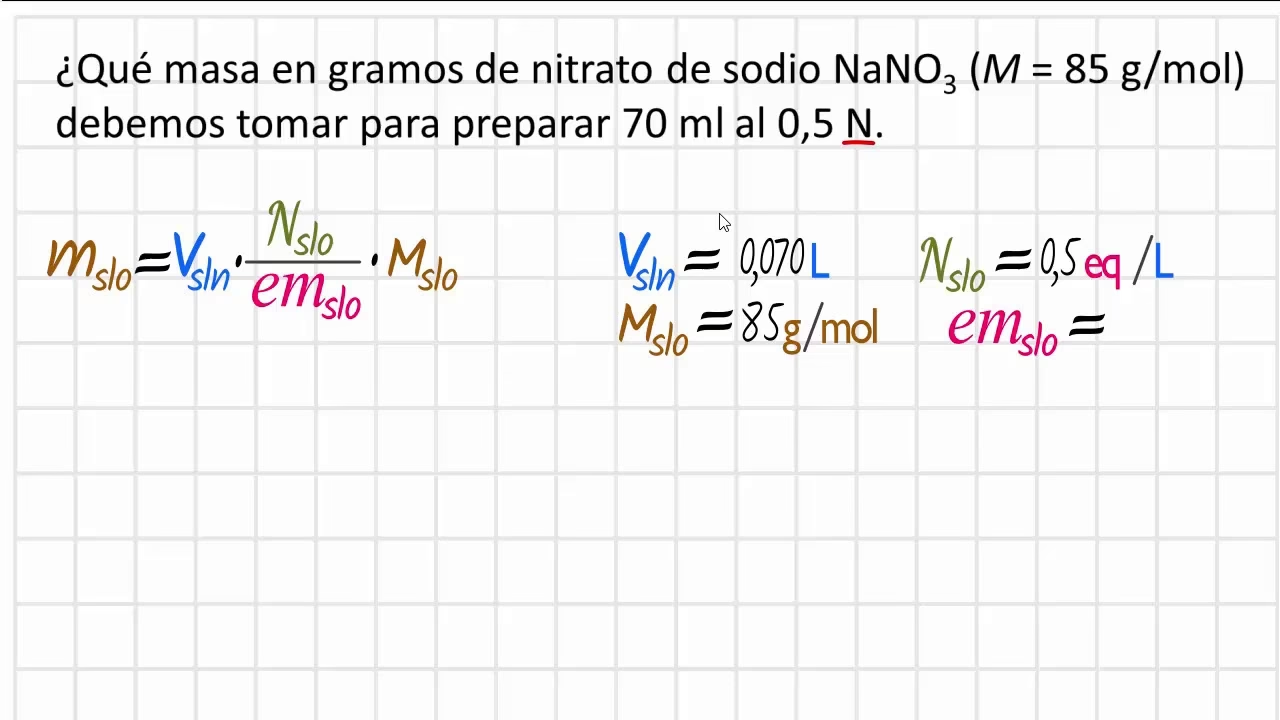
- Preparar soluciones de concentración específica: Las concentraciones se expresan a menudo en moles por litro (molaridad), y para lograr una molaridad deseada, necesitas saber la masa molar del soluto.
- Determinar fórmulas empíricas y moleculares: Los datos de composición porcentual se convierten en moles para encontrar la relación de átomos en un compuesto.
En esencia, la masa molar es el puente indispensable entre la teoría atómica y molecular y la práctica experimental en el laboratorio.
Errores Comunes y Cómo Evitarlos
A pesar de su aparente simplicidad, el cálculo y la comprensión de la masa molecular y molar pueden dar lugar a errores. Aquí te presentamos algunos de los más comunes y cómo evitarlos:
- Confundir masa molecular (uma) con masa molar (g/mol): Aunque numéricamente son iguales, conceptualmente son diferentes. La masa molecular se refiere a una sola molécula, mientras que la masa molar se refiere a un mol de moléculas. Entender esta distinción es clave para la correcta aplicación.
- No considerar los subíndices en la fórmula: Un error frecuente es olvidar multiplicar la masa atómica de un elemento por su subíndice en la fórmula química (ej. en H₂O, son 2 H, no 1). Siempre revisa la fórmula cuidadosamente.
- Usar valores incorrectos de masas atómicas: Asegúrate de usar las masas atómicas promedio de la tabla periódica con la precisión adecuada (generalmente dos decimales son suficientes para la mayoría de los cálculos).
- No incluir las unidades correctas: Siempre especifica las unidades (uma o g/mol) para evitar ambigüedades.
Tabla Comparativa: Masa Molecular vs. Masa Molar
Para reforzar la comprensión, la siguiente tabla resume la relación entre la masa molecular y la masa molar para algunos compuestos comunes:
| Compuesto | Fórmula Química | Masa Atómica (uma) de elementos constituyentes | Cálculo Masa Molecular (uma) | Masa Molecular (uma) | Masa Molar (g/mol) |
|---|---|---|---|---|---|
| Agua | H₂O | H: 1.01, O: 16.00 | (2 × 1.01) + (1 × 16.00) | 18.02 | 18.02 |
| Dióxido de Carbono | CO₂ | C: 12.01, O: 16.00 | (1 × 12.01) + (2 × 16.00) | 44.01 | 44.01 |
| Amoníaco | NH₃ | N: 14.01, H: 1.01 | (1 × 14.01) + (3 × 1.01) | 17.04 | 17.04 |
| Ácido Sulfúrico | H₂SO₄ | H: 1.01, S: 32.07, O: 16.00 | (2 × 1.01) + (1 × 32.07) + (4 × 16.00) | 98.09 | 98.09 |
| Sal de Mesa | NaCl | Na: 22.99, Cl: 35.45 | (1 × 22.99) + (1 × 35.45) | 58.44 | 58.44 |
Preguntas Frecuentes (FAQ)
¿Cuál es la diferencia entre masa atómica y masa molecular?
La masa atómica se refiere a la masa de un solo átomo de un elemento (o el promedio de sus isótopos), mientras que la masa molecular se refiere a la masa de una molécula completa, que está compuesta por dos o más átomos unidos. La masa molecular es la suma de las masas atómicas de todos los átomos en la molécula.
¿La masa molecular y la masa molar son lo mismo?
Numéricamente, sí, son el mismo valor. Conceptualmente, no. La masa molecular (en uma) se refiere a la masa de una molécula individual. La masa molar (en g/mol) se refiere a la masa de un mol (6.022 x 10²³) de esas moléculas. La masa molar es la masa que se mide en el laboratorio.
¿Por qué usamos el concepto de mol en química?
El concepto de mol es crucial porque los átomos y las moléculas son demasiado pequeños para ser medidos individualmente en un laboratorio. El mol proporciona una forma de agrupar una cantidad manejable de estas partículas para que podamos medirlas en gramos y realizar cálculos estequiométricos significativos en el mundo macroscópico.
¿Dónde puedo encontrar las masas atómicas de los elementos para mis cálculos?
Las masas atómicas de todos los elementos se encuentran en la tabla periódica. Generalmente, se muestran debajo del símbolo del elemento. Es importante usar los valores promedio de masa atómica.
¿Siempre es el mismo número en uma que en gramos?
Sí, siempre es el mismo valor numérico. La definición de la unidad de masa atómica (uma) y la del mol están intrínsecamente ligadas para que esto sea cierto. La masa de una molécula en uma es numéricamente idéntica a la masa de un mol de esa sustancia en gramos.
¿La masa molecular se aplica solo a compuestos moleculares?
Sí, el término "masa molecular" se aplica específicamente a compuestos que existen como moléculas discretas (compuestos covalentes). Para compuestos iónicos, se utiliza el término "masa fórmula" o "peso fórmula", que es la suma de las masas atómicas de los iones en la unidad de fórmula, pero el principio de cálculo y la equivalencia numérica con la masa molar en g/mol son los mismos.
Conclusión
Dominar la masa molecular y su conversión a gramos (es decir, entender la masa molar) es una habilidad fundamental para cualquier persona que se adentre en el estudio de la química. Hemos explorado que la masa molecular es la suma de las masas atómicas en una molécula, expresada en unidades de masa atómica (uma). Lo más importante es que hemos aprendido cómo este valor numérico se traduce directamente a la masa de un mol de esa sustancia en gramos (g/mol), un concepto conocido como masa molar.
Esta equivalencia numérica, facilitada por el número de Avogadro y la definición del mol, es el pilar de todos los cálculos estequiométricos en química. Te permite pasar del mundo microscópico de los átomos y moléculas individuales al mundo macroscópico de los gramos que puedes medir en el laboratorio. Al comprender a fondo estos conceptos, estarás bien equipado para resolver problemas químicos, predecir resultados de reacciones y llevar a cabo experimentos con precisión y confianza. ¡Ahora tienes las herramientas para calcular y convertir la masa molecular como un verdadero experto en química!
Si quieres conocer otros artículos parecidos a De UMA a Gramos: Comprendiendo la Masa Molecular puedes visitar la categoría Química.