24/02/2025
La química, aunque a menudo parece compleja, se basa en principios fundamentales que, una vez comprendidos, abren la puerta a un universo de conocimiento. Uno de estos pilares es el concepto de masa molar. Saber cómo calcularla no solo es esencial para cualquier estudiante de química, sino también para profesionales que trabajan con sustancias químicas en diversos campos. Desde la preparación de soluciones hasta la síntesis de nuevos materiales, la masa molar es una herramienta indispensable. En este artículo, desglosaremos este concepto crucial, proporcionando una guía clara y concisa para que puedas calcular la masa molar de cualquier compuesto con confianza y precisión.
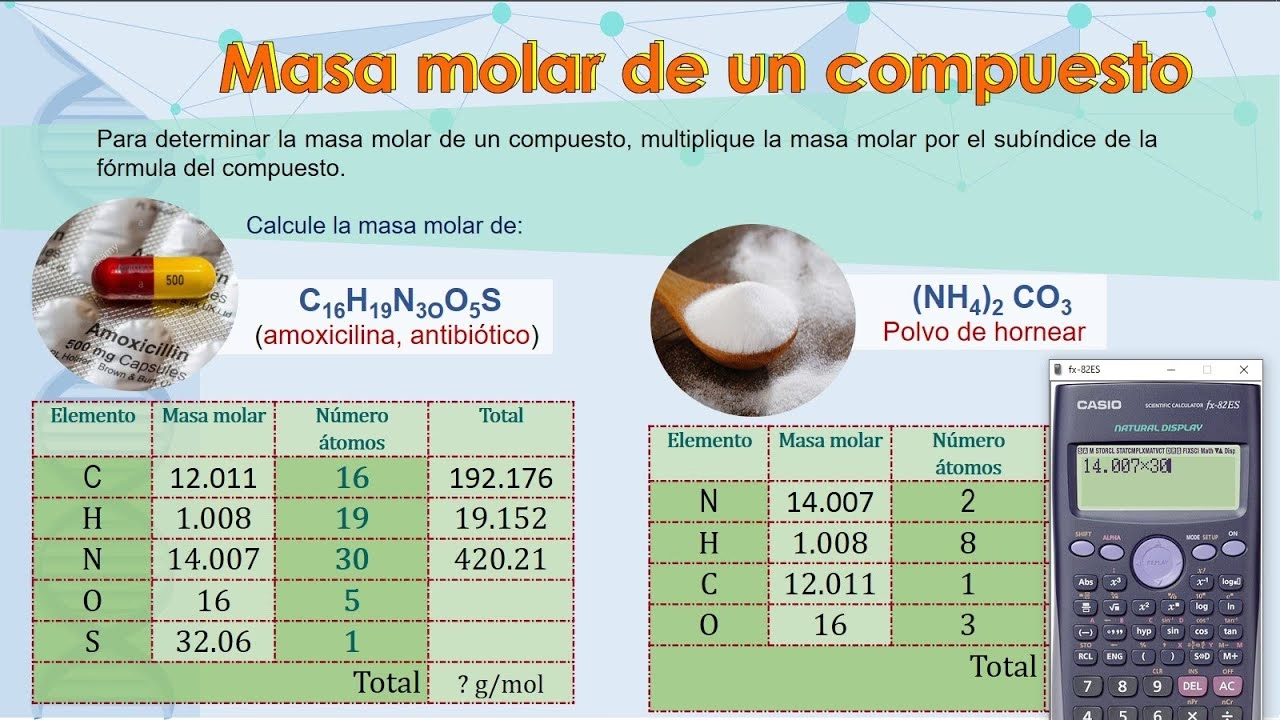
Comprender la masa molar nos permite cuantificar la materia a nivel macroscópico, relacionando la cantidad de sustancia (en moles) con su masa (en gramos). Es el puente entre el mundo invisible de los átomos y moléculas y el mundo que podemos medir en el laboratorio. Así que, prepárate para sumergirte en los secretos de la masa molar y potenciar tus habilidades químicas.
- ¿Qué es la Masa Molar?
- La Tabla Periódica: Tu Herramienta Fundamental
- Guía Paso a Paso para Calcular la Masa Molar
- Ejemplos Adicionales de Cálculo de Masa Molar
- Errores Comunes y Consejos Útiles
- La Importancia de la Masa Molar en la Química
- Masa Molar vs. Peso Molecular vs. Masa Fórmula
- Preguntas Frecuentes (FAQ)
- Conclusión
¿Qué es la Masa Molar?
La masa molar (M) de un compuesto es la masa de un mol de esa sustancia. Se expresa comúnmente en gramos por mol (g/mol). Para entenderlo mejor, recordemos que un mol es una unidad de cantidad de sustancia que contiene aproximadamente 6.022 x 1023 entidades elementales (átomos, moléculas, iones, etc.). Este número, conocido como el número de Avogadro, es una constante fundamental en la química.
En esencia, la masa molar es numéricamente igual a la masa atómica o molecular de una sustancia, pero expresada en unidades de gramos por mol. Por ejemplo, si la masa atómica del carbono es 12.01 uma (unidades de masa atómica), su masa molar es 12.01 g/mol. Esta equivalencia simplifica enormemente los cálculos en el laboratorio, permitiéndonos convertir fácilmente entre masa y moles.
La Tabla Periódica: Tu Herramienta Fundamental
Para calcular la masa molar de cualquier compuesto, tu mejor aliado es la tabla periódica de los elementos. En ella, encontrarás la masa atómica de cada elemento, que es el punto de partida para nuestros cálculos. La masa atómica (o peso atómico) que figura en la tabla periódica es, de hecho, una masa atómica promedio, que tiene en cuenta la abundancia de los diferentes isótopos de un elemento en la naturaleza. Para la mayoría de los cálculos químicos, utilizaremos estos valores directamente.
Es importante notar que, dependiendo de la precisión requerida, puedes redondear las masas atómicas a uno o dos decimales. Para fines educativos y la mayoría de los cálculos introductorios, redondear a un decimal es generalmente suficiente, aunque los valores más precisos te darán resultados más exactos.
Guía Paso a Paso para Calcular la Masa Molar
El cálculo de la masa molar sigue una metodología sencilla y sistemática que se puede aplicar a cualquier compuesto. A continuación, desglosamos los pasos:
Paso 1: Identifica los Elementos y sus Cantidades en la Fórmula Química
El primer paso es examinar la fórmula química del compuesto. Esta fórmula te dirá qué elementos están presentes y cuántos átomos de cada elemento hay en una molécula o unidad de fórmula. Los subíndices en la fórmula indican el número de átomos de un elemento. Si no hay subíndice, se asume que hay un átomo de ese elemento.
Por ejemplo:
- En H2O (agua): Hay 2 átomos de hidrógeno (H) y 1 átomo de oxígeno (O).
- En NaCl (cloruro de sodio): Hay 1 átomo de sodio (Na) y 1 átomo de cloro (Cl).
- En C6H12O6 (glucosa): Hay 6 átomos de carbono (C), 12 átomos de hidrógeno (H) y 6 átomos de oxígeno (O).
Si la fórmula contiene paréntesis, como en Ca(OH)2 (hidróxido de calcio), el subíndice fuera del paréntesis multiplica todos los átomos dentro del paréntesis. Así, en Ca(OH)2, hay 1 átomo de calcio (Ca), 2 átomos de oxígeno (O) y 2 átomos de hidrógeno (H).
Paso 2: Obtén las Masas Atómicas de Cada Elemento
Consulta la tabla periódica para encontrar la masa atómica de cada elemento identificado en el Paso 1. Anota estos valores, generalmente expresados en g/mol.
Ejemplos de masas atómicas aproximadas:
- Hidrógeno (H): 1.01 g/mol
- Oxígeno (O): 16.00 g/mol
- Sodio (Na): 22.99 g/mol
- Cloro (Cl): 35.45 g/mol
- Carbono (C): 12.01 g/mol
- Calcio (Ca): 40.08 g/mol
Paso 3: Multiplica Cada Masa Atómica por su Cantidad en la Fórmula
Para cada elemento, multiplica su masa atómica por el número de veces que aparece ese átomo en la fórmula química del compuesto. Esto te dará la contribución de masa de cada tipo de átomo al total.
Ejemplos:
- Para H2O:
- Hidrógeno (H): 2 átomos * 1.01 g/mol = 2.02 g/mol
- Oxígeno (O): 1 átomo * 16.00 g/mol = 16.00 g/mol
- Para NaCl:
- Sodio (Na): 1 átomo * 22.99 g/mol = 22.99 g/mol
- Cloro (Cl): 1 átomo * 35.45 g/mol = 35.45 g/mol
- Para C6H12O6:
- Carbono (C): 6 átomos * 12.01 g/mol = 72.06 g/mol
- Hidrógeno (H): 12 átomos * 1.01 g/mol = 12.12 g/mol
- Oxígeno (O): 6 átomos * 16.00 g/mol = 96.00 g/mol
Paso 4: Suma las Masas Obtenidas
Finalmente, suma todas las contribuciones de masa individuales que calculaste en el Paso 3. El resultado será la masa molar total del compuesto, expresada en gramos por mol.
Ejemplos:
- Para H2O: 2.02 g/mol (de H) + 16.00 g/mol (de O) = 18.02 g/mol
- Para NaCl: 22.99 g/mol (de Na) + 35.45 g/mol (de Cl) = 58.44 g/mol
- Para C6H12O6: 72.06 g/mol (de C) + 12.12 g/mol (de H) + 96.00 g/mol (de O) = 180.18 g/mol
Ejemplos Adicionales de Cálculo de Masa Molar
Para consolidar tu comprensión, veamos un par de ejemplos más complejos.

Ejemplo 1: Masa Molar del Ácido Sulfúrico (H2SO4)
El ácido sulfúrico es un ácido fuerte muy utilizado en la industria.
- Identificar elementos y cantidades:
2 átomos de Hidrógeno (H)
1 átomo de Azufre (S)
4 átomos de Oxígeno (O) - Obtener masas atómicas:
H ≈ 1.01 g/mol
S ≈ 32.07 g/mol
O ≈ 16.00 g/mol - Multiplicar y sumar:
H: 2 * 1.01 g/mol = 2.02 g/mol
S: 1 * 32.07 g/mol = 32.07 g/mol
O: 4 * 16.00 g/mol = 64.00 g/mol
Masa molar de H2SO4 = 2.02 + 32.07 + 64.00 = 98.09 g/mol
Ejemplo 2: Masa Molar del Hidróxido de Calcio (Ca(OH)2)
Este ejemplo incluye paréntesis, lo que requiere un poco más de atención.
- Identificar elementos y cantidades:
1 átomo de Calcio (Ca)
2 átomos de Oxígeno (O) (el subíndice 2 fuera del paréntesis multiplica la O)
2 átomos de Hidrógeno (H) (el subíndice 2 fuera del paréntesis multiplica la H) - Obtener masas atómicas:
Ca ≈ 40.08 g/mol
O ≈ 16.00 g/mol
H ≈ 1.01 g/mol - Multiplicar y sumar:
Ca: 1 * 40.08 g/mol = 40.08 g/mol
O: 2 * 16.00 g/mol = 32.00 g/mol
H: 2 * 1.01 g/mol = 2.02 g/mol
Masa molar de Ca(OH)2 = 40.08 + 32.00 + 2.02 = 74.10 g/mol
Errores Comunes y Consejos Útiles
Aunque el cálculo de la masa molar es directo, hay algunos errores comunes que se pueden evitar:
- No considerar los subíndices: Olvidar multiplicar la masa atómica por el número de átomos es el error más frecuente.
- Ignorar los paréntesis: Asegúrate de distribuir el subíndice fuera del paréntesis a todos los elementos dentro de él.
- Errores de redondeo: Si bien redondear es aceptable, sé consistente. Para cálculos de alta precisión, usa los valores más exactos de la tabla periódica.
- Unidades incorrectas: Siempre expresa la masa molar en g/mol.
- Confundir masa atómica con número atómico: La masa atómica (generalmente un número decimal) es diferente del número atómico (el número entero que define el elemento). Asegúrate de usar el valor correcto.
Un consejo útil es crear una tabla para organizar tus cálculos, especialmente para compuestos complejos. Esto te ayudará a visualizar cada paso y reducir la probabilidad de errores.
| Elemento | Masa Atómica (g/mol) | Cantidad en Fórmula | Contribución a la Masa (g/mol) |
|---|---|---|---|
| H | 1.01 | 2 | 2.02 |
| O | 16.00 | 1 | 16.00 |
| Total | 18.02 |
La Importancia de la Masa Molar en la Química
La masa molar no es solo un número; es un concepto fundamental con aplicaciones vastas en la química:
- Estequiometría: Permite convertir entre la masa de una sustancia y el número de moles, lo cual es crucial para calcular las cantidades de reactivos y productos en una reacción química. Sin la masa molar, la estequiometría sería imposible.
- Preparación de Soluciones: Para preparar soluciones con concentraciones específicas (como la molaridad), se necesita conocer la masa molar del soluto para medir la cantidad correcta de masa que debe disolverse.
- Determinación de Fórmulas Empíricas y Moleculares: La masa molar experimental de un compuesto es vital para determinar su fórmula molecular a partir de su fórmula empírica.
- Análisis Químico: En técnicas analíticas como la espectrometría de masas, la masa molar es un dato clave para identificar compuestos desconocidos.
- Química Farmacéutica e Industrial: En la producción de fármacos, polímeros, fertilizantes y otros productos químicos, el control preciso de las cantidades de sustancia es esencial, y esto se logra a través de la masa molar.
En resumen, la masa molar es una de las herramientas más poderosas en el arsenal del químico, permitiendo una comprensión y manipulación cuantitativa de la materia.
Masa Molar vs. Peso Molecular vs. Masa Fórmula
Es común encontrar términos como "peso molecular" o "masa fórmula" y preguntarse si son lo mismo que la masa molar. Aunque a menudo se usan indistintamente en contextos informales, técnicamente hay matices:
- Masa Atómica: La masa promedio de un átomo de un elemento, expresada en unidades de masa atómica (uma). Es el valor que encontramos en la tabla periódica.
- Masa Molecular (o Peso Molecular): La suma de las masas atómicas de todos los átomos en una molécula. Se aplica a compuestos moleculares (que forman moléculas discretas, como H2O o C6H12O6) y se expresa en uma.
- Masa Fórmula (o Peso Fórmula): La suma de las masas atómicas de todos los átomos en una unidad de fórmula de un compuesto iónico (que forman redes cristalinas, como NaCl o Ca(OH)2). También se expresa en uma.
- Masa Molar: Es la masa de un mol de cualquier sustancia (ya sea molecular, iónica o atómica), numéricamente igual a la masa molecular o masa fórmula, pero expresada en gramos por mol (g/mol).
En la práctica, cuando hablamos de "masa molar" de un compuesto, nos referimos al valor numérico de su masa molecular o masa fórmula, pero con las unidades g/mol.
Preguntas Frecuentes (FAQ)
¿Cuál es la masa molar de 58.44 g/mol?
La pregunta está formulada de una manera que puede generar confusión. 58.44 g/mol ya es un valor de masa molar. No se calcula una masa molar a partir de un valor de masa molar; más bien, 58.44 g/mol es la masa molar de un compuesto específico. En este caso, como se mencionó en los ejemplos, es la masa molar del cloruro de sodio (NaCl).
¿Cómo se calcula la masa molar promedio?
El término "masa molar promedio" puede referirse a dos conceptos principales:
- Masa Atómica Promedio: Las masas atómicas que aparecen en la tabla periódica (ej. 12.01 g/mol para el carbono) ya son masas atómicas promedio. Estas se calculan tomando el promedio ponderado de las masas de todos los isótopos naturales de un elemento, considerando su abundancia relativa. Por ejemplo, el cloro tiene dos isótopos principales, Cl-35 y Cl-37, y su masa atómica promedio de 35.45 g/mol refleja sus proporciones en la naturaleza.
- Masa Molar Promedio de una Mezcla: Si tienes una mezcla de diferentes compuestos (por ejemplo, una mezcla de gases), la masa molar promedio de la mezcla se calcula como el promedio ponderado de las masas molares de cada componente en la mezcla, donde las ponderaciones son las fracciones molares o fracciones másicas de cada componente. Este cálculo es más complejo y depende de la composición específica de la mezcla. Para este artículo, nos hemos centrado en el cálculo de la masa molar de un *único* compuesto puro.
¿La masa molar siempre es positiva?
Sí, la masa molar siempre será un valor positivo. La masa es una propiedad intrínseca de la materia y no puede ser cero o negativa.
¿Qué significa g/mol?
g/mol significa "gramos por mol". Esta unidad indica cuántos gramos de masa contiene un mol de una sustancia específica. Es una unidad fundamental para relacionar la masa con la cantidad de sustancia en química.
¿Es lo mismo masa molar que peso molecular?
Como se explicó anteriormente, numéricamente son equivalentes, pero las unidades difieren. La masa molecular se expresa en unidades de masa atómica (uma), mientras que la masa molar se expresa en gramos por mol (g/mol). En la práctica, a menudo se usan indistintamente para referirse al mismo valor numérico.
¿Qué hago si no tengo una tabla periódica a mano?
Sin una tabla periódica, no puedes calcular la masa molar de un compuesto, ya que necesitas los valores de las masas atómicas de cada elemento. La tabla periódica es una herramienta indispensable para este cálculo.
Conclusión
El cálculo de la masa molar es una habilidad química básica pero increíblemente poderosa. Al seguir los pasos sencillos de identificar los elementos, obtener sus masas atómicas, multiplicar por la cantidad de cada átomo y sumar los resultados, puedes determinar la masa molar de cualquier sustancia. Este conocimiento no solo te permitirá resolver problemas de química con facilidad, sino que también te dará una comprensión más profunda de cómo los químicos cuantifican y manipulan la materia en el laboratorio y en la industria. Dominar la masa molar es un paso fundamental hacia el éxito en el estudio de la química y sus múltiples aplicaciones.
Si quieres conocer otros artículos parecidos a Masa Molar: Guía Completa para Calcularla puedes visitar la categoría Química.

