24/11/2024
En el vasto y fascinante universo de la química, la capacidad de medir y calcular la masa de las sustancias es una habilidad fundamental. Ya sea que estemos en un laboratorio, en la industria o simplemente tratando de entender el mundo que nos rodea, comprender cómo determinar la masa en gramos es crucial. Los gramos son una unidad de medida estándar que nos permite cuantificar la cantidad de materia en objetos y sustancias, especialmente aquellos de peso ligero. A través de este artículo, exploraremos las distintas metodologías para calcular la masa, desde la conversión de moles hasta la determinación de la masa fórmula de compuestos complejos y sus variantes hidratadas.

- Entendiendo los Gramos: La Unidad Fundamental de Masa
- Cálculo de la Masa a Partir de Moles: La Conexión Cuantitativa
- Masa Fórmula: La Suma de los Pesos Atómicos en un Compuesto
- Hidratos: Compuestos con Agua Incorporada
- Tabla Comparativa: Tipos de Masa y su Cálculo
- Preguntas Frecuentes (FAQs)
- ¿Cuál es la diferencia entre masa atómica y masa fórmula?
- ¿Cómo se usan los subíndices para determinar una masa fórmula cuando hay más de un ion poliatómico presente en una fórmula química?
- ¿Por qué es importante calcular la masa en química?
- ¿Dónde encuentro la masa molar de un elemento?
- ¿La masa fórmula siempre se expresa en amu?
Entendiendo los Gramos: La Unidad Fundamental de Masa
Un gramo (g) es una unidad de masa dentro del Sistema Internacional de Unidades, utilizada comúnmente para describir el peso de objetos o sustancias de tamaño moderado a pequeño. Es la milésima parte de un kilogramo (1 g = 0.001 kg), lo que lo convierte en una medida ideal para ingredientes de cocina, componentes de laboratorio o incluso para cuantificar elementos químicos individuales en una reacción. La notación estándar para un gramo es simplemente 'g', como en '1g'. Para medir la masa de objetos en gramos en la práctica, se utilizan instrumentos como balanzas o básculas de precisión, que proporcionan una lectura directa de la masa.
Cálculo de la Masa a Partir de Moles: La Conexión Cuantitativa
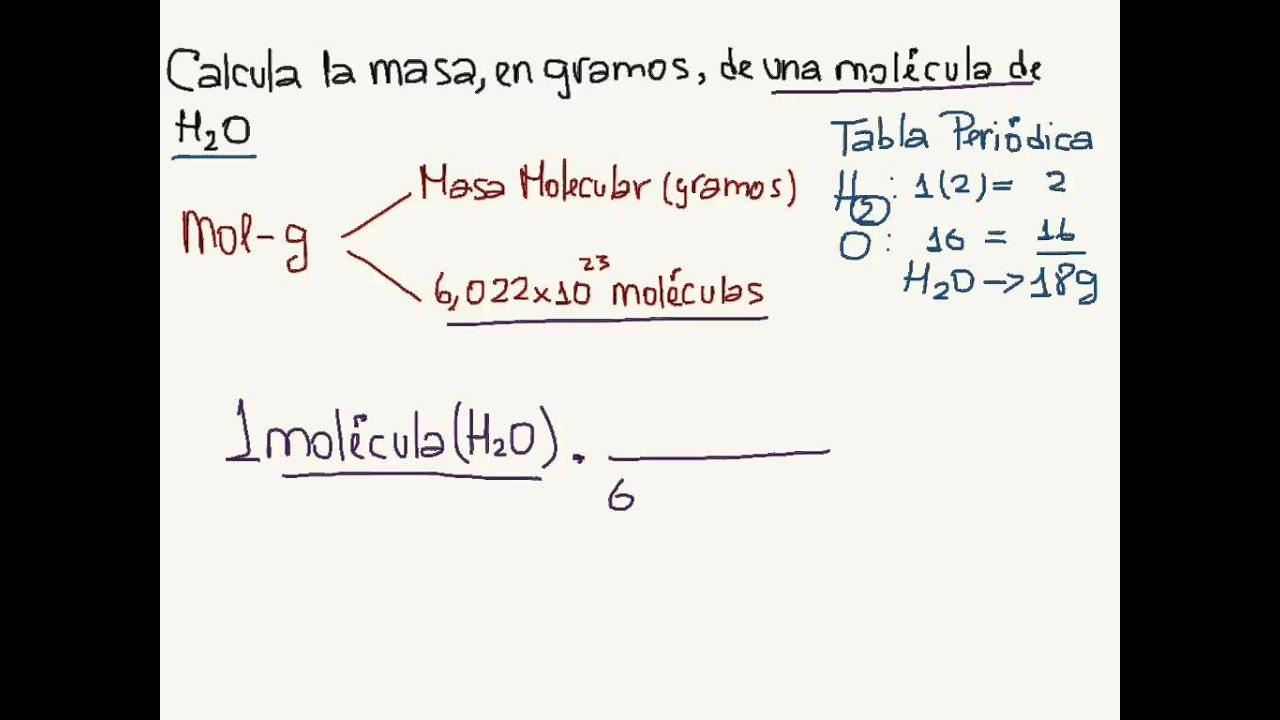
En química, no siempre trabajamos directamente con gramos. A menudo, las cantidades de sustancias se expresan en moles, una unidad que representa una cantidad específica de partículas (átomos, moléculas, iones, etc.). Un mol de cualquier sustancia contiene aproximadamente 6.022 x 1023 partículas, un número conocido como el número de Avogadro. Para convertir moles a gramos, necesitamos conocer la masa molar de la sustancia, que es la masa de un mol de esa sustancia y se expresa en gramos por mol (g/mol).
La masa molar de un elemento se encuentra directamente en la tabla periódica, generalmente debajo del símbolo del elemento. Para compuestos, la masa molar es la suma de las masas molares de todos los átomos en su fórmula química. La fórmula para calcular la masa a partir de moles es sencilla:
Masa (g) = Moles (mol) × Masa Molar (g/mol)
Ejemplo Práctico: Masa de Xenón
Consideremos el cálculo de la masa en gramos de 43.9 mol de Xenón (Xe). El primer paso es determinar la masa molar del Xenón. Consultando la tabla periódica, la masa molar del Xenón (Xe) es aproximadamente 131.29 g/mol.
Ahora, aplicamos la fórmula:
- Moles de Xe = 43.9 mol
- Masa Molar de Xe = 131.29 g/mol
- Masa de Xe = 43.9 mol × 131.29 g/mol
- Masa de Xe = 5765.331 g
Por lo tanto, 43.9 moles de Xenón tienen una masa de aproximadamente 5765.33 gramos.
Masa Fórmula: La Suma de los Pesos Atómicos en un Compuesto
Cuando hablamos de compuestos, especialmente los iónicos, el término "masa fórmula" es crucial. La masa fórmula es la suma de las masas atómicas de cada átomo individual presente en la fórmula química de un compuesto. Aunque las unidades de masa atómica (amu) se utilizan a menudo para la masa fórmula de una sola unidad, numéricamente coincide con la masa molar en g/mol. Dado que una fórmula adecuada de un compuesto iónico es eléctricamente neutra, los iones pueden considerarse como átomos para este cálculo.
Para determinar la masa fórmula, se deben seguir los siguientes pasos:
- Identificar todos los átomos presentes en la fórmula del compuesto.
- Obtener la masa atómica de cada elemento de la tabla periódica (redondeando a dos decimales para mayor precisión, como se sugiere en los ejemplos).
- Multiplicar la masa atómica de cada elemento por el número de veces que aparece en la fórmula.
- Sumar todas estas masas ponderadas para obtener la masa fórmula total.
Cálculo de la Masa Fórmula para Compuestos Simples
Ejemplo 1: Cloruro de Sodio (NaCl)
El cloruro de sodio está compuesto por un átomo de sodio (Na) y un átomo de cloro (Cl).
- Na: 22.99 amu
- Cl: + 35.45 amu
- Total: 58.44 amu
La masa fórmula del NaCl es 58.44 amu.
Ejemplo 2: Fluoruro de Calcio (CaF2)
Aquí tenemos un átomo de calcio (Ca) y dos átomos de flúor (F). Es crucial recordar multiplicar la masa del flúor por 2.

- Ca: 1 × 40.08 = 40.08 amu
- F: 2 × 19.00 = + 38.00 amu
- Total: 78.08 amu
La masa fórmula del CaF2 es 78.08 amu.
Cálculo de la Masa Fórmula con Iones Poliatómicos
Los iones poliatómicos son grupos de átomos unidos covalentemente que llevan una carga neta. Cuando estos iones forman parte de un compuesto iónico, su masa debe incluirse correctamente.
Ejemplo 3: Nitrato de Potasio (KNO3)
El nitrato de potasio contiene un átomo de potasio (K), un átomo de nitrógeno (N) y tres átomos de oxígeno (O).
- K: 1 × 39.10 = 39.10 amu
- N: 1 × 14.01 = + 14.01 amu
- O: 3 × 16.00 = + 48.00 amu
- Total: 101.11 amu
La masa fórmula del KNO3 es 101.11 amu.
Ejemplo 4: Nitrato de Calcio (Ca(NO3)2)
Este compuesto contiene un átomo de calcio (Ca) y dos iones nitrato (NO3). El subíndice 2 fuera del paréntesis indica que hay dos unidades completas del ion nitrato. Esto significa que debemos multiplicar la cantidad de cada átomo dentro del paréntesis por este subíndice.
- Ca: 1 × 40.08 = 40.08 amu
- N: 2 × 14.01 = + 28.02 amu (dos átomos de nitrógeno)
- O: 6 × 16.00 = + 96.00 amu (seis átomos de oxígeno, 3 × 2)
- Total: 164.10 amu
La masa fórmula del Ca(NO3)2 es 164.10 amu. La clave para estos cálculos es contar cada átomo en la fórmula de manera precisa y multiplicar sus masas atómicas correspondientemente.
Hidratos: Compuestos con Agua Incorporada
Algunos compuestos iónicos tienen moléculas de agua (H2O) incorporadas dentro de su unidad fórmula. Estos compuestos se conocen como hidratos y tienen un número característico de unidades de agua asociadas con cada unidad fórmula del compuesto. Es importante destacar que los hidratos son sólidos, no líquidos ni soluciones, a pesar del agua que contienen.
Para escribir la fórmula química de un hidrato, se escribe el número de unidades de agua por unidad de fórmula del compuesto después de su fórmula química, separadas por un punto centrado verticalmente. Por ejemplo, el sulfato de cobre(II) pentahidratado se escribe como CuSO4 • 5H2O, donde el prefijo 'penta-' indica la presencia de cinco unidades de agua.
Cálculo de la Masa Fórmula para Hidratos
Para calcular la masa fórmula de un hidrato, se suman la masa fórmula del compuesto anhidro (sin agua) y la masa total de las moléculas de agua asociadas.
Ejemplo: Sulfato de Cobre(II) Pentahidratado (CuSO4 • 5H2O)
Primero, calculamos la masa fórmula de CuSO4:
- Cu: 1 × 63.55 = 63.55 amu
- S: 1 × 32.07 = 32.07 amu
- O: 4 × 16.00 = + 64.00 amu
- Subtotal (CuSO4): 159.62 amu
Luego, calculamos la masa de una molécula de agua (H2O):
- H: 2 × 1.01 = 2.02 amu
- O: 1 × 16.00 = + 16.00 amu
- Subtotal (H2O): 18.02 amu
Dado que hay cinco moléculas de agua (5H2O), multiplicamos la masa de una molécula de agua por 5:
- Masa de 5H2O = 5 × 18.02 amu = 90.10 amu
Finalmente, sumamos la masa del CuSO4 y la masa de las cinco moléculas de agua:
- Masa Total (CuSO4 • 5H2O) = 159.62 amu + 90.10 amu = 249.72 amu
Usos Comunes de los Hidratos
Los hidratos tienen diversas aplicaciones en la industria y la vida cotidiana:
- Cloruro de aluminio hexahidratado (AlCl3 • 6H2O): Un ingrediente activo en muchos antitranspirantes.
- Sulfato de calcio hemihidratado (CaSO4 • ½H2O), yeso de París: Utilizado para hacer moldes para huesos rotos y otras fundiciones.
- Sulfato de calcio dihidratado (CaSO4 • 2H2O), yeso: Un componente principal de los paneles de yeso.
- Cloruro de cobalto(II) hexahidratado (CoCl2 • 6H2O): Agente secante e indicador de humedad, cambiando de color según la presencia de agua.
- Sulfato de cobre(II) pentahidratado (CuSO4 • 5H2O): Utilizado como fungicida, alguicida y herbicida.
- Sulfato de magnesio heptahidratado (MgSO4 • 7H2O), sales de Epsom: Conocido como sal de baño y laxante.
- Carbonato de sodio decahidratado (Na2CO3 • 10H2O), soda para lavar: Un aditivo y limpiador para la ropa.
Tabla Comparativa: Tipos de Masa y su Cálculo
Para consolidar los conceptos, la siguiente tabla resume los diferentes tipos de masa y cómo se calculan:
| Tipo de Masa | Definición | Unidad Común | Método de Cálculo | Ejemplo |
|---|---|---|---|---|
| Masa Atómica | Masa de un átomo individual de un elemento. | amu (unidades de masa atómica) | Se encuentra directamente en la tabla periódica. | Masa Atómica de C = 12.01 amu |
| Masa Molar | Masa de un mol de una sustancia (átomos, moléculas o iones). | g/mol (gramos por mol) | Suma de las masas atómicas de los elementos en la fórmula, expresada en g/mol. | Masa Molar de H2O = 18.02 g/mol |
| Masa Fórmula | Suma de las masas atómicas de todos los átomos en la unidad fórmula de un compuesto (usado para compuestos iónicos). | amu (unidades de masa atómica) | Suma de las masas atómicas (multiplicadas por subíndices) de todos los átomos en la fórmula. | Masa Fórmula de NaCl = 58.44 amu |
| Masa (en gramos) a partir de Moles | Cantidad total de materia de una sustancia dada en una muestra. | g (gramos) | Masa = Moles × Masa Molar | Masa de 2 moles de O2 = 2 mol × 32.00 g/mol = 64.00 g |
Preguntas Frecuentes (FAQs)
¿Cuál es la diferencia entre masa atómica y masa fórmula?
La masa atómica se refiere a la masa de un solo átomo de un elemento específico, y se expresa en unidades de masa atómica (amu). Por ejemplo, la masa atómica del oxígeno es de aproximadamente 16.00 amu. Por otro lado, la masa fórmula es la suma de las masas atómicas de todos los átomos presentes en la fórmula química de un compuesto, especialmente utilizada para compuestos iónicos. Se calcula sumando las masas atómicas de cada elemento, teniendo en cuenta los subíndices que indican la cantidad de cada átomo. Por ejemplo, la masa fórmula de H2O es (2 × 1.01 amu para H) + (1 × 16.00 amu para O) = 18.02 amu.
¿Cómo se usan los subíndices para determinar una masa fórmula cuando hay más de un ion poliatómico presente en una fórmula química?
Cuando un ion poliatómico aparece entre paréntesis con un subíndice fuera de ellos (por ejemplo, Ca(NO3)2), el subíndice se aplica a todos los átomos dentro del paréntesis. Para calcular la masa fórmula, se debe multiplicar la masa atómica de cada elemento dentro del ion poliatómico por el subíndice correspondiente. En el caso de Ca(NO3)2, el subíndice 2 fuera del paréntesis indica que hay dos iones nitrato completos. Esto significa que hay 2 átomos de nitrógeno (N) y 6 átomos de oxígeno (O) (ya que hay 3 átomos de O en un NO3, y se multiplica por 2). Luego, se suman estas masas al resto de los átomos en el compuesto.
¿Por qué es importante calcular la masa en química?
Calcular la masa es fundamental en química por varias razones. Permite a los científicos realizar mediciones precisas para experimentos, asegurar proporciones estequiométricas correctas en reacciones químicas, determinar la pureza de las sustancias, y en la industria, es vital para el control de calidad y la producción de materiales a gran escala. Es la base para entender las relaciones cuantitativas entre reactivos y productos.
¿Dónde encuentro la masa molar de un elemento?
La masa molar de un elemento se encuentra directamente en la tabla periódica. Generalmente, es el número decimal que aparece debajo del símbolo del elemento. Este valor numéricamente es idéntico a la masa atómica, pero sus unidades son gramos por mol (g/mol) en lugar de unidades de masa atómica (amu), lo que facilita las conversiones a gran escala.
¿La masa fórmula siempre se expresa en amu?
Tradicionalmente, la masa fórmula se expresa en unidades de masa atómica (amu) cuando se refiere a la masa de una única unidad de fórmula de un compuesto. Sin embargo, en la práctica, el valor numérico de la masa fórmula es idéntico al de la masa molar, que se expresa en gramos por mol (g/mol). Por lo tanto, a menudo se usan indistintamente dependiendo del contexto: amu para la escala atómica/molecular individual, y g/mol para cantidades macroscópicas (moles).
Dominar el cálculo de la masa en gramos y sus conceptos relacionados es una habilidad esencial para cualquier persona que se adentre en el estudio de la química. Desde la simple conversión de moles hasta la compleja determinación de la masa fórmula de hidratos, cada paso nos acerca a una comprensión más profunda de la materia y sus propiedades. Con la práctica y la ayuda de la tabla periódica, estos cálculos se convertirán en una segunda naturaleza, abriendo las puertas a un sinfín de posibilidades en el mundo de la ciencia.
Si quieres conocer otros artículos parecidos a ¿Cómo Calcular la Masa en Gramos? puedes visitar la categoría Química.