02/09/2023
En el vasto universo de la química, la acidez es una propiedad fundamental que influye en innumerables reacciones y procesos, desde la digestión de nuestros alimentos hasta la fabricación de productos industriales. A menudo, hablamos de ácidos en términos cualitativos: "este es un ácido fuerte", "aquel es un ácido débil". Sin embargo, para los químicos y para cualquiera que desee comprender a fondo el comportamiento de las sustancias, es crucial ir más allá de las tendencias y las descripciones generales. Necesitamos herramientas que nos permitan cuantificar la acidez, compararla con precisión y predecir cómo reaccionará una sustancia en un entorno dado. Aquí es donde entran en juego dos conceptos esenciales y a menudo confusos: la constante de acidez, Ka, y su logaritmo negativo, pKa. Estas dos medidas nos proporcionan una visión numérica clara de la fuerza de un ácido, permitiéndonos ordenar, predecir y aplicar este conocimiento en un sinfín de situaciones.
- La Constante de Acidez (Ka): La Medida Directa de la Disociación
- La Escala Logarítmica: pKa como Medida de Conveniencia
- Ka y pKa: Una Relación Inseparable
- Más Allá de Arrhenius: La Perspectiva de Brønsted-Lowry
- Aplicaciones Prácticas: De la Cerveza a la Química Diaria
- Tabla Comparativa: Ka vs. pKa
- Preguntas Frecuentes (FAQ)
- ¿Cómo se calcula la Ka a partir de la pKa?
- ¿Por qué el ácido de un limón no quema la lengua pero el ácido clorhídrico concentrado podría destruir un pedazo de metal?
- ¿Cómo determinar la fuerza del ácido a partir de pKa?
- ¿Qué significa una pKa negativa?
- ¿Qué es el efecto de nivelación del solvente y cómo afecta las mediciones de Ka/pKa?
La Constante de Acidez (Ka): La Medida Directa de la Disociación
Para entender la fuerza de un ácido de manera cuantitativa, primero debemos observar lo que ocurre cuando un ácido se disuelve en un solvente, comúnmente agua. Consideremos un ácido genérico, HA, que al disolverse en agua, puede donar un protón (H+) para formar su base conjugada (A-) y un ion hidronio (H3O+). Esta reacción no es unidireccional; también ocurre la reacción inversa, donde la base conjugada reacciona con el hidronio para reformar el ácido. Por lo tanto, estamos hablando de un equilibrio químico.
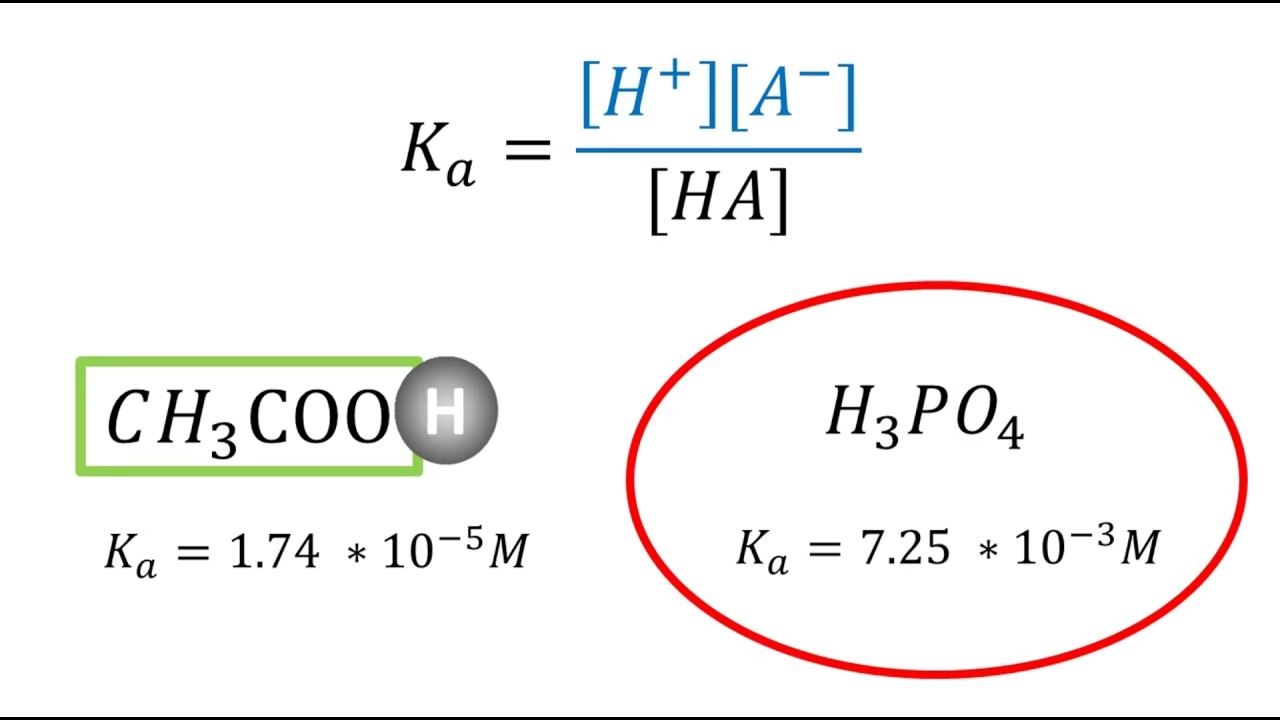
La constante de equilibrio para la disociación de un ácido se define como la constante de acidez, Ka. Se calcula dividiendo el producto de las concentraciones de los productos (iones hidronio y base conjugada) elevadas a sus coeficientes estequiométricos, entre la concentración del ácido no disociado, todo ello en el equilibrio. Para la reacción HA(ac) + H2O(l) ⇌ H3O+(ac) + A-(ac), la expresión de Ka es:
Ka = [H3O+][A-] / [HA]
Un valor alto de Ka indica que el ácido se disocia en gran medida en sus iones, lo que significa que es un ácido fuerte. Por el contrario, un valor bajo de Ka sugiere que el ácido se disocia muy poco, indicando que es un ácido débil. Por ejemplo, el ácido yodhídrico (HI), un ácido muy fuerte, tiene una Ka de aproximadamente 10^10. Esto significa que por cada molécula de HI que permanece sin disociar, hay diez mil millones de iones yoduro (I-) e hidronio (H3O+). Es una disociación casi completa. En el otro extremo del espectro, el metano (CH4), que es un ácido extremadamente débil, tiene una Ka de aproximadamente 10^-50, lo que indica que apenas se disocia en absoluto. El metanol (CH3OH), un ácido débil, tiene una Ka de alrededor de 10^-16.
La Ka es una medida directa y fundamental de la fuerza de un ácido. Sin embargo, trabajar con números tan grandes o tan pequeños, que involucran potencias de diez muy variadas, puede ser incómodo y propenso a errores. Es aquí donde la escala logarítmica de pKa demuestra su valor.
La Escala Logarítmica: pKa como Medida de Conveniencia
Para simplificar la comparación de ácidos con Ka que varían en muchas órdenes de magnitud, los científicos adoptaron una escala logarítmica, similar a la escala Richter para terremotos o la escala de pH para la concentración de iones hidrógeno. En el caso de la acidez, esta escala se conoce como pKa. La pKa se define como el logaritmo negativo (base 10) de la Ka:
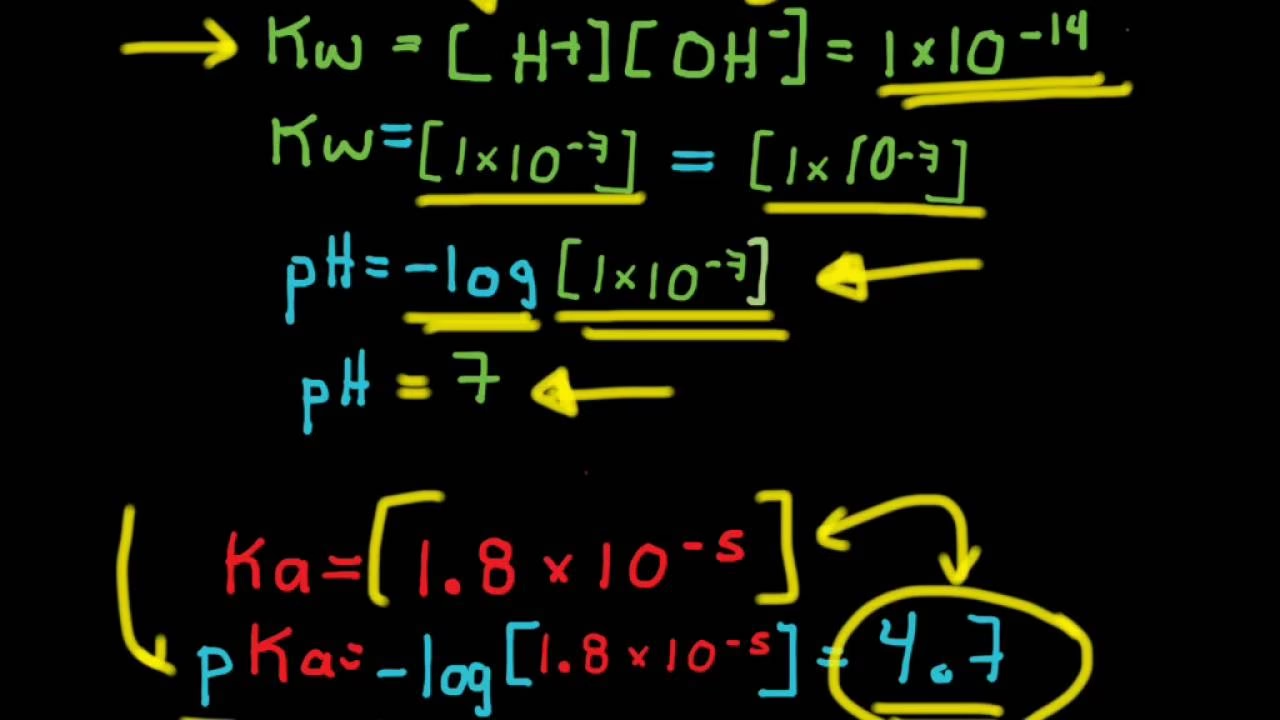
pKa = -log(Ka)
La razón por la que se utiliza el logaritmo negativo es doble: primero, la mayoría de los valores de Ka para ácidos débiles son menores que 1, lo que resultaría en logaritmos negativos. Al tomar el negativo del logaritmo, se obtienen valores positivos para la mayoría de los ácidos débiles, lo que resulta más fácil de manejar. Segundo, convierte una escala multiplicativa (Ka) en una aditiva (pKa), donde cada unidad de pKa representa un cambio de diez veces en la fuerza del ácido. Por ejemplo, un ácido con pKa de 2 es diez veces más fuerte que uno con pKa de 3, y cien veces más fuerte que uno con pKa de 4.
La relación inversa entre Ka y pKa es crucial: cuanto menor sea el valor de pKa, más fuerte será el ácido. Esto se debe a que un pKa bajo corresponde a una Ka alta. Retomando nuestros ejemplos anteriores:
- Para el ácido yodhídrico (HI), con Ka ≈ 10^10, su pKa es -log(10^10) = -10. Un valor negativo y muy bajo, indicando un ácido muy fuerte.
- Para el metanol (CH3OH), con Ka ≈ 10^-16, su pKa es -log(10^-16) = 16. Un valor moderado, típico de un ácido débil.
- Para el metano (CH4), con Ka ≈ 10^-50, su pKa es -log(10^-50) = 50. Un valor muy alto, indicando un ácido extremadamente débil.
La escala de pKa es extraordinariamente amplia, abarcando más de 60 órdenes de magnitud. Para poner esto en perspectiva, esta es la misma magnitud de rango que existe entre la longitud de Planck (la distancia más pequeña concebible, 10^-35 metros) y el ancho del universo observable (aproximadamente 10^26 metros). Esta vasta escala permite comparar la acidez de una diversidad inmensa de compuestos, desde los ácidos más corrosivos hasta las sustancias más levemente ácidas. Las tablas de pKa son herramientas invaluables para los químicos, ya que resumen la fuerza relativa de miles de grupos funcionales y moléculas, y también proporcionan información sobre la basicidad de sus bases conjugadas (un ácido fuerte tiene una base conjugada débil, y viceversa).
Ka y pKa: Una Relación Inseparable
La Ka y la pKa son dos caras de la misma moneda, ambas describen la fuerza de un ácido pero en diferentes escalas. La Ka es la constante de equilibrio directa, que nos da una idea de la proporción de disociación. La pKa es una forma más conveniente de expresar esta misma información, utilizando una escala logarítmica que facilita las comparaciones y los cálculos. Si conocemos una, podemos calcular la otra fácilmente:
- De Ka a pKa:
pKa = -log(Ka) - De pKa a Ka:
Ka = 10^(-pKa)
Es fundamental recordar que un valor de Ka grande se traduce en un valor de pKa pequeño (incluso negativo), lo que indica un ácido fuerte. Por el contrario, un valor de Ka pequeño se traduce en un valor de pKa grande, lo que indica un ácido débil. Comprender esta relación es clave para interpretar correctamente la información sobre la acidez de las sustancias.
Más Allá de Arrhenius: La Perspectiva de Brønsted-Lowry
Mientras que el concepto de Arrhenius define los ácidos como sustancias que producen iones H+ en agua, la teoría de Brønsted-Lowry amplía esta definición. Bajo este enfoque, un ácido es una especie que dona un protón (H+), y una base es una especie que acepta un protón. Esta definición es más amplia y permite considerar la acidez en sistemas no acuosos o para moléculas que no se disocian fácilmente en agua para producir iones hidronio, pero que, sin embargo, pueden donar un protón a otra molécula. La Ka y la pKa son particularmente relevantes para describir la fuerza de los ácidos débiles bajo la teoría de Brønsted-Lowry, ya que estos ácidos no se disocian completamente y, por lo tanto, su equilibrio de disociación es fundamental para determinar su comportamiento.
Por ejemplo, el ácido acético (el componente principal del vinagre) no se disocia completamente en agua. Su reacción de equilibrio es:
CH3COOH(ac) + H2O(l) ⇌ H3O+(ac) + CH3COO-(ac)
Para el ácido acético a 25 °C, la Ka es aproximadamente 1.8 x 10^-5, lo que resulta en una pKa de 4.74. Estos valores nos dicen que el ácido acético es un ácido débil, mucho más débil que el HCl (pKa ≈ -7) pero mucho más fuerte que el metano (pKa ≈ 50). Esta cuantificación permite a los químicos predecir la extensión de la reacción y el pH de una solución.
Aplicaciones Prácticas: De la Cerveza a la Química Diaria
La comprensión de Ka y pKa tiene aplicaciones prácticas en una miríada de campos, desde la química industrial hasta la biología. Nos permite entender por qué el ácido de un limón (ácido cítrico, con pKa alrededor de 3-5) no quema la lengua, mientras que el ácido clorhídrico concentrado (HCl, con pKa de aproximadamente -7) es altamente corrosivo y puede disolver metales. La diferencia radica en su fuerza: el HCl se disocia casi por completo, liberando una gran concentración de iones H+, mientras que el ácido cítrico se disocia en menor medida, liberando muchos menos H+.

Un ejemplo clásico de aplicación en la industria es la preparación de mosto de cerveza. El pH del mosto debe ser óptimo para que las enzimas encargadas de descomponer el almidón funcionen eficazmente. Supongamos que necesitamos un pH de 5.3 y decidimos usar ácido láctico, que tiene una pKa de 3.8. Si agregamos 9 kg de ácido láctico a 1000 L de agua, ¿cuál sería el pH resultante?
Primero, convertimos la pKa del ácido láctico a Ka: Ka = 10^(-3.8) = 0.000158 (o 1.58 x 10^-4).
Luego, calculamos la concentración inicial de ácido láctico (HOLac). La masa molar del ácido láctico (C3H6O3) es aproximadamente 90.08 g/mol. 9 kg son 9000 g.
Moles de ácido láctico = 9000 g / 90.08 g/mol ≈ 99.91 moles
Concentración inicial [HOLac] = 99.91 moles / 1000 L ≈ 0.100 M
La disociación del ácido láctico en agua es:
HOLac(ac) + H2O(l) ⇌ H3O+(ac) + LacO-(ac)
Inicial: [HOLac] = 0.100 M, [H3O+] = 0, [LacO-] = 0
Cambio: [HOLac] = -x, [H3O+] = +x, [LacO-] = +x
Equilibrio: [HOLac] = 0.100 - x, [H3O+] = x, [LacO-] = x
Aplicamos la expresión de Ka:
Ka = [H3O+][LacO-] / [HOLac]
1.58 x 10^-4 = (x)(x) / (0.100 - x)
Dado que Ka es pequeña y la concentración inicial es relativamente grande (más de 1000 veces mayor que Ka), podemos hacer la aproximación de que 0.100 - x ≈ 0.100. Esto simplifica la ecuación:
1.58 x 10^-4 = x^2 / 0.100
x^2 = 1.58 x 10^-5
x = √(1.58 x 10^-5) ≈ 0.00397 M
Dado que x representa la concentración de iones hidronio [H3O+] en el equilibrio, podemos calcular el pH:
pH = -log[H3O+] = -log(0.00397) ≈ 2.40
Este resultado (pH 2.40) es mucho más ácido que el pH objetivo de 5.3 para el mosto de cerveza, lo que indica que agregar 9 kg de ácido láctico a 1000 L de agua es una cantidad excesiva. Este ejemplo ilustra la importancia de Ka y pKa para realizar cálculos precisos y ajustar las condiciones en procesos industriales.
Tabla Comparativa: Ka vs. pKa
Para resumir las diferencias clave entre Ka y pKa, presentamos la siguiente tabla:
| Característica | Ka (Constante de Acidez) | pKa (-log de la Ka) |
|---|---|---|
| Definición | Constante de equilibrio para la disociación de un ácido. | Logaritmo negativo (base 10) de la Ka. |
| Rango de Valores | Varía ampliamente (e.g., 10^10 a 10^-50). | Varía ampliamente (e.g., -10 a 50), más compacta y manejable. |
| Relación con la Fuerza del Ácido | Mayor Ka = Ácido más fuerte. | Menor pKa = Ácido más fuerte. |
| Facilidad de Comparación | Difícil de comparar directamente debido a los exponentes. | Fácil de comparar directamente en una escala lineal. |
| Unidades | No tiene unidades (es una constante de equilibrio). | No tiene unidades. |
Preguntas Frecuentes (FAQ)
¿Cómo se calcula la Ka a partir de la pKa?
Para calcular la Ka a partir de la pKa, simplemente se invierte la operación logarítmica. La fórmula es: Ka = 10^(-pKa). Por ejemplo, si un ácido tiene una pKa de 4.74, su Ka será 10^(-4.74), que es aproximadamente 1.8 x 10^-5.
¿Por qué el ácido de un limón no quema la lengua pero el ácido clorhídrico concentrado podría destruir un pedazo de metal?
La diferencia radica en la fuerza de los ácidos, que se cuantifica con Ka y pKa. El ácido cítrico en un limón es un ácido relativamente débil (pKa ~3-5), lo que significa que solo una pequeña fracción de sus moléculas se disocia en iones H+ en solución. La concentración de iones H+ libres es, por lo tanto, baja. Por otro lado, el ácido clorhídrico (HCl) es un ácido muy fuerte (pKa ≈ -7), lo que significa que se disocia casi por completo en iones H+ y Cl- en solución. Esto resulta en una concentración muy alta de iones H+ libres, que son responsables de la acidez y la corrosividad. Una alta concentración de H+ puede interactuar violentamente con las proteínas de tu lengua o con los átomos de un metal, causando daño.
¿Cómo determinar la fuerza del ácido a partir de pKa?
La fuerza de un ácido es inversamente proporcional a su valor de pKa. Es decir, cuanto menor sea el pKa, más fuerte será el ácido. Un pKa negativo indica un ácido muy fuerte, que se disocia casi por completo en solución. Un pKa alto (positivo y grande) indica un ácido muy débil, que apenas se disocia. Por ejemplo, un ácido con pKa de 1 es mucho más fuerte que uno con pKa de 5, y este último es más fuerte que uno con pKa de 10.
¿Qué significa una pKa negativa?
Una pKa negativa indica un ácido muy fuerte. Recuerda que pKa = -log(Ka). Si la pKa es negativa, significa que el logaritmo de Ka es positivo, lo que a su vez implica que Ka es un número mayor que 1. Los ácidos con Ka mayor que 1 se disocian casi por completo en solución, liberando una gran cantidad de iones H+. Ejemplos incluyen ácidos inorgánicos fuertes como el HCl, HBr, HI, H2SO4, y HNO3.
¿Qué es el efecto de nivelación del solvente y cómo afecta las mediciones de Ka/pKa?
El efecto de nivelación del solvente se refiere a la incapacidad de ciertos solventes (como el agua) para distinguir entre la fuerza de ácidos o bases que son más fuertes que el ácido o la base conjugada del propio solvente. En agua, el ácido más fuerte que puede existir es el ion hidronio (H3O+), y la base más fuerte es el ion hidróxido (OH-). Cualquier ácido más fuerte que el H3O+ (por ejemplo, HCl o H2SO4) reaccionará completamente con el agua para formar H3O+, por lo que todos estos ácidos fuertes parecerán tener la misma fuerza en agua. Esto significa que sus pKa reales (medidos en solventes no niveladores) serán mucho más bajos de lo que se podría medir en agua. Por esta razón, las tablas de pKa a menudo listan valores de pKa para ácidos muy fuertes que son negativos y se obtienen en solventes especiales o por métodos teóricos.
En conclusión, Ka y pKa son herramientas indispensables para cualquier persona que trabaje con ácidos y bases. Proporcionan una forma cuantitativa y precisa de medir y comparar la fuerza de los ácidos, permitiendo una comprensión más profunda de su comportamiento químico. Al dominar estos conceptos, se abren las puertas a la predicción de reacciones, el diseño de experimentos y la resolución de problemas en un sinfín de aplicaciones científicas e industriales.
Si quieres conocer otros artículos parecidos a Ka vs. pKa: Entendiendo la Fuerza de los Ácidos puedes visitar la categoría Química.