31/12/2023
El mundo de la química orgánica está lleno de sorpresas y complejidades, y una de las más intrigantes es, sin duda, el fenómeno del isomerismo. Imagina compuestos que comparten la misma fórmula molecular, es decir, están hechos de los mismos 'bloques de construcción', pero que, sin embargo, se comportan de manera completamente diferente debido a una disposición distinta de sus átomos. Esta es la esencia del isomerismo: la existencia de moléculas con idéntica composición atómica, pero con variaciones en su estructura o en su orientación espacial, lo que les confiere propiedades físicas y químicas distintivas. Comprender y predecir la existencia de estos isómeros es fundamental para la síntesis de nuevos materiales, el desarrollo de fármacos y la comprensión de los procesos biológicos.
- Desentrañando los Tipos de Isómeros
- Estereoisómeros: Enantiómeros y Diastereómeros
- Quiralidad y Centros Estereogénicos: El Corazón de la Estereoquímica
- La Fórmula Universal: La Regla 2^n para el Cálculo de Estereoisómeros
- Excepciones a la Regla 2^n: Los Compuestos Meso
- Identificación de Estereoisómeros: Más Allá de los Átomos Quirales
- Guía Paso a Paso para Identificar Estereoisómeros
- Preguntas Frecuentes (FAQs) sobre Estereoisómeros
- ¿Cómo se calcula el número de estereoisómeros?
- ¿Cuál es la fórmula para calcular los estereoisómeros?
- ¿Cómo se encuentra el número real de estereoisómeros, considerando las excepciones?
- ¿Cómo se obtienen estereoisómeros en el laboratorio?
- ¿Es suficiente la presencia de un centro quiral para que una molécula sea quiral?
- ¿Puede una molécula ser quiral sin tener un centro quiral?
Desentrañando los Tipos de Isómeros
Antes de sumergirnos en el cálculo de los estereoisómeros, es crucial distinguir entre las categorías principales de isómeros:
Isómeros Constitucionales (o Estructurales)
Estos isómeros tienen la misma fórmula molecular, pero difieren en la conectividad de sus átomos. Es decir, los átomos están unidos de una manera diferente. Podemos subdividirlos en isómeros de cadena (diferente ramificación del esqueleto de carbono), de posición (diferente ubicación de un grupo funcional o de un doble/triple enlace) y de grupo funcional (diferentes grupos funcionales).
Estereoisómeros
A diferencia de los isómeros constitucionales, los estereoisómeros poseen la misma conectividad atómica. Esto significa que los átomos están unidos en el mismo orden, pero su diferencia radica en la orientación tridimensional de sus átomos en el espacio. Son como nuestras manos: ambas tienen los mismos dedos conectados de la misma manera, pero una es la imagen especular no superponible de la otra.
Estereoisómeros: Enantiómeros y Diastereómeros
Dentro de la categoría de estereoisómeros, existen dos subgrupos principales que es vital diferenciar para comprender su cálculo y propiedades:
Enantiómeros
Los enantiómeros son estereoisómeros que son imágenes especulares no superponibles entre sí. Piensa en tu mano izquierda y tu mano derecha: son imágenes especulares, pero no puedes superponerlas perfectamente (por ejemplo, al intentar calzar un guante izquierdo en tu mano derecha). En el ámbito molecular, esta característica es fundamental, ya que los enantiómeros suelen tener propiedades físicas idénticas (puntos de fusión, ebullición, densidad) y propiedades químicas similares, excepto en su interacción con la luz polarizada (rotan el plano de la luz polarizada en direcciones opuestas) y en ambientes quirales (como en sistemas biológicos, donde un enantiómero puede ser un fármaco activo y el otro inactivo o incluso tóxico).
Diastereómeros
Los diastereómeros, por otro lado, son estereoisómeros que no son imágenes especulares entre sí. A diferencia de los enantiómeros, los diastereómeros poseen propiedades físicas y químicas diferentes. Esto los hace mucho más fáciles de separar y distinguir en el laboratorio. Su existencia se debe a que tienen múltiples centros estereogénicos, y al menos uno de ellos tiene una configuración diferente, mientras que otro(s) tiene(n) la misma configuración.
La siguiente tabla comparativa resume las diferencias clave entre estos dos tipos de estereoisómeros:
| Característica | Enantiómeros | Diastereómeros |
|---|---|---|
| Relación estructural | Imágenes especulares no superponibles | No son imágenes especulares entre sí |
| Propiedades físicas y químicas | Idénticas (excepto con luz polarizada) | Diferentes |
| Forma molecular | Misma forma molecular | Forma molecular diferente |
| Número de pares | Ocurren en pares | Puede haber varios diastereómeros |
| Centros estereogénicos | Uno o más centros estereogénicos | Dos o más centros estereogénicos |
| Configuración R/S | Configuraciones R y S opuestas en todos los centros | Configuración diferente en algunos centros, igual en otros |
Quiralidad y Centros Estereogénicos: El Corazón de la Estereoquímica
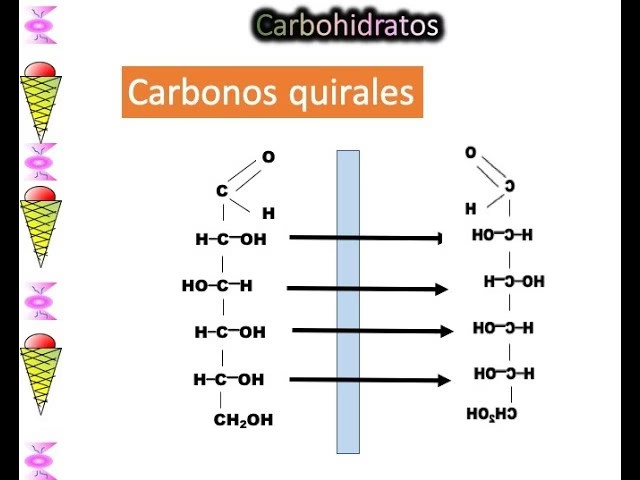
El concepto de quiralidad es fundamental para entender los estereoisómeros. Una molécula es quiral si su imagen especular no es superponible a sí misma. La palabra 'quiral' proviene del griego 'cheir', que significa mano. La mayoría de las moléculas quirales contienen uno o más átomos de carbono con cuatro sustituyentes diferentes unidos a él. Este átomo de carbono, que es el punto de origen de la quiralidad en muchos compuestos, se denomina centro quiral, centro estereogénico o estereocentro. La disposición tridimensional de estos cuatro grupos no idénticos es lo que impide la superposición de la molécula con su imagen especular, a pesar de tener los mismos constituyentes.
Cada centro estereogénico puede existir en dos configuraciones espaciales distintas, denotadas como R (rectus, derecha) y S (sinister, izquierda). Estas designaciones se basan en una convención para describir la orientación relativa de los sustituyentes alrededor del centro quiral. La posibilidad de estas dos configuraciones para cada centro estereogénico es lo que da origen a la multiplicidad de estereoisómeros.

La Fórmula Universal: La Regla 2^n para el Cálculo de Estereoisómeros
A medida que las moléculas aumentan en complejidad y el número de centros estereogénicos se incrementa, también lo hace el número de posibles estereoisómeros. Una molécula con un único centro estereogénico, como el 2-butanol, puede tener dos estereoisómeros: las configuraciones R y S, que son enantiómeros entre sí.
Si consideramos una molécula con dos centros estereogénicos, cada uno de ellos puede ser R o S. Esto nos lleva a cuatro combinaciones posibles de configuraciones: RR, SS, RS y SR. De estas, RR y SS son un par de enantiómeros, mientras que RS y SR son otro par de enantiómeros. Sin embargo, RR es diastereómero de RS y SR, y SS es diastereómero de RS y SR.
Siguiendo esta lógica, para una molécula con tres átomos quirales, las combinaciones posibles se duplican nuevamente, resultando en ocho estereoisómeros posibles: RRR, RRS, RSR, SRR, SSR, SRS, RSS y SSS.
Este patrón exponencial nos lleva a la fórmula general para calcular el número máximo de estereoisómeros:
Número de Estereoisómeros = 2n
Donde 'n' representa el número de centros estereogénicos presentes en la molécula. Esta es la llamada Regla 2n. La fórmula nos indica que el número de estereoisómeros aumenta exponencialmente con cada centro quiral adicional. Por ejemplo, la glucosa, un azúcar común, posee cuatro centros estereogénicos (n=4), lo que según esta regla implicaría un máximo de 24 = 16 estereoisómeros posibles, cada uno con propiedades únicas.
Excepciones a la Regla 2^n: Los Compuestos Meso
Aunque la regla 2n es una herramienta poderosa y generalmente precisa para predecir el número máximo de estereoisómeros, existen casos en los que esta fórmula no proporciona el número real. Esto ocurre en moléculas que poseen un alto grado de simetría interna, lo que lleva a que algunos de los estereoisómeros predichos sean idénticos o aquirales.
Un ejemplo clásico de esta excepción es el 2,3-diclorobutano. Según la regla 2n, con dos centros estereogénicos (n=2), esperaríamos 22 = 4 estereoisómeros. Sin embargo, en la realidad, solo existen tres estereoisómeros:
- Un par de enantiómeros (SS y RR).
- Una tercera molécula que, a pesar de contener centros estereogénicos, es aquiral debido a la presencia de un plano de simetría interno. Esta molécula es su propia imagen especular superponible.
Esta tercera molécula se conoce como compuesto meso. Un compuesto meso es un estereoisómero de un compuesto quiral que, a pesar de contener centros estereogénicos, es globalmente aquiral debido a la presencia de un plano de simetría o un centro de inversión. Esto significa que su imagen especular es superponible. Por lo tanto, en el caso del 2,3-diclorobutano, las combinaciones SR y RS resultan ser idénticas y corresponden al compuesto meso.

La existencia de compuestos meso subraya un punto crucial: la presencia de un átomo con cuatro grupos diferentes unidos a él (un centro quiral) no es en sí misma suficiente para garantizar que toda la molécula sea quiral. La quiralidad de una molécula compleja solo puede determinarse de forma absoluta dibujando su imagen especular y verificando si es superponible a la molécula original. Este es el método más seguro para evitar errores.
Identificación de Estereoisómeros: Más Allá de los Átomos Quirales
Si bien los átomos quirales son la fuente más común de estereoisomería, no son las únicas. Para determinar si una molécula tiene estereoisómeros, es importante considerar otras características moleculares clave. No todas las moléculas quirales contienen un átomo unido a cuatro grupos diferentes; algunas exhiben quiralidad debido a su arquitectura molecular global, como la forma espiral del hexaheliceno.
Para una identificación exhaustiva, debemos enfocarnos en tres fuentes principales de estereoquímica:
1. Átomos Quirales (Estereocentros)
Como ya se mencionó, un átomo quiral es un átomo (comúnmente carbono, pero también nitrógeno, fósforo o azufre) unido a cuatro grupos diferentes. Cada vez que identificas un átomo quiral, existe la posibilidad de un par de enantiómeros. Si hay múltiples centros quirales, el número potencial de estereoisómeros aumenta según la fórmula 2n, aunque este número puede reducirse por la presencia de compuestos meso.
2. Dobles Enlaces (Isomería E/Z)
Los dobles enlaces, especialmente entre átomos de carbono, pueden ser otra fuente de estereoisomería, conocida como isomería geométrica o cis-trans (o más precisamente, E/Z). Para que exista esta estereoisomería, cada carbono del doble enlace debe estar unido a dos grupos diferentes. Si los grupos de mayor prioridad en cada carbono del doble enlace están en el mismo lado, se designa como isómero Z (del alemán 'zusammen', juntos). Si están en lados opuestos, se designa como isómero E (del alemán 'entgegen', opuestos). Estos isómeros E/Z son un tipo de diastereómeros, ya que no son imágenes especulares entre sí y tienen propiedades físicas y químicas distintas.
3. Estructuras Cíclicas (Isomería Cis/Trans en Anillos)
Las estructuras cíclicas, particularmente los anillos disustituidos (con dos sustituyentes), son otra fuente importante de estereoisomería. Incluso si los átomos individuales en el anillo no son quirales, la posición relativa de los sustituyentes en el anillo puede generar estereoisómeros. Si los dos sustituyentes están en el mismo lado del plano del anillo (por ejemplo, ambos apuntando hacia arriba o hacia abajo), la molécula es un isómero cis. Si están en lados opuestos, es un isómero trans. Al igual que los isómeros E/Z, los isómeros cis y trans de anillos son diastereómeros porque no son imágenes especulares no superponibles. Esto es crucial en anillos pequeños donde la rotación libre está restringida, fijando las posiciones relativas de los sustituyentes.
Guía Paso a Paso para Identificar Estereoisómeros
Para determinar sistemáticamente si una molécula tiene estereoisómeros y cuántos, sigue estos pasos:
- Busca Átomos Quirales: Identifica cualquier átomo (principalmente carbono) unido a cuatro grupos diferentes. Si encuentras uno, la molécula es quiral y tendrá al menos un par de enantiómeros. Si hay múltiples centros quirales (n), calcula el número máximo potencial de estereoisómeros usando 2n. Recuerda estar atento a posibles compuestos meso que reducirían este número.
- Verifica los Dobles Enlaces: Para cada doble enlace carbono-carbono, asegúrate de que ambos carbonos del doble enlace tengan dos grupos diferentes unidos. Si es así, el doble enlace puede generar isómeros E/Z, que son diastereómeros.
- Examina las Estructuras Cíclicas: Para moléculas cíclicas, observa la posición de los sustituyentes en el anillo. Determina si están en el mismo lado (cis) o en lados opuestos (trans) del plano del anillo. Estos generarán isómeros cis/trans, que también son diastereómeros.
- Dibuja las Imágenes Especulares: Para confirmar la relación entre dos estereoisómeros (enantiómeros o diastereómeros) o para identificar compuestos meso, el método más seguro es dibujar la imagen especular de la molécula original y verificar si son superponibles. Si no lo son y son imágenes especulares, son enantiómeros. Si no son imágenes especulares y no son superponibles, son diastereómeros. Si son imágenes especulares y superponibles (a pesar de tener centros quirales), es un compuesto meso.
Preguntas Frecuentes (FAQs) sobre Estereoisómeros
¿Cómo se calcula el número de estereoisómeros?
El número máximo de estereoisómeros se calcula utilizando la fórmula 2n, donde 'n' es el número de centros estereogénicos (átomos quirales) en la molécula. Sin embargo, este número puede ser menor si la molécula posee elementos de simetría (como un plano de simetría interno) que den lugar a compuestos meso.

¿Cuál es la fórmula para calcular los estereoisómeros?
La fórmula principal es X = 2n, donde X es el número máximo de estereoisómeros posibles y n es el número de átomos estereogénicos (quirales) presentes en la molécula. Un ejemplo clásico es la glucosa, que tiene cuatro átomos estereogénicos y, por lo tanto, un máximo de 16 estereoisómeros posibles (24 = 16).
¿Cómo se encuentra el número real de estereoisómeros, considerando las excepciones?
Para encontrar el número real de estereoisómeros, primero se aplica la fórmula 2n para obtener el máximo. Luego, se debe identificar si la molécula puede formar compuestos meso. Un compuesto meso es aquiral a pesar de tener centros estereogénicos, debido a una simetría interna. Si se identifica un compuesto meso, este cuenta como un solo estereoisómero aquiral en lugar de un par de enantiómeros (RS y SR se vuelven idénticos). El método más seguro para identificar enantiómeros y compuestos meso es dibujar las imágenes especulares y verificar su superponibilidad.
¿Cómo se obtienen estereoisómeros en el laboratorio?
La obtención de estereoisómeros específicos en el laboratorio es un campo complejo y crucial de la química sintética. Se utilizan diversas técnicas, incluyendo la síntesis asimétrica (usando catalizadores quirales o auxiliares quirales para dirigir la formación de un estereoisómero específico), la resolución de mezclas racémicas (separación de enantiómeros de una mezcla 1:1) o la transformación de precursores con estereoquímica ya definida. Las fuentes clave de estereoquímica que se manipulan son los átomos quirales, los dobles enlaces (para isómeros E/Z) y las estructuras cíclicas (para isómeros cis/trans).
¿Es suficiente la presencia de un centro quiral para que una molécula sea quiral?
No, la presencia de un centro quiral no es siempre suficiente para que una molécula sea quiral. Un claro ejemplo son los compuestos meso, que, aunque contienen uno o más centros quirales, son globalmente aquirales debido a la presencia de un plano de simetría interno o un centro de inversión. La quiralidad de una molécula debe ser evaluada en su totalidad, comprobando si la molécula es superponible con su imagen especular.
¿Puede una molécula ser quiral sin tener un centro quiral?
Sí, absolutamente. Existen moléculas que son quirales debido a su arquitectura molecular, sin poseer un carbono unido a cuatro grupos diferentes. Un ejemplo destacado es el hexaheliceno, una molécula que adopta una forma helicoidal (espiral). Esta estructura en forma de hélice puede ser levógira o dextrógira, lo que la hace no superponible con su imagen especular y, por lo tanto, quiral, a pesar de no tener centros quirales tradicionales.
En resumen, el cálculo y la identificación de estereoisómeros son pilares fundamentales en la química orgánica. Comprender la regla 2n, sus excepciones como los compuestos meso, y las diversas fuentes de estereoquímica (átomos quirales, dobles enlaces, anillos) permite a los químicos predecir y manipular la estructura tridimensional de las moléculas con una precisión asombrosa. Esta capacidad no solo es vital para el avance de la ciencia, sino que también tiene implicaciones directas en nuestra vida diaria, desde la eficacia de los medicamentos hasta el desarrollo de nuevos materiales con propiedades específicas.
Si quieres conocer otros artículos parecidos a Cálculo de Estereoisómeros: Fórmula y Excepciones puedes visitar la categoría Química.
