17/09/2024
¿Alguna vez te has preguntado por qué algunas sustancias se mezclan perfectamente, como el azúcar en el agua, mientras que otras, como el aceite y el agua, se repelen formando capas distintivas? La respuesta a este intrigante fenómeno químico reside en una propiedad fundamental de las moléculas: la polaridad. Comprender la polaridad no solo es esencial para los químicos, sino que también nos ayuda a entender procesos cotidianos, desde la eficacia de un jabón hasta la función de biomoléculas en nuestro cuerpo. En este artículo, desglosaremos qué es la polaridad, cómo se determina en enlaces y moléculas, y por qué es tan crucial en el mundo que nos rodea.
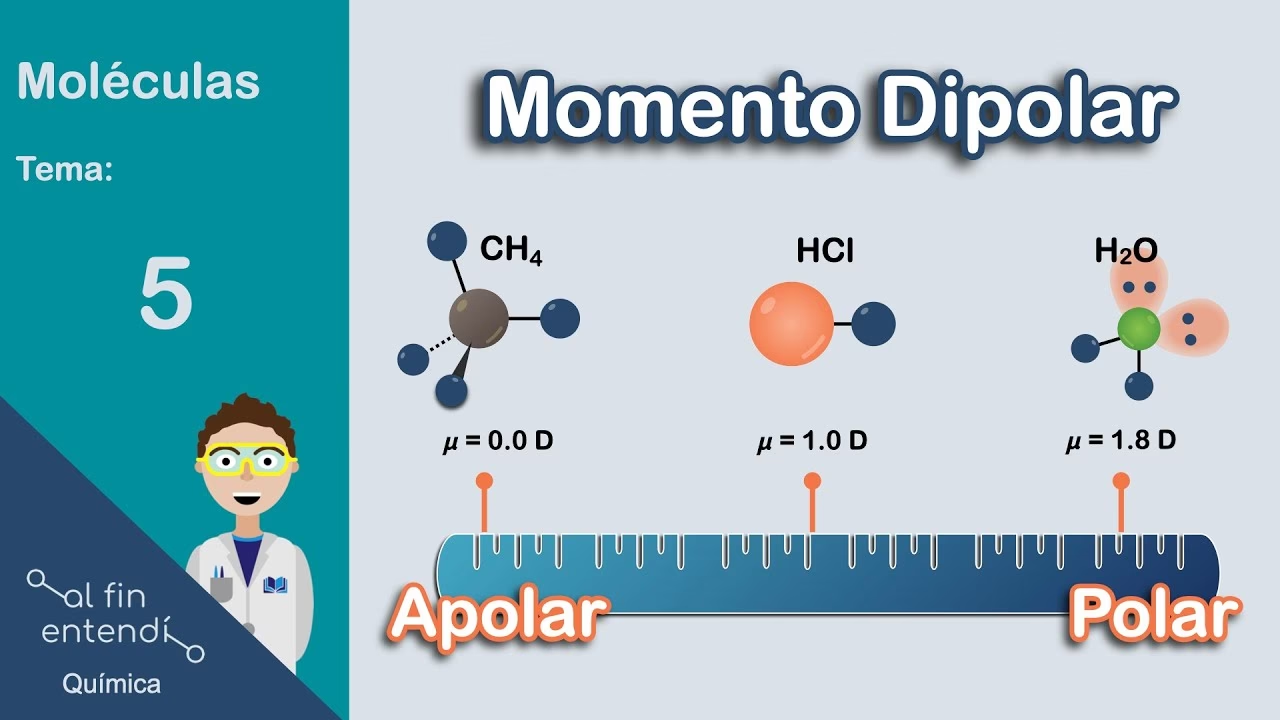
La polaridad es, en esencia, una medida de la distribución de carga eléctrica dentro de una molécula. Esta distribución desigual de electrones crea regiones con una ligera carga positiva y otras con una ligera carga negativa, convirtiendo a la molécula en una especie de pequeño imán. Pero, ¿cómo se origina esta desigualdad y qué factores la influencian? La clave está en los enlaces químicos que unen a los átomos y en la forma tridimensional de la molécula.
La Naturaleza de los Enlaces Covalentes: ¿Puros o Polares?
Para entender la polaridad molecular, primero debemos examinar los enlaces que la componen. Los enlaces covalentes se forman cuando dos átomos comparten uno o más pares de electrones. Sin embargo, la forma en que se comparten estos electrones no siempre es equitativa, y aquí es donde entra en juego la polaridad del enlace.
Enlaces Covalentes No Polares (o Puros)
Un enlace covalente se considera no polar (o puro) cuando los electrones compartidos se distribuyen de manera absolutamente igual entre los dos átomos enlazados. Esto ocurre generalmente cuando los dos átomos son idénticos, es decir, cuando la molécula es homonuclear diatómica. Pensemos en el gas hidrógeno (H₂), el oxígeno (O₂), el nitrógeno (N₂), o el cloro (Cl₂). En cada una de estas moléculas, ambos átomos tienen la misma capacidad para atraer los electrones del enlace, por lo que el par de electrones reside exactamente a medio camino entre los dos núcleos. No hay una separación de cargas neta, y, por lo tanto, el momento dipolar del enlace es cero.
Enlaces Covalentes Polares
Por otro lado, un enlace covalente es polar cuando los electrones del enlace no se comparten por igual entre los dos núcleos. Esta desigualdad surge cuando los átomos enlazados son diferentes y, crucialmente, tienen distintas electronegatividades. La electronegatividad es una propiedad fundamental de los átomos que mide su capacidad para atraer electrones hacia sí mismos dentro de un enlace químico. Cuanto mayor sea la electronegatividad de un átomo, más fuertemente atraerá los electrones compartidos.
Consideremos el enlace entre el hidrógeno (H) y el flúor (F) en la molécula de fluoruro de hidrógeno (HF). El flúor es significativamente más electronegativo que el hidrógeno. Como resultado, el par de electrones compartido se desplaza más hacia el átomo de flúor. Esto crea una pequeña carga parcial negativa (δ-) en el flúor y una pequeña carga parcial positiva (δ+) en el hidrógeno. Esta separación de cargas se conoce como un dipolo de enlace, y se representa a menudo con una flecha que apunta desde el átomo menos electronegativo hacia el más electronegativo. El momento dipolar (µ) de este enlace es diferente de cero, indicando su polaridad.
| Característica | Enlace Covalente No Polar | Enlace Covalente Polar |
|---|---|---|
| Compartición de Electrones | Igualitaria | Desigual |
| Diferencia de Electronegatividad | Cero o muy pequeña (< 0.4) | Significativa (0.4 - 1.7) |
| Átomos Involucrados | Generalmente idénticos | Generalmente diferentes |
| Momentos Dipolares de Enlace | Cero | Diferente de cero |
| Ejemplos | H₂, O₂, Cl₂, N₂ | HF, HCl, H₂O (enlace O-H) |
De la Polaridad del Enlace a la Polaridad Molecular: La Geometría es Clave
Aquí es donde las cosas se vuelven más interesantes y, a veces, un poco contraintuitivas. La presencia de enlaces polares dentro de una molécula NO implica necesariamente que la molécula en su conjunto sea polar. La polaridad molecular es el resultado de la suma vectorial de todos los momentos dipolares individuales de los enlaces y, crucialmente, de la geometría molecular.

El momento dipolar molecular (µ) es una medida cuantitativa de la polaridad de una molécula completa. Si el momento dipolar total es diferente de cero, la molécula es polar. Si es cero, la molécula es apolar. Para determinarlo, debemos considerar tanto la magnitud como la dirección de cada dipolo de enlace y cómo se orientan en el espacio tridimensional.
Casos de Estudio: Ejemplos Ilustrativos
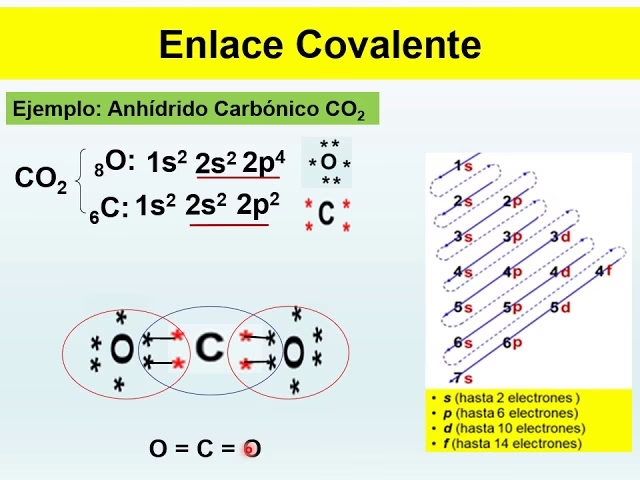
Dióxido de Carbono (CO₂)
Consideremos la molécula de dióxido de carbono (CO₂). Sabemos que el oxígeno es más electronegativo que el carbono, por lo que cada enlace C=O es polar, con un dipolo apuntando hacia cada átomo de oxígeno. Sin embargo, la molécula de CO₂ tiene una geometría lineal. Esto significa que los dos dipolos de enlace son de igual magnitud pero apuntan en direcciones exactamente opuestas (180 grados). Al sumarlos vectorialmente, se anulan mutuamente, dando como resultado un momento dipolar total de cero. Por lo tanto, a pesar de tener enlaces polares, la molécula de CO₂ es apolar.
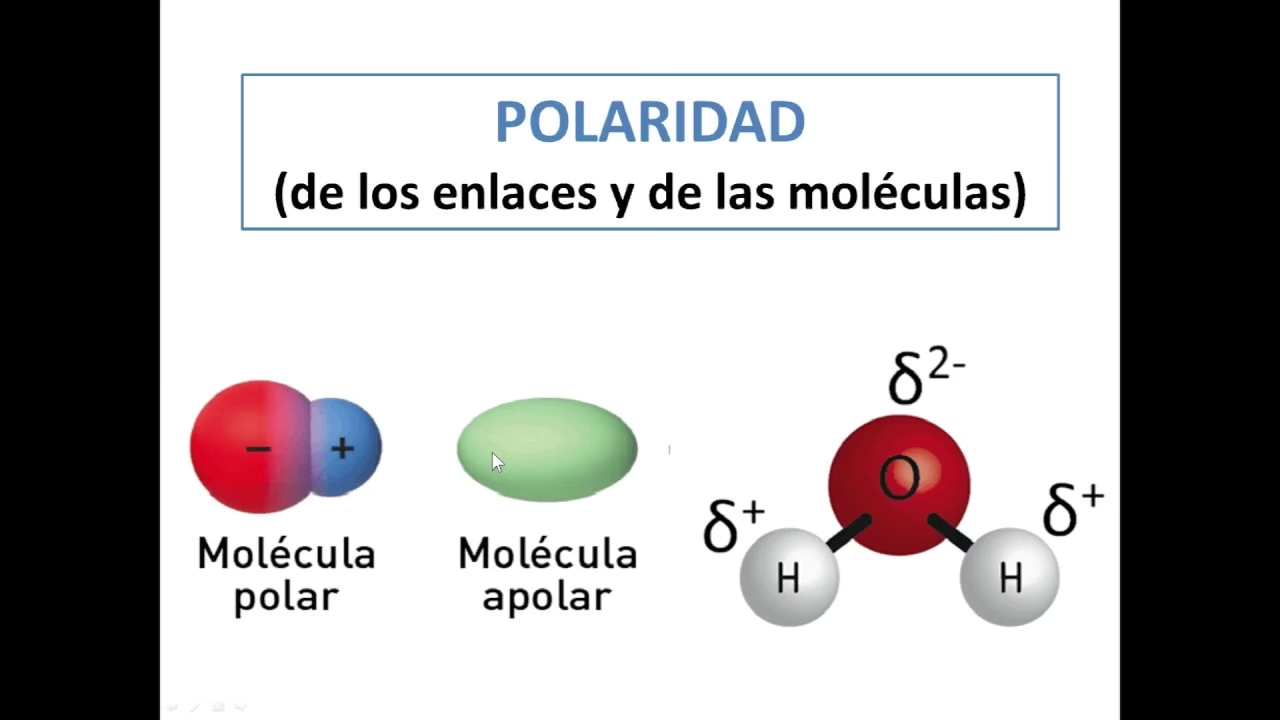
Agua (H₂O)
Ahora veamos la molécula de agua (H₂O). Al igual que en el CO₂, el oxígeno es más electronegativo que el hidrógeno, creando dipolos de enlace O-H que apuntan hacia el oxígeno. Sin embargo, la geometría del agua no es lineal; es angular (o doblada), debido a la presencia de pares de electrones no enlazantes en el átomo central de oxígeno. Debido a esta forma angular, los dos dipolos de enlace no se anulan. En cambio, se suman para producir un momento dipolar resultante significativo, haciendo que la molécula de agua sea altamente polar. Esta polaridad es la razón por la que el agua es un disolvente tan excepcional para muchas sustancias.
Metano (CH₄)
La molécula de metano (CH₄) presenta una geometría tetraédrica. El carbono es ligeramente más electronegativo que el hidrógeno, lo que significa que cada enlace C-H tiene un pequeño momento dipolar apuntando hacia el carbono. Sin embargo, debido a la perfecta simetría de la estructura tetraédrica, estos cuatro dipolos de enlace se distribuyen de tal manera que se anulan mutuamente. El resultado es un momento dipolar total de cero, lo que clasifica al metano como una molécula apolar.
Clorometano (CH₃Cl)
Si reemplazamos uno de los hidrógenos en el metano por un átomo de cloro, obtenemos clorometano (CH₃Cl). El cloro es mucho más electronegativo que el carbono y el hidrógeno. Aunque los enlaces C-H tienen pequeños dipolos y el enlace C-Cl tiene un dipolo grande, la sustitución de un átomo de hidrógeno por un átomo diferente como el cloro rompe la simetría perfecta de la molécula. Los vectores dipolares ya no se anulan entre sí, lo que resulta en un momento dipolar neto diferente de cero. Por lo tanto, el clorometano es una molécula polar.
En resumen, para determinar la polaridad de una molécula, sigue estos pasos:
- Identifica la polaridad de cada enlace individual basándote en la diferencia de electronegatividad entre los átomos.
- Determina la geometría molecular (lineal, angular, tetraédrica, etc.) utilizando la teoría VSEPR (Repulsión de Pares de Electrones de la Capa de Valencia).
- Suma vectorialmente los momentos dipolares de todos los enlaces. Si la suma neta es cero, la molécula es apolar. Si es diferente de cero, la molécula es polar.
| Molécula | Polaridad de Enlaces | Geometría Molecular | Suma de Dipolos | Polaridad Molecular |
|---|---|---|---|---|
| H₂ | No Polar | Lineal | Cero | Apolar |
| HF | Polar | Lineal | Diferente de Cero | Polar |
| CO₂ | Polar (C=O) | Lineal | Cero (se anulan) | Apolar |
| H₂O | Polar (O-H) | Angular | Diferente de Cero (no se anulan) | Polar |
| CH₄ | Ligeramente Polar (C-H) | Tetraédrica | Cero (por simetría) | Apolar |
| CH₃Cl | Polar (C-Cl, C-H) | Tetraédrica (asimétrica) | Diferente de Cero (no se anulan) | Polar |
La Importancia de la Polaridad: ¿Por Qué "Lo Semejante Disuelve a lo Semejante"?
La polaridad no es solo un concepto teórico; tiene profundas implicaciones prácticas, especialmente en el ámbito de la solubilidad. Una de las reglas empíricas más importantes en química es que "lo semejante disuelve a lo semejante". Esto significa que las sustancias polares tienden a disolverse o mezclarse bien con otras sustancias polares, mientras que las sustancias apolares se mezclan con sustancias apolares.
Volvamos al ejemplo del agua y el aceite. El agua es una molécula altamente polar. El aceite, por otro lado, está compuesto principalmente por moléculas de hidrocarburos, que son predominantemente apolares debido a la simetría de sus enlaces C-H y C-C. Cuando intentas mezclar agua y aceite, sus fuerzas intermoleculares son incompatibles. Las moléculas de agua se atraen fuertemente entre sí (a través de puentes de hidrógeno, una forma de interacción dipolar), y las moléculas de aceite se atraen entre sí (a través de fuerzas de dispersión de London). No hay una atracción significativa entre el agua y el aceite, lo que lleva a la formación de dos fases distintas.
Esta regla de "lo semejante disuelve a lo semejante" es fundamental para entender muchos procesos:
- Limpieza: Los jabones y detergentes son sustancias anfipáticas, lo que significa que tienen una parte polar (que interactúa con el agua) y una parte apolar (que interactúa con la grasa y el aceite). Esto les permite "disolver" la grasa y la suciedad en el agua.
- Biología: La estructura de las membranas celulares se basa en la polaridad. Los lípidos que las componen tienen cabezas polares que miran hacia el exterior (hacia el agua) y colas apolares que forman el interior hidrofóbico de la membrana.
- Medicina: La forma en que los medicamentos se disuelven y se transportan en el cuerpo, o cómo interactúan con las proteínas, a menudo depende de su polaridad.
- Industria: En la fabricación de pinturas, plásticos, adhesivos y muchos otros productos, la elección de los disolventes adecuados es crítica y se basa en la polaridad.
Preguntas Frecuentes sobre la Polaridad
A continuación, abordamos algunas de las preguntas más comunes sobre la polaridad de enlaces y moléculas:
¿Qué es la electronegatividad y por qué es tan importante para la polaridad?
La electronegatividad es la capacidad de un átomo para atraer hacia sí mismo los electrones de un enlace químico. Es crucial porque la diferencia en la electronegatividad entre dos átomos enlazados determina si el enlace será polar o no polar. Una gran diferencia implica un enlace polar, mientras que una diferencia nula o muy pequeña resulta en un enlace no polar.
¿Todas las moléculas con enlaces polares son polares?
No, esta es una confusión común. Como vimos con el CO₂ y el CH₄, una molécula puede tener enlaces polares pero ser apolar en su conjunto si la geometría molecular es simétrica y los momentos dipolares de los enlaces se anulan entre sí. La polaridad molecular depende de la suma vectorial de todos los dipolos de enlace.
¿Cómo influye la forma o geometría de la molécula en su polaridad?
La geometría molecular es tan importante como la polaridad de los enlaces. Si los dipolos de enlace se organizan de forma simétrica alrededor del átomo central (como en el CO₂ lineal o el CH₄ tetraédrico), se anulan y la molécula es apolar. Si la geometría es asimétrica (como el H₂O angular o el CH₃Cl tetraédrico asimétrico), los dipolos no se cancelan, y la molécula es polar.
¿Por qué es importante la polaridad en la vida cotidiana?
La polaridad explica por qué el agua disuelve la sal pero no el aceite, la base de cómo funcionan los jabones y detergentes, la forma en que se comportan las membranas biológicas en nuestros cuerpos, y cómo se diseñan muchos productos químicos y farmacéuticos para interactuar con su entorno o con sistemas biológicos específicos.
Conclusión
La polaridad es un concepto fundamental en química que une la estructura atómica con las propiedades macroscópicas de las sustancias. Desde los intrincados detalles de la compartición de electrones en un enlace hasta la forma tridimensional de una molécula, cada factor contribuye a determinar si una sustancia será polar o apolar. Entender esta propiedad no solo nos permite predecir cómo interactuarán diferentes sustancias, sino que también desvela los principios subyacentes a innumerables fenómenos naturales y aplicaciones tecnológicas. La próxima vez que veas el agua y el aceite separarse, recordarás que la polaridad es la invisible pero poderosa fuerza que dicta su comportamiento.
Si quieres conocer otros artículos parecidos a Polaridad: La Clave de Enlaces y Moléculas puedes visitar la categoría Química.