29/07/2022
El universo que nos rodea, desde la tierra que pisamos hasta los fluidos dentro de nuestro cuerpo, está intrínsecamente ligado a una propiedad química fundamental: la acidez o basicidad de las soluciones. Esta propiedad, crucial en campos tan diversos como la agricultura, la medicina, la industria alimentaria y la química en general, se mide comúnmente a través del pH. Sin embargo, existe una medida complementaria y igualmente importante, el pOH, que nos ofrece una visión completa del equilibrio iónico en las soluciones acuosas. Comprender cómo se relacionan y, más importante aún, cómo calcular el pOH, es una habilidad esencial para cualquiera que desee profundizar en la química de las soluciones.

Este artículo tiene como objetivo desglosar el concepto de pOH, explicando su definición, su relación con el pH y las fórmulas necesarias para su cálculo. A través de explicaciones claras, ejemplos prácticos y una estructura detallada, te guiaremos para que domines este aspecto crucial del equilibrio ácido-base, permitiéndote aplicar este conocimiento en diversos contextos.
¿Qué es el pOH y por qué es Importante?
Para entender el pOH, primero debemos recordar el concepto de pH. El pH (potencial de hidrógeno) es una escala logarítmica que mide la concentración de iones de hidrógeno (H+) en una solución acuosa. Esta escala va de 0 a 14, donde un pH menor a 7 indica una solución ácida, un pH mayor a 7 indica una solución básica (alcalina), y un pH de 7 representa una solución neutra, como el agua pura a 25°C. La relevancia del pH es inmensa: el pH del suelo afecta el crecimiento de los cultivos, el pH de la sangre humana debe mantenerse en un rango muy estrecho (7.35-7.45) para la supervivencia, y muchos procesos industriales dependen de un control preciso del pH.
El pOH, por otro lado, es una medida complementaria al pH. Mientras que el pH se centra en los iones H+, el pOH se enfoca en la concentración de iones hidróxido (OH-) en una solución. Al igual que el pH, el pOH también se expresa en una escala logarítmica de 0 a 14. Sin embargo, su interpretación es inversa a la del pH: un pOH bajo (cercano a 0) indica una alta concentración de iones OH-, lo que significa una solución fuertemente básica. Un pOH alto (cercano a 14) indica una baja concentración de iones OH-, lo que se traduce en una solución fuertemente ácida. Un pOH de 7, al igual que el pH de 7, corresponde a una solución neutra.
La importancia del pOH radica en su relación directa con el pH y en su utilidad para caracterizar soluciones básicas. En muchas situaciones, especialmente cuando se trabaja con bases fuertes, es más directo y conveniente calcular primero la concentración de iones OH- y, por ende, el pOH. Además, la relación entre pH y pOH es un pilar fundamental del equilibrio iónico en el agua y las soluciones acuosas.
La Relación Fundamental: pH + pOH = 14
Una de las relaciones más cruciales en el estudio del equilibrio ácido-base es la que existe entre el pH y el pOH. A una temperatura de 25°C, la suma de los valores de pH y pOH de cualquier solución acuosa siempre es igual a 14:
pH + pOH = 14
Esta relación no es arbitraria; deriva de la constante de ionización del agua (Kw). El agua pura tiene la capacidad de autoionizarse, es decir, de disociarse en pequeñas cantidades de iones H+ (o más precisamente, iones hidronio, H3O+) y iones OH-:
H₂O(l) ⇌ H⁺(aq) + OH⁻(aq)
La constante de equilibrio para esta reacción de autoionización se conoce como la constante del producto iónico del agua, Kw. A 25°C, el valor de Kw es:
Kw = [H+][OH-] = 1 x 10⁻¹⁴
Si aplicamos el logaritmo negativo a esta ecuación, obtenemos:
-log(Kw) = -log([H+][OH-])
-log(Kw) = -log[H+] + (-log[OH-])
Sabemos que -log[H+] es pH y -log[OH-] es pOH. Además, -log(1 x 10⁻¹⁴) es 14. Por lo tanto, esta derivación matemática confirma la relación fundamental:
14 = pH + pOH
Esta ecuación es increíblemente útil porque nos permite calcular el pOH si conocemos el pH, y viceversa. Si el pH de una solución es 3, su pOH será 11 (14 - 3 = 11). Si el pOH es 2, su pH será 12 (14 - 2 = 12).
Fórmulas para Calcular el pOH
Existen dos métodos principales para calcular el pOH de una solución, dependiendo de la información de partida que tengamos:
1. Cálculo del pOH a partir de la concentración de iones hidróxido [OH-]
La definición directa del pOH es el logaritmo negativo de la concentración molar de iones hidróxido (OH-) en la solución. La fórmula es la siguiente:
pOH = -log[OH-]
Donde [OH-] se expresa en moles por litro (M). Esta es la forma más fundamental de calcular el pOH.
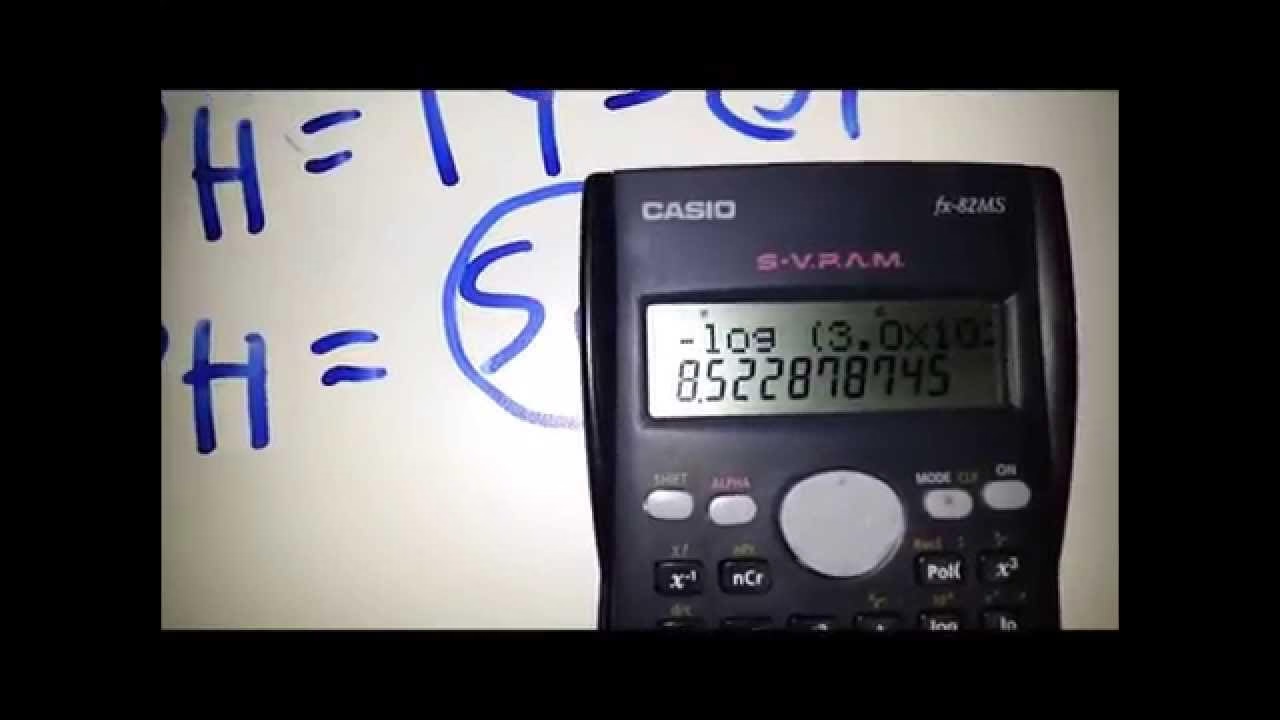
Ejemplo Práctico 1:
Supongamos que tenemos una solución de hidróxido de sodio (NaOH), una base fuerte que se disocia completamente en iones Na+ y OH-. Si la concentración de NaOH es 0.001 M, entonces la concentración de iones OH- también es 0.001 M (o 1 x 10⁻³ M).
- Aplicamos la fórmula: pOH = -log(1 x 10⁻³)
- Usando una calculadora científica, el resultado es: pOH = 3
Esto indica que la solución es básica, como era de esperar para una solución de hidróxido de sodio.
2. Cálculo del pOH a partir del pH
Como ya establecimos, la relación pH + pOH = 14 (a 25°C) es extremadamente útil. Si conocemos el pH de una solución, podemos despejar el pOH de la siguiente manera:
pOH = 14 - pH
Ejemplo Práctico 2:
Si sabemos que el pH de una muestra de jugo de naranja es 3.5.
- Aplicamos la fórmula: pOH = 14 - 3.5
- El resultado es: pOH = 10.5
Este pOH alto es consistente con una solución ácida (pH bajo).
La Importancia de la Temperatura
Es crucial recordar que la relación pH + pOH = 14 y el valor de Kw = 1 x 10⁻¹⁴ son válidos a una temperatura específica de 25°C. La autoionización del agua es un proceso endotérmico, lo que significa que a medida que la temperatura aumenta, la constante Kw también aumenta, lo que resulta en mayores concentraciones de H+ y OH- en agua pura. Esto, a su vez, afecta el punto de neutralidad y la suma de pH y pOH.
Por ejemplo, a 80°C, el Kw del agua es aproximadamente 4.9 x 10⁻¹⁴. Si calculamos el pH y pOH del agua pura a esta temperatura:
- [H+] = [OH-] = √(4.9 x 10⁻¹⁴) ≈ 2.2 x 10⁻⁷ M
- pH = -log(2.2 x 10⁻⁷) ≈ 6.66
- pOH = -log(2.2 x 10⁻⁷) ≈ 6.66
En este caso, pH + pOH = 6.66 + 6.66 = 13.32, que no es 14. Esto demuestra que la neutralidad (pH = pOH) se da a un valor diferente de 7 a otras temperaturas, y la suma de pH y pOH no es necesariamente 14. Sin embargo, en la mayoría de los problemas de química general y aplicaciones prácticas, se asume una temperatura de 25°C a menos que se especifique lo contrario.
Tabla Comparativa: pH vs. pOH
Para visualizar mejor la relación inversa entre pH y pOH, la siguiente tabla muestra valores correspondientes para diversas soluciones a 25°C:
| Tipo de Solución | pH | pOH | [H+] (M) | [OH-] (M) | Ejemplo |
|---|---|---|---|---|---|
| Fuertemente Ácida | 0 | 14 | 1.0 x 10⁰ | 1.0 x 10⁻¹⁴ | Ácido clorhídrico 1M |
| Ácida | 2 | 12 | 1.0 x 10⁻² | 1.0 x 10⁻¹² | Jugo de limón |
| Ligeramente Ácida | 6 | 8 | 1.0 x 10⁻⁶ | 1.0 x 10⁻⁸ | Leche |
| Neutra | 7 | 7 | 1.0 x 10⁻⁷ | 1.0 x 10⁻⁷ | Agua pura |
| Ligeramente Básica | 8 | 6 | 1.0 x 10⁻⁸ | 1.0 x 10⁻⁶ | Bicarbonato de sodio |
| Básica | 12 | 2 | 1.0 x 10⁻¹² | 1.0 x 10⁻² | Agua de cal |
| Fuertemente Básica | 14 | 0 | 1.0 x 10⁻¹⁴ | 1.0 x 10⁰ | Hidróxido de sodio 1M |
Esta tabla ilustra claramente cómo a medida que el pH disminuye (aumenta la acidez), el pOH aumenta (disminuye la basicidad), y viceversa. La suma de pH y pOH siempre se mantiene en 14 a 25°C.
Preguntas Frecuentes sobre pH y pOH
¿Cómo puedo calcular el pH en una calculadora científica?
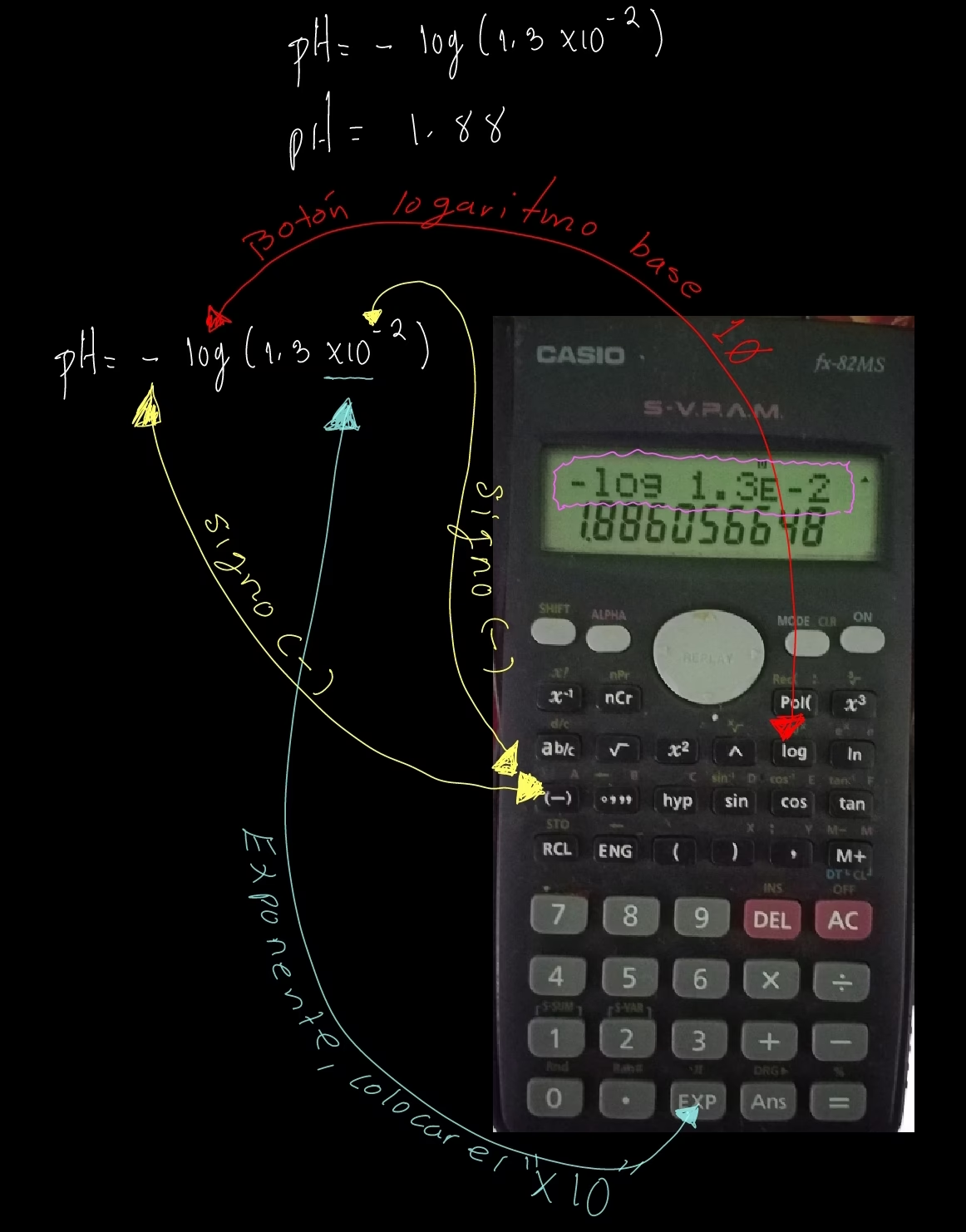
Para calcular el pH usando una calculadora científica, necesitas la concentración de iones de hidrógeno [H+]. La fórmula es pH = -log[H+]. Sigue estos pasos:
- Ingresa la concentración de iones [H+]. Por ejemplo, si [H+] = 1.0 x 10⁻⁵ M, ingresa `1.0E-5` o `1.0 * 10^ -5`.
- Presiona la tecla `log` (logaritmo base 10).
- El resultado será el logaritmo de [H+].
- Finalmente, cambia el signo a negativo (`+/-` o `neg`) para obtener el pH.
Algunas calculadoras requieren presionar `log` primero y luego el número. Asegúrate de conocer el orden de operación de tu calculadora.
¿Cómo se calcula el antilogaritmo en una calculadora científica?
El antilogaritmo (también conocido como 10^x o la función inversa del logaritmo) se utiliza para encontrar la concentración de [H+] o [OH-] a partir de un valor de pH o pOH. Si pH = -log[H+], entonces [H+] = 10^(-pH). De manera similar, si pOH = -log[OH-], entonces [OH-] = 10^(-pOH). Para calcular el antilogaritmo:
- Ingresa el valor del pH o pOH (con el signo negativo si estás yendo de pH a [H+] o de pOH a [OH-]).
- Busca la función `10^x` o `antilog` en tu calculadora. A menudo, se accede presionando `SHIFT` o `2nd F` seguido de la tecla `log`.
- El resultado será la concentración de iones (H+ o OH-).
Por ejemplo, si el pH es 4, [H+] = 10^(-4) = 0.0001 M.
¿Cuánto vale el pOH?
El valor del pOH no es fijo; varía dependiendo de la concentración de iones hidróxido (OH-) en una solución. Puede tomar cualquier valor en la escala de 0 a 14 a 25°C. Un pOH bajo (cercano a 0) indica una solución muy básica, mientras que un pOH alto (cercano a 14) indica una solución muy ácida. Por ejemplo, el pOH del agua pura es 7, el de una solución de amoníaco puede ser alrededor de 3, y el de una solución de ácido clorhídrico 1 M es 14. Su valor está directamente relacionado con el pH por la ecuación pOH = 14 - pH (a 25°C).
Conclusión
El pOH es una medida esencial que complementa al pH en la caracterización de la acidez o basicidad de una solución. Aunque a menudo el pH recibe más atención, el pOH es igualmente importante para comprender plenamente el equilibrio iónico y es particularmente útil cuando se trata de soluciones básicas o concentraciones de iones hidróxido.
Hemos explorado las definiciones clave, las fórmulas para calcular el pOH a partir de la concentración de OH- y, lo que es crucial, a partir del pH. La relación fundamental pH + pOH = 14 es la piedra angular de estos cálculos y se deriva directamente de la constante de ionización del agua (Kw). También hemos enfatizado la importancia de la temperatura, ya que la relación de 14 es específica para 25°C.
Dominar el cálculo del pOH y su interacción con el pH no solo mejora tu comprensión de la química, sino que también te equipa con herramientas prácticas para resolver problemas en diversos campos científicos y aplicaciones cotidianas. La capacidad de interpretar y calcular estas medidas es una habilidad valiosa que te permitirá analizar y predecir el comportamiento de las soluciones acuosas con mayor precisión.
Si quieres conocer otros artículos parecidos a Calcula el pOH: Guía Esencial de Equilibrio Iónico puedes visitar la categoría Química.
