07/11/2022
En el vasto y fascinante universo de la química, las sustancias se presentan en diversas formas, cada una con propiedades y composiciones únicas. Entre ellas, las sales hidratadas ocupan un lugar especial, constituyendo una categoría de compuestos que incorporan moléculas de agua en su estructura cristalina fundamental. Comprender la naturaleza de estas sales y, más importante aún, saber cómo cuantificar la cantidad de agua que contienen, es una habilidad esencial para químicos, estudiantes y entusiastas de la ciencia. Este conocimiento no solo nos permite caracterizar con precisión una sustancia, sino que también es crucial en procesos industriales, de investigación y de control de calidad.
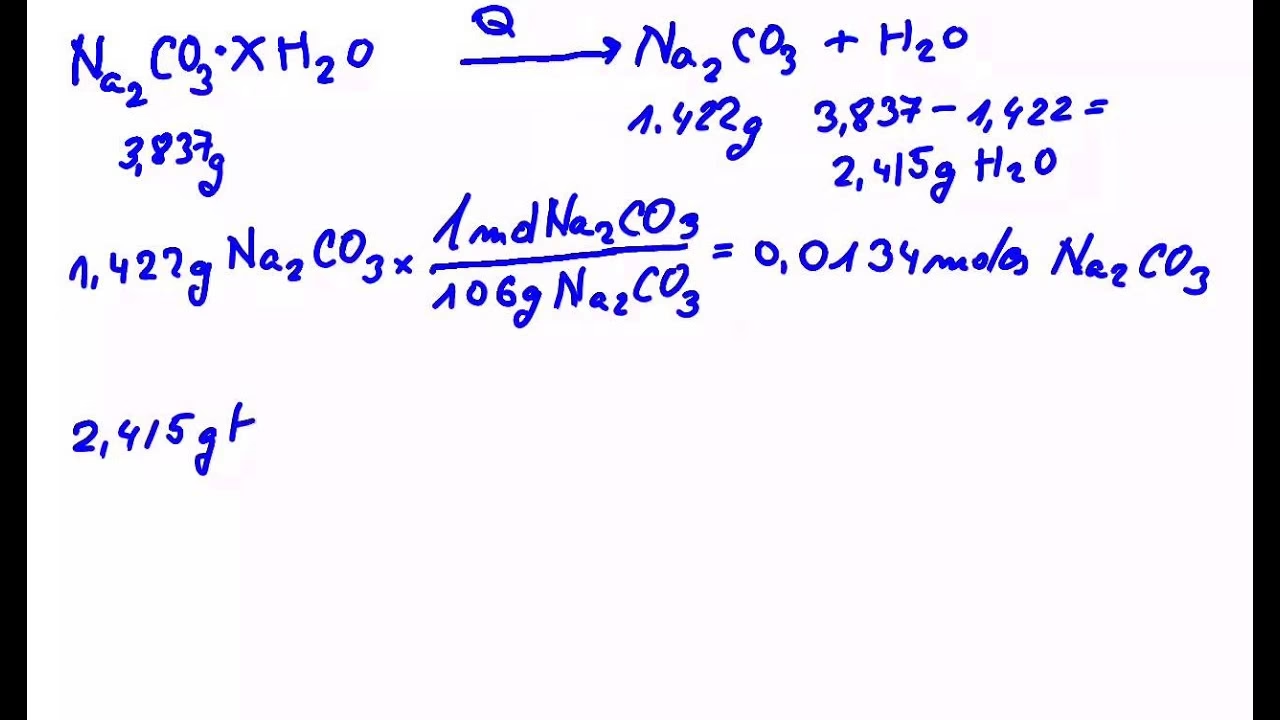
A lo largo de este artículo, exploraremos en profundidad qué son las sales hidratadas, por qué es tan relevante determinar su contenido de agua y, lo más importante, cómo podemos calcular de manera efectiva los moles de agua presentes en ellas. Abordaremos tanto los métodos experimentales como los cálculos teóricos, proporcionando ejemplos claros y detallados para desmitificar este proceso. Prepárese para sumergirse en el mundo de la estequiometría de los hidratos y descubrir cómo una balanza, un mechero y una calculadora pueden revelar los secretos de estos intrigantes compuestos.
- ¿Qué son las Sales Hidratadas?
- La Importancia de Cuantificar el Agua de Hidratación
- Conceptos Fundamentales: Masa Molar y Moles
- Determinación Experimental del Porcentaje de Agua en un Hidrato
- Cálculo Teórico del Porcentaje de Agua de Hidratación
- Cómo Encontrar los Moles de Agua en una Sal Hidratada (n)
- ¿Por qué es Crucial este Cálculo? Aplicaciones Prácticas
- Consideraciones Importantes y Errores Comunes
- Preguntas Frecuentes (FAQ)
¿Qué son las Sales Hidratadas?
Las sales hidratadas son compuestos iónicos que tienen moléculas de agua unidas químicamente a su estructura cristalina. A diferencia del agua de la humedad superficial, el agua en un hidrato está incorporada de una manera definida y estequiométrica, lo que significa que hay un número fijo de moléculas de agua por cada unidad de fórmula de la sal principal. Esta relación se indica en su fórmula química con un punto (•) seguido del número de moléculas de agua y la fórmula del agua (H₂O). La fórmula general de una sal hidratada es M·nH₂O, donde 'M' representa la sal anhidra (sin agua) y 'n' es el número entero de moléculas de agua asociadas a cada unidad de fórmula de la sal.
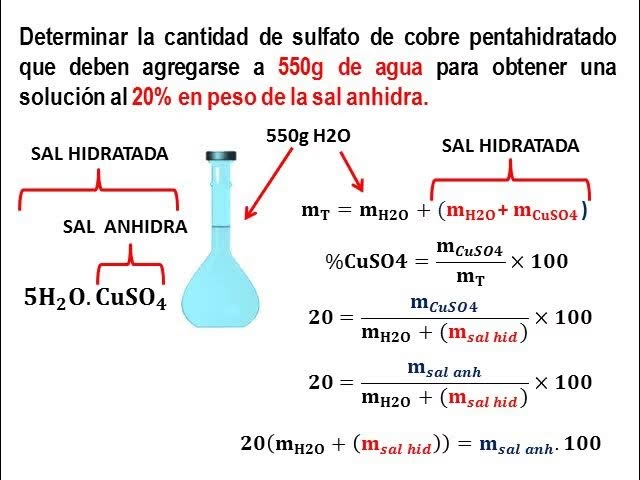
Por ejemplo, el sulfato de cobre(II) es un compuesto que comúnmente se encuentra en su forma hidratada, el sulfato de cobre(II) pentahidratado, cuya fórmula es CuSO₄•5H₂O. Esto significa que por cada unidad de sulfato de cobre (CuSO₄) hay cinco moléculas de agua. Otros ejemplos comunes incluyen:
- Sulfato de calcio dihidratado (yeso): CaSO₄•2H₂O
- Perclorato de litio trihidratado: LiClO₄•3H₂O
- Carbonato de magnesio pentahidratado: MgCO₃•5H₂O
- Cloruro de bario dihidratado: BaCl₂•2H₂O
Estas moléculas de agua, conocidas como "agua de hidratación" o "agua de cristalización", pueden ser eliminadas mediante calentamiento. Cuando todo el agua de hidratación se ha evaporado, el material restante se denomina anhidrato y es la sal pura sin agua.
La Importancia de Cuantificar el Agua de Hidratación
Determinar la cantidad de agua de hidratación en una sal es de vital importancia por varias razones. En primer lugar, afecta directamente la pureza y la masa molar de la sustancia. Una sal hidratada tiene una masa molar diferente a la de su forma anhidra debido a la masa adicional del agua. Esto es crucial en cálculos estequiométricos precisos, donde la cantidad exacta de una sustancia es fundamental para una reacción química o la preparación de una solución.
Además, en la industria farmacéutica y química, el contenido de agua en los hidratos puede influir en la estabilidad, solubilidad y reactividad de los compuestos. Un control de calidad riguroso requiere la verificación del porcentaje de agua para asegurar que el producto cumple con las especificaciones deseadas. Por ejemplo, si se compra una sal hidratada pensando que es anhidra, la cantidad de la sal 'activa' en el producto sería menor de lo esperado, lo que podría llevar a errores significativos en la dosificación o en la eficiencia de una reacción.
Conceptos Fundamentales: Masa Molar y Moles
Antes de sumergirnos en los cálculos, es esencial repasar dos conceptos fundamentales en química que son la piedra angular para comprender la cuantificación de moles de agua en sales hidratadas: la masa molar y los moles.
La Masa Molar: La Llave de Conversión
La masa molar es una propiedad física que define la masa de una sustancia por unidad de cantidad de sustancia, es decir, la masa de un mol de esa sustancia. Se expresa comúnmente en gramos por mol (g/mol). Para calcular la masa molar de un compuesto, simplemente se suman las masas atómicas de todos los átomos presentes en su fórmula química.
Por ejemplo, para el agua (H₂O):
- Masa atómica del Hidrógeno (H) = 1.008 g/mol
- Masa atómica del Oxígeno (O) = 15.999 g/mol
Entonces, la masa molar del agua (H₂O) = (2 × 1.008 g/mol) + (1 × 15.999 g/mol) = 2.016 g/mol + 15.999 g/mol = 18.015 g/mol.
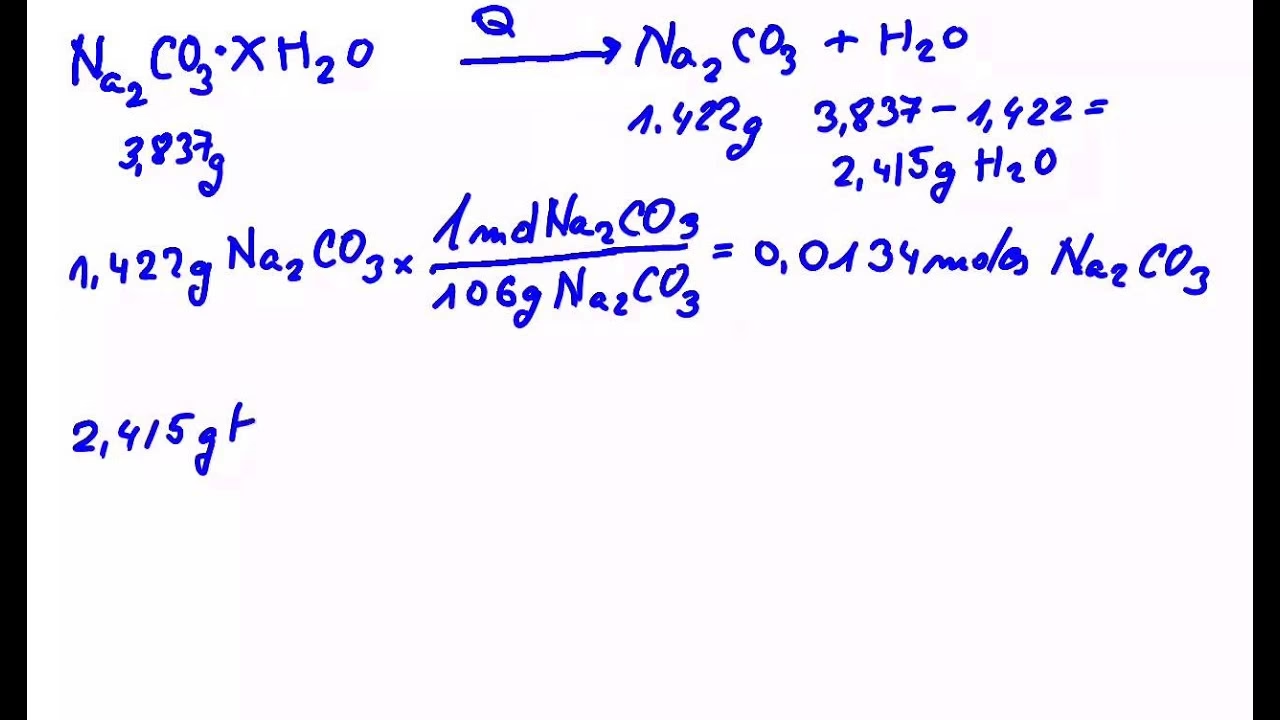
Este valor es fundamental porque nos permite convertir entre la masa de una sustancia y la cantidad de moles de esa sustancia.
Entendiendo los Moles: La Unidad del Químico
El mol es la unidad del Sistema Internacional (SI) para la cantidad de sustancia. Un mol de cualquier sustancia contiene exactamente 6.022 x 10²³ entidades elementales (átomos, moléculas, iones, etc.), un número conocido como el número de Avogadro. En términos prácticos, el mol nos proporciona una forma de contar partículas a escala microscópica, relacionándolas con una masa medible a escala macroscópica.
La relación entre masa (m), moles (n) y masa molar (M) se expresa mediante la fórmula: n = m / M. Esta ecuación es la base para todos los cálculos que realizaremos para determinar los moles de agua en una sal hidratada.
Determinación Experimental del Porcentaje de Agua en un Hidrato
Uno de los métodos más comunes y directos para determinar el porcentaje de agua de hidratación en una sal es el método gravimétrico, que implica calentar la muestra para eliminar el agua y medir la pérdida de masa.
El Proceso Experimental Detallado
El procedimiento experimental típico implica los siguientes pasos:
- Pesaje del crisol vacío: Se pesa un crisol limpio y seco (recipiente resistente al calor) con una balanza analítica de alta precisión.
- Pesaje de la muestra hidratada: Se añade una cantidad conocida de la sal hidratada al crisol y se pesa nuevamente para determinar la masa exacta de la muestra.
- Calentamiento de la muestra: El crisol con la muestra se calienta suavemente al principio y luego más intensamente, generalmente con un mechero Bunsen o en un horno. El objetivo es evaporar completamente el agua de hidratación sin descomponer la sal anhidra. Es crucial que todo el agua sea expulsada.
- Enfriamiento y pesaje: Una vez completado el calentamiento, el crisol se deja enfriar en un desecador (para evitar que la sal anhidra reabsorba humedad del aire) y luego se pesa de nuevo.
- Calentamiento y pesaje repetidos hasta masa constante: Para asegurar que toda el agua ha sido eliminada, se repiten los pasos de calentamiento, enfriamiento y pesaje hasta que dos pesadas consecutivas del crisol con el anhidrato muestren una diferencia mínima o nula (masa constante). Esto indica que ya no hay agua residual. El material restante es la sal anhidrato.
Cálculo del Porcentaje de Agua Perdida
Una vez obtenidas las masas, los cálculos son sencillos:
Ejemplo 1: Determinación Experimental del Porcentaje de Agua en CuSO₄•5H₂O
Supongamos que una muestra de 1.000 g de sulfato de cobre(II) pentahidratado (CuSO₄•5H₂O) fue calentada. La masa de la sal anhidra (CuSO₄) restante fue de 0.6390 g.
- Calcular la masa de agua perdida:
Masa de agua perdida = Masa inicial del hidrato - Masa del anhidrato
Masa de agua perdida = 1.000 g - 0.6390 g = 0.3610 g - Calcular el porcentaje de agua de hidratación:
Porcentaje de agua = (Masa de agua perdida / Masa inicial del hidrato) × 100
Porcentaje de agua = (0.3610 g / 1.000 g) × 100 = 36.10%
Este valor experimental nos da una idea del contenido de agua en la muestra específica que se analizó.
Cálculo Teórico del Porcentaje de Agua de Hidratación
Además del método experimental, podemos calcular el porcentaje de agua de forma teórica si conocemos la fórmula química exacta de la sal hidratada. Este cálculo se basa en las masas molares de la sal anhidra y del agua.
Ejemplo Teórico con CuSO₄•5H₂O
Para calcular el porcentaje teórico de agua en el sulfato de cobre(II) pentahidratado (CuSO₄•5H₂O):
- Calcular la masa molar de la sal anhidra (CuSO₄):
Cu: 1 × 63.55 g/mol = 63.55 g/mol
S: 1 × 32.07 g/mol = 32.07 g/mol
O: 4 × 16.00 g/mol = 64.00 g/mol
Masa molar de CuSO₄ = 63.55 + 32.07 + 64.00 = 159.62 g/mol - Calcular la masa molar del agua de hidratación (5H₂O):
Masa molar de H₂O = 18.015 g/mol
Masa de 5 moléculas de H₂O = 5 × 18.015 g/mol = 90.075 g/mol - Calcular la masa molar total del hidrato (CuSO₄•5H₂O):
Masa molar del hidrato = Masa molar de CuSO₄ + Masa de 5H₂O
Masa molar del hidrato = 159.62 g/mol + 90.075 g/mol = 249.695 g/mol - Calcular el porcentaje teórico de agua:
Porcentaje de agua = (Masa de agua en un mol de hidrato / Masa molar total del hidrato) × 100
Porcentaje de agua = (90.075 g/mol / 249.695 g/mol) × 100 = 36.07%
Comparación entre Valores Experimentales y Teóricos
Es común que exista una ligera diferencia entre el valor experimental y el valor teórico. Esta diferencia (a menudo expresada como porcentaje de error) puede deberse a errores en la medición, impurezas en la muestra, o un calentamiento incompleto o excesivo durante el experimento. La comparación nos ayuda a evaluar la precisión de nuestro experimento y la pureza de nuestra muestra.
| Característica | Cálculo Experimental | Cálculo Teórico |
|---|---|---|
| Fuente de datos | Mediciones de masa (hidrato y anhidrato) | Fórmula química y masas atómicas |
| Propósito | Determinar el porcentaje de agua en una muestra real; verificar pureza | Confirmar la fórmula de un hidrato; valor de referencia |
| Precisión | Depende de la exactitud de las mediciones y la experimentación | Alta, si la fórmula es correcta y las masas atómicas son precisas |
| Limitaciones | Requiere equipo; posibilidad de errores experimentales | Asume la identidad del hidrato y la pureza de la sustancia |
Cómo Encontrar los Moles de Agua en una Sal Hidratada (n)
El objetivo final de muchos experimentos con sales hidratadas es determinar el valor de 'n' en la fórmula M·nH₂O, es decir, el número de moles de agua asociados a cada mol de la sal anhidra. Este es el corazón de la pregunta sobre cómo encontrar los moles de agua en la sal hidratada. Para lograrlo, debemos combinar los conceptos de masa molar y moles con los datos obtenidos experimentalmente.
El Método para Determinar la Relación Molar
El principio es simple: una vez que hemos eliminado el agua y hemos medido las masas del hidrato y del anhidrato, podemos calcular los moles de agua que se perdieron y los moles de sal anhidra que quedaron. La relación entre estos dos valores nos dará el valor de 'n'.
Aquí están los pasos detallados para encontrar los moles de agua (y por ende, el valor de 'n'):
Paso 1: Determinar la masa de agua perdida.
Este es el primer paso y se obtiene directamente de la diferencia entre la masa inicial de la sal hidratada y la masa final de la sal anhidra.Masa de agua (g) = Masa de la sal hidratada (g) - Masa de la sal anhidra (g)Paso 2: Convertir la masa de agua a moles de agua.
Utilizando la masa molar del agua (aproximadamente 18.015 g/mol), convertimos la masa de agua perdida a moles.Moles de H₂O = Masa de agua (g) / Masa molar de H₂O (g/mol)Paso 3: Convertir la masa de la sal anhidra a moles de sal anhidra.
Necesitará la masa molar de la sal anhidra (por ejemplo, BaCl₂, CuSO₄, etc.), que se calcula sumando las masas atómicas de sus elementos. Luego, divida la masa de la sal anhidra obtenida experimentalmente por su masa molar.Moles de Sal Anhidra = Masa de sal anhidra (g) / Masa molar de Sal Anhidra (g/mol)Paso 4: Calcular la relación molar 'n'.
Finalmente, el valor de 'n' se obtiene dividiendo los moles de agua por los moles de la sal anhidra. Este valor debe ser un número entero o muy cercano a un entero, lo que le permitirá determinar la fórmula estequiométrica del hidrato.n = Moles de H₂O / Moles de Sal Anhidra
Ejemplo Práctico: Determinación de 'n' para BaCl₂•nH₂O
Consideremos un experimento donde se busca determinar la fórmula completa del cloruro de bario hidratado (BaCl₂•nH₂O).
- Datos experimentales obtenidos:
- Masa inicial de la muestra de BaCl₂•nH₂O (sal hidratada) = 3.250 g
- Masa de la sal anhidra (BaCl₂) después de calentar hasta masa constante = 2.770 g
Cálculos:
Determinar la masa de agua perdida:
Masa de H₂O = 3.250 g (hidrato) - 2.770 g (anhidrato)
Masa de H₂O = 0.480 gConvertir la masa de agua a moles de agua:
Sabemos que la masa molar de H₂O es 18.015 g/mol.
Moles de H₂O = 0.480 g / 18.015 g/mol
Moles de H₂O ≈ 0.02664 molConvertir la masa de la sal anhidra (BaCl₂) a moles de sal anhidra:
Primero, calculamos la masa molar de BaCl₂:
Masa atómica de Ba = 137.33 g/mol
Masa atómica de Cl = 35.45 g/mol
Masa molar de BaCl₂ = 137.33 + (2 × 35.45) = 137.33 + 70.90 = 208.23 g/molAhora, calculamos los moles de BaCl₂:
Moles de BaCl₂ = 2.770 g / 208.23 g/mol
Moles de BaCl₂ ≈ 0.01330 molCalcular la relación molar 'n':
n = Moles de H₂O / Moles de BaCl₂
n = 0.02664 mol / 0.01330 mol
n ≈ 2.003
Dado que 'n' debe ser un número entero, redondeamos 2.003 a 2. Por lo tanto, el número de moles de agua en la sal hidratada de cloruro de bario es 2, y la fórmula de la sal hidratada es BaCl₂•2H₂O (cloruro de bario dihidratado).

Este proceso sistemático le permitirá determinar la composición estequiométrica de cualquier sal hidratada, siempre y cuando se obtengan datos experimentales precisos.
¿Por qué es Crucial este Cálculo? Aplicaciones Prácticas
La capacidad de determinar con precisión los moles de agua en una sal hidratada, y por extensión su fórmula estequiométrica, tiene implicaciones significativas en diversas áreas:
- Control de Calidad: En la industria, es vital verificar que las materias primas o los productos finales hidratados contengan la cantidad correcta de agua, ya que esto afecta su peso, pureza, y a veces su funcionalidad.
- Investigación y Desarrollo: Los químicos que sintetizan nuevos compuestos a menudo necesitan caracterizar su composición exacta, incluyendo el grado de hidratación, para asegurar la reproducibilidad y la comprensión de sus propiedades.
- Educación: Este tipo de experimentos y cálculos son fundamentales en la enseñanza de la estequiometría y las habilidades de laboratorio, proporcionando una comprensión práctica de los conceptos teóricos.
- Almacenamiento y Formulación: Algunos hidratos son higroscópicos (absorben humedad del aire), lo que puede alterar su composición. Conocer su grado de hidratación inicial es crucial para su correcto almacenamiento y para formular productos con concentraciones precisas.
Consideraciones Importantes y Errores Comunes
Aunque el método experimental para determinar los moles de agua parece sencillo, hay varias consideraciones importantes y posibles fuentes de error que pueden afectar la precisión de los resultados:
- Calentamiento Incompleto: Si no se calienta la muestra el tiempo suficiente o a la temperatura adecuada, no se eliminará todo el agua de hidratación. Esto resultará en una masa de anhidrato incorrectamente alta y, por lo tanto, una masa de agua perdida incorrectamente baja, llevando a un valor de 'n' subestimado.
- Sobrecalentamiento y Descomposición de la Sal Anhidra: Un calentamiento excesivo o a una temperatura demasiado alta puede causar la descomposición de la sal anhidra misma, liberando otros gases además de agua. Esto llevaría a una masa de anhidrato incorrectamente baja y, por lo tanto, una masa de agua perdida incorrectamente alta, lo que resultaría en un valor de 'n' sobreestimado. Es crucial conocer el punto de descomposición de la sal.
- Reabsorción de Humedad (Higroscopia): Muchas sales anhidras son higroscópicas, lo que significa que absorben rápidamente la humedad del aire. Si el crisol no se enfría en un desecador y se pesa inmediatamente, la sal anhidra podría reabsorber agua, llevando a una masa final incorrecta y subestimando la masa de agua perdida.
- Impurezas en la Muestra: Si la muestra inicial de hidrato contiene impurezas no volátiles, la masa del anhidrato será mayor de lo esperado, afectando el cálculo de la masa de agua perdida.
- Precisión de la Balanza: Utilizar una balanza analítica calibrada y leer las masas con la mayor precisión posible es fundamental para obtener resultados exactos.
Preguntas Frecuentes (FAQ)
¿Qué es un anhidrato?
Un anhidrato es la forma de una sal o compuesto químico que no contiene agua de cristalización o de hidratación. Es el resultado de eliminar completamente el agua de una sal hidratada, generalmente mediante calentamiento.
¿La masa molar del agua es siempre 18.015 g/mol?
Para la mayoría de los cálculos químicos estándar, se utiliza el valor de 18.015 g/mol para la masa molar del agua (H₂O). Este valor se deriva de las masas atómicas promedio de hidrógeno (1.008 g/mol) y oxígeno (15.999 g/mol). Aunque existen isótopos con masas ligeramente diferentes, este valor es suficientemente preciso para la gran mayoría de las aplicaciones.
¿Todas las sales pueden formar hidratos?
No, no todas las sales forman hidratos. La capacidad de una sal para formar un hidrato depende de la naturaleza de los iones que la componen, su tamaño, carga y la forma en que se empaquetan en la red cristalina, lo que permite la incorporación de moléculas de agua en su estructura.
¿Qué significa el punto en la fórmula de una sal hidratada (M·nH₂O)?
El punto (•) en la fórmula de una sal hidratada, como en CuSO₄•5H₂O, indica que las moléculas de agua están unidas estequiométricamente a la sal principal dentro de la estructura cristalina, pero no forman enlaces covalentes directos con los átomos de la sal. Es una forma de representar la composición de un compuesto que incluye agua de cristalización.
¿Por qué es importante calentar hasta masa constante?
Calentar una muestra hasta masa constante es crucial en los experimentos de determinación de agua de hidratación porque asegura que toda el agua ha sido eliminada por completo. Si las pesadas consecutivas no coinciden, significa que aún queda agua o que la sal anhidra está perdiendo o ganando masa por otras razones (como descomposición o reabsorción de humedad), lo que invalidaría los cálculos.
En resumen, la capacidad de calcular los moles de agua en una sal hidratada es una habilidad fundamental en química. Ya sea a través de métodos experimentales meticulosos o de cálculos teóricos basados en la fórmula, la comprensión de la estequiometría de los hidratos nos permite caracterizar con precisión los materiales y garantizar la calidad en diversas aplicaciones. Esperamos que este artículo le haya proporcionado las herramientas y el conocimiento necesarios para desentrañar los secretos del agua de hidratación en las sales.
Si quieres conocer otros artículos parecidos a Desentrañando el Agua: Moles en Sales Hidratadas puedes visitar la categoría Química.
