26/04/2022
La fascinante danza de los átomos en el universo se rige por fuerzas y propiedades intrínsecas que determinan cómo interactúan entre sí. Una de las más cruciales, aunque a menudo malinterpretada por su nombre, es la electronegatividad. Lejos de ser un concepto negativo, este término fundamental en química nos revela la capacidad que tiene un átomo de atraer hacia sí los electrones de un enlace químico. Comprender la electronegatividad es abrir la puerta a la predicción del tipo de enlace que se formará entre dos átomos, un pilar esencial para entender la estructura y el comportamiento de toda la materia que nos rodea.
Desde la simple molécula de agua que bebemos hasta las complejas proteínas que nos forman, cada unión atómica tiene su naturaleza definida por esta propiedad. Pero, ¿cómo se mide? ¿Y cómo nos ayuda a distinguir entre un enlace donde los electrones se comparten equitativamente y uno donde son prácticamente transferidos? Acompáñenos en este viaje para desentrañar el significado de la electronegatividad, aprender a calcular su diferencia y, lo más importante, comprender cómo esta diferencia moldea el fascinante mundo de los enlaces químicos.
- ¿Qué es y en qué consiste medir la Electronegatividad?
- ¿Cómo se Establece la Diferencia de Electronegatividad?
- Factores que Influyen en la Electronegatividad: Más allá de las Tendencias Periódicas
- Importancia y Aplicaciones de la Electronegatividad
- Preguntas Frecuentes sobre la Electronegatividad
- Conclusión
¿Qué es y en qué consiste medir la Electronegatividad?
Como se mencionó, la electronegatividad es una medida de la tendencia relativa de un átomo en una molécula para atraer electrones hacia sí mismo cuando está involucrado en un enlace químico. No debe confundirse con la afinidad electrónica, que es la energía liberada o absorbida cuando un átomo aislado en estado gaseoso gana un electrón. La electronegatividad, en cambio, se refiere a la capacidad de atracción de electrones dentro del contexto de un enlace ya formado. Cuanto mayor es su valor, mayor es la capacidad de un átomo para atraer los electrones compartidos de un enlace.
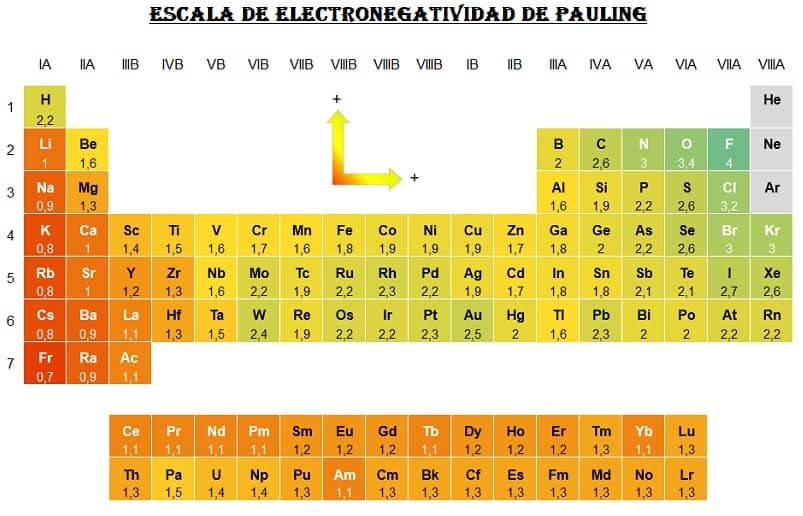
El concepto de electronegatividad fue introducido y popularizado por el renombrado químico Linus Pauling, quien desarrolló una escala numérica para cuantificar esta propiedad. La escala de Pauling es la más utilizada y se basa en datos termoquímicos, asignando un valor numérico a cada elemento. El flúor (F), el elemento más electronegativo, tiene un valor de 3.98 en esta escala, mientras que el francio (Fr) y el cesio (Cs), los elementos menos electronegativos, tienen valores de 0.7. Estos valores son adimensionales y sirven como una referencia relativa para comparar la capacidad de atracción electrónica entre diferentes átomos.
Tendencias Periódicas de la Electronegatividad
La electronegatividad no es una propiedad aleatoria; sigue patrones predecibles dentro de la tabla periódica. Comprender estas tendencias nos permite estimar la electronegatividad de un elemento sin necesidad de consultar una tabla de valores específicos:
- De izquierda a derecha en un período (fila): La electronegatividad aumenta. A medida que nos movemos de izquierda a derecha en una fila, el número de protones en el núcleo (carga nuclear) aumenta, mientras que los electrones se añaden al mismo nivel de energía (o capa de valencia). Esto significa que hay una mayor atracción del núcleo hacia los electrones de valencia, incluyendo los que formarán enlaces, sin un aumento significativo en el efecto de apantallamiento. Por lo tanto, los átomos tienen una mayor tendencia a atraer electrones.
- De arriba hacia abajo en un grupo (columna): La electronegatividad disminuye. Al descender en un grupo, el número de niveles de energía ocupados por electrones aumenta. Esto resulta en un mayor radio atómico y un efecto de apantallamiento más pronunciado (los electrones internos repelen a los electrones de valencia y los 'ocultan' de la atracción nuclear). Aunque la carga nuclear también aumenta, el aumento en la distancia y el apantallamiento superan este efecto, haciendo que la atracción del núcleo por los electrones de valencia y de enlace sea más débil.
Estas tendencias explican por qué los elementos no metálicos en la parte superior derecha de la tabla periódica (como el flúor, oxígeno y cloro) son altamente electronegativos, mientras que los metales alcalinos y alcalinotérreos en la parte inferior izquierda (como el cesio y el francio) son muy poco electronegativos.
¿Cómo se Establece la Diferencia de Electronegatividad?
La verdadera potencia de la electronegatividad reside no solo en su valor individual para cada átomo, sino en la diferencia de electronegatividad entre dos átomos que forman un enlace. Esta diferencia es el factor clave que nos permite predecir el tipo de enlace químico que se establecerá entre ellos.
Para calcular la diferencia de electronegatividad (ΔEN) entre dos átomos A y B, simplemente se toma el valor absoluto de la resta de sus electronegatividades en la escala de Pauling:
ΔEN = |Electronegatividad (A) - Electronegatividad (B)|
Por ejemplo, si queremos calcular la diferencia de electronegatividad entre el cloro (Cl) y el sodio (Na):
- Electronegatividad del Cl = 3.16
- Electronegatividad del Na = 0.93
- ΔEN = |3.16 - 0.93| = 2.23
Este valor, 2.23, es crucial para determinar el tipo de enlace. Generalmente, la química establece umbrales aproximados para clasificar los enlaces basándose en esta diferencia.
Clasificación de Enlaces Químicos según la Diferencia de Electronegatividad
La diferencia de electronegatividad es el criterio principal para distinguir entre los tres tipos fundamentales de enlaces químicos:
1. Enlace Covalente No Polar (o Puro)
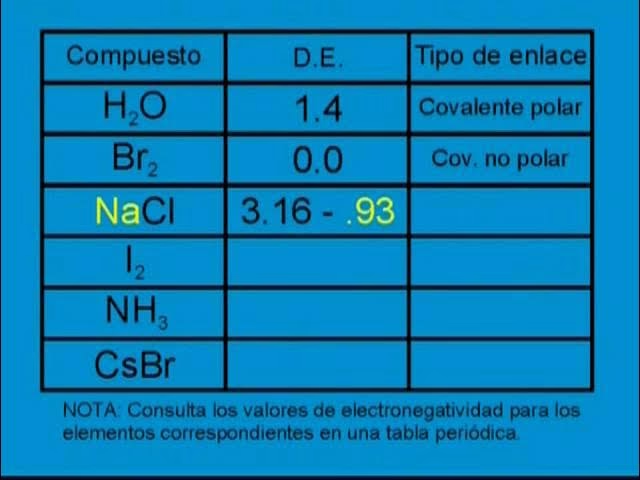
Este tipo de enlace se forma cuando dos átomos comparten los electrones de manera equitativa. Esto ocurre cuando los átomos tienen una electronegatividad muy similar o idéntica. La diferencia de electronegatividad (ΔEN) es muy pequeña, generalmente entre 0 y 0.4.
- Características: Los electrones de enlace pasan un tiempo igual alrededor de ambos núcleos. No se forman cargas parciales.
- Ejemplos: Moléculas diatómicas homonucleares como H₂ (ΔEN = |2.20 - 2.20| = 0), O₂ (ΔEN = |3.44 - 3.44| = 0), N₂ (ΔEN = |3.04 - 3.04| = 0), Cl₂ (ΔEN = |3.16 - 3.16| = 0). También puede ocurrir en enlaces carbono-hidrógeno (C-H) que tienen una ΔEN de aproximadamente 0.35, a menudo considerados no polares en muchos contextos.
2. Enlace Covalente Polar
Cuando la diferencia de electronegatividad entre dos átomos es apreciable pero no lo suficientemente grande como para que ocurra una transferencia completa de electrones, se forma un enlace covalente polar. En este caso, los electrones se comparten de manera desigual, siendo atraídos con mayor fuerza hacia el átomo más electronegativo. La diferencia de electronegatividad (ΔEN) suele estar en el rango de 0.5 a 1.7.
- Características: El átomo más electronegativo adquiere una carga parcial negativa (δ-), y el menos electronegativo adquiere una carga parcial positiva (δ+). Esto crea un dipolo en el enlace.
- Ejemplos: HCl (ΔEN = |3.16 - 2.20| = 0.96), H₂O (enlace O-H, ΔEN = |3.44 - 2.20| = 1.24), NH₃ (enlace N-H, ΔEN = |3.04 - 2.20| = 0.84).
3. Enlace Iónico
Un enlace iónico se forma cuando la diferencia de electronegatividad entre los dos átomos es muy grande, generalmente mayor de 1.7. En este escenario, el átomo más electronegativo tiene una atracción tan fuerte por los electrones que virtualmente los arranca del átomo menos electronegativo, resultando en una transferencia completa de uno o más electrones. Esto conduce a la formación de iones (átomos con carga neta) que se atraen electrostáticamente.
- Características: Formación de cationes (iones positivos) y aniones (iones negativos). La fuerza de atracción entre iones de carga opuesta es la que mantiene el compuesto unido.
- Ejemplos: NaCl (ΔEN = |3.16 - 0.93| = 2.23), KF (ΔEN = |3.98 - 0.82| = 3.16), LiF (ΔEN = |3.98 - 0.98| = 3.0).
Es importante destacar que estos umbrales son aproximados y que la transición entre los tipos de enlace es un continuo, no una división estricta. Un enlace con una ΔEN de 1.7 podría tener un carácter iónico considerable, pero aún conservar algunas propiedades covalentes.
Tabla Comparativa de Tipos de Enlace y Diferencia de Electronegatividad
Para resumir y visualizar mejor la relación entre la diferencia de electronegatividad y el tipo de enlace, presentamos la siguiente tabla:
| Tipo de Enlace | Rango de ΔEN (Aproximado) | Naturaleza de la Compartición de Electrones | Ejemplos Comunes |
|---|---|---|---|
| Covalente No Polar | 0 - 0.4 | Compartición equitativa | H₂, O₂, Cl₂, CH₄ |
| Covalente Polar | 0.5 - 1.7 | Compartición desigual, se forman dipolos | HCl, H₂O, NH₃, CO₂ |
| Iónico | > 1.7 | Transferencia completa de electrones | NaCl, KF, LiF, MgO |
Factores que Influyen en la Electronegatividad: Más allá de las Tendencias Periódicas
Si bien las tendencias periódicas nos dan una buena base para entender la electronegatividad, es importante señalar que esta propiedad no es absolutamente fija para un átomo. El "contexto" químico en el que se encuentra un átomo puede influir en su electronegatividad efectiva. Por ejemplo, la hibridación del orbital o el estado de oxidación de un átomo pueden afectar su capacidad para atraer electrones.
Un átomo en una molécula puede exhibir una electronegatividad ligeramente diferente dependiendo de los otros átomos a los que esté enlazado. Si un átomo está enlazado a uno muy electronegativo, su propia electronegatividad puede parecer un poco más alta de lo esperado, ya que los electrones son fuertemente retirados del átomo menos electronegativo, haciéndolo "más propenso" a atraer electrones adicionales de otras fuentes. Sin embargo, para propósitos generales y cálculos de tipo de enlace, los valores estándar de la escala de Pauling son suficientes y ampliamente utilizados.
Importancia y Aplicaciones de la Electronegatividad
La comprensión de la electronegatividad y su diferencia es fundamental en la química por varias razones:
- Predicción de Tipos de Enlace: Como hemos explorado, es la herramienta principal para determinar si un enlace será iónico, covalente polar o no polar.
- Polaridad Molecular: La polaridad de los enlaces dentro de una molécula influye directamente en la polaridad general de la molécula. Las moléculas polares tienen regiones con cargas parciales positivas y negativas, lo que afecta sus propiedades físicas como el punto de ebullición, la solubilidad y las interacciones intermoleculares. Por ejemplo, el agua es un disolvente excelente para muchas sustancias iónicas y polares precisamente por su alta polaridad.
- Reacciones Químicas: La electronegatividad puede predecir la reactividad de los elementos y la dirección de las reacciones. Los elementos altamente electronegativos tienden a ser oxidantes fuertes (aceptores de electrones), mientras que los poco electronegativos son reductores fuertes (donadores de electrones).
- Fuerzas Intermoleculares: La polaridad resultante de los enlaces covalentes polares da lugar a fuerzas intermoleculares como las interacciones dipolo-dipolo y los puentes de hidrógeno, que son cruciales para las propiedades de los líquidos y sólidos, y vitales en sistemas biológicos.
Preguntas Frecuentes sobre la Electronegatividad
¿Por qué el flúor es el elemento más electronegativo?
El flúor (F) es el elemento más electronegativo de la tabla periódica con un valor de 3.98 en la escala de Pauling. Esto se debe a una combinación de factores: su pequeño radio atómico y su alta carga nuclear efectiva. Al ser el elemento con el radio atómico más pequeño en su período y tener una alta carga nuclear sin un apantallamiento excesivo de electrones internos, el núcleo del flúor ejerce una atracción muy fuerte sobre los electrones de valencia y los electrones compartidos en un enlace. Solo necesita un electrón para completar su octeto, lo que lo hace extremadamente ávido de electrones.
¿La electronegatividad es una propiedad fija e inmutable?
Aunque los valores de electronegatividad en la escala de Pauling son útiles y ampliamente aceptados, es más preciso considerar la electronegatividad como una propiedad que puede variar ligeramente según el entorno químico del átomo. Factores como el estado de oxidación del átomo, su hibridación, y la naturaleza de los otros átomos a los que está enlazado pueden influir en su electronegatividad efectiva. Sin embargo, para la mayoría de los propósitos educativos y de predicción de enlaces, los valores tabulados de Pauling son lo suficientemente precisos y consistentes.
¿Cómo se relaciona la electronegatividad con el tamaño atómico?
Existe una relación inversa general entre la electronegatividad y el tamaño atómico. Los átomos más pequeños tienden a ser más electronegativos. Esto se debe a que en un átomo más pequeño, los electrones de valencia están más cerca del núcleo. Una menor distancia entre el núcleo cargado positivamente y los electrones de valencia cargados negativamente resulta en una mayor fuerza de atracción. Por el contrario, en átomos más grandes, los electrones de valencia están más alejados del núcleo y son más apantallados por los electrones internos, lo que disminuye la atracción del núcleo y, por lo tanto, reduce la electronegatividad.
¿La electronegatividad solo aplica a enlaces entre dos átomos?
El concepto de diferencia de electronegatividad se utiliza principalmente para analizar la polaridad de enlaces individuales entre dos átomos. Sin embargo, la electronegatividad de los átomos que componen una molécula poliatómica influye en la polaridad general de la molécula. Aunque un enlace individual pueda ser polar, la geometría de la molécula y la disposición de estos dipolos de enlace determinarán si la molécula en su conjunto es polar o no polar. Por ejemplo, el dióxido de carbono (CO₂) tiene enlaces C=O polares, pero la molécula es lineal y los dipolos se cancelan, resultando en una molécula no polar.
Conclusión
La electronegatividad es, sin duda, una de las propiedades más poderosas y reveladoras en el estudio de la química. Nos proporciona una lente a través de la cual podemos observar y predecir el comportamiento de los átomos cuando interactúan para formar moléculas. Desde la forma en que los elementos se posicionan en la tabla periódica hasta la fuerza con la que se atraen los electrones en un enlace químico, esta propiedad subyace a gran parte de lo que entendemos sobre la materia.
Al dominar el cálculo de la diferencia de electronegatividad, hemos desvelado la clave para clasificar los enlaces en iónicos, covalentes polares y no polares, un conocimiento que no solo es fundamental para los estudiantes de química, sino para cualquiera que desee apreciar la elegancia y la lógica inherente al mundo molecular. Recordar que los valores de Pauling son una guía y que el contexto puede influir ligeramente en esta propiedad, nos permite tener una comprensión más matizada. En última instancia, la electronegatividad es un testimonio de la simplicidad y la belleza de los principios fundamentales que rigen las uniones atómicas, el verdadero pegamento del universo.
Si quieres conocer otros artículos parecidos a Electronegatividad: Cálculo y Tipos de Enlace puedes visitar la categoría Química.
