26/12/2024
En el vasto universo de la física y la ingeniería, donde la materia se transforma y la energía fluye, pocos conceptos son tan fundamentales y a la vez tan intrigantes como el de la presión de saturación. Esta propiedad define el delicado punto de equilibrio dinámico entre una sustancia en su estado líquido y su estado gaseoso, o incluso entre un sólido y su vapor. Entenderla es crucial no solo para el diseño de tecnologías avanzadas, como las cámaras de vapor, sino también para comprender fenómenos tan cotidianos como la evaporación de un charco o la formación de la humedad en el aire.
A menudo, pensamos en la ebullición como el único camino hacia el vapor, pero la presión de saturación nos revela un proceso más sutil y constante: la coexistencia de fases. Cuando un líquido se encuentra a una temperatura específica, sus moléculas poseen una cierta energía cinética. Algunas de estas moléculas, las más energéticas, logran escapar de la superficie del líquido y pasar al estado gaseoso, creando vapor. Simultáneamente, algunas moléculas de vapor pierden energía y regresan al estado líquido. La presión de saturación es precisamente la presión que ejerce ese vapor cuando las velocidades de evaporación y condensación se igualan, creando un equilibrio donde la cantidad neta de líquido y vapor permanece constante, siempre y cuando ambas fases estén presentes.
- ¿Qué es la Presión de Saturación?
- Factores Clave que Influyen en la Presión de Saturación
- Presión de Saturación y Cámaras de Vapor: Un Vínculo Esencial
- Fenómenos de Capilaridad y Evaporación/Condensación
- Presión de Saturación en la Vida Cotidiana y sus Implicaciones
- Propiedades de Saturación del Agua
- Preguntas Frecuentes (FAQ)
- ¿Qué es la presión de saturación?
- ¿Cómo afecta la temperatura a la presión de saturación?
- ¿Influye la curvatura en la presión de saturación?
- ¿Puede un campo eléctrico modificar la presión de saturación?
- ¿Cuál es la temperatura de saturación del agua a 1 atmósfera?
- ¿Por qué es importante la presión de saturación en las cámaras de vapor?
- ¿Qué es el punto triple del agua?
- Conclusión
¿Qué es la Presión de Saturación?
La presión de saturación, también conocida como presión de vapor, es la presión a la cual, para una temperatura determinada, la fase líquida y la fase vapor de una sustancia pura se encuentran en equilibrio dinámico. Esto significa que las moléculas que abandonan la fase líquida para convertirse en vapor lo hacen a la misma velocidad que las moléculas de vapor que regresan a la fase líquida. Es un valor intrínseco de la sustancia a esa temperatura específica y es independiente de las cantidades relativas de líquido y vapor presentes, siempre y cuando ambas fases coexistan.
Este fenómeno no es exclusivo de los líquidos. Los sólidos también exhiben una presión de vapor a través de un proceso llamado sublimación, donde pasan directamente al estado gaseoso sin transitar por la fase líquida. En ambos casos, cuando se alcanza este equilibrio, las fases se denominan 'líquido saturado' y 'vapor saturado'.
La magnitud de la presión de saturación está inversamente relacionada con las fuerzas de atracción intermoleculares de la sustancia. Cuanto más fuertes sean estas fuerzas, mayor será la energía requerida para que las moléculas escapen de la fase condensada, y por lo tanto, menor será la presión de saturación a una temperatura dada. Por ejemplo, el agua, con sus fuertes enlaces de hidrógeno, tiene una presión de saturación relativamente baja en comparación con sustancias con fuerzas intermoleculares más débiles a la misma temperatura.
Imaginemos un recipiente sellado al vacío, manteniendo una temperatura constante. Si introducimos una pequeña cantidad de líquido, este comenzará a evaporarse rápidamente. A medida que la cantidad de vapor aumenta, la presión en el recipiente se eleva, y la velocidad de condensación también se incrementa. Eventualmente, ambas velocidades se igualan, y la presión dentro del recipiente alcanza su máximo valor posible para esa temperatura: la presión de saturación. Este equilibrio se logra más rápidamente si la superficie de contacto entre el líquido y el vapor es mayor, facilitando la evaporación, aunque la presión final de equilibrio será la misma.
El factor más determinante de la presión de saturación es la naturaleza química del líquido. En general, para líquidos de estructura similar, aquellos con mayor peso molecular suelen tener presiones de vapor más bajas a una temperatura dada, debido a fuerzas intermoleculares generalmente más fuertes.
Factores Clave que Influyen en la Presión de Saturación
Aunque la temperatura es el factor más obvio y conocido que influye en la presión de saturación (a mayor temperatura, mayor presión de saturación), existen otros elementos menos intuitivos pero igualmente importantes que pueden modificarla. Estos incluyen la curvatura de la interfaz líquido-vapor y, en ciertos contextos, la presencia de un campo eléctrico.

La Ecuación de Kelvin y el Efecto de Curvatura
La curvatura de una superficie líquido-vapor tiene un efecto notable sobre la presión de saturación. Este fenómeno es descrito por la ecuación de Kelvin, un principio fundamental en la termodinámica que explica por qué las gotas muy pequeñas se evaporan más fácilmente o por qué las burbujas muy pequeñas necesitan menos presión para formarse en un líquido.
La ecuación de Kelvin, en su forma simplificada para una gota de líquido en su propio vapor, nos dice que la presión de saturación sobre una superficie curva es diferente de la presión de saturación sobre una superficie plana (infinita). Para una gota de radio r, la presión de saturación p es mayor que la presión de saturación sobre una superficie plana p∞. Esto se debe a que las moléculas en la superficie curva de una gota pequeña tienen menos vecinos a los que unirse, lo que reduce las fuerzas intermoleculares que las retienen, facilitando su escape al vapor:
p = p∞ * exp( (2 * σ * vl) / (r * R * T) )
Donde σ es la tensión superficial, vl es el volumen específico del líquido, R es la constante de los gases y T es la temperatura. Esta ecuación muestra que a medida que el radio de la gota disminuye, la presión de saturación aumenta.
Por el contrario, para una burbuja de vapor sumergida en un líquido, la curvatura es negativa, y el efecto se invierte: la presión de saturación dentro de la burbuja disminuye a medida que su radio se hace más pequeño. Esto es crucial para entender la nucleación de burbujas y la ebullición, ya que una burbuja más pequeña requiere una presión de vapor menor para mantenerse en equilibrio.
El Impacto del Campo Eléctrico en la Presión de Saturación
Un factor menos convencional, pero de creciente interés en aplicaciones de alta tecnología, es el efecto de un campo eléctrico externo sobre la presión de saturación. Investigaciones han demostrado que la presencia de un campo eléctrico puede modificar la presión de saturación de un fluido de trabajo.
En general, un aumento en la intensidad del campo eléctrico puede incrementar la presión de saturación. Este efecto puede ser particularmente significativo cuando la fuerza del campo eléctrico supera un valor crítico, provocando un aumento notable en la presión de saturación. Este fenómeno tiene implicaciones fascinantes, por ejemplo, al intentar explicar cómo la presencia de campos eléctricos en las nubes (como los asociados a los rayos) podría influir en la lluvia, al afectar la evaporación y condensación del agua.
Para sistemas ingenieriles como las cámaras de vapor, un campo eléctrico lo suficientemente fuerte podría permitir el control eléctrico de los procesos de evaporación y condensación, abriendo nuevas vías para la gestión térmica de dispositivos electrónicos.
Presión de Saturación y Cámaras de Vapor: Un Vínculo Esencial
Las cámaras de vapor son dispositivos de transferencia de calor altamente eficientes, fundamentales en la refrigeración de componentes electrónicos de alto rendimiento, como CPUs y GPUs. Su funcionamiento se basa enteramente en los principios de evaporación y condensación, procesos que dependen críticamente de la presión de saturación.

Para que una cámara de vapor funcione correctamente, debe contener un fluido de trabajo puro, con una composición química homogénea e invariable. Este fluido es el que experimenta los cambios de fase. En la sección del evaporador, el calor de la fuente (por ejemplo, un chip) hace que el líquido se evapore, absorbiendo una gran cantidad de calor latente. El vapor resultante se mueve hacia el condensador, donde cede su calor latente al disipador de calor y se condensa de nuevo en líquido, completando el ciclo.
La eficiencia de este ciclo y la capacidad de transferencia de calor de la cámara de vapor están directamente ligadas a la diferencia de presiones y temperaturas de saturación entre el evaporador y el condensador. Una comprensión precisa de cómo la temperatura, la curvatura y, potencialmente, los campos eléctricos afectan la presión de saturación, permite optimizar el diseño y el rendimiento de estas cámaras.
Fenómenos de Capilaridad y Evaporación/Condensación
La curvatura no solo afecta la presión de saturación de gotas o burbujas aisladas, sino que también juega un papel crucial en fenómenos de capilaridad que ocurren en estructuras porosas, como las mechas de las cámaras de vapor o incluso en materiales cotidianos.
Consideremos una superficie con poros, como la mecha de una cámara de vapor. Cuando se añade calor, la evaporación hace que la interfaz líquido-vapor se retraiga hacia las esquinas o dentro de los poros, disminuyendo el radio del menisco. Debido a esta variación de la curvatura, la presión de saturación del fluido de trabajo se reduce localmente. Esta reducción de presión de saturación puede llevar a un ligero sobrecalentamiento del líquido a una temperatura de pared dada, lo que paradójicamente puede mejorar la transferencia de calor por evaporación. Este fenómeno se conoce como evaporación capilar.
De manera similar, en el proceso de condensación, una disminución del tamaño de los poros en la estructura de la mecha también puede mejorar la transferencia de calor por condensación. Esto explica por qué alimentos con estructuras porosas, como la avena, absorben fácilmente la humedad en ambientes húmedos (condensación capilar). La humedad relativa del aire, definida como la relación entre la presión parcial del vapor de agua y la presión de vapor saturado, también se ve afectada por la curvatura en los poros, lo que facilita la condensación en dichos materiales.
Presión de Saturación en la Vida Cotidiana y sus Implicaciones
Más allá de la ingeniería, la presión de saturación permea nuestra vida diaria y tiene implicaciones importantes:
- Humedad Relativa: La humedad relativa de la atmósfera se define como la relación entre la presión parcial del vapor de agua en el aire y la presión de saturación del agua a esa temperatura. Cuando la humedad relativa alcanza el 100%, el aire está saturado de vapor de agua, y el equilibrio dinámico significa que la evaporación neta cesa. Es por eso que la ropa no se seca en días muy húmedos, incluso si hace calor, a menos que haya un aporte extra de energía (como la radiación solar) que acelere la evaporación.
- Ollas a Presión: Un ejemplo práctico de cómo la presión afecta la temperatura de ebullición (y, por ende, la presión de saturación) son las ollas a presión. Al cocinar en una olla a presión, se eleva la presión dentro del recipiente, lo que a su vez eleva la temperatura de ebullición del agua por encima de los 100°C. Esto permite cocinar los alimentos más rápido.
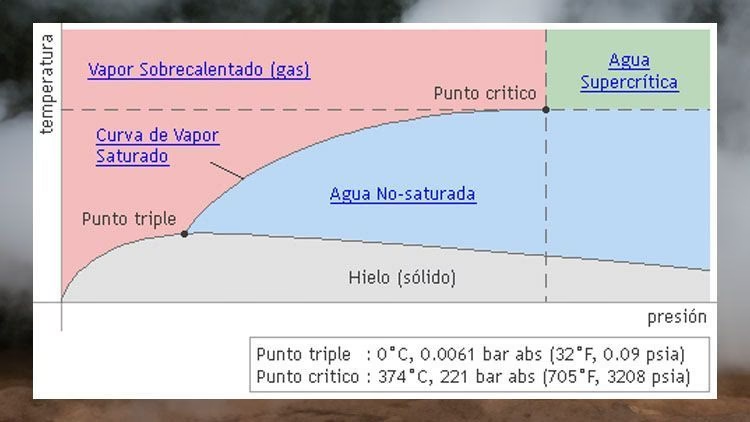
- El Punto Triple del Agua: Existe una presión y temperatura únicas (611.73 Pa y 273.16 K, o 0.01°C) donde el agua puede coexistir en sus tres fases: sólida (hielo), líquida y gaseosa (vapor) en equilibrio térmico. Este es el punto triple del agua, un punto de referencia fundamental en la termodinámica.
- Anomalía de la Densidad del Agua: Aunque no directamente la presión de saturación, está relacionada con las propiedades termodinámicas del agua. El agua es única porque su densidad máxima ocurre a 4°C, no a 0°C. Esta anomalía es vital para la vida acuática, ya que permite que los lagos se congelen desde la superficie hacia abajo, dejando el agua más densa (a 4°C) en el fondo, protegiendo la vida subacuática.
- Derecho Ambiental: En un contexto más amplio, la presión de vapor es un parámetro crucial para evaluar el riesgo de sustancias químicas. El Índice de Peligrosidad (Ip) de una sustancia se calcula a menudo como el cociente entre su presión de vapor y su Concentración Máxima Permitida (CMP) en condiciones estándar. Un Ip alto indica una mayor probabilidad de que la sustancia se volatilice, lo que es relevante para la seguridad y la regulación ambiental.
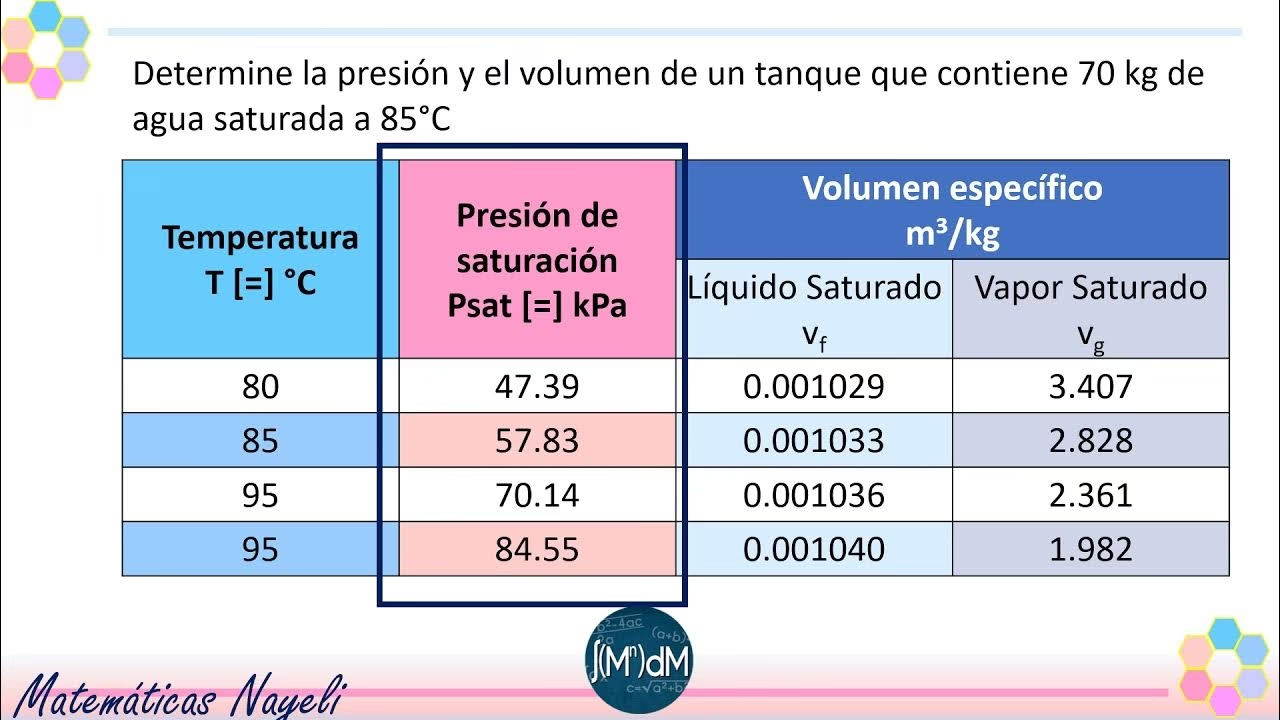
Propiedades de Saturación del Agua
El agua es la sustancia más estudiada en lo que respecta a sus propiedades de saturación debido a su omnipresencia en la naturaleza y la ingeniería. A continuación, se presenta una tabla que muestra la relación entre la presión de saturación y la temperatura para el agua, un ejemplo claro de cómo estas dos propiedades están intrínsecamente ligadas:
| Temperatura (°C) | Presión de Saturación (kPa) |
|---|---|
| 0 | 0.6105 |
| 5 | 0.8722 |
| 10 | 1.228 |
| 20 | 2.338 |
| 30 | 4.243 |
| 40 | 7.376 |
| 50 | 12.33 |
| 60 | 19.92 |
| 70 | 31.16 |
| 80 | 47.34 |
| 90 | 70.10 |
| 100 | 101.3 |
Esta tabla ilustra claramente que a medida que la temperatura del agua aumenta, su presión de saturación también se incrementa de forma no lineal, casi exponencial. A 100°C, la presión de saturación del agua es de aproximadamente 101.3 kPa, que es la presión atmosférica estándar a nivel del mar, explicando por qué el agua hierve a esta temperatura en condiciones normales.
Preguntas Frecuentes (FAQ)
¿Qué es la presión de saturación?
Es la presión a la cual un líquido y su vapor (o un sólido y su vapor) se encuentran en equilibrio dinámico a una temperatura dada. En este punto, la velocidad de evaporación (o sublimación) es igual a la velocidad de condensación (o deposición).
¿Cómo afecta la temperatura a la presión de saturación?
La temperatura es el factor más influyente. Generalmente, a medida que la temperatura de una sustancia aumenta, también lo hace su presión de saturación. Esto se debe a que más moléculas tienen suficiente energía para escapar de la fase líquida o sólida y formar vapor.
¿Influye la curvatura en la presión de saturación?
Sí, la curvatura de la interfaz líquido-vapor afecta la presión de saturación, según la ecuación de Kelvin. Para gotas muy pequeñas, la presión de saturación es mayor que sobre una superficie plana. Para burbujas de vapor en un líquido, la presión de saturación es menor a medida que el radio de la burbuja disminuye.
¿Puede un campo eléctrico modificar la presión de saturación?
Sí, estudios han demostrado que un campo eléctrico puede influir en la presión de saturación, generalmente aumentándola. Este efecto es más pronunciado a intensidades de campo eléctrico elevadas y tiene potencial para el control de la evaporación y condensación en aplicaciones tecnológicas.
¿Cuál es la temperatura de saturación del agua a 1 atmósfera?
A una presión atmosférica estándar de 101.3 kPa (aproximadamente 1 atmósfera), la temperatura de saturación del agua es de aproximadamente 99.98°C (o 373.13 K). Esta es la temperatura a la que el agua hierve a nivel del mar.
¿Por qué es importante la presión de saturación en las cámaras de vapor?
Es fundamental porque las cámaras de vapor operan mediante la evaporación y condensación de un fluido de trabajo. La presión de saturación determina las condiciones bajo las cuales estos cambios de fase ocurren, influyendo directamente en la eficiencia de la transferencia de calor del dispositivo.
¿Qué es el punto triple del agua?
El punto triple del agua es una combinación única de presión y temperatura (611.73 Pa y 0.01°C) donde el agua puede coexistir en sus tres fases: sólida, líquida y gaseosa, en equilibrio térmico.
Conclusión
La presión de saturación es un concepto de una riqueza y complejidad fascinantes, que va mucho más allá de una simple definición de equilibrio. Es el corazón de numerosos procesos naturales y tecnológicos, desde el ciclo del agua en la atmósfera hasta el funcionamiento de los sistemas de refrigeración más avanzados. Su dependencia de factores como la temperatura, la curvatura y el campo eléctrico revela la intrincada danza de las moléculas y la energía. Comprender la presión de saturación no solo nos equipa con herramientas para el análisis y diseño en ingeniería, sino que también nos permite apreciar la elegancia de los principios fundamentales que rigen el comportamiento de la materia en nuestro universo.
Si quieres conocer otros artículos parecidos a La Presión de Saturación: Un Concepto Esencial puedes visitar la categoría Física.

