18/11/2022
Desde la antigüedad, la humanidad se ha preguntado de qué está hecha la materia. A lo largo de los siglos, diversos pensadores y científicos propusieron modelos para describir la unidad fundamental, el átomo. Sin embargo, no fue hasta principios del siglo XX, con el avance de la física y la química, que se lograron avances significativos. El modelo atómico de Niels Bohr, propuesto en 1913, marcó un hito crucial en esta búsqueda, ofreciendo una explicación revolucionaria para la estabilidad de los átomos y la naturaleza de la luz emitida por ellos, sentando las bases para lo que hoy conocemos como la mecánica cuántica.
- El Átomo Antes de Bohr: Los Desafíos del Modelo de Rutherford
- Niels Bohr y la Cuantización de la Energía
- El Éxito Espectacular: Explicando el Espectro del Hidrógeno
- Cálculos Clave del Modelo de Bohr
- Limitaciones y la Evolución hacia la Mecánica Cuántica
- El Legado de Bohr
- Preguntas Frecuentes (FAQ)
- Conclusión
El Átomo Antes de Bohr: Los Desafíos del Modelo de Rutherford
Antes de Bohr, el modelo atómico predominante era el de Ernest Rutherford, propuesto en 1911. Rutherford había descubierto que el átomo consistía en un núcleo pequeño, denso y cargado positivamente, alrededor del cual los electrones, con carga negativa, giraban en órbitas, similar a un sistema planetario. Este modelo, conocido como el modelo planetario, fue un gran avance al demostrar que la mayor parte del átomo es espacio vacío y que la masa se concentra en el núcleo.
Sin embargo, el modelo de Rutherford enfrentaba dos problemas fundamentales que la física clásica no podía resolver:
- Estabilidad del Átomo: Según las leyes del electromagnetismo clásico, una carga eléctrica en movimiento acelerado (como un electrón girando en órbita) debería emitir continuamente energía en forma de radiación electromagnética. Al perder energía, el electrón debería spiralizarse hacia el núcleo y colapsar en una fracción de segundo. Esto implicaba que los átomos no podían ser estables, lo cual contradecía la evidencia experimental de la estabilidad de la materia.
- Espectros Discretos: Cuando los átomos de un gas son excitados (por ejemplo, al calentarlos o aplicar una descarga eléctrica), emiten luz. Esta luz, al pasar por un prisma, no produce un espectro continuo (como el arcoíris), sino un espectro de líneas discretas, es decir, solo se observan ciertas longitudes de onda de luz. El modelo de Rutherford no podía explicar por qué los átomos emitían solo frecuencias específicas de luz.
Estos desafíos indicaban que se necesitaba una nueva forma de entender el comportamiento de los electrones dentro del átomo, una que fuera más allá de las leyes de la física clásica.
Niels Bohr y la Cuantización de la Energía
Inspirado por las ideas de Max Planck sobre la cuantización de la energía (que la energía se emite o absorbe en paquetes discretos, o cuantos) y la explicación de Albert Einstein del efecto fotoeléctrico, Niels Bohr propuso su modelo atómico en 1913. Su genialidad residió en aplicar el concepto de cuantización a las órbitas de los electrones alrededor del núcleo. Bohr postuló que los electrones no podían ocupar cualquier órbita, sino solo ciertas órbitas específicas, cada una asociada con un nivel de energía fijo y discreto.
Para describir estas órbitas y el comportamiento de los electrones, Bohr formuló tres postulados fundamentales:
Primer Postulado: Las Órbitas Estables (Estacionarias)
El primer postulado de Bohr establece que los electrones describen órbitas circulares alrededor del núcleo del átomo sin irradiar energía. Esto significa que, a pesar de estar en movimiento acelerado, en estas órbitas específicas los electrones no pierden energía. Este postulado fue una ruptura radical con la física clásica y se introdujo para resolver el problema de la estabilidad atómica.
Para que el electrón se mantenga en una órbita circular, la fuerza de atracción electrostática (fuerza de Coulomb) entre el núcleo positivo y el electrón negativo debe ser igual a la fuerza centrípeta necesaria para el movimiento circular. Matemáticamente, esto se expresa como:
k * Z * e^2 / r^2 = m_e * v^2 / r
Donde:
kes la constante de Coulomb.Zes el número atómico (número de protones en el núcleo).ees la carga elemental del electrón.m_ees la masa del electrón.ves la velocidad del electrón en la órbita.res el radio de la órbita.
De esta ecuación, podemos despejar el radio: r = k * Z * e^2 / (m_e * v^2). La energía total del electrón en una órbita, que es la suma de su energía cinética y potencial, viene dada por: E = (1/2) * m_e * v^2 - k * Z * e^2 / r = -(1/2) * k * Z * e^2 / r. Esta expresión muestra que la energía de una órbita circular para el electrón está inversamente relacionada con su radio.
Segundo Postulado: La Cuantización del Momento Angular
Este postulado es el corazón de la cuantización en el modelo de Bohr. Establece que las únicas órbitas permitidas para un electrón son aquellas para las cuales su momento angular (L) es un múltiplo entero de la constante de Planck reducida (ℏ = h / (2π), donde h es la constante de Planck). Es decir:
L = m_e * v * r = n * ℏ
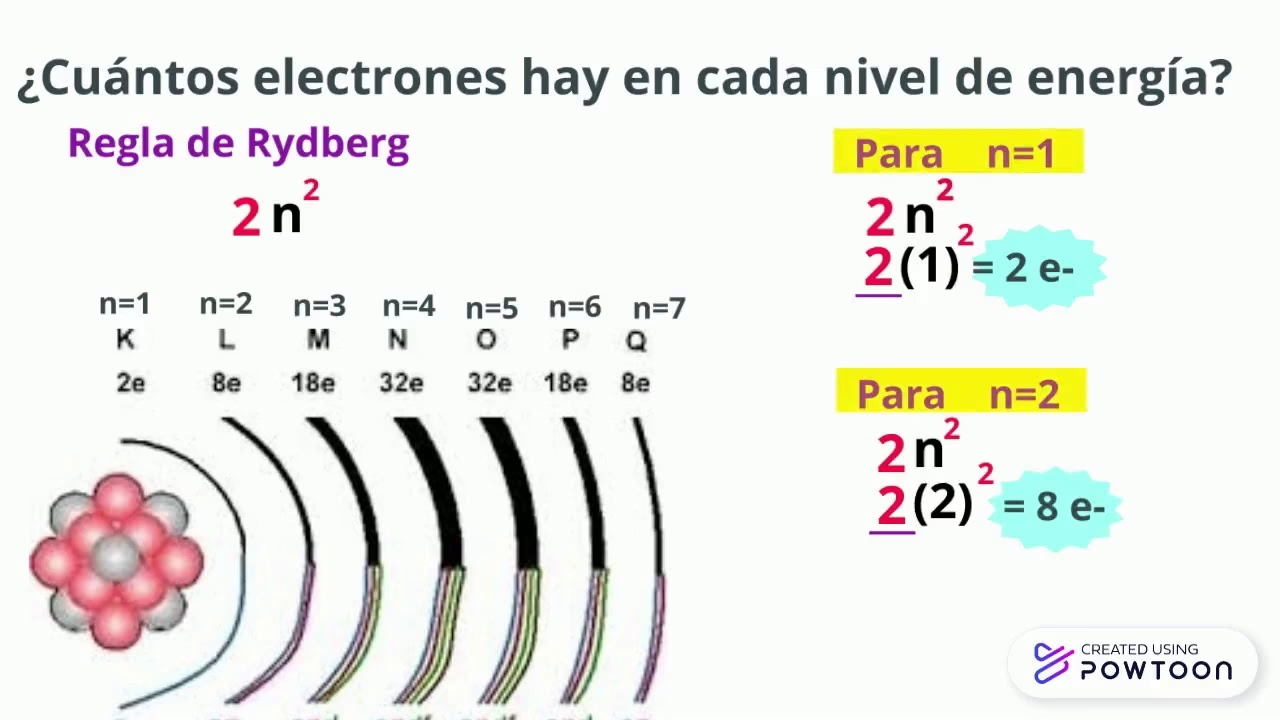
Aquí, n es un número entero positivo (n = 1, 2, 3, ...) conocido como el número cuántico principal. Este número identifica cada nivel de energía permitido. Originalmente, Bohr también se refería a estos niveles con letras (K, L, M, N, O, P, Q), donde K correspondía a n=1.
Al combinar este postulado con la expresión del radio del primer postulado, Bohr pudo derivar una fórmula para los radios de las órbitas permitidas:
r_n = (n^2 * ℏ^2) / (k * m_e * Z * e^2)
Esta ecuación revela que los radios de las órbitas no pueden tomar cualquier valor, sino que están cuantizados. El radio más pequeño permitido, para el átomo de hidrógeno (Z=1) y el primer nivel (n=1), se conoce como el radio de Bohr (a_0):
a_0 = ℏ^2 / (k * m_e * e^2) = 0.529 Å (ángstroms)
De manera análoga, al sustituir los radios permitidos en la expresión de la energía, se obtiene la energía correspondiente a cada nivel:
E_n = -(1/2) * (k^2 * m_e * Z^2 * e^4) / (n^2 * ℏ^2)
Para el átomo de hidrógeno (Z=1) y el primer nivel (n=1), la energía del estado fundamental (E_0) es:
E_0 = -(1/2) * (k^2 * m_e * e^4) / ℏ^2 = -13.6 eV (electronvoltios)
Así, la energía de cualquier nivel para cualquier átomo hidrogenoide (átomos con un solo electrón, como He+, Li2+, etc.) se puede expresar como: E_n = (Z^2 / n^2) * E_0.
Tercer Postulado: Transiciones Electrónicas y Espectros Atómicos
El tercer postulado aborda la emisión y absorción de energía. Bohr propuso que un electrón solo emite o absorbe energía cuando salta de una órbita permitida a otra. Si un electrón se mueve de una órbita de mayor energía (E_ni) a una de menor energía (E_nf), emite un fotón. Si absorbe energía, salta de una órbita de menor energía a una de mayor energía.
La energía del fotón emitido o absorbido es exactamente igual a la diferencia de energía entre los dos niveles, de acuerdo con la ley de Planck (E_gamma = h * nu):
E_gamma = h * nu = E_nf - E_ni
Donde nu es la frecuencia del fotón. A partir de esta relación y las fórmulas de energía, se puede derivar la frecuencia de los fotones emitidos o absorbidos:
nu = (k^2 * m_e * Z^2 * e^4) / (2 * h * ℏ^2) * (1/nf^2 - 1/ni^2)
O, en términos de la inversa de la longitud de onda (1/lambda, también conocida como número de onda, ν̄, donde c es la velocidad de la luz):
ν̄ = 1/lambda = (k^2 * m_e * Z^2 * e^4) / (2 * h * c * ℏ^2) * (1/nf^2 - 1/ni^2)
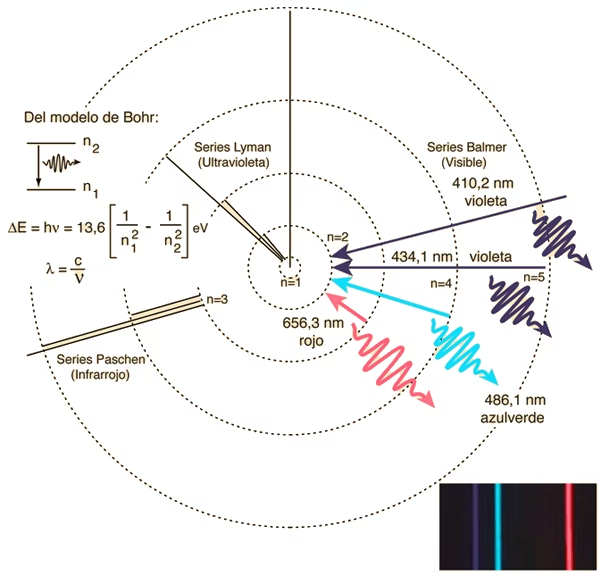
El Éxito Espectacular: Explicando el Espectro del Hidrógeno
El mayor triunfo del modelo de Bohr fue su capacidad para explicar con asombrosa precisión las líneas de emisión y absorción del espectro del átomo de hidrógeno. Durante décadas, los científicos habían observado estas líneas sin poder darles una explicación teórica. La fórmula empírica de Balmer (1885) ya describía las longitudes de onda de una serie de líneas en el espectro visible del hidrógeno:
1/lambda = R_H (1/2^2 - 1/n^2), con n = 3, 4, 5, ...
Donde R_H es la constante de Rydberg para el hidrógeno, un valor determinado experimentalmente. Bohr demostró que su ecuación teórica para la longitud de onda era idéntica a la fórmula de Balmer si el estado final (n_f) era igual a 2. Además, la constante teórica que él derivó para R_H (-E_1 / hc) coincidía casi perfectamente con el valor experimental conocido (1.097 * 10^7 m^-1).
Esta coincidencia no fue una mera casualidad; fue una verificación poderosa de que los postulados de Bohr capturaban una verdad fundamental sobre la estructura atómica. Por primera vez, una constante experimental como R_H pudo ser calculada a partir de constantes fundamentales de la naturaleza (masa y carga del electrón, constante de Planck, velocidad de la luz). El modelo de Bohr explicó que las líneas de la serie de Balmer corresponden a transiciones de electrones desde niveles de energía más altos (n=3, 4, 5, etc.) hacia el segundo nivel de energía (n=2). Del mismo modo, predijo otras series espectrales (como la serie de Lyman con n_f = 1 o la serie de Paschen con n_f = 3), que fueron posteriormente confirmadas experimentalmente.
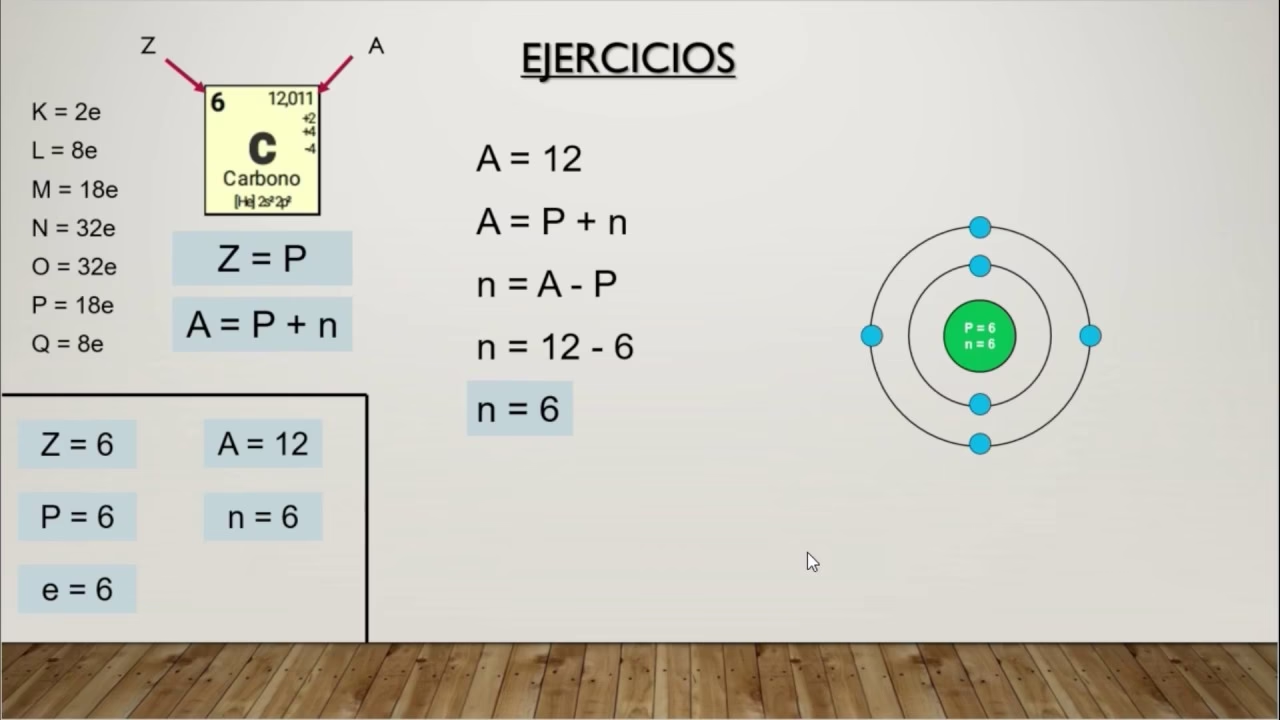
Cálculos Clave del Modelo de Bohr
Para resumir, las dos magnitudes más importantes que el modelo de Bohr permitió calcular con éxito para átomos hidrogenoides son:
| Magnitud | Fórmula General (para Z protones) | Fórmula para Hidrógeno (Z=1) | Valor para n=1 (Hidrógeno) |
|---|---|---|---|
Radio de Órbita (r_n) | r_n = (n^2 * ℏ^2) / (k * m_e * Z * e^2) | r_n = n^2 * a_0 | a_0 = 0.529 Å (Radio de Bohr) |
Energía de Órbita (E_n) | E_n = -(1/2) * (k^2 * m_e * Z^2 * e^4) / (n^2 * ℏ^2) | E_n = E_0 / n^2 | E_0 = -13.6 eV (Energía del estado fundamental) |
Donde n es el número cuántico principal (1, 2, 3...), Z es el número atómico, y las demás son constantes fundamentales.
Limitaciones y la Evolución hacia la Mecánica Cuántica
A pesar de su éxito rotundo en la explicación del átomo de hidrógeno, el modelo de Bohr presentaba varias limitaciones significativas:
- Átomos Multielectrónicos: El modelo de Bohr no pudo explicar con precisión los espectros de átomos con más de un electrón, como el helio o el sodio. La interacción compleja entre múltiples electrones y el núcleo no podía ser manejada por este modelo simple.
- Estructura Fina: El modelo no explicaba la "estructura fina" de las líneas espectrales, que son pequeñas divisiones en las líneas que se observan con instrumentos de mayor resolución.
- Efecto Zeeman y Stark: No podía explicar completamente el desdoblamiento de las líneas espectrales en presencia de campos magnéticos (efecto Zeeman) o eléctricos (efecto Stark) sin añadir supuestos ad hoc.
- Incompatibilidad con el Principio de Incertidumbre: El modelo de Bohr asume que los electrones tienen órbitas y velocidades bien definidas, lo cual contradice el principio de incertidumbre de Heisenberg, que establece que no se puede conocer simultáneamente con precisión la posición y el momento de una partícula.
- Momento Angular del Estado Fundamental: El modelo de Bohr predice un momento angular no nulo para el estado fundamental (n=1), lo cual es incompatible con la mecánica cuántica moderna, que predice un momento angular cero para los orbitales s.
Estas limitaciones llevaron a la necesidad de refinamientos y, eventualmente, a un modelo atómico completamente nuevo. Arnold Sommerfeld, en el modelo de Bohr-Sommerfeld, introdujo órbitas elípticas y un segundo número cuántico para explicar la estructura fina. Sin embargo, este modelo también era fundamentalmente inconsistente y no resolvía todas las paradojas.
Finalmente, el modelo de Bohr fue suplantado por la mecánica cuántica moderna, desarrollada por físicos como Erwin Schrödinger (con su ecuación de onda) y Werner Heisenberg (con la mecánica de matrices). El modelo cuántico-mecánico no describe los electrones en órbitas definidas, sino en "orbitales" o regiones de probabilidad donde es más probable encontrar un electrón, representadas como una "nube de electrones". Este modelo, aunque más abstracto, ha demostrado ser extraordinariamente exitoso para describir el comportamiento de los átomos y las moléculas con una precisión sin precedentes.
El Legado de Bohr
A pesar de sus limitaciones, el modelo de Bohr fue un paso gigantesco en la comprensión de la estructura atómica. Fue el primer modelo que introdujo con éxito la idea de la cuantización de los niveles de energía y el momento angular, explicando la estabilidad atómica y el origen de los espectros discretos. Actuó como un puente crucial entre la física clásica y la mecánica cuántica, abriendo el camino para el desarrollo de la teoría cuántica completa. Su simplicidad conceptual lo hace aún hoy una herramienta pedagógica valiosa para introducir los conceptos de cuantización en la física atómica.
Preguntas Frecuentes (FAQ)
¿Cómo se define 'n' en el modelo de Bohr?
En el modelo de Bohr, 'n' se define como el número cuántico principal. Es un número entero positivo (1, 2, 3, y así sucesivamente) que identifica cada una de las órbitas o niveles de energía permitidos para el electrón alrededor del núcleo. Un valor de 'n' más alto indica una órbita más grande y con mayor energía, más alejada del núcleo.
¿Qué es el radio de Bohr?
El radio de Bohr (a_0) es el radio de la órbita más pequeña permitida para un electrón en un átomo de hidrógeno, es decir, cuando el número cuántico principal n=1. Su valor es aproximadamente 0.529 ángstroms (0.529 * 10^-10 metros). Es una constante fundamental en física atómica que representa la distancia promedio del electrón al núcleo en el estado fundamental del hidrógeno.
¿Por qué el modelo de Bohr no es el modelo atómico actual?
Aunque fue un avance fundamental, el modelo de Bohr fue superado porque no podía explicar fenómenos más complejos, como los espectros de átomos con múltiples electrones, la estructura fina de las líneas espectrales, o el comportamiento de los átomos en campos magnéticos o eléctricos intensos. Además, su concepto de órbitas definidas para los electrones contradecía el principio de incertidumbre de Heisenberg, que es una piedra angular de la mecánica cuántica moderna. El modelo actual, basado en la mecánica cuántica, describe los electrones mediante funciones de onda y regiones de probabilidad (orbitales).
¿Pudo el modelo de Bohr explicar todos los átomos?
No, el modelo de Bohr fue extraordinariamente exitoso para explicar el átomo de hidrógeno y otros sistemas "hidrogenoides" (iones con un solo electrón, como He+ o Li2+). Sin embargo, fracasó al intentar describir con precisión átomos con dos o más electrones, como el helio (dos electrones) o el sodio (once electrones), debido a las complejas interacciones electrón-electrón que no podía considerar.
¿Cuál fue el mayor éxito del modelo de Bohr?
El mayor éxito del modelo de Bohr fue su capacidad para explicar teóricamente el espectro de emisión y absorción del átomo de hidrógeno. Pudo derivar y validar la fórmula empírica de Balmer para las líneas espectrales del hidrógeno, demostrando que la constante de Rydberg, previamente solo conocida por experimentación, podía calcularse a partir de constantes fundamentales. Esto proporcionó una poderosa evidencia de la cuantización de los niveles de energía atómicos.
Conclusión
El modelo atómico de Bohr, con sus postulados audaces sobre la cuantización de las órbitas y la energía, fue una pieza clave en el rompecabezas de la física del siglo XX. Aunque posteriormente fue superado por la mecánica cuántica más completa, su contribución a nuestra comprensión del átomo es innegable. Nos enseñó que la energía en el mundo atómico no es continua, sino que existe en paquetes discretos, y que los electrones ocupan niveles de energía específicos. Este concepto de cuantización sigue siendo central en la física moderna y es la base de tecnologías que van desde los láseres hasta la resonancia magnética nuclear.
Si quieres conocer otros artículos parecidos a El Modelo Atómico de Bohr: Un Puente a la Cuántica puedes visitar la categoría Física.
