23/12/2025
Cuando dos cuerpos con temperaturas diferentes entran en contacto, se inicia un proceso fascinante y fundamental en la naturaleza: el flujo de calor. Este intercambio energético no se detiene hasta que ambos cuerpos alcanzan la misma temperatura, un estado que conocemos como equilibrio térmico. En este punto, el flujo neto de calor se detiene, y el sistema ha alcanzado su balance energético. Este fenómeno no solo es una curiosidad científica, sino que es la base de innumerables procesos cotidianos y aplicaciones tecnológicas, desde el funcionamiento de un termómetro hasta la climatización de edificios o la preparación de alimentos. Comprender cómo se llega a este equilibrio y, más importante aún, cómo podemos predecir la temperatura final, es clave para entender gran parte del mundo que nos rodea.
La intuición nos dice que el objeto más caliente cederá energía al más frío. Esta transferencia de energía, que llamamos calor, siempre ocurre de la región de mayor temperatura a la de menor temperatura. Piénselo como un río que fluye cuesta abajo, nunca al revés, a menos que se aplique una fuerza externa. Este flujo continúa hasta que no hay más 'cuestas' de temperatura que descender, es decir, hasta que las temperaturas se igualan. En ese momento, aunque las partículas de ambos cuerpos siguen moviéndose y chocando, el intercambio neto de energía se anula, y el sistema ha alcanzado su estado de equilibrio. Este concepto es fundamental en la termodinámica y nos permite predecir el comportamiento de sistemas térmicos complejos.
La Ciencia Detrás del Cálculo: ¿Cómo Predecimos la Temperatura Final?
Predecir la temperatura de equilibrio entre dos cuerpos no es solo una cuestión de adivinanza; es un cálculo preciso basado en el principio de conservación de la energía. En un sistema aislado, donde no hay pérdida ni ganancia de calor con el entorno, el calor cedido por el cuerpo más caliente es igual al calor ganado por el cuerpo más frío. Este principio es la piedra angular para determinar la temperatura final.
Para realizar este cálculo, necesitamos conocer algunas propiedades clave de los materiales involucrados:
- Masa (m): La cantidad de sustancia de cada cuerpo, generalmente medida en kilogramos (kg) o gramos (g).
- Temperatura Inicial (Ti): La temperatura de cada cuerpo antes de que entren en contacto, medida en grados Celsius (°C) o Kelvin (K).
- Capacidad Calorífica Específica (c): Esta es una propiedad intrínseca de cada material que nos dice cuánta energía se necesita para elevar la temperatura de una unidad de masa de esa sustancia en un grado. Se mide comúnmente en Joules por kilogramo por grado Celsius (J/kg°C) o calorías por gramo por grado Celsius (cal/g°C). Un material con una alta capacidad calorífica específica, como el agua, requiere mucha energía para cambiar su temperatura.
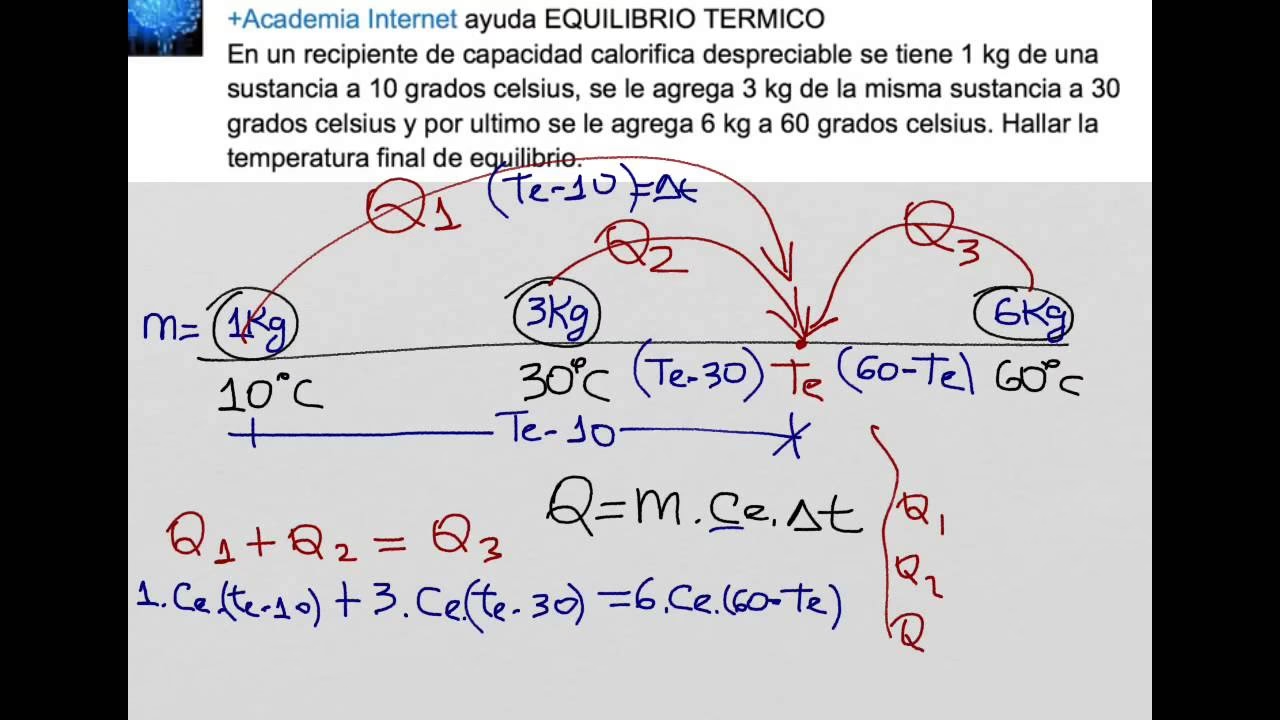
La fórmula general para el calor transferido (Q) es:
Q = m * c * ΔT
Donde ΔT es el cambio de temperatura (Temperatura Final - Temperatura Inicial). Siguiendo el principio de conservación de la energía, si tenemos dos cuerpos (1 y 2) en un sistema aislado, el calor cedido por uno será igual al calor ganado por el otro, pero con signo opuesto:
Q1 + Q2 = 0
Expandiendo esto, obtenemos:
m1 * c1 * (Tf - T1) + m2 * c2 * (Tf - T2) = 0
Donde Tf es la temperatura de equilibrio final. Nuestro objetivo es despejar Tf de esta ecuación:
m1 * c1 * Tf - m1 * c1 * T1 + m2 * c2 * Tf - m2 * c2 * T2 = 0
Agrupamos los términos con Tf:
Tf * (m1 * c1 + m2 * c2) = m1 * c1 * T1 + m2 * c2 * T2
Finalmente, despejamos Tf:
Tf = (m1 * c1 * T1 + m2 * c2 * T2) / (m1 * c1 + m2 * c2)
Esta fórmula es increíblemente poderosa porque nos permite predecir con precisión la temperatura a la que se equilibrará un sistema de dos cuerpos. Es importante notar que esta fórmula asume un sistema aislado, es decir, que no hay intercambio de calor con el entorno, y que no hay cambios de fase (como hielo derritiéndose o agua hirviendo), lo que añadiría calor latente a la ecuación.
Factores Clave que Influyen en el Equilibrio Térmico
La temperatura de equilibrio no es simplemente un promedio de las temperaturas iniciales. Depende fundamentalmente de la masa y la capacidad calorífica específica de cada material. Estos factores determinan la 'inercia térmica' de cada cuerpo, es decir, su resistencia a cambiar de temperatura.
- Masa: Un cuerpo con mayor masa tendrá una mayor 'capacidad' para almacenar o ceder calor. Si pones una pequeña cuchara caliente en un gran balde de agua fría, la temperatura del agua apenas cambiará, mientras que la cuchara se enfriará drásticamente. La masa del agua es mucho mayor, y por lo tanto, su influencia en la temperatura final es dominante.
- Capacidad Calorífica Específica: Este factor es crucial. Materiales como el agua tienen una capacidad calorífica específica muy alta, lo que significa que pueden absorber o liberar una gran cantidad de calor con un cambio de temperatura relativamente pequeño. Por el contrario, los metales suelen tener capacidades caloríficas específicas bajas, lo que los hace ideales para conducir el calor y cambiar su temperatura rápidamente. Por eso, una olla de metal se calienta mucho más rápido que el agua que contiene.
- Aislamiento del Sistema: Para que la fórmula sea precisa, el sistema debe estar lo más aislado posible del entorno. En la realidad, siempre hay alguna pérdida o ganancia de calor con el aire circundante, las superficies de contacto, etc. Sin embargo, para muchos propósitos prácticos, podemos asumir un buen aislamiento si el proceso es rápido o si el sistema está diseñado para minimizar las pérdidas.
Ejemplos Cotidianos y Aplicaciones Prácticas del Equilibrio Térmico
El equilibrio térmico es un concepto omnipresente en nuestras vidas, a menudo sin que nos demos cuenta. Aquí hay algunos ejemplos que ilustran su importancia:
- El Termómetro Clínico: Cuando colocas un termómetro debajo de tu lengua, el calor fluye de tu cuerpo (más caliente) al mercurio o alcohol del termómetro (más frío) hasta que ambos alcanzan la misma temperatura: tu temperatura corporal. El tiempo que tarda el termómetro en estabilizarse es el tiempo que se necesita para alcanzar el equilibrio térmico.
- Enfriar una Bebida: Si agregas cubitos de hielo a una bebida caliente, el calor de la bebida se transfiere al hielo, derritiéndolo y elevando la temperatura del agua derretida, hasta que toda la mezcla alcanza una temperatura de equilibrio más baja. Si los cubos son pequeños y la bebida es mucha, la temperatura no bajará tanto. Si, por el contrario, son muchos cubos y poca bebida, la temperatura final será mucho más baja.
- Cocina y Conservación de Alimentos: Cuando colocas una olla caliente en el fregadero lleno de agua fría, el calor de la olla se transfiere al agua hasta que ambos alcanzan una temperatura intermedia. De manera similar, un refrigerador funciona extrayendo calor de los alimentos hasta que alcanzan la temperatura de equilibrio deseada del interior del aparato, ralentizando el crecimiento bacteriano.
- Climatización de Edificios: Los sistemas de calefacción o aire acondicionado trabajan para llevar la temperatura interior de un edificio a un equilibrio deseado con el aire que se introduce. La eficiencia energética depende de qué tan bien aislado esté el edificio para evitar que la temperatura exterior afecte el equilibrio interior.
- Fenómenos Meteorológicos: Las brisas marinas y terrestres son un excelente ejemplo. Durante el día, la tierra se calienta más rápido que el mar (debido a su menor capacidad calorífica específica), creando una diferencia de presión que genera una brisa del mar hacia la tierra. Por la noche, la tierra se enfría más rápido, invirtiendo el proceso.
- Procesos Industriales: En la industria, los intercambiadores de calor se utilizan para transferir calor eficientemente entre fluidos a diferentes temperaturas, por ejemplo, para calentar un fluido de proceso usando el calor residual de otro, optimizando el uso de energía y alcanzando temperaturas de equilibrio específicas para diferentes reacciones o procesos.
Tabla Comparativa: Capacidades Caloríficas Específicas de Materiales Comunes
Para facilitar la comprensión de cómo los diferentes materiales influyen en el cálculo de la temperatura de equilibrio, presentamos una tabla con valores aproximados de capacidades caloríficas específicas para algunas sustancias comunes. Tenga en cuenta que estos valores pueden variar ligeramente dependiendo de la presión y la temperatura exactas.
| Material | Capacidad Calorífica Específica (J/kg°C) |
|---|---|
| Agua (líquida) | 4186 |
| Hielo | 2090 |
| Vapor de agua | 2010 |
| Aluminio | 900 |
| Hierro | 450 |
| Cobre | 385 |
| Vidrio | 840 |
| Aire (a presión constante) | 1000 |
| Madera | 1700 |
Como se puede observar, el agua tiene una capacidad calorífica específica significativamente más alta que la mayoría de los metales, lo que explica por qué el agua tarda más en calentarse y enfriarse, y por qué es tan efectiva para transferir o almacenar calor en muchos sistemas.
Preguntas Frecuentes sobre el Equilibrio Térmico
A continuación, abordamos algunas de las preguntas más comunes relacionadas con el equilibrio térmico para aclarar conceptos y resolver dudas.
¿Es el equilibrio térmico un tipo de equilibrio termodinámico?
Sí, el equilibrio térmico es una condición necesaria para el equilibrio termodinámico completo. El equilibrio termodinámico implica no solo la igualdad de temperaturas (equilibrio térmico), sino también la ausencia de cambios netos de presión (equilibrio mecánico) y de composición química (equilibrio químico) dentro del sistema y con su entorno. En otras palabras, el equilibrio térmico es un componente clave de un estado de equilibrio termodinámico más amplio.
¿Qué sucede si hay un cambio de fase durante el proceso de equilibrio?
Si un cambio de fase (como la fusión del hielo o la ebullición del agua) ocurre durante el proceso de alcanzar el equilibrio, la fórmula simple que utilizamos debe ser modificada. Durante un cambio de fase, se absorbe o libera una cantidad de calor llamada calor latente, sin que haya un cambio en la temperatura. Por ejemplo, el hielo a 0°C absorbe calor latente de fusión para convertirse en agua a 0°C. Si esto ocurre, debemos añadir el término de calor latente (Q = m * L, donde L es el calor latente específico) a la ecuación de balance de energía, lo que complica el cálculo, pero sigue siendo un proceso predecible.
¿Siempre se alcanza el equilibrio térmico?
En teoría, sí. La segunda ley de la termodinámica establece que el calor fluirá espontáneamente de una región de mayor temperatura a una de menor temperatura hasta que el equilibrio térmico se establezca. En la práctica, puede llevar mucho tiempo en sistemas muy grandes o mal conductores, pero el proceso siempre tiende hacia ese estado.
¿Por qué es importante el concepto de capacidad calorífica específica?
La capacidad calorífica específica es fundamental porque nos permite cuantificar la 'inercia térmica' de un material. Es la clave para entender por qué algunos materiales son buenos aislantes (alta capacidad calorífica, cambian poco su temperatura) y otros son buenos conductores (baja capacidad calorífica, cambian mucho su temperatura). Es un dato esencial para cualquier cálculo de transferencia de calor y diseño de sistemas térmicos.
¿Cómo afecta la presión al equilibrio térmico?
Si bien la presión no influye directamente en la definición de equilibrio térmico (que se centra en la temperatura), sí puede afectar la capacidad calorífica específica de los materiales, especialmente los gases. Además, la presión es crucial en los cambios de fase, ya que el punto de fusión o ebullición de una sustancia depende de la presión ambiente. Por lo tanto, en un análisis completo de un sistema termodinámico, la presión es un factor importante a considerar.
El estudio del equilibrio térmico y la capacidad de calcular la temperatura final de un sistema no es solo un ejercicio académico. Es una habilidad práctica que nos permite entender y manipular el mundo físico. Desde el diseño de sistemas de calefacción eficientes hasta la simple tarea de enfriar una taza de café, el principio de conservación de la energía y las propiedades térmicas de los materiales son herramientas indispensables. Al dominar estos conceptos, uno puede apreciar la sofisticación con la que la naturaleza busca su propio balance energético, un equilibrio que, en última instancia, define gran parte de nuestra experiencia diaria.
Si quieres conocer otros artículos parecidos a Cálculo de la Temperatura de Equilibrio puedes visitar la categoría Física.
