12/11/2023
En el fascinante mundo de la biología molecular, la capacidad de cuantificar con precisión la expresión génica es fundamental para desentrañar los mecanismos de la vida. La Reacción en Cadena de la Polimerasa en Tiempo Real, o PCR en tiempo real (qPCR), se ha consolidado como una herramienta indispensable en este campo, permitiendo el estudio de la expresión de genes de baja abundancia con una sensibilidad y rapidez sin precedentes. Esta técnica no solo ha revolucionado la investigación, sino que también ha encontrado aplicaciones críticas en el diagnóstico clínico y la detección de patógenos. Sin embargo, para dominar verdaderamente la qPCR, es esencial comprender no solo cómo se realiza, sino también las fórmulas matemáticas que rigen su cuantificación y cómo interpretar los datos generados.
- ¿Qué es la PCR en Tiempo Real (qPCR)?
- Fundamentos de la Cuantificación en qPCR
- La Fórmula Clave para la Cuantificación Relativa en qPCR
- Interpretación de los Resultados de qPCR: El Valor Ct
- Evaluación del Rendimiento de una Reacción de qPCR
- Pasos para Realizar una Reacción de qPCR
- Consideraciones Clave para un Análisis Preciso
- Preguntas Frecuentes (FAQ)
- ¿Qué indica un valor Ct bajo en qPCR?
- ¿Por qué es crucial la eficiencia de la PCR en tiempo real?
- ¿Cuál es la diferencia entre cuantificación relativa y absoluta en qPCR?
- ¿Se pueden comparar los valores Ct directamente entre diferentes experimentos o laboratorios?
- ¿Qué son los genes de referencia o housekeeping genes?
¿Qué es la PCR en Tiempo Real (qPCR)?
La PCR en tiempo real, también conocida como PCR cuantitativa (qPCR), es una técnica altamente sensible y específica utilizada para amplificar y cuantificar secuencias de ADN o ARN (previamente transcrito a ADNc) en tiempo real, es decir, a medida que la reacción progresa. A diferencia de la PCR convencional, que detecta los productos de ADN al final de la reacción, la qPCR monitorea la acumulación de estos productos ciclo a ciclo. Esto se logra mediante el uso de fluorocromos que emiten una señal de fluorescencia proporcional a la cantidad de ADN amplificado.
La capacidad de la qPCR para cuantificar transcritos raros y pequeños cambios en la expresión génica la convierte en la técnica de elección para analizar la expresión de ARNm. Es fácil de realizar, proporciona la precisión necesaria y produce resultados de cuantificación fiables y rápidos. Es particularmente adecuada para estudios de pequeños subconjuntos de genes, aunque requiere que la secuencia del gen diana específico sea conocida para el diseño de los cebadores.
Fundamentos de la Cuantificación en qPCR
La cuantificación precisa de ácidos nucleicos mediante qPCR requiere una metodología reproducible y un modelo matemático adecuado para el análisis de datos. Generalmente, existen dos tipos principales de cuantificación en la qPCR:
Cuantificación Relativa vs. Absoluta
- Cuantificación Relativa: Se basa en la expresión relativa de un gen diana en comparación con un gen de referencia. Es el método más común para investigar cambios fisiológicos en la expresión génica, ya que es adecuado para la mayoría de los propósitos de investigación. Su objetivo es determinar cuánto se ha regulado al alza o a la baja un gen en una condición experimental en comparación con un control.
- Cuantificación Absoluta: Se basa en una curva de calibración interna o externa. Utilizar una curva de calibración requiere que la metodología esté altamente validada y que se confirme la identidad de las eficiencias de amplificación de la PCR para el material estándar y el ADNc diana. Sin embargo, la generación de material estándar estable y fiable (ADN o ARN recombinante) es muy laboriosa y debe cuantificarse con precisión.
La Importancia de los Genes de Referencia
Para la cuantificación relativa, se recomienda normalizar el gen diana con un estándar endógeno. Para ello, se utilizan principalmente genes de referencia (también conocidos como genes housekeeping o de mantenimiento), que se supone que tienen una expresión estable y no regulada en diversas condiciones. Ejemplos comunes incluyen GAPDH (G3PDH), albúmina, actinas, tubulinas, ciclofilina, ARNr 18S o ARNr 28S. Estos genes son esenciales para la supervivencia celular básica y se asume que su síntesis de ARNm es constante incluso bajo tratamientos experimentales. No obstante, numerosos estudios han demostrado que la expresión de estos genes housekeeping puede variar bajo ciertas condiciones experimentales, lo que subraya la necesidad de una validación cuidadosa.
La Fórmula Clave para la Cuantificación Relativa en qPCR
Para abordar la complejidad y el alto costo de los modelos de cuantificación basados en curvas de calibración y la necesidad de normalización, se ha desarrollado un nuevo y simple modelo matemático para el análisis de datos. Este modelo permite calcular la razón de expresión relativa de un gen diana basándose únicamente en las eficiencias de la PCR en tiempo real y la desviación del punto de cruce (CP) de una muestra problema en comparación con un control. Este modelo no requiere una curva de calibración, lo que simplifica significativamente el proceso.
La ecuación principal para la cuantificación relativa es la siguiente:
R = (EtargetΔCPtarget) / (ErefΔCPref)
Donde:
- R: Representa la razón de expresión relativa del gen diana.
- Etarget: Es la eficiencia de la PCR en tiempo real del transcrito del gen diana.
- Eref: Es la eficiencia de la PCR en tiempo real del transcrito del gen de referencia.
- ΔCPtarget: Es la desviación del punto de cruce (CP) entre la muestra control y la muestra problema del transcrito del gen diana (CPcontrol - CPmuestra).
- ΔCPref: Es la desviación del punto de cruce (CP) entre la muestra control y la muestra problema del transcrito del gen de referencia (CPcontrol - CPmuestra).
El CP se define como el punto en el que la fluorescencia se eleva apreciablemente por encima de la fluorescencia de fondo. Para el cálculo de R, es necesario conocer las eficiencias individuales de la PCR en tiempo real y la desviación del CP (ΔCP) de los transcritos investigados.
Cálculo de la Eficiencia (E)
La eficiencia de la PCR en tiempo real (E) para cada ciclo en la fase exponencial se calcula a partir de la pendiente de la curva estándar (generada a partir de una serie de diluciones del ADNc) usando la siguiente ecuación:
E = 10(-1/pendiente)
Una eficiencia de 2 (o 100%) indica que la cantidad de ADN se duplica en cada ciclo. Los transcritos investigados suelen mostrar altas tasas de eficiencia de PCR en tiempo real, con coeficientes de correlación de Pearson (r) superiores a 0.95, indicando una alta linealidad.

Otros Modelos Matemáticos de Cuantificación Relativa
Existen otros modelos matemáticos para la cuantificación relativa en PCR en tiempo real, aunque el modelo presentado busca ofrecer una comprensión más clara y una mayor fiabilidad:
- Modelo calibrado por eficiencia (Roche Diagnostics): Este modelo (Ecuación 3), en principio, es similar al presentado y arroja resultados idénticos en cuanto a la razón de expresión relativa. Sin embargo, el método de cálculo puede ser más difícil de entender.
- Método Delta-Delta Ct (ΔΔCt) (PE Applied Biosystems): Este método (Ecuación 4) es ampliamente conocido y se expresa como:
Cantidad Relativa = 2-ΔΔCt. La Ecuación 4 asume eficiencias de amplificación óptimas e idénticas (E = 2 o 100%) para el gen diana y el gen de referencia. Si bien es útil para una estimación rápida, es una simplificación de la Ecuación 1 bajo la condición de que Etarget = Eref = 2. Nuestro modelo presentado combina ambos para una comprensión más profunda y una expresión génica relativa más fiable y exacta.
Interpretación de los Resultados de qPCR: El Valor Ct
La interpretación de los resultados de qPCR se centra en el valor Ct (cycle threshold) o Cq (quantification cycle). Es un dato de alto valor derivado de cada curva de amplificación, que permite calcular las cantidades iniciales del gen diana.
¿Qué es el Valor Ct?
El valor Ct es el punto de intersección entre una curva de amplificación y una línea de umbral. Es una medida relativa de la concentración del gen diana en la reacción de PCR. Cuanto menor sea el valor Ct, mayor será la cantidad inicial del gen diana en la muestra. Esto se debe a que una mayor cantidad de material de partida hará que la señal de fluorescencia alcance el umbral en un número menor de ciclos.
En un gráfico de amplificación, el eje vertical representa las unidades de fluorescencia (a menudo ΔRn, que es una señal de reportero normalizada y con línea de base restada), y el eje horizontal, el número de ciclos de PCR.
- Línea de Base: Son los datos de los primeros ciclos de PCR, antes de que la señal de amplificación sea detectable. En esta fase, la amplificación puede estar ocurriendo, pero la señal de fluorescencia aún no se ha acumulado lo suficiente para ser visible. El algoritmo de sustracción de la línea de base en el software de qPCR reduce esta variación inicial.
- Umbral: Es un valor de fluorescencia (ΔRn) seleccionado dentro de la fase exponencial de la PCR. La intersección del umbral con la curva de amplificación de cada muestra produce el valor Ct. Los umbrales se establecen idealmente en la fase exponencial, donde la acumulación de producto es más consistente y la eficiencia es máxima.
Factores que Influyen en el Valor Ct
Aunque el valor Ct se correlaciona directamente con la concentración inicial del gen diana, muchos otros factores independientes de la plantilla pueden influir en su valor absoluto, lo que significa que los valores Ct de reacciones ejecutadas bajo diferentes condiciones o con diferentes reactivos no pueden compararse directamente.
- Composición de la Mezcla Maestra (Master Mix): La intensidad de la fluorescencia de cualquier molécula depende de factores ambientales como el pH y la concentración de sal de una solución. Diferentes composiciones de master mix pueden afectar la intensidad de la señal de fluorescencia y, por lo tanto, la línea de base y el valor Ct, incluso si la concentración del gen diana es la misma.
- El Colorante de Referencia Pasivo ROX: El valor Rn (fluorescencia del colorante reportero dividida por la fluorescencia del colorante ROX) es crucial. Una menor cantidad de ROX produciría un valor Rn más alto, lo que llevaría a un aumento de la línea de base Rn y, en consecuencia, a un ΔRn menor y un valor Ct diferente. Las concentraciones bajas de ROX también pueden aumentar la desviación estándar del valor Ct, reduciendo la confianza al distinguir pequeñas diferencias en la concentración del gen diana.
- La Eficiencia de la Reacción de PCR: La eficiencia de la reacción de PCR afecta directamente el valor Ct. Una baja eficiencia significa que se necesitan más ciclos para alcanzar el umbral, lo que resulta en un valor Ct posterior. Una serie de diluciones amplificadas en condiciones de baja eficiencia producirá una curva estándar con una pendiente diferente a la de las condiciones de alta eficiencia. Generalmente, una eficiencia entre 90% y 110% (pendiente de -3.3 ± 10%) se considera aceptable.
Evaluación del Rendimiento de una Reacción de qPCR
Para comparar dos reacciones de qPCR donde se ha cambiado una condición (por ejemplo, diferentes master mixes o instrumentos), es fundamental evaluar los siguientes parámetros:
Rango Dinámico
Para evaluar correctamente la eficiencia de la PCR, es necesario un mínimo de 3 réplicas y un mínimo de 5 logs de concentración de la plantilla. Esta rigurosidad es crucial porque, incluso si el ensayo es 100% eficiente, un rango de 70% a 170% puede obtenerse al probar diluciones en un solo log, debido a la desviación estándar en una dilución. Con un rango de 5 logs, el artefacto potencial es de solo ±8%, lo que asegura una determinación precisa de la eficiencia.
Valor R2
Otro parámetro crítico para evaluar la eficiencia de la PCR es el valor R2 (coeficiente de determinación), que es un término estadístico que indica qué tan bien un valor predice otro. Un valor R2 > 0.99 proporciona una buena confianza en la correlación entre las cantidades de plantilla y los valores Ct, indicando una alta linealidad de la curva estándar.

Precisión
La desviación estándar es la medida más común de la precisión. Si muchos puntos de datos están cerca de la media, la desviación estándar es pequeña. Para poder cuantificar una dilución de 2 veces en más del 99.7% de los casos, la desviación estándar debe ser ≤ 0.167. Para poder discriminar entre una dilución de 2 veces en más del 95% de los casos, la desviación estándar debe ser ≤ 0.250.
Sensibilidad
Cualquier sistema capaz de amplificar y detectar eficazmente una copia de la plantilla inicial ha alcanzado el nivel máximo de sensibilidad. La eficiencia es un factor clave para determinar la sensibilidad de una reacción. Para la detección de números de copias muy bajos, la distribución normal de la plantilla no se aplica; en su lugar, se sigue una distribución de Poisson. Esto predice que en un gran número de réplicas que contienen un promedio de una copia de la plantilla inicial, aproximadamente el 37% no debería tener copias, solo el 37% debería contener una copia y el 18% debería contener dos copias. Por lo tanto, para una detección fiable de copias bajas, es necesario un gran número de réplicas para proporcionar significación estadística.
La siguiente tabla resume los criterios para la evaluación del rendimiento de la qPCR:
| Factor | Recomendaciones | Criterios |
|---|---|---|
| Eficiencia | Dilución en serie con 5 logs de diluciones | Pendiente: ~ -3.3, R2 > 0.99 |
| Precisión | Mínimo de 3 réplicas | Desviación estándar < 0.167 |
| Sensibilidad | Alto número de réplicas para muestras con bajo número de copias debido a la distribución de Poisson | Análisis estadístico |
Pasos para Realizar una Reacción de qPCR
La realización de una reacción de PCR en tiempo real implica dos pasos principales:
Transcipción Inversa (RT)
El primer paso en una reacción de qPCR, cuando se trabaja con ARN, es la conversión del ARN a ADN complementario (ADNc). Este proceso, conocido como transcripción inversa, es crucial para el análisis de la expresión génica, ya que la PCR amplifica ADN, no ARN. Se utiliza una transcriptasa inversa (como Superscript II) y cebadores aleatorios de hexámeros para generar el ADNc a partir del ARN total.
Amplificación y Detección en Tiempo Real
Una vez obtenido el ADNc, se procede a la reacción de PCR propiamente dicha, utilizando reporteros fluorescentes para amplificar y detectar genes específicos. Los dos tipos más comunes de reporteros fluorescentes son SYBR Green y las sondas TaqMan:
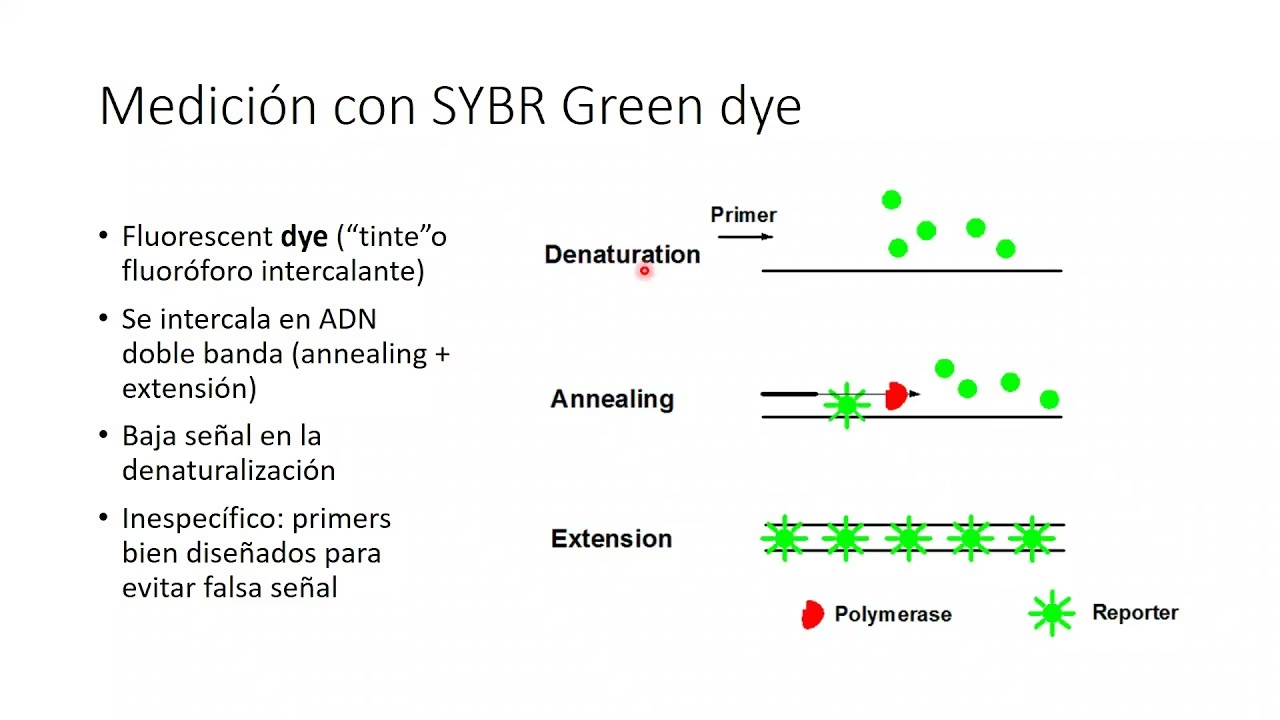
- SYBR Green: Es un colorante que fluoresce únicamente cuando se une al ADN de doble cadena (es decir, el producto de PCR). A medida que se sintetiza más producto de PCR, más SYBR Green se une y más fluorescencia se emite. Es una técnica sencilla y rentable, pero puede unirse a cualquier ADN de doble cadena, incluidos los dímeros de cebadores, lo que puede afectar la especificidad.
- Sondas TaqMan: Son sondas de ácido nucleico específicas del gen, unidas a moléculas reporteras y quencher (apagadoras). La sonda se une al ADN entre el cebador directo y el inverso. Mientras el reportero y el quencher están unidos a la sonda, el quencher absorbe la fluorescencia emitida por el reportero. Durante la fase de extensión de la reacción de PCR, la actividad 5'-exonucleasa de la ADN polimerasa degrada la sonda, liberando el reportero y permitiendo que su fluorescencia sea detectada. La ventaja del método TaqMan es su alta especificidad y la posibilidad de combinar sondas con diferentes colores de reporteros en ensayos multiplex.
Para ambos métodos, la cantidad de fluorescencia en una muestra se detecta en tiempo real y se grafica contra el número de ciclo. La cantidad de fluorescencia es proporcional a la cantidad de producto de PCR. El punto en el tiempo en el que la fluorescencia alcanza un umbral definido es relativo al nivel de expresión génica.
Consideraciones Clave para un Análisis Preciso
La alta precisión y reproducibilidad son esenciales en la qPCR. Se deben considerar varios factores para asegurar la fiabilidad de los resultados:
Reproducibilidad y Precisión
La precisión intra-ensayo (dentro de una misma corrida) y la variación inter-ensayo (entre diferentes corridas) deben ser bajas. Para lograr esto, es crucial una determinación exacta de las eficiencias de amplificación en tiempo real y una baja variabilidad del CP. El modelo matemático presentado en este artículo ha demostrado alta precisión y un error relativo inferior al 2.5%.
La Importancia del RT de Dos Pasos
En el proceso de RT-PCR de dos pasos (primero la transcripción inversa, luego la PCR), todas las posibles interferencias durante la RT (como la integridad del ARN, la eficiencia de la RT o las variaciones en la carga de la muestra de ADNc) influirán en todos los transcritos diana y en el transcrito de referencia interno de manera paralela. Cualquier fuente de error durante la RT será compensada por el modelo mismo, ya que las variaciones solo desaparecen durante la PCR en tiempo real. Los modelos de RT-PCR de un solo paso, ampliamente distribuidos, no son tan aplicables porque en cada configuración de reacción y para cada factor investigado, pueden surgir condiciones de RT individuales y ligeramente diferentes. Por lo tanto, la variación en una RT-PCR de dos pasos siempre será menor y la reproducibilidad del ensayo será mayor que en una RT-PCR de un solo paso.

Preguntas Frecuentes (FAQ)
¿Qué indica un valor Ct bajo en qPCR?
Un valor Ct bajo indica que la señal de fluorescencia alcanzó el umbral en un número menor de ciclos. Esto se correlaciona directamente con una mayor cantidad inicial de la secuencia diana en la muestra. En otras palabras, cuanto antes aparece la señal, más abundante era el material genético de partida.
¿Por qué es crucial la eficiencia de la PCR en tiempo real?
La eficiencia de la PCR en tiempo real es fundamental porque afecta directamente la precisión y la sensibilidad de la cuantificación. Si la eficiencia no es óptima (idealmente 100%, es decir, el ADN se duplica en cada ciclo), los valores Ct no reflejarán con exactitud la cantidad inicial de la plantilla, lo que puede llevar a una subestimación o sobreestimación de la expresión génica. Una baja eficiencia también reduce la capacidad de detectar bajas concentraciones de la diana.
¿Cuál es la diferencia entre cuantificación relativa y absoluta en qPCR?
La cuantificación relativa compara la expresión de un gen diana entre diferentes muestras o condiciones, normalizando los resultados con un gen de referencia (que se asume estable). Su resultado es una razón o un factor de cambio. La cuantificación absoluta, en cambio, determina la cantidad molecular exacta o la concentración de una diana en una muestra, generalmente utilizando una curva de calibración de estándares conocidos. El resultado se expresa en unidades como copias/mL o ng/µL.
¿Se pueden comparar los valores Ct directamente entre diferentes experimentos o laboratorios?
Generalmente, no. El valor absoluto de Ct puede ser influenciado por numerosos factores independientes de la plantilla, como la composición de la mezcla maestra, la concentración del colorante de referencia (ROX), la eficiencia de la reacción, el equipo utilizado y el algoritmo de software para determinar el Ct. Por lo tanto, las comparaciones directas de valores Ct solo son significativas cuando todos los parámetros de la reacción son idénticos. Para comparaciones entre experimentos, es preferible utilizar métodos de cuantificación relativa o absoluta que normalicen estas variaciones.
¿Qué son los genes de referencia o housekeeping genes?
Los genes de referencia, o genes housekeeping, son genes cuya expresión se considera estable y constante en todas las células y bajo diversas condiciones experimentales. Se utilizan para normalizar la cantidad de ARNm total en cada muestra y compensar variaciones en la cantidad de ARN de partida, la eficiencia de la transcripción inversa y la carga de la muestra. Ejemplos comunes incluyen GAPDH, actina y ARNr 18S. Sin embargo, su estabilidad debe ser validada para cada tipo de tejido y condición experimental.
Si quieres conocer otros artículos parecidos a La Fórmula de la PCR en Tiempo Real y su Interpretación puedes visitar la categoría Cálculos.
