20/03/2024
En el vasto universo de la ciencia, la energía y sus transformaciones son pilares fundamentales para comprender cómo funciona nuestro mundo. Una de las formas más comunes de energía que experimentamos y medimos constantemente es el calor. ¿Alguna vez te has preguntado cómo los científicos logran cuantificar el calor que se transfiere en una reacción química o un cambio físico? La respuesta a menudo reside en una rama de la termodinámica conocida como calorimetría, y dentro de ella, un concepto crucial emerge: el equivalente de agua. Este término, aunque pueda sonar técnico, es una herramienta ingeniosa que nos permite comparar y cuantificar la capacidad de diferentes sustancias para absorber calor, utilizando el agua como nuestro estándar de referencia universal.

Imagínate que quieres comparar cuánto calor puede almacenar una cuchara de metal frente a un vaso de agua. No es una tarea intuitiva, ¿verdad? El equivalente de agua simplifica esta comparación al expresar la capacidad calorífica de cualquier sustancia en términos de una masa equivalente de agua. En este artículo, exploraremos en detalle qué es el equivalente de agua, por qué es tan importante en la calorimetría, cómo se calcula y se determina experimentalmente, y desvelaremos su relevancia en el estudio de las transformaciones energéticas.
- ¿Qué es el Equivalente de Agua?
- La Ciencia Detrás: Calorimetría y Transferencia de Calor
- Un Vistazo Histórico a la Calorimetría
- ¿Cómo se Calcula el Equivalente de Agua?
- El Equivalente de Agua en la Práctica: El Calorímetro
- Determinación Experimental del Equivalente de Agua de un Calorímetro
- Importancia y Aplicaciones
- Preguntas Frecuentes (FAQ)
- Conclusión
¿Qué es el Equivalente de Agua?
El equivalente de agua de una sustancia o de un objeto (como un calorímetro) se define como la masa de agua que absorbería la misma cantidad de calor que la sustancia u objeto, cuando ambos experimentan el mismo cambio de temperatura. En esencia, es una forma de expresar la capacidad calorífica de un material en unidades de masa de agua. Esto es particularmente útil porque el agua tiene propiedades térmicas bien conocidas y se utiliza comúnmente como medio de referencia en experimentos de calorimetría.
Para entenderlo mejor, consideremos un ejemplo práctico. Si tenemos un objeto de metal que, al absorber 100 julios de calor, eleva su temperatura en 5°C, y sabemos que 10 gramos de agua también elevan su temperatura en 5°C al absorber 100 julios, entonces diríamos que el equivalente de agua de ese objeto de metal es de 10 gramos. Esto nos permite “traducir” la capacidad de almacenamiento de calor del metal a una cantidad comparable y más familiar de agua.
La Ciencia Detrás: Calorimetría y Transferencia de Calor
Para apreciar plenamente el concepto de equivalente de agua, es fundamental comprender el contexto de la calorimetría. La calorimetría es la rama de la ciencia que se ocupa de la medición de los cambios de calor asociados con reacciones químicas o cambios físicos. El dispositivo principal utilizado para estas mediciones es el calorímetro, un instrumento diseñado para aislar el sistema bajo estudio del entorno, permitiendo que todo el calor liberado o absorbido dentro del sistema sea contenido y medido.

El calor (Q) absorbido o liberado por una sustancia se relaciona con su masa (m), su calor específico (c) y el cambio de temperatura (ΔT) mediante la fórmula fundamental de la calorimetría: Q = m · c · ΔT. El calor específico (c) es una propiedad intrínseca de cada sustancia que indica la cantidad de calor necesaria para elevar la temperatura de una unidad de masa de esa sustancia en un grado Celsius (o Kelvin). El agua es conocida por tener un calor específico relativamente alto (aproximadamente 4.184 J/g°C o 1 cal/g°C), lo que significa que requiere una cantidad considerable de energía para cambiar su temperatura, haciéndola un excelente medio para absorber y liberar calor en experimentos.
La capacidad calorífica (C) de un objeto o sistema se define como la cantidad de calor necesaria para elevar su temperatura en un grado. Se relaciona con el calor específico y la masa mediante C = m · c. Así, el equivalente de agua (W) de un cuerpo es, de hecho, la masa de agua que tiene la misma capacidad calorífica que ese cuerpo. Por lo tanto, el equivalente de agua (W) se puede expresar como:
W = msustancia · csustancia / cagua
Dado que el calor específico del agua es aproximadamente 1 cal/g°C (o 4.184 J/g°C), si utilizamos el calor específico del agua como referencia unitaria, la fórmula simplificada que se usa a menudo es:
W = msustancia · csustancia
donde 'm' es la masa de la sustancia y 'c' es su calor específico. Es importante recordar que 'c' aquí debe estar en unidades consistentes con el calor específico del agua si se busca una equivalencia directa en masa de agua.
Un Vistazo Histórico a la Calorimetría
La historia de la calorimetría es tan fascinante como la ciencia misma. El médico escocés Joseph Black (1728-1799) es a menudo reconocido como el «Padre de la Calorimetría». Black fue pionero en distinguir claramente entre calor y temperatura, y sus experimentos sentaron las bases para comprender el calor latente y el calor específico. Sus ideas revolucionaron la forma en que los científicos abordaban las mediciones de calor.
Más tarde, el químico francés Pierre Eugène Marcellin Berthelot (1827-1907) hizo contribuciones significativas a las técnicas modernas de calorimetría. Berthelot no solo estudió a fondo los problemas asociados con la medición del calor, sino que también construyó el primer calorímetro moderno, conocido como el calorímetro de bomba, que permitió mediciones precisas del calor de combustión. También se le atribuye la acuñación de los términos «reacciones endotérmicas» y «exotérmicas» para describir los procesos químicos que absorben o liberan calor, respectivamente.
¿Cómo se Calcula el Equivalente de Agua?
El cálculo del equivalente de agua es directo una vez que se conocen la masa y el calor específico de la sustancia o del aparato en cuestión. La fórmula es:
W = m ⋅ c
Donde:
- W es el equivalente de agua (generalmente en gramos o kilogramos de agua).
- m es la masa de la sustancia o del componente del calorímetro (en gramos o kilogramos).
- c es el calor específico de la sustancia o del material del componente (en J/g°C, J/kg°C, cal/g°C, etc.).
Ejemplo de Cálculo:
Supongamos que tenemos un componente de un calorímetro hecho de cobre con una masa de 500 gramos (0.5 kg) y el calor específico del cobre es aproximadamente 0.385 J/g°C. Para calcular su equivalente de agua:
W = 500 g ⋅ 0.385 J/g°C
W = 192.5 J/°C
Para expresar esto en masa de agua, dividimos por el calor específico del agua (aproximadamente 4.184 J/g°C):
W = 192.5 J/°C / 4.184 J/g°C
W ≈ 46.01 g de agua
Esto significa que 500 gramos de cobre tienen la misma capacidad para absorber calor que aproximadamente 46.01 gramos de agua. Este valor es crucial para corregir las mediciones de calor en un calorímetro, ya que el propio calorímetro absorberá una parte del calor de la reacción.
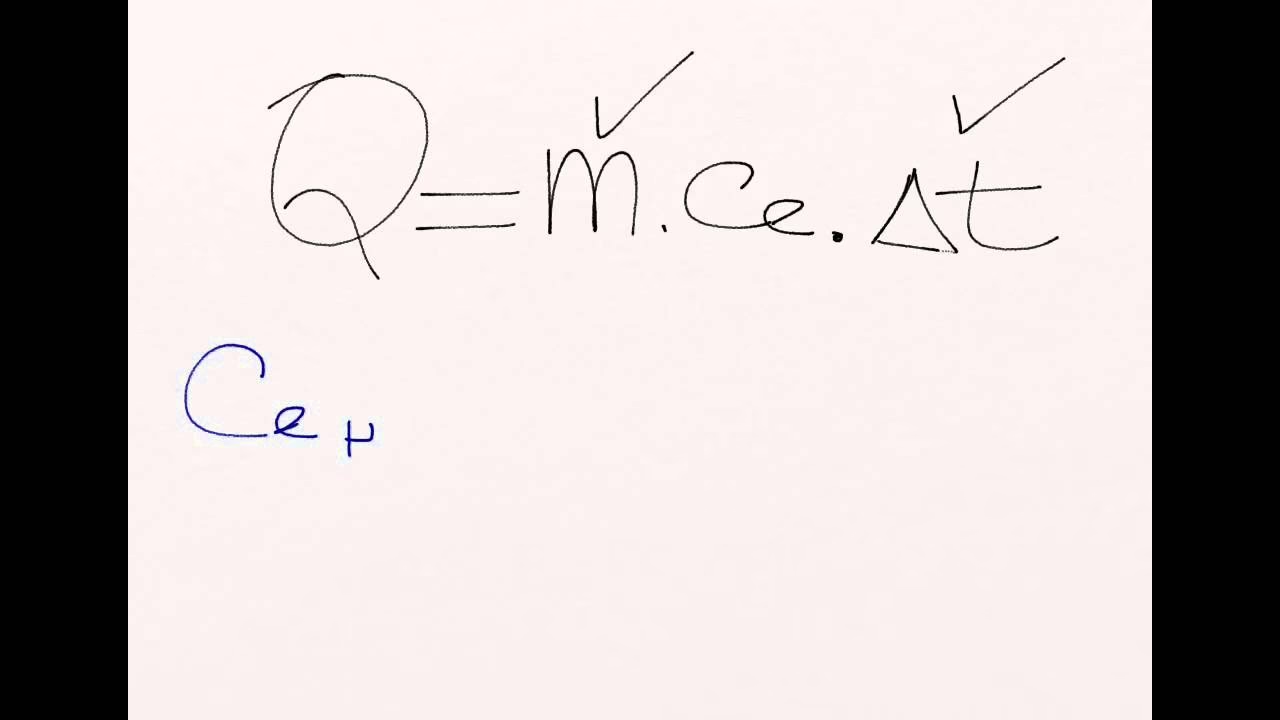
El Equivalente de Agua en la Práctica: El Calorímetro
En el diseño y uso de un calorímetro, es imposible que el aparato en sí no absorba o pierda calor. Las paredes, el agitador, el termómetro y otros componentes del calorímetro tienen su propia capacidad calorífica. Para obtener mediciones precisas del calor de una reacción o proceso, es fundamental tener en cuenta el calor absorbido o liberado por el propio calorímetro. Aquí es donde el equivalente de agua del calorímetro se vuelve indispensable.
El equivalente de agua de un calorímetro es la masa de agua que tendría la misma capacidad calorífica que todas las partes del calorímetro que entran en contacto con el medio de reacción (generalmente agua). Al conocer este valor, los científicos pueden ajustar sus cálculos para contabilizar el calor que no fue absorbido por la sustancia principal, sino por el aparato. Esto se logra sumando el equivalente de agua del calorímetro a la masa de agua presente en el calorímetro, obteniendo una 'masa efectiva' de agua que representa toda la capacidad calorífica del sistema de medición.
Tipos de Calorímetro donde se Aplica:
Aunque el principio es el mismo, el equivalente de agua se aplica en diferentes tipos de calorímetros:
- Calorímetro de Bomba: Utilizado para medir el calor de combustión de compuestos. Consiste en un recipiente de acero resistente (la 'bomba') sumergido en un volumen conocido de agua. El equivalente de agua de este sistema incluiría la bomba, el agitador, el termómetro y el propio recipiente de agua.
- Calorímetro de Taza de Café: Un calorímetro más simple, a menudo hecho de vasos de poliestireno, utilizado para reacciones que ocurren a presión constante (como reacciones de neutralización o disolución). Aunque más sencillo, las tazas, la tapa y el termómetro también tienen un equivalente de agua que debe considerarse para mediciones precisas.
Determinación Experimental del Equivalente de Agua de un Calorímetro
La determinación experimental del equivalente de agua de un calorímetro es un procedimiento estándar en muchos laboratorios de química y física. El principio se basa en la ley de conservación de la energía, donde el calor perdido por un cuerpo caliente es igual al calor ganado por un cuerpo frío y el calorímetro. Aquí se describe un método común:
Procedimiento Típico:
- Paso 1: Preparación del Agua Caliente. Se toman 50 mL (o una masa conocida, mcaliente) de agua en un vaso de precipitados y se calienta a una temperatura elevada, por ejemplo, alrededor de 60°C. Esta es la temperatura inicial del agua caliente (Tcaliente_inicial).
- Paso 2: Preparación del Calorímetro con Agua Fría. Se mide una cantidad conocida de agua fría (mfría), por ejemplo, 50 mL, y se vierte en el calorímetro previamente pesado y vacío. Se registra la temperatura inicial del agua fría y del calorímetro (Tfría_inicial), asumiendo que están en equilibrio térmico.
- Paso 3: Transferencia y Equilibrio Térmico. Se transfiere rápidamente el agua caliente del vaso de precipitados al calorímetro que contiene el agua fría. Se cierra el calorímetro con la tapa, se inserta el termómetro y el agitador.
- Paso 4: Medición de la Temperatura Final. Se agita suavemente el contenido del calorímetro y se registra la temperatura de la mezcla a intervalos regulares (por ejemplo, cada 30 segundos) hasta que la temperatura se estabilice y alcance una temperatura final constante (Tfinal_mezcla). Esta es la temperatura de equilibrio del sistema (agua caliente + agua fría + calorímetro).
- Paso 5: Gráfico de Temperatura vs. Tiempo. Si se desea mayor precisión, se puede graficar la temperatura en función del tiempo para identificar la temperatura de equilibrio con mayor exactitud, compensando posibles pérdidas de calor al ambiente.
El principio subyacente es que el calor perdido por el agua caliente es absorbido por el agua fría y por el calorímetro. Matemáticamente, esto se expresa como:
Calor perdido por el agua caliente = Calor ganado por el agua fría + Calor ganado por el calorímetro
mcaliente ⋅ cagua ⋅ (Tcaliente_inicial - Tfinal_mezcla) = mfría ⋅ cagua ⋅ (Tfinal_mezcla - Tfría_inicial) + Wcalorímetro ⋅ cagua ⋅ (Tfinal_mezcla - Tfría_inicial)
Dado que el calor específico del agua (cagua) aparece en todos los términos, se puede simplificar (o se puede asumir que el equivalente de agua ya incorpora el cagua si se usa en unidades de masa):
mcaliente ⋅ (Tcaliente_inicial - Tfinal_mezcla) = (mfría + Wcalorímetro) ⋅ (Tfinal_mezcla - Tfría_inicial)
Despejando Wcalorímetro (el equivalente de agua del calorímetro), se puede calcular su valor. Este valor se utiliza luego en todos los experimentos posteriores realizados con ese calorímetro para corregir la absorción de calor del aparato.
Importancia y Aplicaciones
El concepto de equivalente de agua es de vital importancia en cualquier experimento calorimétrico que requiera una alta precisión. Sin él, las mediciones de calor serían imprecisas, ya que una parte significativa de la energía estaría siendo absorbida por el propio equipo de medición en lugar de por las sustancias de interés. Sus aplicaciones incluyen:
- Determinación de Calores de Reacción: Para calcular con precisión el calor de formación, combustión, neutralización o disolución de sustancias.
- Cálculo de Calores Específicos: Al conocer el equivalente de agua del calorímetro, se puede determinar el calor específico de otras sustancias con mayor exactitud.
- Estudios Termodinámicos: Fundamental para la investigación en termodinámica química y física, donde la cuantificación precisa de los cambios de energía es esencial.
Preguntas Frecuentes (FAQ)
¿Cuál es la diferencia entre equivalente de agua y calor específico?
El calor específico es una propiedad intensiva de una sustancia (no depende de la cantidad) que indica cuánto calor se necesita para elevar la temperatura de una unidad de masa de esa sustancia en un grado. Se expresa en J/g°C o cal/g°C. El equivalente de agua, por otro lado, es una propiedad extensiva (depende de la cantidad y del material del objeto) que representa la masa de agua que tiene la misma capacidad calorífica total que un objeto o una masa específica de una sustancia. Es una forma de "normalizar" la capacidad calorífica de un objeto con respecto al agua.
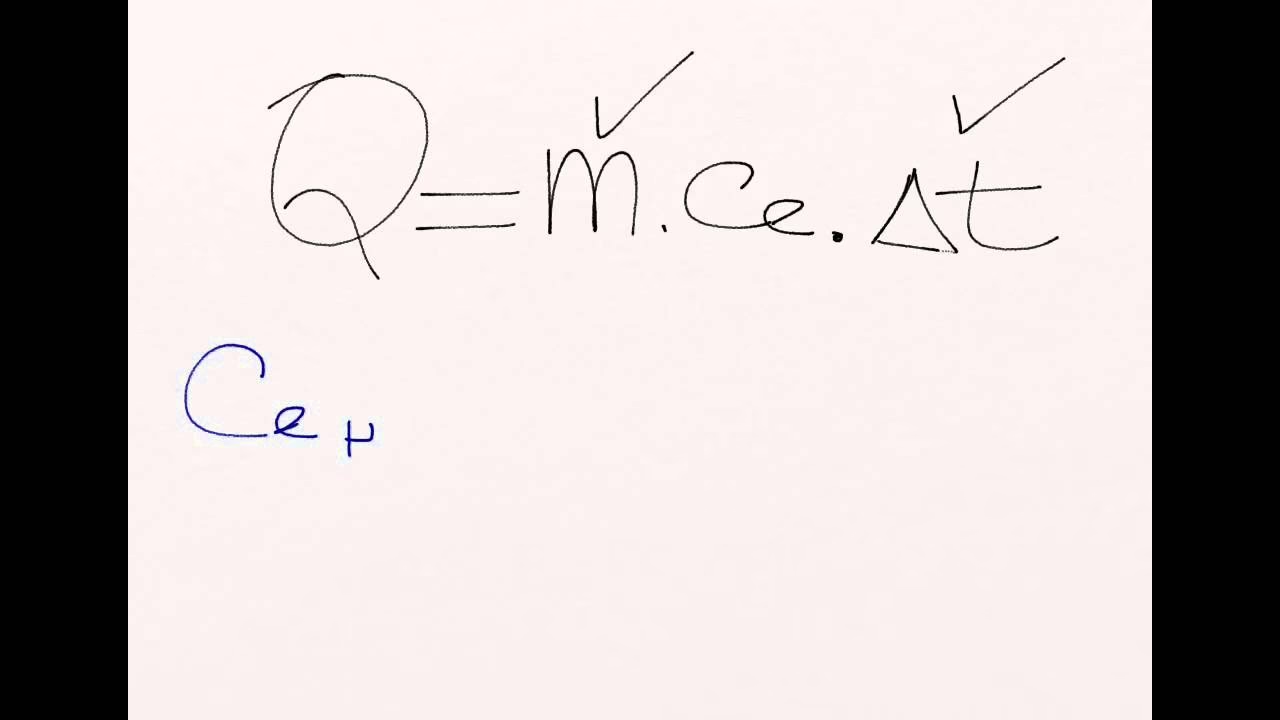
¿Por qué se usa el agua como referencia para el equivalente de agua?
El agua se utiliza como referencia por varias razones: tiene un calor específico relativamente alto, lo que la convierte en un excelente medio para absorber y liberar calor sin grandes cambios de temperatura; es abundante y fácil de obtener; y sus propiedades térmicas están muy bien caracterizadas y son conocidas con gran precisión en un amplio rango de temperaturas.
¿Puede el equivalente de agua ser cero?
No, el equivalente de agua de un objeto real nunca puede ser cero. Si un objeto tiene masa y está hecho de algún material con un calor específico distinto de cero, siempre tendrá una capacidad para absorber calor, lo que se traduce en un equivalente de agua distinto de cero. Un equivalente de agua de cero implicaría que el objeto no absorbe calor, lo cual es físicamente imposible para cualquier material real.
¿Es lo mismo el equivalente de agua termodinámico que la masa equivalente de agua en química?
No, son conceptos completamente diferentes, aunque la terminología pueda parecer similar y genere confusión. El "equivalente de agua" en termodinámica y calorimetría, como hemos discutido, se refiere a la masa de agua con la misma capacidad calorífica que un objeto o sustancia. La "masa equivalente de agua" o "peso equivalente" en química se refiere a la masa de una sustancia que reacciona con o es equivalente a una cantidad específica de otra sustancia en una reacción química particular (por ejemplo, la masa de un ácido que contiene un mol de iones H+ que pueden ser neutralizados). El ejemplo de "El peso molecular del H₂O es de 18 gramos. Su factor n es 2. Su peso equivalente es 18/2 = 9 g" se refiere a este último concepto químico, que no está relacionado con la absorción de calor o la calorimetría.
Conclusión
El equivalente de agua es un concepto fundamental en el campo de la calorimetría, proporcionando una forma práctica y estandarizada de cuantificar la capacidad de un sistema (ya sea una sustancia o un aparato) para absorber calor. Al expresar esta capacidad en términos de una masa equivalente de agua, los científicos pueden realizar mediciones de calor más precisas y fiables, compensando la absorción de energía por parte del propio equipo. Desde los pioneros como Joseph Black hasta las aplicaciones modernas en laboratorios de investigación y desarrollo, el equivalente de agua sigue siendo una herramienta indispensable para desentrañar los misterios de las transformaciones energéticas en el universo.
Si quieres conocer otros artículos parecidos a Equivalente de Agua: Un Concepto Esencial en Calorimetría puedes visitar la categoría Cálculos.
