21/05/2025
En el fascinante mundo de la química y la física, la forma en que las soluciones conducen la electricidad es un campo de estudio crucial. Particularmente, la conductividad de los electrolitos, sustancias que se disocian en iones cuando se disuelven, juega un papel vital en innumerables procesos, desde las baterías hasta las reacciones biológicas. Sin embargo, no todos los electrolitos se comportan de la misma manera. Mientras que los electrolitos fuertes se disocian completamente, los débiles presentan un desafío único, especialmente cuando se intenta determinar su conductividad en condiciones de dilución extrema. Es aquí donde la ingeniosa Ley de Kohlrausch emerge como una herramienta indispensable, permitiéndonos desvelar el comportamiento de estas sustancias cuando su concentración se acerca a cero.
La dilución infinita representa una condición idealizada donde las interacciones entre los iones son mínimas, permitiendo que cada ion contribuya de manera independiente a la conductividad total. Comprender cómo se comportan los electrolitos, y en particular los electrolitos débiles, bajo estas circunstancias es fundamental para predecir su comportamiento en soluciones de baja concentración y para aplicaciones prácticas en diversos campos científicos e industriales.
- ¿Qué es la Conductividad Molar?
- La Conductividad Molar a Dilución Infinita: Un Valor Límite
- La Ley de Kohlrausch: La Clave para Electrolitos Débiles
- ¿Cómo se Mide la Conductividad de una Disolución?
- Preguntas Frecuentes
- ¿Cuál es la conductividad equivalente de un electrolito débil en dilución infinita?
- ¿Cómo se diferencia la conductividad molar de un electrolito fuerte de uno débil a dilución infinita?
- ¿Por qué no se puede extrapolar la conductividad molar de un electrolito débil para obtener su valor a dilución infinita?
- ¿Cuáles son las unidades de la conductividad molar?
- ¿Cómo se calcula la constante de celda en la medición de conductividad?
¿Qué es la Conductividad Molar?
Antes de sumergirnos en la Ley de Kohlrausch y su aplicación a los electrolitos débiles, es esencial comprender el concepto de conductividad molar. La conductividad molar, representada como Λm, es una medida de la eficiencia con la que un electrolito dado transporta la corriente eléctrica en una disolución. Se define como la conductividad (κ) de la disolución dividida por la concentración estequiométrica molar (c) del electrolito. Es decir:
Λm = κ / c
Esta magnitud no solo depende del electrolito en sí, sino también del disolvente en el que está disuelto. Nos indica la conductancia de un volumen de solución que contiene un mol de electrolito, situado entre dos electrodos de área unitaria y separados por una distancia unitaria. A medida que la concentración de una disolución electrolítica disminuye, su conductividad molar tiende a aumentar. Esto se debe a que, a menor concentración, el volumen total que contiene un mol de electrolito es mayor, y las interacciones interiónicas que podrían obstaculizar el movimiento de los iones son significativamente reducidas, permitiendo que los iones se muevan con mayor libertad y eficiencia.
Las unidades de la conductividad molar en el Sistema Internacional (SI) son S m2 mol-1 (Siemens metro cuadrado por mol). Para ponerlo en perspectiva, si la conductividad de una disolución acuosa de KCl de 1,00 mol dm-3 a 25 ºC es 0,112 S cm-1, su conductividad molar se calcularía convirtiendo las unidades adecuadamente, obteniendo un valor que refleja su capacidad de conducción por cada mol de electrolito presente.
La Conductividad Molar a Dilución Infinita: Un Valor Límite
El concepto de dilución infinita es crítico. Se refiere al valor de la conductividad molar cuando la concentración del electrolito se aproxima a cero (c → 0). Este valor límite se conoce como conductividad molar límite o conductividad molar a dilución infinita, y se denota como Λm°. Para los electrolitos fuertes, aquellos que se disocian completamente en iones en solución, determinar Λm° es relativamente sencillo. Se puede obtener graficando la conductividad molar (Λm) frente a la raíz cuadrada de la concentración (c1/2) y extrapolando la línea recta resultante hasta c1/2 = 0. Esta relación lineal es una característica distintiva de los electrolitos fuertes en soluciones diluidas.
Sin embargo, la situación cambia drásticamente para los electrolitos débiles. A diferencia de los fuertes, los electrolitos débiles se disocian solo parcialmente en solución. Su grado de disociación (α) aumenta significativamente a medida que la solución se diluye, ya que hay más espacio para que los iones se separen y menos oportunidades para que se recombinen. Esto provoca que la conductividad molar de un electrolito débil aumente de forma muy pronunciada a bajas concentraciones. Como resultado, la gráfica de Λm frente a c1/2 para un electrolito débil no es una línea recta, sino una curva que asciende bruscamente a medida que la concentración disminuye. Por lo tanto, la extrapolación directa a concentración cero no es un método viable ni preciso para determinar su conductividad molar límite (Λm°).
La Ley de Kohlrausch: La Clave para Electrolitos Débiles
Fue el físico y químico alemán Friedrich Kohlrausch quien, a finales del siglo XIX, observó regularidades en los valores de las conductividades molares límite de los electrolitos fuertes. Basándose en sus observaciones, propuso una ley fundamental que hoy lleva su nombre: la Ley de Kohlrausch, también conocida como la Ley de Migración Independiente de los Iones.
La Ley de Kohlrausch establece que la conductividad molar límite de un electrolito (ya sea fuerte o débil) es igual a la suma de las contribuciones individuales de las conductividades iónicas límite de sus cationes y aniones constituyentes. En otras palabras, en dilución infinita, cuando las interacciones interiónicas son prácticamente inexistentes, cada ion se mueve y contribuye a la conductividad total de manera independiente de los demás iones presentes en la solución.
Matemáticamente, la Ley de Kohlrausch se expresa como:
Λm° = ν+λ+° + ν-λ-°
Donde:
- Λm° es la conductividad molar límite del electrolito.
- ν+ y ν- son el número de moles de cationes y aniones, respectivamente, que se forman por la disociación de un mol del electrolito.
- λ+° y λ-° son las conductividades iónicas límite de los cationes y aniones, respectivamente.
Por ejemplo, la conductividad molar límite del cloruro de sodio (NaCl), un electrolito fuerte, puede determinarse sumando las conductividades iónicas límite del ion sodio (Na+) y del ion cloruro (Cl-). Los datos experimentales muestran que la conductividad molar a dilución infinita para NaCl es aproximadamente 12.556 S·m2/mol.
Aplicaciones Cruciales de la Ley de Kohlrausch
La Ley de Kohlrausch no es solo un principio teórico; tiene aplicaciones prácticas de enorme importancia, especialmente en el estudio de los electrolitos débiles:
Determinación de la Conductividad Molar Límite (Λm°) para Electrolitos Débiles:
Como mencionamos, la extrapolación directa no funciona para los electrolitos débiles. La Ley de Kohlrausch proporciona una solución elegante. Podemos calcular la Λm° de un electrolito débil utilizando los valores de las conductividades iónicas límite de sus iones, que a menudo se obtienen de electrolitos fuertes que comparten esos iones. Por ejemplo, para determinar la Λm° del ácido acético (un electrolito débil), se podría usar la Λm° de electrolitos fuertes como el HCl, el CH3COONa y el NaCl, aplicando la ley de aditividad.
Cálculo del Grado de Disociación (α):
La ley de Kohlrausch permite calcular el grado de disociación (α) de un electrolito débil a una concentración dada. El grado de disociación es la fracción del electrolito que se ha disociado en iones. Se calcula como la relación entre la conductividad molar (Λm) a una concentración dada y la conductividad molar límite (Λm°):
α = Λm / Λm°
Este valor es fundamental para comprender el comportamiento de los electrolitos débiles en solución.

El documento presenta datos experimentales sobre la conductividad de NaCl en solución acuosa para diferentes concentraciones. Incluye un gráfico de \u039b vs C1/2 y una regresión lineal basada en la Ley de Kolrausch, que muestra que la conductividad molar a dilución infinita es de 12.556 S·m/mol. Cálculo de la Constante de Disociación (Ka o Kb):
Una vez que se conoce el grado de disociación (α) y la concentración (c) del electrolito débil, se puede calcular su constante de disociación (Ka para ácidos débiles o Kb para bases débiles) utilizando la ley de dilución de Ostwald. Para un electrolito débil AB que se disocia en A+ y B-:
K = (cα2) / (1 - α)
Esta constante es una medida de la fuerza del electrolito débil.
Cálculo de la Solubilidad de Sales Poco Solubles:
La ley de Kohlrausch también puede aplicarse para determinar la solubilidad de sales que son muy poco solubles en agua. Dado que la conductividad de una solución saturada de una sal poco soluble se debe únicamente a los iones de esa sal, y su concentración es muy baja (casi dilución infinita), la conductividad molar de la sal en su solución saturada es prácticamente igual a su conductividad molar límite. Así, midiendo la conductividad de la solución saturada y conociendo la Λm° de la sal (calculada a partir de las conductividades iónicas límite de sus iones), se puede determinar la concentración de la sal disuelta, que es su solubilidad.
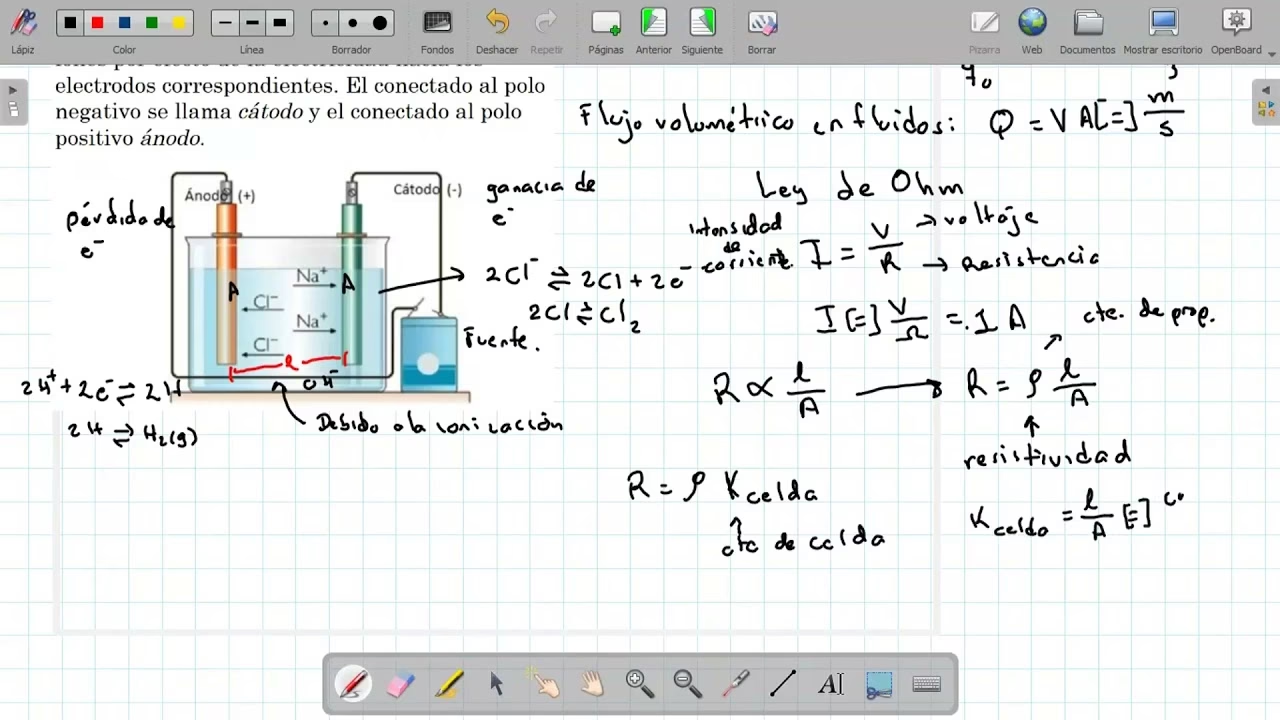
¿Cómo se Mide la Conductividad de una Disolución?
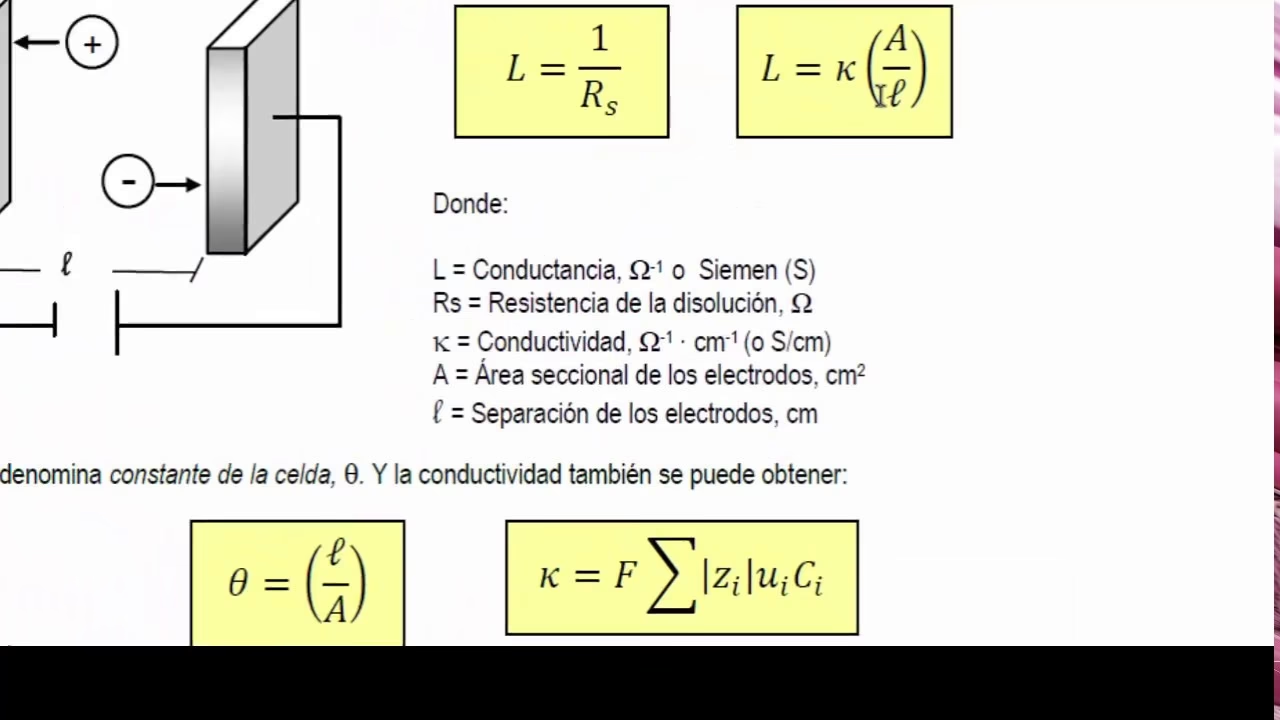
La medición de la conductividad de una disolución se realiza utilizando un conductímetro, que consta de una celda de conductividad y un puente de Wheatstone o un circuito electrónico similar. La celda de conductividad generalmente tiene dos electrodos de platino platinizado (cubiertos con una capa de negro de platino para aumentar su superficie y reducir efectos de polarización) de área conocida y separados por una distancia fija. La resistencia de la disolución entre estos electrodos se mide, y la conductancia (inversa de la resistencia) se calcula. La conductividad específica (κ) de la disolución se obtiene multiplicando la conductancia medida por la constante de la celda (Kcelda).
La constante de la celda es una propiedad geométrica de la celda de conductividad (relación entre la distancia entre los electrodos y el área de los electrodos). Para determinar la constante de la celda, se mide la conductividad de una disolución patrón de KCl (cloruro de potasio) de concentración conocida y conductividad específica bien establecida a una temperatura específica. La constante de la celda se calcula entonces como Kcelda = κestándar / Cestándar, donde κestándar es la conductividad específica conocida de la disolución patrón y Cestándar es la conductancia medida de la disolución patrón.
Preguntas Frecuentes
¿Cuál es la conductividad equivalente de un electrolito débil en dilución infinita?
La conductividad equivalente de un electrolito débil en dilución infinita (Λeq°) es igual a la suma de las conductividades iónicas límite de sus iones constituyentes (cationes y aniones), ponderadas por sus respectivas valencias, si se usa la definición de conductividad equivalente. Sin embargo, la Ley de Kohlrausch, tal como se aplica generalmente hoy en día, se refiere más comúnmente a la conductividad molar límite (Λm°), que es la suma de las conductividades iónicas límite de los cationes y aniones multiplicadas por el número de moles de cada ion producido por la disociación de un mol de electrolito. Para un electrolito débil, este valor no puede obtenerse por extrapolación directa, sino que se calcula utilizando los valores de conductividad iónica límite de los iones individuales, que a menudo se derivan de datos de electrolitos fuertes.

¿Cómo se diferencia la conductividad molar de un electrolito fuerte de uno débil a dilución infinita?
Ambos electrolitos, fuertes y débiles, alcanzan su máxima conductividad molar a dilución infinita, ya que las interacciones interiónicas son mínimas y la movilidad iónica es máxima. La diferencia fundamental radica en cómo se llega a este valor y cómo se comporta su conductividad molar a concentraciones intermedias. Para los electrolitos fuertes, la conductividad molar aumenta linealmente con la raíz cuadrada de la concentración decreciente, permitiendo una extrapolación directa. Para los electrolitos débiles, la conductividad molar aumenta drásticamente a bajas concentraciones debido al aumento del grado de disociación, lo que hace inviable la extrapolación directa. La Ley de Kohlrausch es la herramienta clave para determinar la conductividad molar límite de los electrolitos débiles.
¿Por qué no se puede extrapolar la conductividad molar de un electrolito débil para obtener su valor a dilución infinita?
La extrapolación no funciona para los electrolitos débiles porque su grado de disociación (α) no es constante y aumenta significativamente a medida que la concentración disminuye. A medida que se diluye un electrolito débil, más de sus moléculas se disocian en iones. Este aumento en el número de portadores de carga (iones) provoca un aumento no lineal y muy pronunciado de la conductividad molar a bajas concentraciones, lo que impide una extrapolación lineal fiable a concentración cero.
¿Cuáles son las unidades de la conductividad molar?
Las unidades de la conductividad molar en el Sistema Internacional (SI) son Siemens metro cuadrado por mol (S m2 mol-1). También se pueden expresar en unidades más fundamentales como kg-1 s3 A2 mol-1.
¿Cómo se calcula la constante de celda en la medición de conductividad?
La constante de celda (Kcelda) se calcula midiendo la conductancia (C) de una disolución patrón de conductividad específica (κ) conocida. La fórmula para la constante de celda es Kcelda = κ / C. Por ejemplo, se utiliza una disolución de KCl de concentración y temperatura conocidas, cuya conductividad específica es un valor estándar bien establecido.
En resumen, la Ley de Kohlrausch es un pilar fundamental en la electroquímica, especialmente para comprender el comportamiento de los electrolitos débiles. Nos proporciona los medios para determinar sus propiedades a dilución infinita, lo que de otro modo sería imposible mediante métodos directos. Esta ley no solo enriquece nuestra comprensión teórica de la migración iónica, sino que también ofrece herramientas prácticas para calcular el grado y la constante de disociación, elementos clave para caracterizar y aplicar estos importantes compuestos en diversas áreas de la ciencia y la tecnología.
Si quieres conocer otros artículos parecidos a Kohlrausch: La Conductividad de Electrolitos Débiles puedes visitar la categoría Cálculos.
