29/03/2023
En el vasto universo de la bioquímica, las enzimas son los catalizadores incansables que impulsan la vida. Entender cómo funcionan, a qué velocidad operan y cuán eficientemente interactúan con sus sustratos es fundamental para desentrañar los misterios de los procesos biológicos. Aquí es donde entran en juego dos parámetros cruciales: la constante de Michaelis (Km) y la velocidad máxima (Vmax). Estos valores no solo nos dan una idea de la eficiencia de una enzima, sino que también son vitales para aplicaciones en medicina, farmacología e industria. A menudo, el desafío reside en cómo determinar estos valores de forma precisa a partir de datos experimentales, y es aquí donde herramientas como Microsoft Excel se convierten en aliados indispensables, especialmente al aplicar métodos de linealización como el gráfico de Lineweaver-Burk.
Es importante aclarar que, aunque la abreviatura “Km” puede evocar la idea de “kilómetros” en otros contextos, en el ámbito de la bioquímica, Km se refiere exclusivamente a la constante de Michaelis, un parámetro fundamental en la cinética enzimática, y no tiene relación alguna con el control de kilometraje de vehículos. Este artículo se centrará únicamente en la determinación y significado de Km y Vmax en el contexto de las reacciones enzimáticas.
Desentrañando Km y Vmax: Los Pilares de la Cinética Enzimática
La actividad enzimática se describe mediante una relación entre la velocidad de reacción y la concentración de sustrato. Para la mayoría de las enzimas, esta relación es de naturaleza hiperbólica. Al principio, a bajas concentraciones de sustrato, la velocidad de reacción aumenta drásticamente con cada incremento en la concentración de sustrato. Esto se debe a que los sitios catalíticos de la enzima están disponibles y esperando para unirse al sustrato. La velocidad está limitada por la disponibilidad de sustrato.
Sin embargo, a medida que la concentración de sustrato sigue aumentando, la enzima comienza a saturarse. Llega un punto en el que los sitios catalíticos están casi siempre ocupados. En este estado, la velocidad de formación del producto ya no depende de la concentración de sustrato, sino de la eficiencia intrínseca de la enzima para procesar el sustrato unido. La adición de más sustrato no aumentará significativamente la velocidad de reacción. Esta velocidad máxima alcanzada cuando la enzima está saturada se conoce como la velocidad máxima (Vmax).
La constante de Michaelis (Km), por otro lado, es una medida inversa de la afinidad de la enzima por su sustrato. En términos prácticos, Km es la concentración de sustrato a la cual la enzima alcanza la mitad de su velocidad máxima (0.5 Vmax). Una enzima con un Km bajo indica una alta afinidad por su sustrato, lo que significa que puede alcanzar la mitad de su Vmax a una concentración de sustrato relativamente baja. Por el contrario, un Km alto sugiere una baja afinidad, requiriendo una mayor concentración de sustrato para lograr la mitad de su Vmax.
La Importancia de Determinar Km y Vmax
La determinación de Km y Vmax es vital por varias razones:
- Predicción del comportamiento enzimático: Conocer el Km de una enzima en relación con la concentración fisiológica de su sustrato permite predecir si la velocidad de formación del producto se verá afectada por la disponibilidad del sustrato. Si el Km es bajo en comparación con la concentración fisiológica, la enzima estará normalmente saturada y operará a una velocidad constante. Si el Km es alto, su actividad variará con la concentración de sustrato.
- Estudios de competencia: Si varias enzimas compiten por el mismo sustrato en diferentes vías metabólicas, los valores de Km y Vmax para cada una permiten predecir el destino metabólico del sustrato y cuánto fluirá a través de cada vía bajo diversas condiciones.
- Cuantificación de enzimas: Para determinar la cantidad de una enzima en una muestra de tejido, es crucial asegurar que la actividad medida sea la limitante, no la disponibilidad de sustrato. Esto significa que la concentración de sustrato debe ser lo suficientemente alta para que la enzima actúe a Vmax (generalmente 10-20 veces el Km).
- Diseño de ensayos: Si una enzima se utiliza para medir la concentración de un sustrato en una muestra (como la glucosa oxidasa para medir la glucosa en plasma), el sustrato debe ser el factor limitante. Esto implica que la concentración de sustrato debe estar por debajo del Km, para que la velocidad de formación del producto aumente pronunciadamente con el aumento de la concentración de sustrato, proporcionando un ensayo sensible.
La Ecuación de Michaelis-Menten y el Desafío de la Linealización
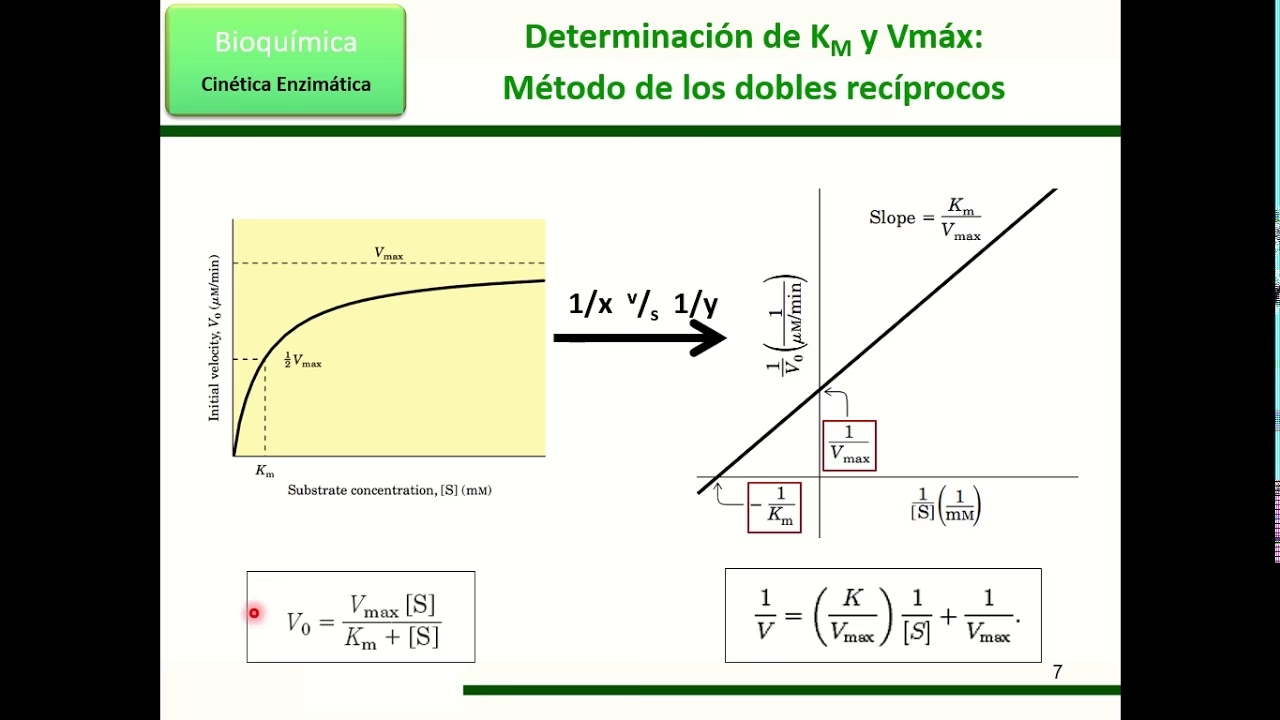
La relación entre la velocidad de reacción (v), la concentración de sustrato ([S]), Km y Vmax se describe mediante la ecuación de Michaelis-Menten:
v = (Vmax * [S]) / (Km + [S])
Aunque esta ecuación describe con precisión el comportamiento enzimático, la representación gráfica directa de v frente a [S] produce una curva hiperbólica. Ajustar la "mejor" hipérbola a los puntos experimentales y estimar Vmax (el límite de la hipérbola a concentración infinita de sustrato) con precisión puede ser notoriamente difícil. Para superar esta dificultad, se han desarrollado varias transformaciones de la ecuación de Michaelis-Menten que linealizan los datos, permitiendo un ajuste más preciso a los puntos experimentales y una estimación más fiable de Km y Vmax.

El Gráfico de Lineweaver-Burk: La Transformación Doble Recíproca
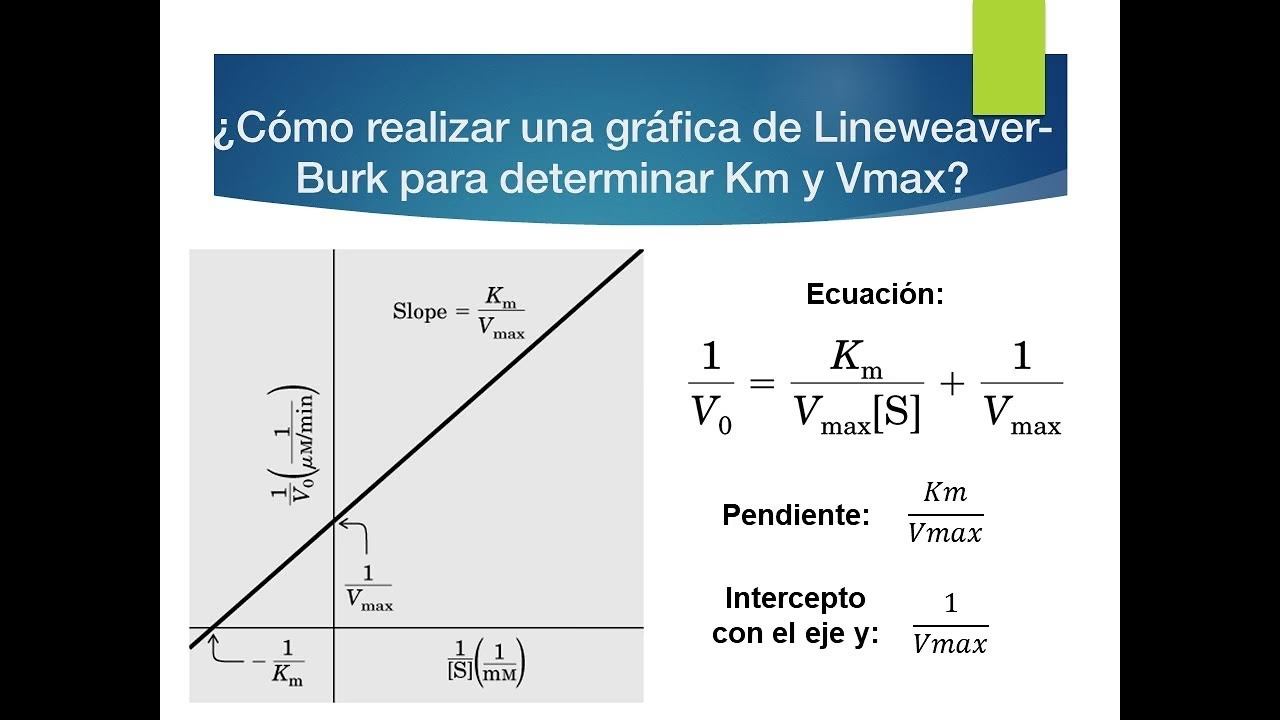
El gráfico de Lineweaver-Burk, también conocido como el gráfico de doble recíproco, es la transformación lineal más utilizada de la ecuación de Michaelis-Menten. Reorganiza la ecuación de la siguiente manera:
1/v = (1/Vmax) + (Km/Vmax) * (1/[S])
Al graficar el recíproco de la velocidad de reacción (1/v) en el eje Y contra el recíproco de la concentración de sustrato (1/[S]) en el eje X, se obtiene una línea recta. Esta linealización facilita enormemente la determinación de Km y Vmax a partir de las intersecciones y la pendiente de la línea:
- La intersección con el eje Y (cuando 1/[S] es 0) es igual a 1/Vmax.
- La intersección con el eje X (cuando 1/v es 0) es igual a -1/Km.
- La pendiente de la línea es igual a Km/Vmax.
Ventajas: Es el método más utilizado y generalmente ofrece la mejor precisión para las estimaciones de Km y Vmax.
Desventajas: Su principal inconveniente es que da un peso desproporcionado a los puntos obtenidos a bajas concentraciones de sustrato (que corresponden a los valores más altos de 1/[S] y 1/v). Estos son precisamente los puntos donde la precisión en la determinación de la velocidad de reacción suele ser menor debido a la pequeña cantidad de producto formado, lo que puede amplificar los errores experimentales.
Otras Métodos de Linealización: Eadie-Hofstee y Hanes
Aunque el gráfico de Lineweaver-Burk es el más popular, existen otras linealizaciones que buscan mitigar sus desventajas:
Gráfico de Eadie-Hofstee
Esta transformación reorganiza la ecuación de Michaelis-Menten como:
v = Vmax - Km * (v/[S])
Al graficar v en el eje Y contra v/[S] en el eje X, se obtiene una línea recta:
- La intersección con el eje Y es Vmax.
- La pendiente de la línea es -Km.
- La intersección con el eje X es Vmax/Km.
Ventajas: Supera el problema del espaciado desigual de los puntos y el peso excesivo a bajas concentraciones de sustrato.
Desventajas: Utiliza la variable dependiente (v) en ambos ejes, lo que puede multiplicar los errores en la medición de la velocidad de reacción, resultando en una menor precisión en las estimaciones de Km y Vmax.
Gráfico de Hanes
Esta transformación reorganiza la ecuación de Michaelis-Menten como:
[S]/v = (Km/Vmax) + ([S]/Vmax)
Al graficar [S]/v en el eje Y contra [S] en el eje X, se obtiene una línea recta:
- La intersección con el eje Y es Km/Vmax.
- La pendiente de la línea es 1/Vmax.
- La intersección con el eje X es -Km.
Ventajas: También aborda el problema del espaciado desigual de los puntos y el peso excesivo a bajas concentraciones de sustrato.
Desventajas: Utiliza la concentración de sustrato ([S]) en ambos ejes. Esto significa que los errores de pipeteo o en la determinación de la concentración real del sustrato se multiplican, lo que puede reducir la precisión de las estimaciones de Km y Vmax.

A pesar de estas desventajas, cada método tiene su lugar y puede ser útil dependiendo de la naturaleza de los datos experimentales y los errores asociados.
Cómo Calcular Km y Vmax en Excel Usando el Gráfico de Lineweaver-Burk
Microsoft Excel es una herramienta poderosa y accesible para realizar análisis cinéticos enzimáticos. A continuación, se detalla una guía paso a paso para determinar Km y Vmax utilizando el método de Lineweaver-Burk en Excel:
Paso 1: Preparar los Datos Experimentales
Necesitarás datos de velocidad de reacción (v) a diferentes concentraciones de sustrato ([S]). Organiza tus datos en dos columnas en Excel, por ejemplo:
Columna A: Concentración de Sustrato ([S])
Columna B: Velocidad de Reacción (v)
Luego, debes calcular los recíprocos de estos valores para el gráfico de Lineweaver-Burk:
Columna C (1/[S]): En la celda C2, escribe la fórmula =1/A2 y arrastra hacia abajo para aplicarla a todas tus concentraciones de sustrato.
Columna D (1/v): En la celda D2, escribe la fórmula =1/B2 y arrastra hacia abajo para aplicarla a todas tus velocidades de reacción.
Asegúrate de que tus datos de [S] y v estén en unidades consistentes (por ejemplo, micromolar para [S] y micromolar/minuto para v) para que Km y Vmax tengan unidades significativas.
Paso 2: Crear el Gráfico de Dispersión (Lineweaver-Burk Plot)
- Selecciona los datos: Resalta las columnas C (1/[S]) y D (1/v). Es crucial que la columna de 1/[S] sea la primera que selecciones, ya que será el eje X.
- Insertar gráfico de dispersión: Ve a la pestaña "Insertar" en la cinta de opciones de Excel. En el grupo "Gráficos", haz clic en "Dispersión" y elige el tipo de gráfico de dispersión simple (solo puntos).
- Personaliza los ejes (Opcional pero recomendado):
- Haz clic en el gráfico. Ve a la pestaña "Diseño de gráfico". Haz clic en "Agregar elemento de gráfico" > "Títulos de eje" > "Horizontal principal" y etiqueta el eje X como "1/[S] (1/µM)".
- Haz clic en "Agregar elemento de gráfico" > "Títulos de eje" > "Vertical principal" y etiqueta el eje Y como "1/v (min/µM)".
- También puedes agregar un título al gráfico, como "Gráfico de Lineweaver-Burk".
Paso 3: Añadir la Línea de Tendencia y la Ecuación
- Selecciona los puntos de datos: Haz clic con el botón derecho en cualquiera de los puntos de datos en el gráfico.
- Agregar línea de tendencia: En el menú contextual que aparece, selecciona "Agregar línea de tendencia...".
- Configurar la línea de tendencia: Se abrirá un panel lateral "Formato de línea de tendencia".
- Asegúrate de que la opción "Lineal" esté seleccionada.
- Marca las casillas "Mostrar ecuación en el gráfico" y "Mostrar valor R cuadrado en el gráfico". El valor R cuadrado te dará una idea de qué tan bien se ajustan tus datos a una línea recta (cuanto más cerca de 1, mejor).
Paso 4: Extraer Km y Vmax de la Ecuación de la Línea de Tendencia
En el gráfico, verás la ecuación de la línea de tendencia en el formato y = mx + b. Para el gráfico de Lineweaver-Burk, esto se traduce a:
1/v = (pendiente) * (1/[S]) + (intersección Y)
Donde:
m(la pendiente) es igual a Km/Vmax.b(la intersección con el eje Y) es igual a 1/Vmax.
Ahora, puedes calcular Km y Vmax:
- Calcular Vmax: Como
b = 1/Vmax, entoncesVmax = 1/b. Simplemente divide 1 por el valor de la intersección Y que aparece en la ecuación de la línea de tendencia. - Calcular Km: Como
m = Km/Vmax, entoncesKm = m * Vmax. Multiplica la pendiente (m) por el valor de Vmax que acabas de calcular. Alternativamente, puedes usar la relación de la intersección X. La intersección X es-b/m. Dado que la intersección X también es-1/Km, entonces-1/Km = -b/m, lo que significaKm = m/b. Ambos métodos deberían darte el mismo resultado para Km.
Ejemplo: Si la ecuación de tu línea de tendencia es y = 0.5x + 0.02:
- Intersección Y (b) = 0.02
- Pendiente (m) = 0.5
Cálculos:
- Vmax = 1 / 0.02 = 50
- Km = 0.5 * 50 = 25 (o Km = 0.5 / 0.02 = 25)
Recuerda incluir las unidades apropiadas para Km y Vmax basadas en las unidades de tus datos originales.
Aplicaciones Prácticas de la Determinación de Km y Vmax
El dominio de estas técnicas no es meramente académico; tiene repercusiones profundas en diversos campos:
- Diseño de Fármacos: Comprender el Km y Vmax de una enzima diana es fundamental para diseñar fármacos que actúen como inhibidores o activadores. Los inhibidores enzimáticos son la base de muchos medicamentos modernos, desde antibióticos hasta tratamientos contra el cáncer. Un fármaco puede ser diseñado para tener una alta afinidad (bajo Km aparente) por la enzima diana o para afectar su velocidad máxima.
- Diagnóstico de Enfermedades: Las alteraciones en los valores de Km o Vmax de ciertas enzimas pueden ser indicadores de enfermedades metabólicas o disfunciones orgánicas. Por ejemplo, en algunos trastornos genéticos, una enzima puede producirse con una Km más alta de lo normal, lo que significa que requiere más sustrato para funcionar eficientemente.
- Biotecnología e Industria: En la producción de productos químicos, alimentos o biocombustibles, las enzimas se utilizan como catalizadores industriales. Optimizar las condiciones de reacción para maximizar la producción implica conocer y controlar el Km y Vmax de las enzimas utilizadas. Esto asegura que los procesos sean lo más eficientes y rentables posible.
- Estudios de Mecanismos de Reacción: La cinética enzimática, y en particular el análisis de Lineweaver-Burk, es una herramienta poderosa para estudiar el mecanismo de acción de las enzimas, incluyendo la identificación de estados intermedios y la caracterización de inhibidores.
Preguntas Frecuentes (FAQs) sobre Km y Vmax
Aquí respondemos algunas de las preguntas más comunes relacionadas con la determinación de Km y Vmax y el uso del gráfico de Lineweaver-Burk:
1. ¿Qué representa Km en la cinética enzimática?
Km, la constante de Michaelis, es la concentración de sustrato a la cual la velocidad de reacción enzimática es la mitad de la velocidad máxima (Vmax). Es una medida inversa de la afinidad de la enzima por su sustrato: un Km bajo indica una alta afinidad, mientras que un Km alto sugiere una baja afinidad.

2. ¿Qué indica Vmax?
Vmax, la velocidad máxima, es la velocidad máxima de reacción que una enzima puede alcanzar cuando está completamente saturada con su sustrato. Representa la velocidad intrínseca de la enzima para convertir el sustrato en producto, asumiendo que hay una cantidad ilimitada de sustrato disponible.
3. ¿Por qué se utiliza el gráfico de Lineweaver-Burk en lugar de la curva directa?
El gráfico de Lineweaver-Burk linealiza la relación hiperbólica entre la velocidad de reacción y la concentración de sustrato descrita por la ecuación de Michaelis-Menten. Esto facilita la determinación precisa de Km y Vmax a partir de las intersecciones y la pendiente de una línea recta, que son más fáciles de ajustar y analizar que una curva hiperbólica.
4. ¿Cómo obtengo Km y Vmax a partir de la ecuación de la línea de tendencia en Excel?
Una vez que Excel te proporciona la ecuación de la línea de tendencia en el formato y = mx + b (donde y = 1/v y x = 1/[S]), puedes calcularlos así: Vmax se calcula como 1/b (el recíproco de la intersección Y). Km se calcula como m * Vmax (la pendiente multiplicada por la Vmax calculada) o directamente como m/b.
5. ¿Existen otros métodos para determinar Km y Vmax?
Sí, además del Lineweaver-Burk, existen otros gráficos de linealización como el gráfico de Eadie-Hofstee (v vs. v/[S]) y el gráfico de Hanes ([S]/v vs. [S]). Cada uno tiene sus propias ventajas y desventajas en cuanto a la distribución de errores experimentales, pero todos buscan linealizar la ecuación de Michaelis-Menten para una determinación más sencilla de Km y Vmax.
En resumen, la determinación de Km y Vmax es un pilar de la bioquímica y su comprensión es esencial para cualquier estudio de enzimas. Con herramientas como Microsoft Excel y la aplicación correcta de métodos de linealización como el gráfico de Lineweaver-Burk, transformar datos experimentales en valiosos parámetros cinéticos es un proceso claro y accesible, abriendo puertas a una comprensión más profunda de la vida a nivel molecular.
Si quieres conocer otros artículos parecidos a Calculando Km y Vmax con Excel: Enzimas al Límite puedes visitar la categoría Cálculos.