08/03/2024
La comprensión de la relación entre la presión, el volumen y la temperatura de los gases es una piedra angular de la física y la química. Desde el siglo XVII, impulsados por la curiosidad científica y la ambición de volar en globos, diversos científicos se dedicaron a desentrañar estas complejas interacciones. Aunque sus mediciones iniciales no eran tan precisas como las actuales, lograron establecer relaciones matemáticas fundamentales que describen el comportamiento de los gases, especialmente en un modelo hipotético conocido como gas ideal. Estas leyes individuales, con el tiempo, se fusionaron en una única y potente ecuación: la Ley de los Gases Ideales, una herramienta indispensable para predecir el comportamiento de los gases bajo diversas condiciones. En este artículo, exploraremos cómo la temperatura y el volumen impactan directamente en la presión de un gas, y cómo utilizar las fórmulas clave para realizar cálculos precisos.

- Las Raíces Históricas de la Comprensión de los Gases
- La Ley de Amontons (o Ley de Gay-Lussac): Presión y Temperatura
- La Ley de Charles: Volumen y Temperatura
- La Ley de Boyle: Volumen y Presión
- La Ley de Avogadro: Volumen y Cantidad de Gas
- La Ley de los Gases Ideales: Unificando las Piezas
- La Ley de los Gases Combinados: Un Escenario Más Completo
- Aplicaciones Prácticas de las Leyes de los Gases
- Tabla Resumen de las Leyes de los Gases
- Preguntas Frecuentes (FAQ)
- Conclusión
Las Raíces Históricas de la Comprensión de los Gases
La fascinación por los gases no es nueva. Figuras como Robert Boyle, Jacques Charles, Guillaume Amontons y Amedeo Avogadro sentaron las bases para nuestro entendimiento actual. Sus experimentos, a menudo ingeniosos para su época, revelaron cómo la presión, el volumen, la temperatura y la cantidad de gas están intrínsecamente conectados. Estos descubrimientos no solo avanzaron el conocimiento científico, sino que también tuvieron aplicaciones prácticas inesperadas, como el desarrollo de los primeros globos aerostáticos, que asombraron al mundo y demostraron el poder de estas nuevas teorías.
La Ley de Amontons (o Ley de Gay-Lussac): Presión y Temperatura
Imagina un recipiente rígido y sellado que contiene un gas. Si enfrías este recipiente, la presión del gas en su interior disminuye. Por el contrario, si lo calientas, la presión aumenta. Esta observación empírica, donde el volumen y la cantidad de gas se mantienen constantes, fue establecida por Guillaume Amontons y refinada por Joseph Louis Gay-Lussac. Esta ley establece que la presión de una cantidad fija de gas es directamente proporcional a su temperatura en la escala Kelvin, siempre que el volumen se mantenga constante.
Matemáticamente, se expresa como:
- P ∝ T
- P = k × T
- O, para dos condiciones diferentes (1 y 2): P₁/T₁ = P₂/T₂
Donde 'k' es una constante de proporcionalidad y 'T' debe estar siempre en Kelvin. El cero absoluto (0 K o -273.15 °C) es la temperatura más baja posible, donde la presión teóricamente sería cero.
Ejemplo de Cálculo: Cambio de Presión por Temperatura
Una lata de laca para el cabello, vacía excepto por el gas propulsor isobutano, está inicialmente a 24 °C y 360 kPa. La lata tiene un volumen constante de 350 mL. Si la lata se deja en un automóvil que alcanza los 50 °C en un día caluroso, ¿cuál es la nueva presión de la lata?
Solución:
Primero, convertimos las temperaturas a Kelvin:
- T₁ = 24 °C + 273.15 = 297.15 K (aproximadamente 297 K)
- T₂ = 50 °C + 273.15 = 323.15 K (aproximadamente 323 K)
Aplicamos la Ley de Amontons:
P₁/T₁ = P₂/T₂
360 kPa / 297 K = P₂ / 323 K
Despejamos P₂:
P₂ = (360 kPa × 323 K) / 297 K
P₂ ≈ 390 kPa
El aumento de la temperatura provoca un aumento proporcional de la presión, lo que explica por qué las advertencias en los aerosoles recomiendan no exponerlos a altas temperaturas.
La Ley de Charles: Volumen y Temperatura
Si inflas un globo y lo metes en un refrigerador, observarás que se encoge. Al sacarlo y calentarlo, el globo se expande de nuevo. Esta es la Ley de Charles en acción. Establece que el volumen de una cantidad fija de gas a presión constante es directamente proporcional a su temperatura absoluta (en Kelvin). Jacques Alexandre César Charles fue el científico que la formuló.
Matemáticamente, se expresa como:
- V ∝ T
- V = k × T
- O, para dos condiciones diferentes (1 y 2): V₁/T₁ = V₂/T₂
Donde 'k' es una constante de proporcionalidad y 'T' debe estar en Kelvin.
Ejemplo de Cálculo: Cambio de Volumen por Temperatura
Una muestra de dióxido de carbono (CO₂) ocupa 0.300 L a 10 °C y 750 torr. ¿Qué volumen tendrá el gas a 30 °C y 750 torr?
Solución:
Convertimos las temperaturas a Kelvin:
- T₁ = 10 °C + 273.15 = 283.15 K (aproximadamente 283 K)
- T₂ = 30 °C + 273.15 = 303.15 K (aproximadamente 303 K)
Aplicamos la Ley de Charles:
V₁/T₁ = V₂/T₂
0.300 L / 283 K = V₂ / 303 K
Despejamos V₂:
V₂ = (0.300 L × 303 K) / 283 K
V₂ ≈ 0.321 L
Como se esperaba, el aumento de temperatura resultó en un aumento del volumen.
La Ley de Boyle: Volumen y Presión
Si tienes una jeringa llena de aire y empujas el émbolo manteniendo la temperatura constante, el volumen del aire disminuye y su presión aumenta. Si tiras del émbolo, el volumen aumenta y la presión disminuye. Esta relación inversa entre volumen y presión a temperatura y cantidad de gas constantes es la Ley de Boyle, formulada por Robert Boyle.
Matemáticamente, se expresa como:
- P ∝ 1/V
- P = k / V
- P × V = k
- O, para dos condiciones diferentes (1 y 2): P₁V₁ = P₂V₂
Donde 'k' es una constante.
Ejemplo de Cálculo: Cambio de Presión por Volumen
Una muestra de gas tiene un volumen de 15.0 mL a una presión de 13.0 psi. Determina la presión del gas a un volumen de 7.5 mL, asumiendo temperatura constante.
Solución:
Aplicamos la Ley de Boyle:
P₁V₁ = P₂V₂
13.0 psi × 15.0 mL = P₂ × 7.5 mL
Despejamos P₂:
P₂ = (13.0 psi × 15.0 mL) / 7.5 mL
P₂ = 26 psi
La disminución del volumen a la mitad resulta en el doble de presión, confirmando la relación inversa.
La Ley de Avogadro: Volumen y Cantidad de Gas
Aunque no se centra directamente en la presión con volumen y temperatura, la Ley de Avogadro es crucial para la Ley de los Gases Ideales. Propuesta por Amedeo Avogadro, establece que volúmenes iguales de todos los gases, medidos en las mismas condiciones de temperatura y presión, contienen el mismo número de moléculas (o moles). Esto significa que el volumen (V) y el número de moles (n) son directamente proporcionales si la presión y la temperatura se mantienen constantes.
Matemáticamente: V ∝ n o V₁/n₁ = V₂/n₂.
La Ley de los Gases Ideales: Unificando las Piezas
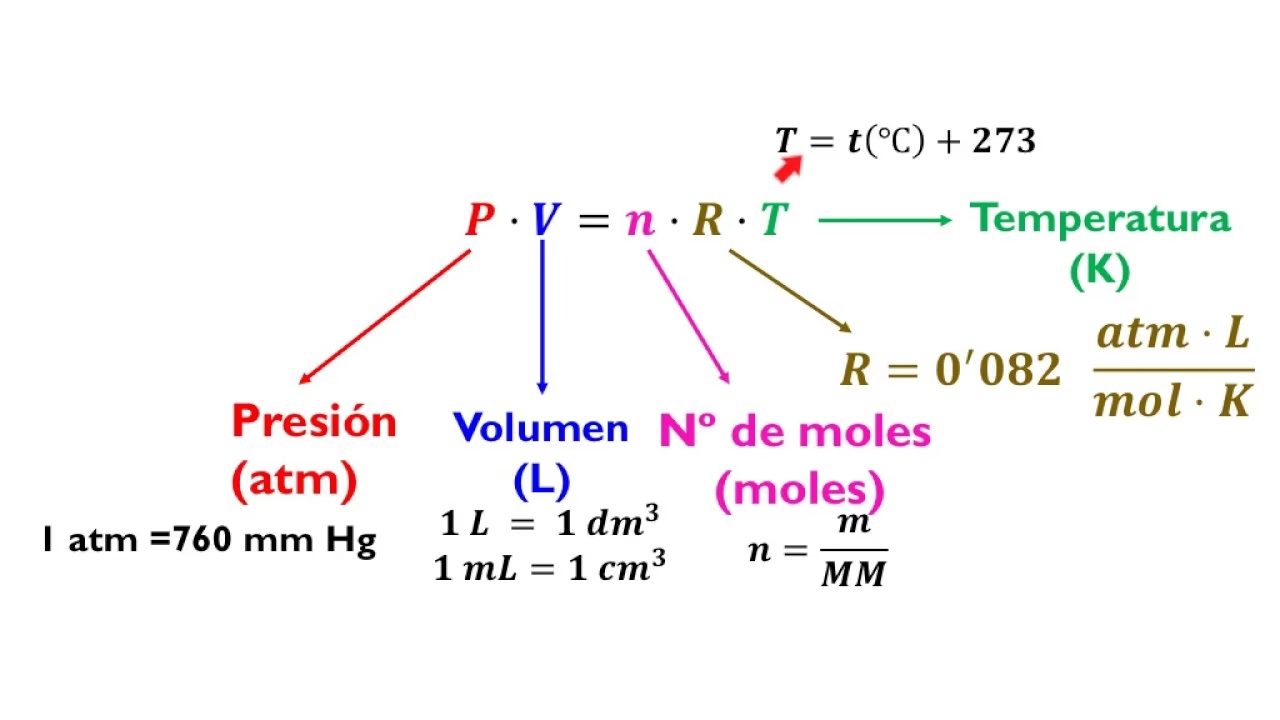
La culminación de estas leyes individuales es la Ley de los Gases Ideales, una ecuación que describe el comportamiento de un gas ideal, una construcción hipotética a la que los gases reales se aproximan bajo ciertas condiciones (bajas presiones y temperaturas moderadas). Esta ley integra la presión (P), el volumen (V), el número de moles (n) y la temperatura (T) en una única fórmula:
PV = nRT
Donde:
- P = Presión del gas (en atmósferas, Pascales, kPa, etc.)
- V = Volumen del gas (en litros, metros cúbicos, etc.)
- n = Número de moles del gas
- R = Constante de los gases ideales (su valor depende de las unidades de P y V. Los valores comunes son 0.08206 L·atm/(mol·K) o 8.314 J/(mol·K) o 8.314 kPa·L/(mol·K))
- T = Temperatura del gas (SIEMPRE en Kelvin)
Esta ecuación es increíblemente versátil. Si conoces cualquier combinación de cuatro de estas variables, puedes calcular la quinta.
Ejemplo de Cálculo: Usando la Ley de los Gases Ideales
El metano (CH₄) se considera como combustible alternativo. Un galón de gasolina podría ser reemplazado por 655 g de CH₄. ¿Cuál es el volumen de esta cantidad de metano a 25 °C y 745 torr?
Solución:
Necesitamos convertir las unidades a las que son compatibles con el valor de R (usaremos R = 0.08206 L·atm/(mol·K)).
1. Masa a moles (n): La masa molar del CH₄ es aproximadamente 16.043 g/mol.
n = 655 g CH₄ × (1 mol / 16.043 g CH₄) ≈ 40.83 moles
2. Temperatura a Kelvin (T):
T = 25 °C + 273.15 = 298.15 K (aproximadamente 298 K)
3. Presión a atmósferas (P):
P = 745 torr × (1 atm / 760 torr) ≈ 0.980 atm
Ahora, reordenamos la ecuación PV = nRT para resolver para V:
V = nRT / P
V = (40.83 mol × 0.08206 L·atm/(mol·K) × 298 K) / 0.980 atm
V ≈ 1020 L
Este ejemplo demuestra que se necesitaría un volumen considerable de metano gaseoso a presión atmosférica para reemplazar un galón de gasolina, lo que resalta el desafío de almacenamiento para combustibles gaseosos.
La Ley de los Gases Combinados: Un Escenario Más Completo
Cuando el número de moles de un gas se mantiene constante, pero la presión, el volumen y la temperatura pueden cambiar, podemos combinar las leyes individuales en la Ley de los Gases Combinados:
P₁V₁/T₁ = P₂V₂/T₂
Esta fórmula es particularmente útil para problemas donde las condiciones de un gas cambian de un estado inicial (1) a un estado final (2). Nuevamente, las temperaturas deben estar en Kelvin.
Ejemplo de Cálculo: Usando la Ley de los Gases Combinados
Una botella de buceo típica con un volumen de 13.2 L tiene una presión de 153 atm cuando está llena de aire a 27 °C. Si la temperatura del cuerpo de un buceador es de 37 °C y la presión a una profundidad de 70 pies es de 3.13 atm, ¿cuántos litros de aire proporcionará este tanque a los pulmones del buceador?
Solución:
Convertimos las temperaturas a Kelvin:
- T₁ (tanque) = 27 °C + 273.15 = 300.15 K (aproximadamente 300 K)
- T₂ (pulmones) = 37 °C + 273.15 = 310.15 K (aproximadamente 310 K)
Aplicamos la Ley de los Gases Combinados:
P₁V₁/T₁ = P₂V₂/T₂
(153 atm × 13.2 L) / 300 K = (3.13 atm × V₂) / 310 K
Despejamos V₂:
V₂ = (153 atm × 13.2 L × 310 K) / (300 K × 3.13 atm)
V₂ ≈ 667 L
Este cálculo demuestra la gran cantidad de aire que un tanque de buceo compacto puede proporcionar al buceador bajo el agua, gracias a la compresión del gas a alta presión.
Aplicaciones Prácticas de las Leyes de los Gases
Las leyes de los gases no son meras abstracciones teóricas; tienen profundas implicaciones en nuestra vida diaria y en diversas industrias:
- La Respiración: Nuestra propia respiración es un ejemplo perfecto de la Ley de Boyle. Cuando inhalamos, el diafragma se contrae, aumentando el volumen de nuestra cavidad torácica. Esto disminuye la presión dentro de los pulmones, creando un vacío parcial que succiona el aire del exterior. Al exhalar, el proceso se invierte, el volumen disminuye, la presión aumenta y el aire es expulsado.
- Buceo Submarino: Los buceadores son expertos en aplicar las leyes de los gases para su seguridad. A medida que descienden, la presión aumenta significativamente (1 atmósfera adicional por cada 10 metros de profundidad en agua salada). Esto comprime el aire en sus pulmones y en sus equipos de flotación (BCD). Deben ecualizar la presión en sus oídos y senos paranasales para evitar lesiones. Al ascender, deben liberar aire de sus BCD para evitar una expansión incontrolada del aire que podría llevar a un ascenso rápido y peligroso, o incluso a la ruptura de los pulmones.
- Neumáticos de Automóviles: El inflado de los neumáticos se basa en la presión del aire. Los cambios de temperatura ambiente afectan la presión dentro de los neumáticos (Ley de Amontons). En invierno, la presión puede disminuir, requiriendo un re-inflado.
- Aerosoles y Recipientes a Presión: La advertencia de no incinerar o exponer aerosoles a altas temperaturas se debe a la Ley de Amontons, ya que el aumento de temperatura eleva drásticamente la presión interna, con riesgo de explosión.
Tabla Resumen de las Leyes de los Gases
| Ley | Relación | Constantes | Fórmula |
|---|---|---|---|
| Amontons (Gay-Lussac) | Presión y Temperatura (directamente proporcional) | Volumen, Moles | P₁/T₁ = P₂/T₂ |
| Charles | Volumen y Temperatura (directamente proporcional) | Presión, Moles | V₁/T₁ = V₂/T₂ |
| Boyle | Presión y Volumen (inversamente proporcional) | Temperatura, Moles | P₁V₁ = P₂V₂ |
| Avogadro | Volumen y Moles (directamente proporcional) | Presión, Temperatura | V₁/n₁ = V₂/n₂ |
| Gases Ideales | Presión, Volumen, Moles, Temperatura | Constante R | PV = nRT |
| Gases Combinados | Presión, Volumen, Temperatura | Moles | P₁V₁/T₁ = P₂V₂/T₂ |
Preguntas Frecuentes (FAQ)
¿Cómo se usa la fórmula PV=nRT para calcular la presión?
Para calcular la presión (P) usando la Ley de los Gases Ideales (PV=nRT), necesitas conocer el volumen (V), el número de moles (n), la temperatura (T) y el valor de la constante de los gases ideales (R). La fórmula se reorganiza para despejar P de la siguiente manera:
P = nRT / V
Asegúrate de que todas las unidades sean consistentes con el valor de R que estás utilizando. Por ejemplo, si R = 0.08206 L·atm/(mol·K), entonces V debe estar en litros, n en moles, y T en Kelvin. El resultado de P estará en atmósferas.
¿Por qué la temperatura debe estar siempre en Kelvin en los cálculos de gases?
La escala Kelvin es una escala de temperatura absoluta, donde 0 K representa el cero absoluto, el punto en el que el movimiento molecular cesa teóricamente. Las leyes de los gases (como Amontons y Charles) establecen una proporcionalidad directa entre la presión/volumen y la temperatura. Si usáramos grados Celsius o Fahrenheit, que tienen puntos cero arbitrarios, esta proporcionalidad directa no se mantendría, ya que un 'cero' en esas escalas no significa ausencia de energía térmica. Usar Kelvin asegura que las relaciones matemáticas sean válidas y que no haya divisiones por cero o valores negativos de temperatura que no tengan sentido físico en las ecuaciones.
¿Qué es un gas ideal y por qué es importante?
Un gas ideal es un modelo teórico de gas que se comporta de manera predecible según las leyes de los gases ideales. Sus partículas se consideran puntos sin volumen propio y sin fuerzas intermoleculares entre ellas, moviéndose aleatoriamente y chocando elásticamente. Aunque ningún gas real es perfectamente ideal, este modelo es una excelente aproximación para la mayoría de los gases a presiones bajas y temperaturas moderadas. Es importante porque simplifica los cálculos y permite comprender los principios fundamentales que rigen el comportamiento de los gases, sirviendo como base para estudiar gases reales en condiciones más complejas.
¿Cuándo se utiliza la Ley de los Gases Combinados en lugar de la Ley de los Gases Ideales?
La Ley de los Gases Ideales (PV=nRT) se utiliza cuando se conocen o se desea calcular las propiedades de un gas en un momento específico, y se conoce el número de moles. La Ley de los Gases Combinados (P₁V₁/T₁ = P₂V₂/T₂) se utiliza cuando las condiciones de un gas cambian de un estado inicial a un estado final, y el número de moles del gas permanece constante. Es decir, si tienes un gas confinado y cambias su presión, volumen o temperatura, y quieres saber cómo afectará a las otras variables, la ley combinada es la herramienta adecuada.
Conclusión
La capacidad de calcular la presión de un gas en función de su volumen y temperatura es fundamental en numerosos campos, desde la ingeniería hasta la medicina. Las leyes de los gases, desarrolladas a lo largo de siglos de observación y experimentación, nos proporcionan un marco robusto para comprender y predecir el comportamiento de estas sustancias. La Ley de los Gases Ideales, en particular, se erige como una herramienta poderosa y versátil, permitiéndonos realizar cálculos precisos y aplicar estos principios a escenarios del mundo real. Al dominar estas ecuaciones y sus aplicaciones, desbloqueamos una comprensión más profunda del mundo molecular que nos rodea.
Si quieres conocer otros artículos parecidos a Dominando el Cálculo de Presión: Volumen y Temperatura puedes visitar la categoría Cálculos.

