22/08/2023
La comprensión de cómo se comportan los gases es fundamental en diversas áreas de la ciencia y la ingeniería, y en el corazón de este entendimiento se encuentra la intrínseca relación entre la presión, el volumen y la temperatura. Estos tres parámetros no actúan de forma aislada, sino que están constantemente interactuando, definiendo el estado de cualquier gas. Desde el aire que respiramos hasta los procesos industriales más complejos, la danza entre presión, volumen y temperatura es un pilar de la física.
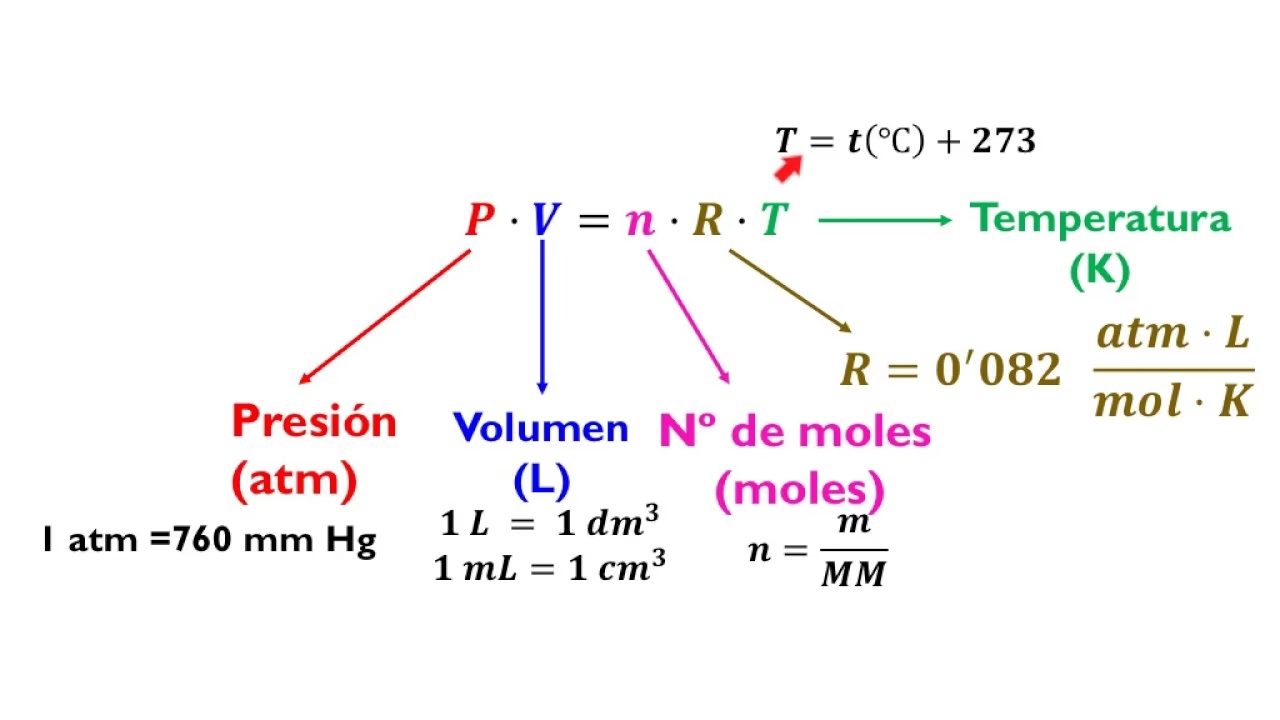
A menudo, nos preguntamos cómo podemos calcular la presión si conocemos el volumen y la temperatura, o viceversa. Para desentrañar esta cuestión, es crucial adentrarnos en las leyes que gobiernan el comportamiento de los gases. Si bien existen leyes que relacionan estos tres factores de manera conjunta, la base de nuestro entendimiento a menudo comienza con el estudio de cómo dos de estas variables se relacionan mientras la tercera se mantiene constante. Una de las leyes más célebres y fundamentales en este campo es la Ley de Boyle-Mariotte, que nos ofrece una visión clara de la relación entre la presión y el volumen a temperatura constante.
La Ley de Boyle-Mariotte: Presión y Volumen a Temperatura Constante
La Ley de Boyle-Mariotte, comúnmente conocida como la Ley de Boyle, es una de las piedras angulares de las leyes de los gases. Esta ley establece una relación crucial entre el volumen y la presión de una cantidad determinada de gas, siempre y cuando su temperatura se mantenga constante. Fue formulada de manera independiente por el físico y químico irlandés Robert Boyle en 1662 y, años más tarde, por el físico y botánico francés Edme Mariotte en 1676.
En su esencia, la Ley de Boyle expresa que:
La presión absoluta ejercida por una dada masa de un gas ideal es inversamente proporcional al volumen que ocupa si la temperatura y la cantidad de gas permanecen invariables dentro de un sistema cerrado.
Esto significa que si aumentamos la presión sobre un gas, su volumen disminuirá; y si disminuimos la presión, su volumen aumentará. La relación es de proporcionalidad inversa. Matemáticamente, esta ley se puede expresar de varias maneras:
P ∝ 1/V (La presión es inversamente proporcional al volumen)
O, de forma más común y útil:
PV = k
Donde P es la presión del gas, V es el volumen del gas, y k es una constante que se mantiene para una temperatura y cantidad de gas dadas. Este producto constante (k) es una característica distintiva de los procesos isotérmicos (a temperatura constante) en los gases.
Cuando necesitamos comparar el mismo gas bajo dos conjuntos diferentes de condiciones, pero manteniendo la temperatura y la cantidad de gas constantes, la ley se vuelve aún más práctica:
P₁V₁ = P₂V₂
Esta ecuación nos permite calcular una de las variables (presión o volumen) si conocemos las condiciones iniciales y una de las condiciones finales. Por ejemplo, si conocemos la presión inicial (P₁) y el volumen inicial (V₁) de un gas, y el volumen final (V₂), podemos despejar la presión final (P₂).

En términos prácticos, esto implica que si el volumen de un gas se reduce a la mitad, su presión se duplicará. Del mismo modo, si el volumen se duplica, la presión se reducirá a la mitad. Esta relación inversa es crucial para entender muchos fenómenos naturales y aplicaciones tecnológicas.
Simbología Clave en la Ley de Boyle
Para trabajar con la Ley de Boyle, es útil conocer la simbología estándar:
| Símbolo | Nombre | Unidad |
|---|---|---|
k | Constante | Pa·m³ |
p | Presión | Pa (Pascal) |
p₁ | Presión inicial | Pa |
p₂ | Presión final | Pa |
V | Volumen | m³ |
V₁ | Volumen inicial | m³ |
V₂ | Volumen final | m³ |
Deducciones Prácticas de la Ley de Boyle
La ecuación P₁V₁ = P₂V₂ es extraordinariamente versátil. Podemos despejar cualquier incógnita para encontrar su valor:
| Ecuación General | Despejando la Incógnita |
|---|---|
p₁V₁ = p₂V₂ | p₁ = (p₂V₂)/V₁ |
p₁V₁ = p₂V₂ | p₂ = (p₁V₁)/V₂ |
p₁V₁ = p₂V₂ | V₁ = (p₂V₂)/p₁ |
p₁V₁ = p₂V₂ | V₂ = (p₁V₁)/p₂ |
Estas fórmulas son una aplicación directa de la "regla de tres" en el contexto de los gases, permitiéndonos predecir el comportamiento de un gas bajo diferentes condiciones de presión o volumen, siempre que la temperatura se mantenga constante.
El Experimento de Robert Boyle y Edme Mariotte
La relación entre presión y volumen fue notada por primera vez por Richard Towneley y Henry Power en el siglo XVII. Sin embargo, fue Robert Boyle quien la confirmó a través de experimentos rigurosos, publicando sus hallazgos. Se cree que su asistente, Robert Hooke, fue clave en la construcción del aparato experimental.
Boyle utilizó un tubo en forma de J, cerrado por un extremo. Vertiendo mercurio por el lado abierto, logró comprimir el aire atrapado en el extremo cerrado. Al variar la cantidad de mercurio, observó cómo el volumen del aire disminuía a medida que la presión ejercida por el mercurio aumentaba. Tras repetir el experimento varias veces con diferentes cantidades de mercurio, descubrió la relación inversamente proporcional entre la presión y el volumen del gas a temperatura constante.
Edme Mariotte, por su parte, llegó a la misma conclusión de forma independiente en 1679. Su método implicó introducir un gas en un cilindro con un émbolo y medir las presiones resultantes al bajar el émbolo. Los datos de su experimento ilustran perfectamente la ley:
| P (atm) | V (L) | P · V (atm·L) |
|---|---|---|
| 0,5 | 60 | 30 |
| 1,0 | 30 | 30 |
| 1,5 | 20 | 30 |
| 2,0 | 15 | 30 |
| 2,5 | 12 | 30 |
| 3,0 | 10 | 30 |
Como se puede observar en la tabla, a medida que la presión (P) aumenta, el volumen (V) disminuye. Sin embargo, el producto de la presión por el volumen (P · V) se mantiene constante, en este caso, en 30 atm·L. Este valor constante es la 'k' de la Ley de Boyle.
Gráficamente, la relación entre presión y volumen se representa como una hipérbola. Si se repiten los experimentos a diferentes temperaturas, se obtiene una familia de hipérbolas, cada una de las cuales es una isoterma (una curva que representa un proceso a temperatura constante).

¿Cómo Varía la Presión Según la Temperatura?
Aunque la Ley de Boyle-Mariotte se centra en la relación entre presión y volumen a temperatura constante, la temperatura juega un papel crucial en el comportamiento general de los gases. La presión del aire, por ejemplo, está directamente influenciada por los cambios de temperatura.
Existe una relación fundamental: el aire caliente tiende a elevarse, lo que resulta en una baja presión. Por el contrario, el aire frío es más denso y tiende a descender, provocando un aumento de la presión atmosférica. Esta observación es clave para entender fenómenos meteorológicos y muchos otros procesos físicos. A mayor temperatura, las moléculas de un gas se mueven con mayor energía, y si el volumen se mantiene constante, esto se traduce en más colisiones contra las paredes del recipiente, y por ende, mayor presión. Sin embargo, para cálculos precisos que involucren los tres parámetros simultáneamente, se requiere una ley que los unifique.
Aplicaciones en la Vida Cotidiana: El Sistema Respiratorio Humano
La Ley de Boyle-Mariotte no es solo un concepto teórico; tiene aplicaciones prácticas directas en nuestra vida diaria, siendo una de las más fascinantes el funcionamiento de nuestro propio sistema respiratorio. La respiración es un ejemplo perfecto de cómo los cambios de volumen conducen a cambios de presión, permitiendo el flujo de aire.
Cuando inhalamos, el diafragma se contrae y se mueve hacia abajo, y los músculos intercostales se contraen, expandiendo la cavidad torácica. Este aumento en el volumen de los pulmones provoca una disminución en la presión del aire dentro de ellos, de acuerdo con la Ley de Boyle. Como resultado, la presión dentro de los pulmones se vuelve menor que la presión atmosférica exterior. Esta diferencia de presión crea un gradiente que hace que el aire fluya desde la atmósfera (alta presión) hacia los pulmones (baja presión), permitiéndonos tomar aire.
Por el contrario, cuando exhalamos, el diafragma se relaja y se mueve hacia arriba, y los músculos intercostales también se relajan, reduciendo el volumen de la cavidad torácica. Esta disminución del volumen pulmonar aumenta la presión del aire dentro de los pulmones. Una vez que la presión interna supera la presión atmosférica externa, el aire es expulsado de los pulmones hacia el exterior, completando el ciclo respiratorio. Este proceso continuo de inhalación y exhalación es un testimonio directo de la aplicación de la Ley de Boyle en uno de los sistemas biológicos más vitales.

Preguntas Frecuentes sobre Presión, Volumen y Temperatura
¿Qué es la Ley de Boyle y qué establece?
La Ley de Boyle, o Ley de Boyle-Mariotte, es una ley de los gases que establece que la presión y el volumen de un gas tienen una relación inversa cuando la temperatura y la cantidad de gas se mantienen constantes. Esto significa que si el volumen aumenta, la presión disminuye, y viceversa.
¿Cómo se relaciona la presión con el volumen a temperatura constante?
A temperatura constante, la presión y el volumen de un gas son inversamente proporcionales. Esto se expresa matemáticamente como P₁V₁ = P₂V₂, donde el producto de la presión y el volumen es una constante. Si duplicas la presión, el volumen se reduce a la mitad.
¿Cómo afecta la temperatura a la presión de un gas?
Aunque la Ley de Boyle se enfoca en la temperatura constante, la temperatura general sí afecta la presión. El aire caliente tiende a elevarse y está asociado con una presión más baja, mientras que el aire frío desciende y está asociado con una presión atmosférica más alta. En términos generales, para un volumen constante, un aumento de temperatura tiende a aumentar la presión de un gas.
¿Dónde podemos ver la Ley de Boyle en acción en la vida cotidiana?
Un excelente ejemplo de la Ley de Boyle en acción es el sistema respiratorio humano. Cuando inhalamos, el volumen de nuestros pulmones aumenta, lo que disminuye la presión interna y permite que el aire entre. Al exhalar, el volumen pulmonar disminuye, aumentando la presión y expulsando el aire. Otros ejemplos incluyen el funcionamiento de jeringas, el buceo (cambios de volumen de los pulmones con la profundidad) y el inflado de neumáticos.
En resumen, la interacción entre presión, volumen y temperatura es un campo de estudio fascinante y fundamental en la física de los gases. La Ley de Boyle-Mariotte nos proporciona una herramienta poderosa para comprender la relación inversa entre presión y volumen a temperatura constante, mientras que las observaciones sobre cómo la temperatura afecta la presión nos dan una visión más completa del comportamiento dinámico de los gases en nuestro mundo. Comprender estas leyes no solo es crucial para la ciencia, sino que también nos permite apreciar la complejidad y la elegancia de los fenómenos que nos rodean, desde la respiración más simple hasta los patrones climáticos más complejos.
Si quieres conocer otros artículos parecidos a Presión, Volumen y Temperatura: Un Vínculo Esencial puedes visitar la categoría Física.
