19/03/2025
La voltamperometría es una de las técnicas electroquímicas más versátiles y poderosas, permitiéndonos explorar el comportamiento de las especies químicas en una interfase electrodo-solución. Al medir la corriente que fluye a través de un electrodo como función de un potencial aplicado, podemos obtener información crucial sobre las reacciones de oxidación y reducción. Esta metodología no solo es fundamental en la investigación básica, sino que también tiene aplicaciones vitales en campos que van desde el análisis ambiental y farmacéutico hasta la ciencia de materiales y la biología. Para comprender a fondo su potencial, es esencial desentrañar conceptos clave como la corriente límite, la voltamperometría hidrodinámica y el potencial de media-onda, pilares que nos permiten interpretar los complejos voltamogramas.
- La Voltamperometría: Una Ventana a las Reacciones Electroquímicas
- La Corriente Límite: El Techo de la Reacción Electroquímica
- Voltamperometría Hidrodinámica: Controlando el Flujo para un Análisis Preciso
- El Potencial de Media-Onda: La Huella Dactilar de una Especie
- Aplicaciones y Relevancia en la Ciencia Moderna
- Preguntas Frecuentes
- ¿Por qué es importante la corriente límite en voltamperometría?
- ¿Qué ventajas ofrece la voltamperometría hidrodinámica sobre la voltamperometría cíclica?
- ¿Qué información nos proporciona el potencial de media-onda?
- ¿Cómo se controla el flujo en la voltamperometría hidrodinámica?
- ¿La corriente límite siempre es independiente del potencial?
- Conclusión
La Voltamperometría: Una Ventana a las Reacciones Electroquímicas
En su esencia, la voltamperometría se basa en la relación entre la corriente y el potencial. Un sistema voltamperométrico típico consta de tres electrodos: un electrodo de trabajo, donde ocurre la reacción de interés; un electrodo de referencia, que mantiene un potencial constante; y un contraelectrodo, que completa el circuito eléctrico. Al variar el potencial aplicado al electrodo de trabajo y medir la corriente resultante, se genera un gráfico conocido como voltamograma. La forma de este voltamograma es una verdadera huella dactilar de las especies electroactivas presentes en la solución y de los procesos redox que estas experimentan. La interpretación de estas curvas nos permite determinar la concentración de analitos, investigar mecanismos de reacción, estudiar la cinética electroquímica y caracterizar materiales.
La Corriente Límite: El Techo de la Reacción Electroquímica
Uno de los parámetros más importantes que se observan en un voltamograma es la corriente límite. Esta corriente representa un valor de corriente que se alcanza en una región específica del voltamograma, típicamente entre el primer y el segundo dígito, donde la corriente se estabiliza y se vuelve casi independiente del potencial aplicado. ¿Qué significa esto? Significa que la velocidad a la que la especie electroactiva reacciona en la superficie del electrodo ha alcanzado su máximo. En este punto, la concentración de la especie electroactiva en la superficie del electrodo se ha reducido prácticamente a cero. Esto se debe a que la velocidad de transporte de la especie desde el seno de la solución hasta la superficie del electrodo (ya sea por difusión, migración o convección) se convierte en el factor limitante de la reacción.
Imaginemos una situación en la que estamos aplicando un potencial cada vez más reductor. Inicialmente, a medida que el potencial se vuelve más negativo, la velocidad de la reacción aumenta y, por ende, la corriente. Sin embargo, llega un punto en el que, por muy negativo que hagamos el potencial, no podemos hacer que las moléculas o iones reaccionen más rápido porque simplemente no llegan a la superficie del electrodo a una velocidad mayor. Es como una cola de personas en la caja de un supermercado: por muy rápido que trabaje el cajero, si las personas no llegan a la caja a una cierta velocidad, el rendimiento máximo está limitado por la llegada de los clientes. En este caso, la corriente límite es ese rendimiento máximo, y su valor es directamente proporcional a la concentración de la especie electroactiva en la solución, lo que la convierte en una herramienta invaluable para el análisis cuantitativo.
Voltamperometría Hidrodinámica: Controlando el Flujo para un Análisis Preciso
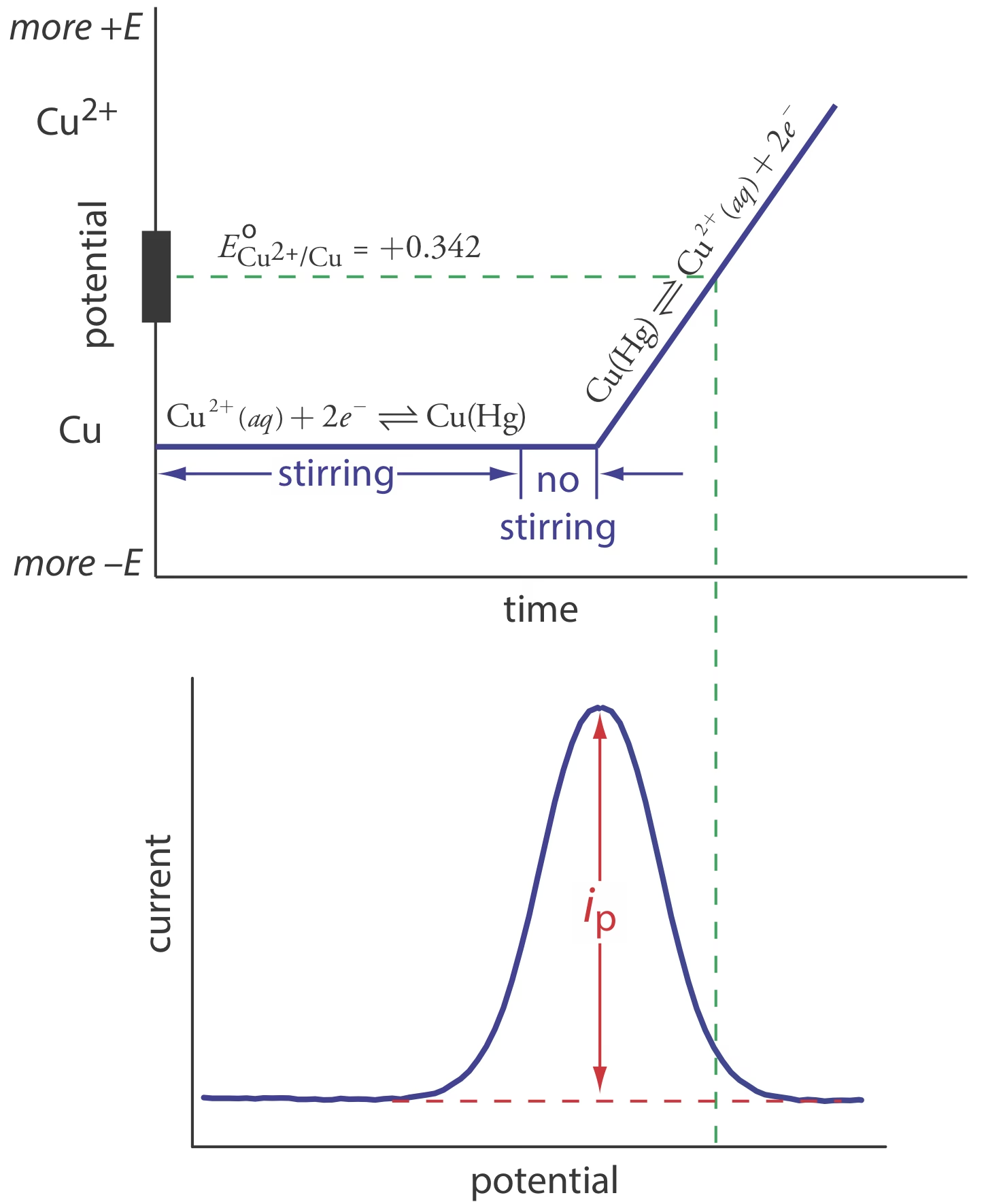
Mientras que en la voltamperometría cíclica o lineal tradicional el transporte de masa está dominado por la difusión (y la migración), la voltamperometría hidrodinámica introduce un elemento crucial: el flujo de la solución. A diferencia de los experimentos en soluciones quietas (estáticas), donde la corriente de estado estacionario está limitada por la difusión del substrato a través de una capa de difusión que se expande con el tiempo, las técnicas hidrodinámicas crean un flujo laminar de solución a través del electrodo de trabajo. Este flujo constante y controlado asegura un suministro continuo y renovado de la especie electroactiva a la superficie del electrodo.
La configuración experimental de la voltamperometría hidrodinámica puede variar ampliamente, aunque la configuración de tres electrodos sigue siendo la norma. Las configuraciones más comunes implican la rotación del electrodo de trabajo para generar el flujo laminar. Ejemplos prominentes son el electrodo de disco rotatorio (RDE, por sus siglas en inglés) y el electrodo de anillo-disco rotatorio (RRDE). En un RDE, el electrodo de disco gira a una velocidad controlada, creando un flujo de solución predecible hacia su superficie. Esto resulta en una corriente de estado estacionario que es determinada por la velocidad de flujo (velocidad de rotación) en lugar de la difusión transitoria. La ecuación de Levich, por ejemplo, describe matemáticamente esta relación, permitiendo la determinación precisa de coeficientes de difusión y velocidades de reacción.
Las ventajas de la voltamperometría hidrodinámica son significativas. Al establecer un flujo laminar, se logran señales de estado estacionario, lo que simplifica la interpretación de los voltamogramas y mejora la reproducibilidad. Además, el transporte de masa convectivo es mucho más eficiente que el difusivo, lo que a menudo conduce a corrientes más altas y, por lo tanto, a una mayor sensibilidad en el análisis. Las configuraciones como el RRDE son particularmente potentes porque permiten el estudio de intermediarios de reacción. En el RRDE, la especie generada en el electrodo de disco puede ser detectada en el electrodo de anillo adyacente, proporcionando información detallada sobre los mecanismos de reacción electroquímicos.

Otras configuraciones hidrodinámicas incluyen celdas de flujo, donde las bombas dirigen la solución hacia o a través del electrodo de trabajo. Es importante destacar que, si bien la voltamperometría hidrodinámica se asocia comúnmente con la voltamperometría de barrido lineal, no se limita a ella. La configuración de muchas celdas, como el RRDE, permite que el substrato pase de un electrodo de trabajo a otro. El potencial de un electrodo puede variarse mientras el otro se mantiene constante o se varía de forma independiente. Incluso la velocidad de flujo puede ajustarse para modificar el lapso temporal que experimentan los substratos entre los electrodos de trabajo, abriendo un abanico de posibilidades para estudios cinéticos y de mecanismos complejos.
Comparación: Voltamperometría Cíclica vs. Voltamperometría Hidrodinámica
Para entender mejor el valor de la voltamperometría hidrodinámica, es útil compararla con la voltamperometría cíclica (VC), una técnica de voltamperometría estática ampliamente utilizada:
| Característica | Voltamperometría Cíclica (Estática) | Voltamperometría Hidrodinámica |
|---|---|---|
| Estado de la Solución | Quieta, sin agitación externa | Flujo laminar controlado (rotación, bombas) |
| Tipo de Señal | Transitoria, picos anódicos y catódicos | Estacionaria, mesetas de corriente |
| Transporte de Masa Principal | Difusión (y migración) | Convección y difusión |
| Dependencia del Tiempo | La capa de difusión crece con el tiempo | Capa de difusión de estado estacionario |
| Información Obtenida | Mecanismos de reacción, cinética, reversibilidad, adsorción | Concentración, coeficientes de difusión, cinética de reacción, intermediarios estables |
| Sensibilidad para Cuantificación | Buena, pero puede ser afectada por fenómenos transitorios | Alta, señales estables y reproducibles para cuantificación |
| Aplicaciones Típicas | Investigación fundamental, caracterización de materiales, estudios de superficies | Análisis cuantitativo de rutina, control de calidad, estudios cinéticos detallados |
El Potencial de Media-Onda: La Huella Dactilar de una Especie
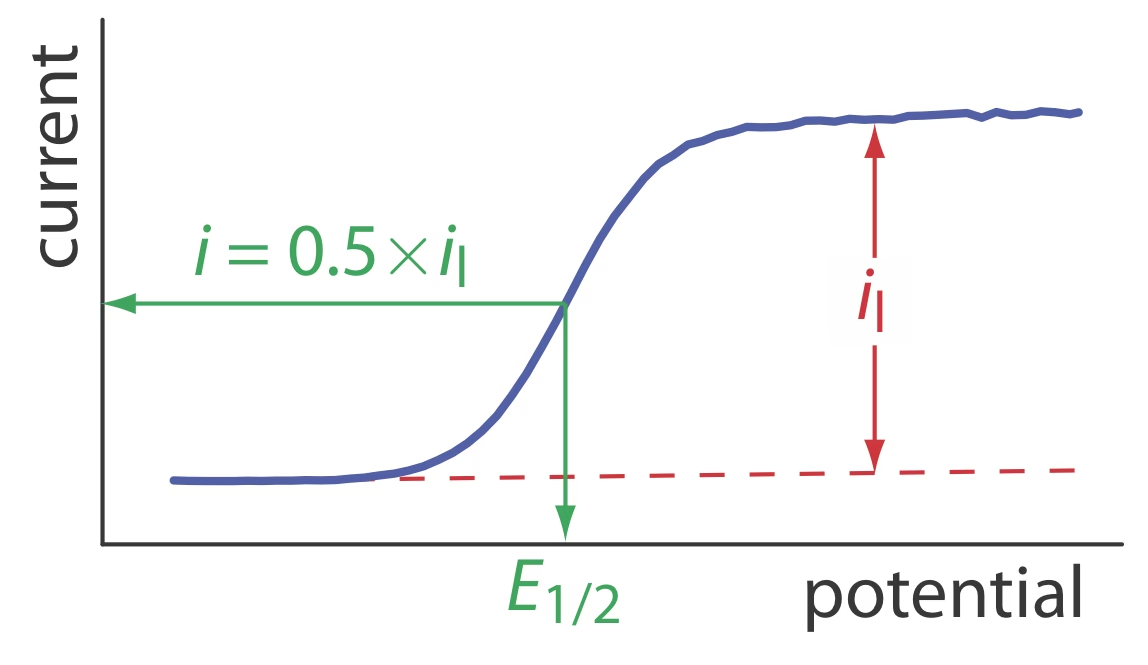
El potencial de media-onda (E1/2) es otro concepto fundamental, especialmente en polarografía (un tipo de voltamperometría con electrodo de gota de mercurio). El E1/2 corresponde al punto medio de la distancia entre la corriente residual (la pequeña corriente que fluye antes de que comience la reacción electroquímica del analito) y la meseta de la corriente limitante en un polarograma. Es decir, es el potencial al cual la corriente alcanza la mitad de su valor limitante.
La importancia del E1/2 radica en que es una característica intrínseca de la especie electroactiva y del sistema redox en el que participa. Proporciona información cualitativa sobre la identidad de la especie. En condiciones ideales, el potencial de media-onda está estrechamente relacionado con el potencial estándar de reducción (E°) de la reacción redox, aunque puede diferir ligeramente debido a factores como la cinética de la reacción, la difusión y las interacciones con la superficie del electrodo. Cada especie electroactiva exhibe un potencial de media-onda único bajo condiciones dadas (pH, fuerza iónica, temperatura, etc.), lo que lo convierte en un valioso parámetro para la identificación cualitativa de analitos en una mezcla.
Aplicaciones y Relevancia en la Ciencia Moderna
La comprensión de la corriente límite, la voltamperometría hidrodinámica y el potencial de media-onda es indispensable para aprovechar al máximo el potencial de las técnicas voltamperométricas. Estas herramientas no solo nos permiten cuantificar analitos con alta precisión y sensibilidad, sino también desentrañar los intrincados mecanismos de las reacciones electroquímicas.
Por ejemplo, en la industria farmacéutica, la voltamperometría se utiliza para el control de calidad de medicamentos y para estudiar la electroactividad de nuevos compuestos. En el monitoreo ambiental, permite la detección de metales pesados o contaminantes orgánicos en agua y suelos. En la investigación de materiales, ayuda a caracterizar la conductividad de polímeros, el rendimiento de baterías y celdas de combustible, o la resistencia a la corrosión de metales. Los estudios de cinética de reacción, la determinación de coeficientes de difusión y la elucidación de vías de reacción complejas son posibles gracias a la información que proporcionan estos parámetros fundamentales.
Preguntas Frecuentes
¿Por qué es importante la corriente límite en voltamperometría?
La corriente límite es crucial porque su valor es directamente proporcional a la concentración del analito en la solución, lo que permite realizar análisis cuantitativos precisos. Además, indica el punto en el que la reacción electroquímica está limitada por el transporte de masa, proporcionando información sobre la cinética del proceso.

¿Qué ventajas ofrece la voltamperometría hidrodinámica sobre la voltamperometría cíclica?
La voltamperometría hidrodinámica ofrece señales de estado estacionario, lo que mejora la reproducibilidad y simplifica la interpretación. También permite un transporte de masa más eficiente, resultando en mayor sensibilidad para la cuantificación. Las configuraciones como el RRDE son excelentes para estudiar intermediarios de reacción y mecanismos complejos.
¿Qué información nos proporciona el potencial de media-onda?
El potencial de media-onda (E1/2) es una característica cualitativa de una especie electroactiva. Indica el potencial al cual la reacción electroquímica alcanza la mitad de su corriente limitante, y su valor es indicativo de la identidad de la especie y de su potencial redox en las condiciones experimentales dadas.
¿Cómo se controla el flujo en la voltamperometría hidrodinámica?
El flujo en la voltamperometría hidrodinámica se controla principalmente mediante la rotación del electrodo de trabajo (como en el RDE o RRDE), donde la velocidad de rotación determina la velocidad del flujo laminar. Otra forma es mediante el uso de celdas de flujo con bombas que dirigen la solución a una velocidad controlada sobre el electrodo.
¿La corriente límite siempre es independiente del potencial?
Una vez que se alcanza la corriente límite, es prácticamente independiente del potencial en el rango de potencial donde la especie electroactiva aún reacciona. Esto ocurre porque la velocidad de reacción ya no está limitada por la transferencia de electrones, sino por la velocidad a la que la especie llega a la superficie del electrodo.
Conclusión
La voltamperometría, con sus diversas modalidades, se erige como una técnica analítica y fundamental indispensable en el mundo científico. Conceptos como la corriente límite, la voltamperometría hidrodinámica y el potencial de media-onda no son meros términos técnicos, sino las claves para desbloquear la riqueza de información que estos experimentos ofrecen. Dominar estas ideas permite a los investigadores y analistas no solo cuantificar con precisión, sino también comprender los intrincados mecanismos de las reacciones electroquímicas. En un mundo que demanda cada vez más soluciones innovadoras en campos tan diversos como la salud, el medio ambiente y la energía, la voltamperometría continúa siendo una herramienta fundamental, impulsando el avance del conocimiento y la tecnología.
Si quieres conocer otros artículos parecidos a Voltamperometría: Desentrañando la Corriente Límite y el Potencial de Media-Onda puedes visitar la categoría Cálculos.