10/12/2022
Las proteínas son las arquitectas y operarias de la vida, desempeñando roles fundamentales en cada proceso biológico, desde la construcción de estructuras celulares hasta la dirección de complejas reacciones metabólicas. Comprender y cuantificar su actividad es crucial en campos tan diversos como la medicina, la biotecnología y la investigación fundamental. Pero, ¿cómo se mide exactamente la función de estas intrincadas moléculas? Y, más importante aún, ¿cómo podemos cuantificar su eficiencia y pureza en una preparación? Este artículo desglosará los conceptos clave de la actividad proteica, con un enfoque particular en la actividad enzimática y la actividad específica, proporcionando una guía detallada para su cálculo y comprensión.
La capacidad de una proteína para llevar a cabo su función es lo que conocemos como su actividad biológica. Para las enzimas, que son proteínas catalíticas, esta actividad se refiere a su habilidad para acelerar una reacción química específica. Medir esta actividad nos permite no solo entender cómo funcionan, sino también evaluar la calidad y concentración de una preparación proteica. Si bien el concepto puede parecer complejo al principio, con una comprensión clara de los principios y métodos, cualquier persona puede adentrarse en este fascinante aspecto de la bioquímica.
- Comprendiendo la Actividad Enzimática: El Motor de la Vida
- La Importancia de la Actividad Específica: Un Indicador de Pureza
- Métodos para Medir la Actividad Proteica: Más Allá de las Enzimas
- Cálculo Práctico de la Actividad Específica: Paso a Paso
- Desafíos y Consideraciones en la Medición de Actividad Proteica
- Preguntas Frecuentes sobre la Actividad Proteica y su Medición
- ¿Cuál es la diferencia entre actividad y actividad específica?
- ¿Por qué es importante medir la actividad específica en la purificación de proteínas?
- ¿Qué factores pueden afectar la actividad de una proteína?
- ¿Se puede medir la actividad específica de cualquier proteína?
- ¿Cómo se relacionan las unidades de actividad enzimática (UI) y el katal?
Comprendiendo la Actividad Enzimática: El Motor de la Vida
Las enzimas son verdaderas maravillas moleculares, capaces de aumentar la velocidad de las reacciones químicas millones de veces sin consumirse en el proceso. Su actividad es lo que permite que la vida funcione a las velocidades necesarias. Pero, ¿cómo cuantificamos esta 'velocidad'? La actividad enzimática se define generalmente como la cantidad de producto formado o sustrato consumido por unidad de tiempo, bajo condiciones específicas de temperatura, pH y concentración de sustrato. Esta medida nos da una idea directa de cuánto 'trabajo' está realizando la enzima.
La unidad estándar para la actividad enzimática es la Unidad Internacional (UI o U), definida como la cantidad de enzima que cataliza la transformación de 1 micromol de sustrato por minuto. En el Sistema Internacional de Unidades (SI), la unidad es el katal (kat), que representa la cantidad de enzima que cataliza la transformación de 1 mol de sustrato por segundo. Aunque el katal es la unidad SI, la UI sigue siendo ampliamente utilizada en la práctica de laboratorio debido a su conveniencia.
Para medir la actividad enzimática, se diseña un ensayo donde la reacción catalizada por la enzima es monitoreada. Esto a menudo implica el uso de un espectrofotómetro para medir cambios en la absorbancia de un sustrato o producto que tiene una señal óptica distintiva. Por ejemplo, si un producto absorbe luz a una longitud de onda específica, se puede seguir su formación a lo largo del tiempo. La pendiente de la curva de absorbancia versus tiempo, junto con el coeficiente de extinción molar del compuesto, permite calcular la velocidad de la reacción y, por ende, la actividad enzimática.
La Importancia de la Actividad Específica: Un Indicador de Pureza
Una vez que hemos medido la actividad total de una preparación enzimática, surge una pregunta crucial: ¿qué tan pura es nuestra enzima? Aquí es donde entra en juego el concepto de actividad específica. La actividad específica es una medida de la pureza de una preparación enzimática y se define como la actividad enzimática por unidad de masa de proteína. Se expresa comúnmente en unidades por miligramo (U/mg) o katales por miligramo (kat/mg).

¿Por qué es tan importante la actividad específica? Imagina que tienes dos preparaciones de la misma enzima. Ambas pueden tener la misma actividad total si diluyes una más que la otra. Sin embargo, si una preparación contiene 10 mg de proteína y la otra solo 1 mg para lograr la misma actividad total, la segunda preparación es diez veces más pura. La actividad específica nos permite comparar la pureza de diferentes preparaciones o seguir el progreso de un proceso de purificación. A medida que una enzima se purifica, su actividad específica debería aumentar, ya que la proporción de enzima activa con respecto a otras proteínas contaminantes se incrementa.
El cálculo de la actividad específica es sencillo una vez que se tienen los dos componentes clave:
- La actividad enzimática total (en U o kat).
- La cantidad total de proteína en la preparación (en mg).
La fórmula es: Actividad Específica = Actividad Enzimática Total / Masa Total de Proteína
Por ejemplo, si una solución contiene 50 Unidades de actividad enzimática y se determina que tiene 2 mg de proteína total, la actividad específica sería 50 U / 2 mg = 25 U/mg. Este valor es una métrica fundamental en la purificación de proteínas y en el control de calidad de productos biotecnológicos.
Métodos para Medir la Actividad Proteica: Más Allá de las Enzimas
Aunque nos hemos centrado en las enzimas, la actividad de las proteínas en general puede medirse de diversas maneras, dependiendo de su función. Las proteínas no enzimáticas, como los factores de crecimiento, los anticuerpos o las proteínas estructurales, tienen actividades biológicas que no implican la catálisis de una reacción. Para estas, la medición de la actividad es a menudo más compleja y requiere de bioensayos.
Un bioensayo mide la respuesta biológica de un sistema vivo (células, tejidos o un organismo completo) a la proteína de interés. Algunos ejemplos incluyen:
- Ensayo de proliferación celular: Para proteínas que estimulan el crecimiento celular.
- Ensayo de quimiotaxis: Para proteínas que atraen o repelen células.
- Ensayo de unión a receptores: Para proteínas que interactúan con receptores específicos en la superficie celular.
- ELISA funcional: Una variante del ELISA tradicional que no solo detecta la presencia de una proteína, sino que también evalúa su capacidad para unirse a un ligando o inducir una respuesta.
Para calcular la actividad específica de proteínas no enzimáticas, el principio es el mismo: se divide la actividad biológica medida (que puede expresarse en unidades arbitrarias o en una concentración que induce una respuesta específica) por la cantidad total de proteína presente en la muestra. La clave es tener un ensayo robusto y reproducible para cuantificar la función biológica.
Medición de Proteínas Totales: El Denominador Crucial
Para calcular la actividad específica, es imprescindible conocer la concentración de proteína total en la muestra. Existen varios métodos para medir las proteínas totales, cada uno con sus ventajas y limitaciones:
- Método de Bradford: Basado en el cambio de color de un colorante (Coomassie Brilliant Blue G-250) en presencia de proteínas. Es rápido y sensible, pero puede ser afectado por detergentes.
- Método de Lowry: Implica una reacción de dos pasos que resulta en un color azul intenso. Es muy sensible, pero requiere más tiempo y es susceptible a interferencias.
- Método de BCA (Ácido Bicinchonínico): Similar al Lowry en principio, pero más estable y menos propenso a interferencias.
- Absorbancia a 280 nm: Las proteínas que contienen triptófano y tirosina absorben luz a 280 nm. Es un método rápido y no destructivo, pero su precisión depende de la composición de aminoácidos de la proteína y puede ser afectado por ácidos nucleicos.
La elección del método dependerá de la muestra, la presencia de interferencias y la sensibilidad requerida. Es fundamental que la medición de proteínas totales sea precisa, ya que cualquier error en este valor se propagará al cálculo de la actividad específica.
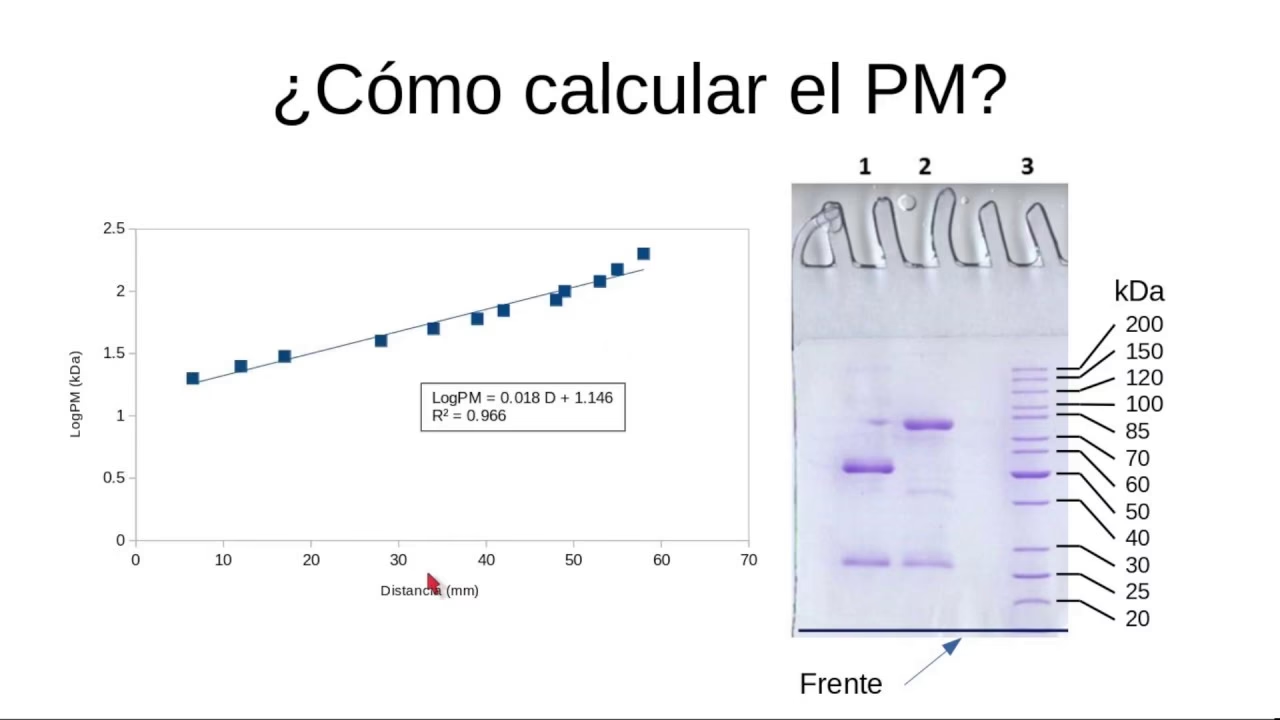
Cálculo Práctico de la Actividad Específica: Paso a Paso
Vamos a ilustrar el cálculo de la actividad específica con un ejemplo práctico. Supongamos que estamos purificando una enzima y hemos realizado un ensayo de actividad y una medición de proteína total en una de nuestras fracciones de purificación.
Escenario:
Tenemos una fracción de purificación de una enzima. Realizamos un ensayo para medir su actividad y obtenemos los siguientes datos:
- Volumen de la muestra: 0.5 mL
- En el ensayo, la enzima convierte 10 micromoles de sustrato en producto en 5 minutos.
- Para medir la proteína total, tomamos 0.1 mL de la misma muestra y determinamos que contiene 0.05 mg de proteína.
Paso a Paso del Cálculo:
1. Calcular la Actividad Enzimática Total (en U):
- La enzima convierte 10 µmol en 5 minutos.
- Actividad = 10 µmol / 5 min = 2 µmol/min.
- Como 1 U = 1 µmol/min, la actividad en el ensayo es de 2 U.
- Esta actividad corresponde al volumen de muestra utilizado en el ensayo (0.5 mL).
- Para obtener la actividad total en nuestra muestra original, multiplicamos por el factor de dilución o volumen total si la muestra fue diluida. En este caso, la actividad de 2 U se obtuvo de 0.5 mL de la muestra. Asumamos que nuestra muestra inicial era de 1 mL, entonces la actividad total en 1 mL sería (2 U / 0.5 mL) * 1 mL = 4 U. (Ajustar según el volumen de la muestra original si se conoce).
- Para este ejemplo, consideremos que los 0.5 mL analizados son representativos de la actividad total de la muestra, o que la actividad se reporta por mL. Si la actividad es 2 U por 0.5 mL, la actividad por mL es 4 U/mL.
2. Calcular la Cantidad de Proteína Total (en mg):
- Determinamos que 0.1 mL de la muestra contiene 0.05 mg de proteína.
- Para obtener la concentración de proteína en mg/mL: 0.05 mg / 0.1 mL = 0.5 mg/mL.
- Si la actividad se calculó por mL (4 U/mL), entonces usamos la concentración de proteína por mL.
3. Calcular la Actividad Específica:
- Actividad Específica = Actividad Enzimática (U/mL) / Concentración de Proteína (mg/mL)
- Actividad Específica = 4 U/mL / 0.5 mg/mL = 8 U/mg.
Este valor de 8 U/mg es la actividad específica de nuestra preparación enzimática. Si en una etapa posterior de purificación logramos 16 U/mg, sabríamos que hemos duplicado la pureza de nuestra enzima.
Desafíos y Consideraciones en la Medición de Actividad Proteica
La medición de la actividad proteica, aunque fundamental, no está exenta de desafíos. Varios factores pueden influir en la actividad de una proteína y, por lo tanto, en la precisión de su medición:
- Condiciones del Ensayo: El pH, la temperatura, la fuerza iónica y la presencia de cofactores o inhibidores pueden afectar drásticamente la actividad de una enzima. Es crucial optimizar y mantener constantes estas condiciones para obtener resultados reproducibles.
- Estabilidad de la Proteína: Las proteínas pueden desnaturalizarse o degradarse con el tiempo, lo que lleva a una pérdida de actividad. El almacenamiento adecuado y la manipulación cuidadosa son esenciales.
- Interferencias de la Muestra: Componentes de la muestra (sales, detergentes, otras proteínas) pueden interferir con el ensayo de actividad o con la medición de proteína total, llevando a resultados erróneos.
- Heterogeneidad de la Muestra: Si una preparación contiene múltiples formas de una proteína o isoenzimas, la actividad medida puede ser un promedio de todas ellas, lo que dificulta la caracterización precisa de una sola entidad.
- Sensibilidad del Ensayo: Algunos ensayos pueden no ser lo suficientemente sensibles para detectar bajas actividades o concentraciones de proteína.
- Unidades de Actividad: Asegurarse de utilizar las unidades correctas y consistentes (U, kat, etc.) en todo el proceso de cálculo es vital para evitar errores.
Para mitigar estos desafíos, es fundamental realizar curvas de calibración para los ensayos de proteína total, controles negativos y positivos en los ensayos de actividad, y replicar las mediciones para asegurar la reproducibilidad.
Tabla Comparativa de Ensayos de Actividad Proteica
| Tipo de Ensayo | Descripción | Aplicaciones Típicas | Ventajas | Desventajas |
|---|---|---|---|---|
| Enzimático (espectrofotométrico) | Mide cambio de absorbancia de sustrato/producto | Enzimas que catalizan reacciones con cambios ópticos | Cuantitativo, relativamente rápido, buena sensibilidad | Requiere cromóforo/fluoróforo, posibles interferencias |
| Bioensayo (celular) | Mide respuesta biológica en células vivas | Factores de crecimiento, citocinas, hormonas | Mide actividad funcional relevante, alta especificidad | Largo, costoso, variabilidad biológica, menos cuantitativo |
| ELISA Funcional | Detecta interacción proteína-ligando o respuesta in vitro | Anticuerpos, receptores, proteínas de unión | Cuantitativo, alta especificidad, menos variabilidad que bioensayos | Requiere reactivos específicos, solo evalúa una función |
| Unión (SPR, ITC) | Mide la afinidad y cinética de interacción molecular | Proteínas que interactúan con otras moléculas (receptores, ligando) | Proporciona parámetros termodinámicos y cinéticos, sin marcaje | Equipamiento costoso, requiere proteínas puras, no mide actividad catalítica |
Preguntas Frecuentes sobre la Actividad Proteica y su Medición
¿Cuál es la diferencia entre actividad y actividad específica?
La actividad (o actividad total) se refiere a la cantidad total de 'trabajo' que una enzima o proteína realiza en una muestra, generalmente expresada como unidades por volumen (ej., U/mL). La actividad específica, por otro lado, es la actividad por unidad de masa de proteína (ej., U/mg). Es una medida de la pureza de la preparación. Una alta actividad específica indica que una mayor proporción de la proteína total en la muestra es la proteína activa de interés.
¿Por qué es importante medir la actividad específica en la purificación de proteínas?
La medición de la actividad específica es crucial en la purificación de proteínas porque permite monitorear la eficiencia de cada paso de purificación. A medida que se eliminan las proteínas contaminantes, la cantidad de proteína total disminuye, mientras que la actividad de la enzima de interés se mantiene (o idealmente aumenta si se eliminan inhibidores). Esto resulta en un aumento de la actividad específica, lo que indica que la enzima se está volviendo más pura. Es el principal indicador de progreso en un proceso de purificación.
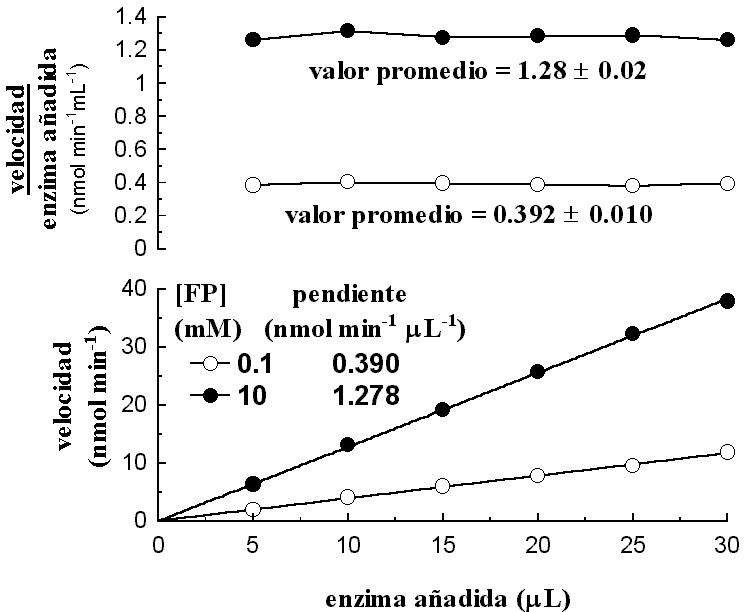
¿Qué factores pueden afectar la actividad de una proteína?
La actividad de una proteína puede verse afectada por varios factores ambientales, incluyendo el pH, la temperatura, la fuerza iónica, la presencia de cofactores (iones metálicos, moléculas orgánicas), la concentración de sustrato (para enzimas), y la presencia de inhibidores o activadores. La estructura tridimensional de la proteína es sensible a estos factores; cualquier cambio que altere su conformación óptima puede reducir o eliminar su actividad.
¿Se puede medir la actividad específica de cualquier proteína?
En principio, sí, siempre que se pueda definir y medir su actividad biológica o funcional de manera cuantitativa, y se pueda determinar con precisión la concentración de proteína total en la muestra. Para las enzimas, la actividad catalítica es clara. Para otras proteínas, como factores de crecimiento o anticuerpos, se utilizan bioensayos que miden su efecto sobre células o moléculas, expresando esa actividad en unidades biológicas o funcionales que luego se dividen por la masa de proteína.
¿Cómo se relacionan las unidades de actividad enzimática (UI) y el katal?
La Unidad Internacional (UI o U) se define como la cantidad de enzima que convierte 1 micromol (µmol) de sustrato por minuto. El katal (kat), la unidad del SI, se define como la cantidad de enzima que convierte 1 mol de sustrato por segundo. La conversión es la siguiente: 1 kat = 60,000,000 UI (1 mol/s = 10^6 µmol/s = 10^6 µmol / (1/60) min = 60 x 10^6 µmol/min). Por lo tanto, 1 UI = 16.67 nanokatales (nkat).
Dominar el cálculo de la actividad proteica, y en particular la actividad específica, es una habilidad esencial para cualquier profesional o investigador en el campo de la bioquímica y la biotecnología. No solo proporciona una medida cuantitativa del 'trabajo' que realizan estas moléculas vitales, sino que también es un indicador indispensable de la pureza de las preparaciones proteicas. Al comprender los principios subyacentes y los métodos prácticos, se abren las puertas a una investigación más precisa, al desarrollo de terapias y diagnósticos más efectivos, y a una comprensión más profunda de los intrincados mecanismos de la vida.
Si quieres conocer otros artículos parecidos a Calculando la Actividad Proteica: Guía Completa puedes visitar la categoría Cálculos.

