22/12/2024
La Calorimetría Diferencial de Barrido, comúnmente conocida como DSC por sus siglas en inglés (Differential Scanning Calorimetry), es una técnica analítica de gran potencia y versatilidad utilizada en innumerables campos, desde la ciencia de los materiales hasta la industria farmacéutica y la investigación química. Su principal fortaleza reside en su capacidad para medir cambios en el flujo de calor asociados con transiciones y reacciones que ocurren en una muestra a medida que esta es calentada, enfriada o mantenida a una temperatura constante. Comprender cómo se miden y calculan propiedades termodinámicas fundamentales, como la entalpía, es esencial para aprovechar al máximo esta herramienta.
La entalpía, una función de estado termodinámica, representa el contenido total de calor de un sistema. En el contexto del análisis térmico, los cambios de entalpía (ΔH) son indicadores directos de la energía absorbida o liberada durante procesos como la fusión, la cristalización, las transiciones de fase, o las reacciones químicas. Medir estos cambios energéticos con precisión permite a los científicos y ingenieros caracterizar materiales, predecir su comportamiento, optimizar procesos y garantizar la calidad de los productos.
- ¿Qué es la Calorimetría Diferencial de Barrido (DSC)? Un Vistazo al Principio
- La Entalpía de Reacción y Transición: ¿Cómo se Calcula en DSC?
- Más Allá de la Entalpía: Determinación del Calor Específico (Cp) con DSC
- Aplicaciones Clave de las Mediciones de Entalpía y Cp por DSC
- Factores que Influyen en la Precisión de las Mediciones DSC
- Tabla Comparativa de Eventos Térmicos y su Entalpía en DSC
- Preguntas Frecuentes sobre la Entalpía en DSC
- Conclusión
¿Qué es la Calorimetría Diferencial de Barrido (DSC)? Un Vistazo al Principio
El funcionamiento del DSC se basa en un principio ingenioso: la medición de la diferencia de flujo de calor entre una muestra y una referencia inerte. Ambas se someten exactamente al mismo régimen de temperatura controlada. Imagina un pequeño horno donde, en lugar de una sola bandeja, tienes dos: una para tu material de estudio y otra, vacía, sirviendo como referencia.
El proceso comienza con la preparación meticulosa de la muestra. Una pequeña cantidad de material, típicamente unos pocos miligramos, se coloca en un recipiente diminuto, a menudo llamado crisol. Este crisol, junto con un crisol de referencia idéntico pero vacío (o que contiene un material de referencia inerte), se inserta cuidadosamente en el calorímetro DSC. Una vez dentro, se establece un programa de temperatura predefinido. Este programa puede implicar un calentamiento constante y gradual, un enfriamiento controlado, o ciclos de calentamiento y enfriamiento a velocidades precisas.
A medida que la temperatura del sistema cambia, el equipo DSC registra con suma precisión la diferencia en el flujo de calor necesario para mantener la muestra y la referencia a la misma temperatura. El principio subyacente es que cualquier transición térmica en la muestra, como la fusión (que absorbe energía) o la cristalización (que libera energía), requerirá una cantidad diferente de calor en comparación con la referencia. Esta diferencia de energía se detecta y se traduce en una señal eléctrica.

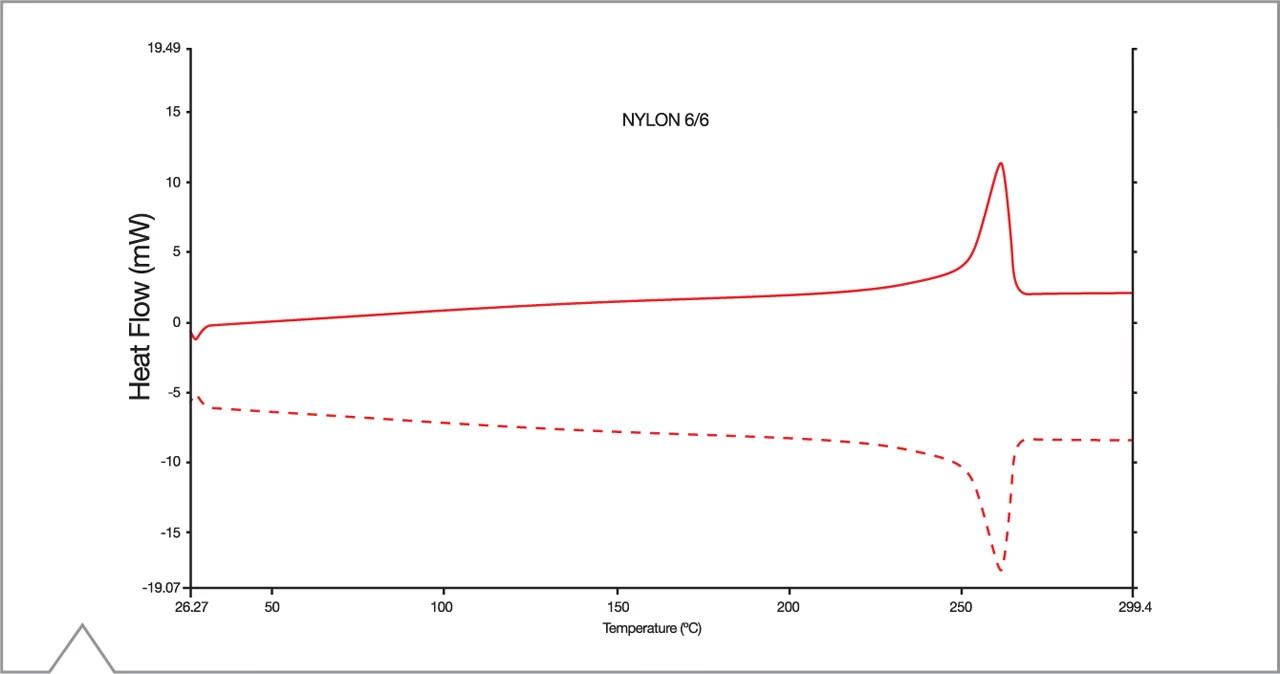
La señal resultante se grafica en lo que se conoce como un termograma DSC, que es una curva de flujo de calor (en vatios o milivatios) en función de la temperatura o el tiempo. En este gráfico, los picos y valles son las huellas digitales de los eventos térmicos específicos que ocurren en la muestra. Por ejemplo, un pico endotérmico (hacia abajo) indica un proceso que absorbe calor, como la fusión o la evaporación, mientras que un pico exotérmico (hacia arriba) señala un proceso que libera calor, como la cristalización o una reacción de curado. La interpretación detallada de estos gráficos es lo que permite a los científicos deducir propiedades térmicas cruciales, como temperaturas de transición, pureza del material, estabilidad térmica y el comportamiento bajo diversas condiciones de temperatura.
La Entalpía de Reacción y Transición: ¿Cómo se Calcula en DSC?
La capacidad del DSC para cuantificar los cambios de energía lo convierte en una herramienta invaluable para determinar la entalpía asociada a diversos procesos. La entalpía de reacción o de una transición de fase se obtiene directamente del termograma mediante un proceso de integración. Este proceso implica calcular el área bajo el pico termodinámico correspondiente y por encima de una línea base interpolada.
Imagina un pico en tu termograma que representa la fusión de un polímero. La máquina DSC registra el flujo de calor en cada punto de temperatura. El área de este pico, desde el inicio de la transición hasta su finalización, representa la cantidad total de energía absorbida o liberada durante ese evento. Para aislar la energía específica de la transición, se traza una línea base. Esta línea base es esencialmente una interpolación entre el punto de inicio de la reacción o transición y el punto en que esta finaliza. La integración del área entre la curva del pico y esta línea base proporciona el valor de la entalpía.
Por ejemplo, si el DSC detecta un pico de reacción y, al integrar su área con la línea base interpolada, se determina una entalpía de 242,35 J/g, esto significa que cada gramo de la muestra experimentó un cambio energético de esa magnitud durante la reacción. Esta entalpía suele expresarse en julios por gramo (J/g), lo que indica la energía por unidad de masa, una medida fundamental para la caracterización de materiales. Es crucial que el equipo esté correctamente calibrado en términos de flujo de calor para obtener valores de entalpía precisos.

Más Allá de la Entalpía: Determinación del Calor Específico (Cp) con DSC
Aunque la entalpía es una medida de la energía total de una transición, el DSC también es una herramienta excelente para determinar otra propiedad térmica fundamental: el calor específico (Cp). El calor específico es la cantidad de energía necesaria para elevar la temperatura de una unidad de masa de una sustancia en un grado Celsius (o Kelvin). A diferencia de la entalpía, que se asocia con transiciones de fase o reacciones, el Cp se refiere a la energía necesaria para un cambio de temperatura sin cambio de fase.
En un DSC ideal, la línea base de un crisol vacío se mantendría en cero milivatios (unidades de flujo de calor). Sin embargo, cuando se calienta una muestra, la línea base se desplaza. Este desplazamiento no es un pico, sino un cambio gradual en el flujo de calor que se mantiene constante a medida que la temperatura aumenta. Este cambio en el flujo de calor es directamente proporcional al calor específico de la muestra. La relación se describe mediante la siguiente ecuación:
dQ/dt = Cp * β * W
Donde:
- dQ/dt es el flujo de calor medido por el DSC (en vatios o milivatios).
- Cp es el calor específico de la muestra (en J/g·°C o J/g·K).
- β es la velocidad de calentamiento (en °C/min o K/min).
- W es la masa de la muestra (en gramos).
Para determinar el Cp de una muestra, se suelen realizar tres corridas DSC: una con el crisol vacío, una con un material de referencia con Cp conocido (como el zafiro), y una con la muestra problema. Comparando los desplazamientos de la línea base de estas tres corridas, y utilizando la ecuación anterior, se puede calcular el Cp de la muestra a diferentes temperaturas. Esto es particularmente útil para estudiar la capacidad de un material para almacenar energía térmica o para predecir su comportamiento en aplicaciones donde los cambios de temperatura son comunes.
Aplicaciones Clave de las Mediciones de Entalpía y Cp por DSC
Las mediciones de entalpía y calor específico con DSC tienen un impacto significativo en diversas industrias y campos de investigación. Aquí se presentan algunas de las aplicaciones más importantes:
- Caracterización de Polímeros: El DSC es indispensable en la ciencia de los polímeros. Permite determinar la temperatura de transición vítrea (Tg), temperaturas y entalpías de fusión (ΔHfusión), y temperaturas y entalpías de cristalización (ΔHcristalización). También se utiliza para estudiar el curado de resinas, la polimerización y la degradación térmica. Por ejemplo, la entalpía de fusión de un polímero puede indicar su cristalinidad, lo que influye directamente en sus propiedades mecánicas y ópticas.
- Análisis Farmacéutico: En la industria farmacéutica, el DSC es crucial para el estudio de polimorfismo, es decir, la existencia de diferentes formas cristalinas de un mismo compuesto. Cada polimorfo puede tener diferentes propiedades de solubilidad, estabilidad y biodisponibilidad, y el DSC puede diferenciar entre ellos por sus distintas entalpías de fusión. También se usa para evaluar la pureza de los fármacos y la estabilidad de las formulaciones, detectando posibles reacciones de degradación.
- Estudios de Materiales Metálicos y Cerámicos: Aunque más comúnmente asociado con polímeros, el DSC también se aplica a metales y cerámicas para estudiar transformaciones de fase, recristalización, y transiciones magnéticas. Las entalpías asociadas a estas transiciones son vitales para entender el procesamiento y el rendimiento de estos materiales.
- Seguridad y Procesos Químicos: La medición de la entalpía de reacción (calor de reacción) es fundamental para la seguridad en procesos químicos. Permite identificar reacciones exotérmicas que podrían ser peligrosas si no se controlan adecuadamente, ayudando a diseñar procesos más seguros y eficientes.
- Control de Calidad: En la fabricación, el DSC se utiliza para asegurar la consistencia del material de un lote a otro. Al verificar que las entalpías de fusión, cristalización o reacción caen dentro de un rango aceptable, los fabricantes pueden garantizar que las propiedades del producto final cumplen con las especificaciones.
Factores que Influyen en la Precisión de las Mediciones DSC
Para obtener resultados precisos y fiables en las mediciones de entalpía y calor específico con DSC, es fundamental considerar varios factores que pueden influir en la calidad de los datos:
- Calibración: Una calibración precisa del equipo es el pilar de cualquier medición cuantitativa con DSC. Esto incluye la calibración de la temperatura (usando materiales con puntos de fusión conocidos como indio, estaño o zinc) y la calibración de la entalpía (utilizando materiales con entalpías de fusión conocidas). Una calibración inadecuada puede llevar a errores significativos en los valores de entalpía y Cp.
- Preparación de la Muestra: La masa de la muestra debe ser precisa, generalmente en el rango de 1 a 20 mg, dependiendo de la sensibilidad del equipo y la magnitud de la transición. La homogeneidad de la muestra, el tamaño de partícula y el empaquetamiento en el crisol son también cruciales. Una muestra mal preparada puede resultar en picos anchos, superpuestos o en una señal débil.
- Velocidad de Calentamiento/Enfriamiento: La velocidad a la que se barre la temperatura (β) afecta la resolución y la sensibilidad del termograma. Velocidades más lentas suelen proporcionar una mejor resolución de picos superpuestos, mientras que velocidades más rápidas pueden aumentar la sensibilidad para transiciones débiles. Sin embargo, velocidades muy altas pueden desplazar las temperaturas de transición y reducir la precisión de la integración de la entalpía.
- Atmósfera del Horno: La atmósfera dentro del horno del DSC (aire, nitrógeno, argón, etc.) puede influir en los resultados, especialmente si la muestra es sensible al oxígeno o a la humedad. El uso de un gas inerte (como nitrógeno) es común para evitar reacciones de oxidación o degradación durante el calentamiento.
- Línea Base: La estabilidad y la correcta corrección de la línea base son fundamentales para una integración precisa del área del pico. Una línea base inestable o con pendiente incorrecta puede introducir errores sustanciales en el cálculo de la entalpía. A menudo se realizan corridas de línea base con crisoles vacíos para restar cualquier contribución instrumental.
Tabla Comparativa de Eventos Térmicos y su Entalpía en DSC
| Evento Térmico | Descripción | Medición de Entalpía |
|---|---|---|
| Fusión | Transición de estado sólido a líquido. | Entalpía de Fusión (ΔHfusión): Energía absorbida por la muestra. |
| Cristalización | Transición de estado líquido a sólido (ordenamiento molecular). | Entalpía de Cristalización (ΔHcristalización): Energía liberada por la muestra. |
| Reacción Química | Proceso químico que absorbe o libera energía (ej. polimerización, curado). | Entalpía de Reacción (ΔHreacción): Energía neta absorbida o liberada. |
| Transición Vítrea (Tg) | Transición de un estado rígido y vítreo a un estado más blando y gomoso (en polímeros amorfos). | Cambio en el Calor Específico (ΔCp), no una entalpía de transición directa (es un cambio de línea base, no un pico). |
| Evaporación/Sublimación | Transición de líquido a vapor o sólido a vapor. | Entalpía de Vaporización/Sublimación: Energía absorbida. |
Preguntas Frecuentes sobre la Entalpía en DSC
¿Qué es exactamente la entalpía en el contexto del DSC?
La entalpía, en este contexto, es la cantidad de energía térmica (calor) que una muestra absorbe o libera durante un proceso físico o químico, como la fusión, la cristalización o una reacción. El DSC mide este cambio energético y lo cuantifica como el área bajo el pico en un termograma.
¿Por qué es importante medir la entalpía con DSC?
Medir la entalpía es crucial porque proporciona información cuantitativa sobre la energía de los procesos. Esto permite caracterizar materiales, entender su comportamiento térmico, determinar la pureza, estudiar la cinética de reacciones, evaluar la estabilidad y optimizar procesos de fabricación en diversas industrias.

¿Qué tipos de muestras se pueden analizar con DSC para medir entalpía?
El DSC es una técnica muy versátil que puede analizar una amplia gama de materiales, incluyendo polímeros (termoplásticos, termoestables, elastómeros), productos farmacéuticos, alimentos, materiales biológicos, cerámicas, metales y aleaciones. La muestra debe ser relativamente pequeña (unos pocos miligramos) y puede estar en forma sólida, líquida o en polvo.
¿Cómo se asegura la precisión en las mediciones de entalpía con DSC?
La precisión se asegura mediante una rigurosa calibración del equipo (temperatura y flujo de calor), una cuidadosa preparación de la muestra (masa, homogeneidad), el uso de velocidades de calentamiento apropiadas, el control de la atmósfera del horno y una correcta definición e integración de la línea base en el termograma.
¿Cuál es la diferencia entre la entalpía y el calor específico en DSC?
La entalpía (ΔH) es la energía total absorbida o liberada durante una transición de fase o una reacción, y se mide como el área de un pico en el termograma. El calor específico (Cp), por otro lado, es la energía necesaria para cambiar la temperatura de una sustancia sin que haya un cambio de fase, y se mide por el desplazamiento de la línea base en el termograma. Ambos son parámetros termodinámicos fundamentales, pero describen diferentes aspectos del comportamiento térmico de un material.
Conclusión
La Calorimetría Diferencial de Barrido (DSC) es una herramienta indispensable en el laboratorio moderno, ofreciendo una ventana única al comportamiento térmico de los materiales. Su capacidad para cuantificar la entalpía de transiciones y reacciones, así como para determinar el calor específico, la convierte en una técnica fundamental para la investigación, el desarrollo y el control de calidad. Al comprender los principios detrás de estas mediciones y las complejidades de su aplicación, los científicos e ingenieros pueden desbloquear el potencial completo del DSC para innovar y mejorar una vasta gama de productos y procesos. La precisión de sus mediciones de entalpía y calor específico continúa siendo un pilar para el avance en la ciencia de materiales y más allá.
Si quieres conocer otros artículos parecidos a Entalpía en DSC: Medición y Significado puedes visitar la categoría Cálculos.
