12/05/2024
En el corazón de la termodinámica yace un concepto fundamental: la energía interna de un sistema, denotada como ΔU. Comprender cómo calcular este cambio energético es crucial para analizar cualquier proceso físico o químico, desde el funcionamiento de un motor hasta la complejidad del metabolismo humano. La energía interna es una propiedad intrínseca de un sistema que nos permite entender cómo la energía se transforma y se conserva. A menudo, el cálculo de ΔU se realiza a través de la Primera Ley de la Termodinámica, una de las leyes más potentes de la física que nos permite cuantificar las interacciones de energía entre un sistema y su entorno.

A lo largo de este artículo, exploraremos en profundidad el concepto de energía interna, su relación con el calor y el trabajo, y cómo la Primera Ley de la Termodinámica nos proporciona las herramientas para calcularla. Nos centraremos en la convención de signos adoptada en exámenes como el College Board AP Physics 2, donde la ecuación se expresa como ΔU = Q + W, con W representando el trabajo realizado sobre el sistema. Prepárate para desentrañar los misterios de la energía y su impacto en nuestro mundo.
- ¿Qué es la Energía Interna (ΔU)?
- La Primera Ley de la Termodinámica: ΔU = Q + W
- Calor (Q) y Trabajo (W): Formas de Transferencia de Energía
- La Independencia de la Trayectoria de la Energía Interna
- Ejemplos Prácticos de Cálculo de ΔU
- El Metabolismo Humano y la Primera Ley
- Energía Interna de un Gas Ideal y su Relación con la Temperatura
- Capacidad Calorífica Molar a Volumen Constante (Cv)
- Trabajo de Expansión y Compresión
- Resumen de Términos Clave en Termodinámica
- Preguntas Frecuentes (FAQ)
- ¿Cómo se describe una tetera hirviendo en términos termodinámicos?
- ¿En qué se diferencian la Primera Ley de la Termodinámica y la conservación de la energía?
- ¿Puedes dar ejemplos de energía en tránsito y energía almacenada?
- ¿Cuál es la diferencia entre transferencia de calor y energía interna?
- ¿Qué le ocurre a la energía cinética y potencial cuando bajas escaleras y te detienes?
- ¿Cómo se relaciona la energía de los alimentos (calorías) con la energía potencial molecular?
- Identifica el tipo de energía transferida a tu cuerpo en situaciones específicas: (a) tomar el sol; (b) comer; (c) subir en un ascensor.
¿Qué es la Energía Interna (ΔU)?
La energía interna (U) de un sistema es la suma de todas las energías cinéticas y potenciales de sus átomos y moléculas. Piensa en ella como la energía total almacenada dentro de un sistema a nivel microscópico. A nivel atómico y molecular, esta energía incluye la energía cinética de traslación, rotación y vibración de las partículas, así como la energía potencial debida a las inter interacciones entre ellas. Es una propiedad de estado, lo que significa que su valor depende únicamente del estado actual del sistema (definido por variables como la presión, el volumen y la temperatura), y no de cómo llegó a ese estado. Esto la convierte en una magnitud independiente de la trayectoria, un concepto fundamental en termodinámica.
Cuando hablamos de ΔU, nos referimos al cambio en la energía interna del sistema, es decir, la diferencia entre la energía interna final y la energía interna inicial. Este cambio es lo que podemos medir y calcular en la práctica, ya que la energía interna absoluta de un sistema es muy difícil de determinar.
La Primera Ley de la Termodinámica: ΔU = Q + W
La Primera Ley de la Termodinámica es esencialmente una declaración del principio de conservación de la energía, aplicada a sistemas donde la transferencia de calor (Q) y la realización de trabajo (W) son los métodos de transferencia de energía hacia o desde el sistema. Esta ley establece que el cambio en la energía interna de un sistema (ΔU) es igual al calor neto transferido al sistema (Q) más el trabajo neto realizado sobre el sistema (W).
En su forma matemática, y siguiendo la convención de signos utilizada en el College Board AP Physics 2, la Primera Ley de la Termodinámica se expresa como:
ΔU = Q + W
Donde:
- ΔU es el cambio en la energía interna del sistema.
- Q es la transferencia de calor neta hacia el sistema.
- W es el trabajo neto realizado sobre el sistema.
Convención de Signos Crucial para ΔU = Q + W
La correcta aplicación de esta ecuación depende de una comprensión clara de las convenciones de signos para Q y W:
- Para Q (Calor):
- Si Q es positivo (+), significa que hay una transferencia neta de calor hacia el sistema. El sistema absorbe calor.
- Si Q es negativo (-), significa que hay una transferencia neta de calor fuera del sistema. El sistema libera calor al entorno.
- Para W (Trabajo):
- Si W es positivo (+), significa que se realiza trabajo sobre el sistema por parte del entorno. Por ejemplo, al comprimir un gas.
- Si W es negativo (-), significa que el sistema realiza trabajo sobre el entorno. Por ejemplo, un gas que se expande y empuja un pistón.
Es importante notar que existen otras convenciones de signos en termodinámica (por ejemplo, donde W es positivo cuando el sistema realiza trabajo). Sin embargo, para los propósitos de este artículo y para alinearnos con la convención específica mencionada, nos ceñiremos estrictamente a ΔU = Q + W, donde W es el trabajo realizado *sobre* el sistema.
La Primera Ley de la Termodinámica es fundamental porque nos dice que la energía no se crea ni se destruye, solo se transforma. Cualquier cambio en la energía interna de un sistema debe ser el resultado de la transferencia de calor o de la realización de trabajo.
Calor (Q) y Trabajo (W): Formas de Transferencia de Energía
El calor y el trabajo son las dos formas principales en las que la energía puede ser transferida hacia o desde un sistema. Aunque ambos pueden producir resultados similares, como un aumento de temperatura, son procesos fundamentalmente diferentes:
- Calor (Q): Es la transferencia de energía que ocurre debido a una diferencia de temperatura entre el sistema y su entorno. Es un proceso menos organizado, impulsado por el movimiento aleatorio de las moléculas. Por ejemplo, el Sol calentando el aire en un neumático de bicicleta. El calor no se almacena como tal en un sistema; es energía en tránsito.
- Trabajo (W): Es la transferencia de energía que implica una fuerza macroscópica que actúa a través de una distancia. Es un proceso organizado y ordenado. Por ejemplo, cuando un ciclista bombea aire en un neumático, se realiza trabajo sobre el aire. Al igual que el calor, el trabajo no se almacena en el sistema; es energía en tránsito.
La clave es que, una vez que la energía ha sido transferida y ha cambiado la energía interna del sistema, es imposible distinguir si ese cambio fue causado por calor o por trabajo. Ambos contribuyen al cambio en la energía interna, pero no son formas de energía almacenada en sí mismas.
La Independencia de la Trayectoria de la Energía Interna
Uno de los conceptos más importantes de la energía interna es su independencia de la trayectoria. Esto significa que el cambio en la energía interna (ΔU) entre dos estados de equilibrio dados de un sistema es siempre el mismo, independientemente de la serie de pasos (la trayectoria) que el sistema haya seguido para pasar del estado inicial al estado final. En contraste, tanto el calor (Q) como el trabajo (W) son dependientes de la trayectoria; sus valores pueden variar significativamente según cómo se realice el proceso.
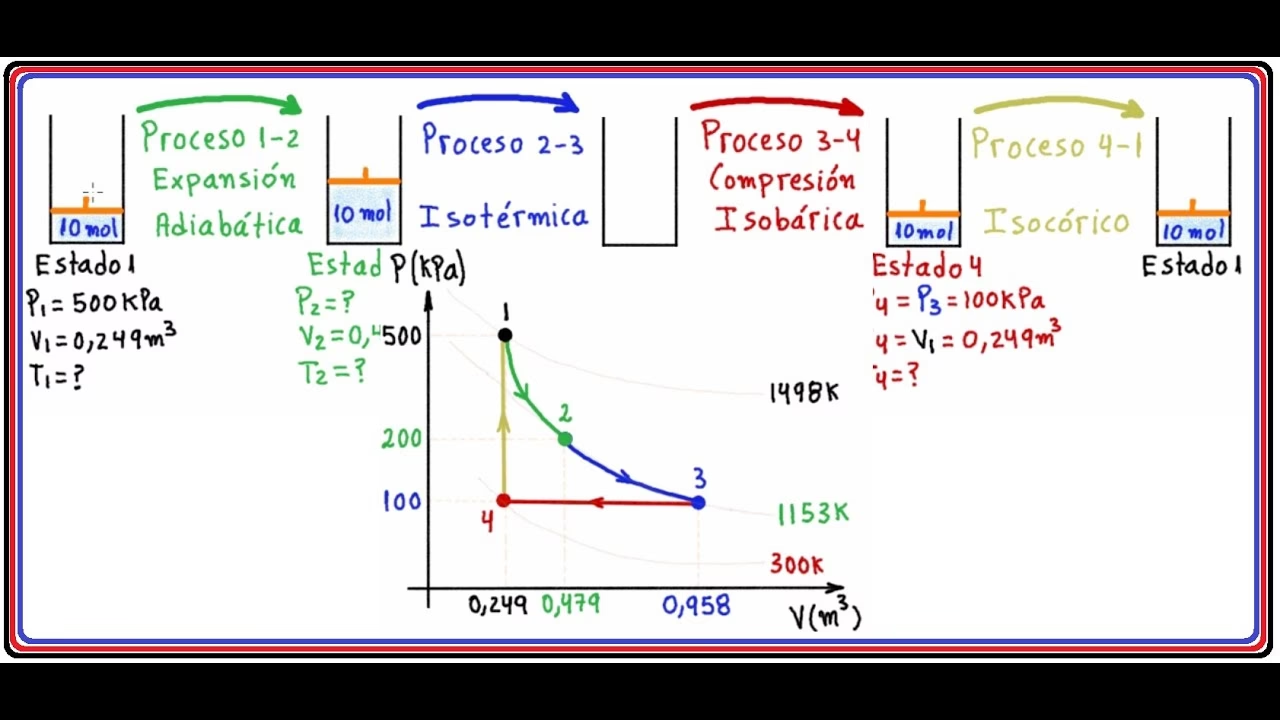
Esta independencia de la trayectoria hace que la energía interna sea una propiedad de estado muy útil. Si conocemos el estado inicial y final de un sistema (por ejemplo, su presión, volumen y temperatura), podemos determinar el cambio en su energía interna sin necesidad de conocer los detalles exactos de cómo se llevó a cabo la transformación.
Ejemplos Prácticos de Cálculo de ΔU
Veamos cómo aplicar la Primera Ley de la Termodinámica con la convención de ΔU = Q + W (trabajo realizado sobre el sistema) a algunos ejemplos concretos.
Caso 1: Múltiples Procesos
Supongamos un sistema que experimenta dos procesos consecutivos:
- Primero, se transfieren 40.00 J de calor al sistema, y el sistema realiza 10.00 J de trabajo sobre el entorno.
- Luego, se transfieren 25.00 J de calor fuera del sistema, mientras que se realizan 4.00 J de trabajo sobre el sistema.
¿Cuál es el cambio neto en la energía interna del sistema?
Estrategia:
Para resolver esto, primero debemos determinar el calor neto (Q) y el trabajo neto (W) para cada paso, aplicando las convenciones de signos. Luego, usaremos ΔU = Q + W para cada paso y sumaremos los resultados.
Solución:
Paso 1:
- Transferencia de calor al sistema: Q₁ = +40.00 J (positivo porque entra).
- Trabajo realizado por el sistema: 10.00 J. Como W en nuestra ecuación es trabajo sobre el sistema, W₁ = -10.00 J (negativo porque el sistema lo realiza).
- Cambio en energía interna para el Paso 1: ΔU₁ = Q₁ + W₁ = 40.00 J + (-10.00 J) = 30.00 J.
Paso 2:
- Transferencia de calor fuera del sistema: Q₂ = -25.00 J (negativo porque sale).
- Trabajo realizado sobre el sistema: 4.00 J. Como W en nuestra ecuación es trabajo sobre el sistema, W₂ = +4.00 J (positivo porque se realiza sobre el sistema).
- Cambio en energía interna para el Paso 2: ΔU₂ = Q₂ + W₂ = -25.00 J + 4.00 J = -21.00 J.
Cambio neto en energía interna:
- ΔU_neto = ΔU₁ + ΔU₂ = 30.00 J + (-21.00 J) = 9.00 J.
Discusión:
Este ejemplo ilustra que, sin importar si analizamos el proceso global o lo dividimos en pasos, el cambio total en la energía interna es el mismo. Esto refuerza la idea de que ΔU es una función de estado.
Caso 2: Proceso Directo
¿Cuál es el cambio en la energía interna de un sistema cuando un total de 150.00 J de transferencia de calor ocurre fuera del sistema y se realizan 159.00 J de trabajo sobre el sistema?
Solución:
- Transferencia de calor fuera del sistema: Q = -150.00 J (negativo porque sale).
- Trabajo realizado sobre el sistema: W = +159.00 J (positivo porque se realiza sobre el sistema).
- Cambio en energía interna: ΔU = Q + W = -150.00 J + 159.00 J = 9.00 J.
Discusión:
Curiosamente, un proceso muy diferente en este segundo caso produce el mismo cambio de 9.00 J en la energía interna que en el Caso 1. Esto subraya nuevamente la independencia de la trayectoria de ΔU; el estado final del sistema es el mismo en ambos escenarios, a pesar de que los caminos tomados (las combinaciones de Q y W) fueron distintos.
El Metabolismo Humano y la Primera Ley
El metabolismo humano es un ejemplo fascinante de la Primera Ley de la Termodinámica en acción. Si consideramos el cuerpo humano como el sistema de interés, podemos analizar cómo el calor, el trabajo y la energía interna interactúan en actividades cotidianas, desde el sueño hasta el ejercicio intenso.
Nuestro cuerpo mantiene una temperatura constante mediante la transferencia de calor al entorno. Esto implica que, en condiciones normales, la transferencia de calor (Q) desde el cuerpo es negativa (sale energía). Además, el cuerpo suele realizar trabajo sobre el mundo exterior (mover objetos, caminar), lo que significa que el trabajo realizado *por* el sistema es positivo, y por nuestra convención, el trabajo *sobre* el sistema (W) es negativo. En estas situaciones, el cuerpo tiende a perder energía interna (ΔU sería negativo).
Sin embargo, la ingesta de alimentos aumenta la energía interna del cuerpo al añadir energía potencial química. El metabolismo es un proceso de oxidación que libera esta energía. Si la ingesta de alimentos es adecuada para compensar las pérdidas por calor y trabajo, nuestra energía interna promedio se mantiene constante.

Las Calorías: Una Unidad de Energía Vital
La energía de los alimentos se mide en una unidad especial conocida como Calorie (con 'C' mayúscula). Una Calorie dietética equivale a una kilocaloría para un químico (1 Cal = 1 kcal = 1000 calorías). Una caloría (con 'c' minúscula) se define como la energía necesaria para elevar la temperatura de un gramo de agua pura en un grado Celsius.
Cuando comemos en exceso, nuestra ΔU es constantemente positiva, y el cuerpo almacena esta energía extra como grasa. Por el contrario, si comemos muy poco, ΔU es negativa, y el cuerpo metaboliza su propia grasa para mantener la temperatura y realizar trabajo, lo que lleva a la pérdida de peso. El ejercicio ayuda a la pérdida de peso no solo por el calor liberado y el trabajo realizado, sino también porque eleva la tasa metabólica basal (TMB), que es la velocidad a la que los alimentos se convierten en calor y trabajo en reposo.
Los sistemas vivos, como el cuerpo humano, no están en equilibrio térmico y exhiben procesos irreversibles. Por ejemplo, aunque la grasa corporal se puede convertir en trabajo y calor, el trabajo realizado sobre el cuerpo y la transferencia de calor hacia él no se pueden convertir en grasa corporal. La fotosíntesis en plantas es otro ejemplo de proceso irreversible, donde la energía luminosa se convierte en energía potencial química.
Energía Interna de un Gas Ideal y su Relación con la Temperatura
Para un gas ideal, la energía interna tiene una relación particularmente simple con la temperatura. La energía interna total de un gas ideal puede considerarse como la energía cinética total de todas sus moléculas. Dado que la energía cinética promedio de las moléculas de un gas ideal es directamente proporcional a la temperatura absoluta, la energía interna de un gas ideal depende solo de su temperatura. Matemáticamente, para un gas monoatómico ideal, la energía interna (U) se puede expresar como:
U = (3/2) nRT o U = (3/2) NkT
Donde:
- n es el número de moles del gas.
- R es la constante de los gases ideales.
- N es el número de moléculas.
- k es la constante de Boltzmann.
- T es la temperatura absoluta en Kelvin.
Esta relación es crucial porque simplifica considerablemente el análisis termodinámico de los gases ideales, ya que cualquier cambio en su energía interna está directamente ligado a un cambio en su temperatura.
Capacidad Calorífica Molar a Volumen Constante (Cv)
Un concepto derivado de la Primera Ley y la energía interna es la capacidad calorífica molar a volumen constante (Cᵥ). Si un gas se encuentra en un recipiente rígido (volumen constante), no puede expandirse ni contraerse, por lo que no realiza trabajo sobre su entorno, ni el entorno realiza trabajo sobre él (W = 0).
En este caso, la Primera Ley de la Termodinámica se simplifica a:
ΔU = Q + 0 => ΔU = Q
Esto significa que todo el calor que entra o sale del sistema a volumen constante se traduce directamente en un cambio en su energía interna. La capacidad calorífica molar a volumen constante se define como la cantidad de calor necesaria para elevar la temperatura de un mol de gas en un grado Celsius (o Kelvin) a volumen constante. Matemáticamente:
Cᵥ = (dQ / dT)V = (dU / dT)V
Para un gas ideal, esta relación nos permite vincular directamente la energía interna con la temperatura y la capacidad de absorber calor.
Trabajo de Expansión y Compresión
El trabajo (W) en termodinámica, especialmente en gases, a menudo se relaciona con cambios de volumen. Cuando un gas se expande, realiza trabajo sobre su entorno (W negativo según nuestra convención). Cuando un gas se comprime, el entorno realiza trabajo sobre él (W positivo).
La cantidad de trabajo realizado depende de la trayectoria termodinámica seguida. Algunos procesos comunes incluyen:
- Proceso Isobárico: Ocurre a presión constante. El trabajo es W = -PΔV (si W es trabajo por el sistema), o W = PΔV (si W es trabajo sobre el sistema, como en nuestra convención).
- Proceso Isotérmico: Ocurre a temperatura constante. Para un gas ideal, esto implica que ΔU = 0, por lo que Q = -W.
- Proceso Adiabático: No hay transferencia de calor (Q = 0). Todo el cambio en la energía interna se debe al trabajo (ΔU = W).
- Proceso Isocórico: Ocurre a volumen constante (ΔV = 0), por lo que no se realiza trabajo (W = 0). En este caso, ΔU = Q.
Estos diferentes procesos ilustran cómo el trabajo, siendo dependiente de la trayectoria, influye en el cambio de energía interna junto con el calor.

Resumen de Términos Clave en Termodinámica
Para consolidar la comprensión, presentamos una tabla comparativa de los términos fundamentales relacionados con la Primera Ley de la Termodinámica:
| Término | Definición | Dependencia de la Trayectoria | Signo Positivo Implica... |
|---|---|---|---|
| Energía Interna (ΔU) | Suma de las energías cinéticas y potenciales de los átomos y moléculas de un sistema. | Independiente de la trayectoria (función de estado). | Aumento de la energía interna del sistema. |
| Calor (Q) | Energía transferida debido a una diferencia de temperatura. Proceso menos organizado. | Dependiente de la trayectoria. | Transferencia de calor hacia el sistema. |
| Trabajo (W) | Energía transferida por una fuerza que actúa a través de una distancia. Proceso organizado. | Dependiente de la trayectoria. | Trabajo realizado sobre el sistema. |
Preguntas Frecuentes (FAQ)
¿Cómo se describe una tetera hirviendo en términos termodinámicos?
Una tetera hirviendo es un excelente ejemplo termodinámico. El calor se transfiere al agua desde la fuente de energía (cocina). Este calor aumenta la energía interna del agua, elevando su temperatura hasta el punto de ebullición. Una vez que hierve, parte del calor se convierte en trabajo a medida que el vapor se expande y escapa, o incluso puede mover una pequeña tapa. La tetera mantiene su energía interna siempre y cuando se le siga suministrando calor, compensando la energía que se pierde en forma de vapor y calor al ambiente.
¿En qué se diferencian la Primera Ley de la Termodinámica y la conservación de la energía?
La Primera Ley de la Termodinámica es, de hecho, una forma específica de la ley de conservación de la energía, pero adaptada a sistemas donde las transferencias de energía ocurren principalmente como calor y trabajo. Mientras que la conservación de la energía es un principio universal que abarca todas las formas de energía (cinética, potencial, química, etc.), la Primera Ley se enfoca en cómo el calor y el trabajo afectan la energía interna de un sistema termodinámico.
¿Puedes dar ejemplos de energía en tránsito y energía almacenada?
Claro. El calor (Q) y el trabajo (W) son ejemplos de energía en tránsito; no se almacenan en un sistema. Por ejemplo, la electricidad que fluye por un cable es energía en tránsito. La energía interna (ΔU), en cambio, es energía almacenada dentro del sistema, como la energía química en una batería o la energía térmica de un gas en un recipiente cerrado.
¿Cuál es la diferencia entre transferencia de calor y energía interna?
La transferencia de calor es el proceso por el cual la energía se mueve entre un sistema y su entorno debido a una diferencia de temperatura. La energía interna es la energía total almacenada dentro del sistema a nivel microscópico. El calor es una forma de transferencia, mientras que la energía interna es una propiedad del estado del sistema. El calor puede cambiar la energía interna, pero no es la energía interna en sí misma.
¿Qué le ocurre a la energía cinética y potencial cuando bajas escaleras y te detienes?
Cuando bajas escaleras, tu energía potencial gravitatoria disminuye y tu energía cinética aumenta. Al detenerte, tu energía cinética se convierte principalmente en calor debido a la fricción interna en tus músculos y articulaciones, y se disipa en el entorno. La energía potencial que perdiste también se convierte en calor o se utiliza para realizar trabajo sobre el entorno (por ejemplo, el sonido de tus pasos).
¿Cómo se relaciona la energía de los alimentos (calorías) con la energía potencial molecular?
La energía de los alimentos, medida en calorías, puede verse como energía potencial química almacenada en las moléculas complejas (carbohidratos, grasas, proteínas). Cuando metabolizamos estos alimentos, las reacciones químicas rompen estos enlaces moleculares, liberando la energía almacenada. Esta energía liberada aumenta la energía interna de nuestro cuerpo, que luego se utiliza para realizar trabajo y generar calor, de acuerdo con la Primera Ley de la Termodinámica.
Identifica el tipo de energía transferida a tu cuerpo en situaciones específicas: (a) tomar el sol; (b) comer; (c) subir en un ascensor.
- (a) Tomar el sol: Se transfiere energía a tu cuerpo principalmente como calor (Q), específicamente radiación térmica.
- (b) Comer: La energía se transfiere a tu cuerpo como energía interna, almacenada en forma de energía potencial química en los alimentos, que luego se metaboliza.
- (c) Subir en un ascensor: Se realiza trabajo (W) sobre tu cuerpo por parte del ascensor, aumentando tu energía potencial gravitatoria (y por lo tanto, tu energía interna, aunque en este contexto es más una transformación de energía potencial que una transferencia de calor o trabajo en el sentido termodinámico de un sistema cerrado).
La comprensión de la energía interna y la Primera Ley de la Termodinámica es un pilar para el estudio de la física y la ingeniería. Nos permite no solo cuantificar los cambios energéticos en diversos sistemas, sino también apreciar la intrincada danza de calor y trabajo que rige nuestro universo. Desde el motor más simple hasta los complejos procesos biológicos, la conservación de la energía y sus transformaciones son constantes, recordándonos que la energía es una fuerza omnipresente y siempre en evolución.
Si quieres conocer otros artículos parecidos a Desentrañando ΔU: La Energía Interna en Termodinámica puedes visitar la categoría Cálculos.
