05/08/2022
La sal, o cloruro de sodio (NaCl), es una sustancia omnipresente en nuestra vida diaria y en una vasta gama de industrias. Su concentración es un parámetro crítico que debe ser medido y controlado con precisión, ya sea en la industria alimentaria para la conservación y el sabor, en el sector de la salud para soluciones fisiológicas, en la agricultura para la salinidad del suelo o en procesos industriales para evitar la corrosión. Entender cómo se calcula y determina la concentración de sal es fundamental para garantizar la calidad, la seguridad y la eficiencia en múltiples aplicaciones. Este artículo explorará diferentes métodos y conceptos clave para desentrañar el misterio detrás de la concentración de sal.
- ¿Qué es la Concentración y Por Qué es Importante la Sal?
- Determinación de la Concentración de Sal: El Método Volhard
- Cálculo del Porcentaje de Sal a Partir del Sodio en Alimentos
- ¿Cómo se Calcula la Concentración Normal de una Sal?
- Tabla Comparativa de Unidades de Concentración
- Preguntas Frecuentes (FAQs)
- Conclusión
¿Qué es la Concentración y Por Qué es Importante la Sal?
La concentración, en el ámbito de la química, se refiere a la cantidad de soluto disuelto en una cantidad dada de disolvente o de solución. Se puede expresar de diversas maneras, como porcentaje en masa, porcentaje en volumen, molaridad, molalidad o, como veremos, normalidad. Cada una de estas unidades ofrece una perspectiva diferente sobre la composición de una mezcla.
La sal, específicamente el cloruro de sodio (NaCl), juega un papel vital en numerosas áreas. En la alimentación, es un conservante natural y un potenciador del sabor insustituible. En la medicina, soluciones salinas con concentraciones precisas son esenciales para hidratación y tratamientos. En la industria, se utiliza en la producción de cloro, soda cáustica y en procesos de ablandamiento de agua. Dada su importancia, la capacidad de determinar y controlar su concentración con exactitud es de suma relevancia, impactando desde la salud pública hasta la eficiencia de procesos productivos.
Determinación de la Concentración de Sal: El Método Volhard
Cuando se requiere una determinación precisa de la concentración de iones cloruro (y por ende, de sal) en una muestra, uno de los métodos clásicos y más fiables en química analítica es el método de Volhard. Este método es una titulación por retroceso, o titulación por retroceso, lo que significa que en lugar de valorar directamente el analito, se añade un exceso conocido de un reactivo y luego se titula el exceso no reaccionado. Es particularmente útil para determinar iones cloruro en presencia de iones que pueden interferir en otras titulaciones directas.
Principio y Procedimiento del Método Volhard
El método Volhard se basa en la precipitación de los iones cloruro con iones plata (Ag⁺) y la posterior titulación del exceso de plata. A continuación, se detalla el procedimiento:
- Preparación de la Muestra: La muestra que contiene la sal (cloruro de sodio) debe ser preparada adecuadamente. En muchos casos, especialmente con muestras orgánicas o complejas, se requiere una fase de digestión. El texto menciona que la muestra "se incinera en húmedo". Esto generalmente se refiere a una digestión húmeda, un proceso en el que la muestra se trata con ácidos fuertes (como ácido nítrico concentrado, HNO₃, o una mezcla de ácidos) a temperaturas elevadas para descomponer la materia orgánica y liberar los iones cloruro en una solución acuosa. Este paso es crucial para eliminar interferencias y asegurar que todo el cloruro esté disponible para la reacción.
- Adición de Nitrato de Plata (AgNO₃): Una vez preparada la muestra, se le añade una cantidad medida y conocida (en exceso) de una solución estándar de nitrato de plata (AgNO₃). Los iones cloruro (Cl⁻) de la sal reaccionan con los iones plata (Ag⁺) para formar un precipitado insoluble de cloruro de plata (AgCl):
Ag⁺(ac) + Cl⁻(ac) → AgCl(s) - Acidificación: Después de la adición del AgNO₃, se añade ácido nítrico concentrado (HNO₃). La presencia de HNO₃ es fundamental para acidificar la solución. Esto ayuda a prevenir la hidrólisis del indicador de hierro (si se usa alumbre férrico) y, más importante, a evitar la precipitación de otras sales de plata (como Ag₂CO₃ o Ag₃PO₄) que podrían formarse en condiciones neutras o básicas, asegurando que solo el AgCl precipite y que no haya interferencias. También previene que el tiocianato de plata (AgSCN) se disuelva durante la titulación de retroceso.
- Filtración (Opcional, pero Recomendado): Aunque no se menciona explícitamente en el extracto, en algunas variaciones del método Volhard, el precipitado de AgCl se filtra para removerlo antes de la titulación. Esto es porque el AgCl puede reaccionar con el tiocianato durante la titulación de retroceso, lo que llevaría a resultados erróneos. Sin embargo, en la práctica moderna, a menudo se añade un disolvente orgánico (como nitrobenceno) para recubrir el AgCl y evitar esta interferencia.
- Titulación por Retroceso con Tiocianato de Potasio (KSCN): Una vez que todo el cloruro ha reaccionado con la plata, el exceso de iones plata (Ag⁺) que no reaccionaron con el cloruro se titula por retrointensidad con una solución estándar de tiocianato de potasio (KSCN). Los iones tiocianato (SCN⁻) reaccionan con los iones plata restantes para formar un precipitado de tiocianato de plata (AgSCN):
Ag⁺(exceso) + SCN⁻(ac) → AgSCN(s) - Punto Final: El punto final de la titulación se detecta utilizando un indicador como el alumbre férrico (FeNH₄(SO₄)₂·12H₂O). Cuando todo el exceso de iones plata ha reaccionado con el tiocianato, la siguiente gota de KSCN reacciona con los iones férricos del indicador para formar un complejo de tiocianato de hierro (III) de color rojo sangre, señalando el punto final de la titulación:
Fe³⁺(ac) + SCN⁻(ac) → Fe(SCN)₂⁺(ac) (color rojo)
Cálculo de la Concentración de Cloruro
Para calcular la cantidad de cloruro en la muestra, se resta la cantidad de plata que reaccionó con el tiocianato (exceso) de la cantidad total de plata añadida inicialmente. La diferencia representa la cantidad de plata que reaccionó con los iones cloruro de la muestra. A partir de esta cantidad, se puede determinar la masa de cloruro y, por consiguiente, la concentración de sal en la muestra.
Cálculo del Porcentaje de Sal a Partir del Sodio en Alimentos
En el contexto de la nutrición y las etiquetas de alimentos, es común encontrar la cantidad de sodio (Na) en lugar de la cantidad de sal (NaCl). Esto se debe a que el sodio es el componente dietético que los profesionales de la salud monitorean debido a su impacto en la presión arterial y la salud cardiovascular. Sin embargo, es posible y a menudo necesario convertir la cantidad de sodio a una cantidad equivalente de sal para una mejor comprensión del contenido total de sal.
La Relación entre Sodio y Sal
El cloruro de sodio (NaCl) está compuesto por un átomo de sodio (Na) y un átomo de cloro (Cl). Sus masas atómicas son aproximadamente 22.99 g/mol para el sodio y 35.45 g/mol para el cloro. Por lo tanto, la masa molar del NaCl es 22.99 + 35.45 = 58.44 g/mol.

Para determinar qué porcentaje de la sal es sodio, dividimos la masa atómica del sodio por la masa molar de la sal:
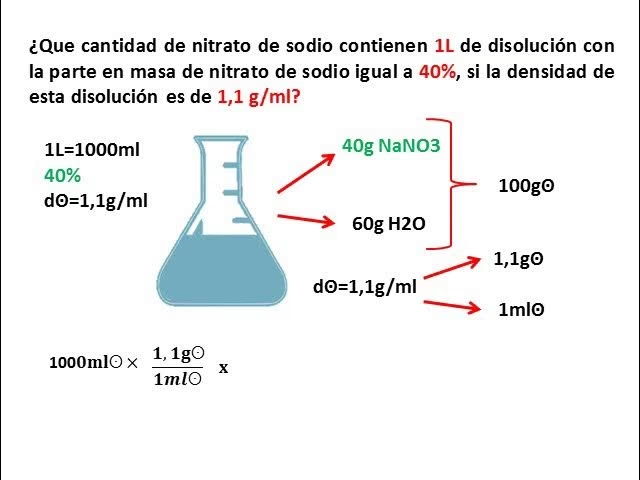
Porcentaje de Sodio en Sal = (Masa de Na / Masa de NaCl) * 100 = (22.99 / 58.44) * 100 ≈ 39.34%
Esto significa que el sodio representa aproximadamente el 40% del contenido total de sal en peso. Por lo tanto, si conocemos la cantidad de sodio, podemos estimar la cantidad de sal utilizando un factor de conversión.
Fórmula de Conversión
El documento menciona un factor de conversión de 2.54. Este factor se deriva de la relación inversa del porcentaje de sodio en la sal (1 / 0.3934 ≈ 2.541). Es decir, para obtener la cantidad de sal a partir de la cantidad de sodio, multiplicamos por este factor:
- Para calcular la cantidad de sal a partir de la cantidad de sodio:
Cantidad de Sal (mg) = Cantidad de Sodio (mg) × 2.54 - Para calcular la cantidad de sodio a partir de la cantidad de sal:
Cantidad de Sodio (mg) = Cantidad de Sal (mg) / 2.54
Ejemplo: Si una etiqueta nutricional indica 200 mg de sodio por porción, la cantidad equivalente de sal sería:200 mg de Sodio × 2.54 = 508 mg de Sal
Esto es muy útil para los consumidores que desean monitorear su ingesta de sal, ya que las etiquetas a menudo solo reportan el sodio.
¿Cómo se Calcula la Concentración Normal de una Sal?
La concentración normal, o Normalidad (N), es una unidad de concentración que expresa el número de equivalentes de soluto por litro de solución. Aunque menos común en la química moderna que la molaridad, sigue siendo relevante en ciertos contextos, especialmente en titulaciones y reacciones redox, donde los equivalentes reaccionan en proporciones simples.
Definición de Equivalente Químico
Para entender la normalidad, primero debemos comprender el concepto de un equivalente químico. Un equivalente de una sustancia es la cantidad de esa sustancia que puede reaccionar con, o ser equivalente a, un mol de iones hidrógeno (H⁺) en una reacción ácido-base, o un mol de electrones en una reacción redox. Para una sal, el número de equivalentes por mol depende de la carga total de los iones positivos (o negativos) que se disocian en solución.
Cálculo de la Normalidad para una Sal
La fórmula general para la normalidad es:
Normalidad (N) = Número de Equivalentes de Soluto / Volumen de Solución (en Litros)
Alternativamente, la normalidad se puede calcular a partir de la molaridad (M):
Normalidad (N) = Molaridad (M) × Número de Equivalentes por Mol (n)
Donde 'n' es el factor de valencia o el número de equivalentes por mol de la sal. Para una sal, 'n' es la carga total de los cationes o aniones que se disocian de una molécula de la sal.
Ejemplos:
1. Cloruro de Sodio (NaCl):
Cuando el NaCl se disuelve en agua, se disocia en Na⁺ y Cl⁻. Cada mol de NaCl produce un mol de iones Na⁺ con una carga de +1 y un mol de iones Cl⁻ con una carga de -1. Por lo tanto, el número de equivalentes por mol (n) para NaCl es 1.
Si tienes una solución 0.5 M de NaCl:N = 0.5 M × 1 = 0.5 N
2. Cloruro de Calcio (CaCl₂):
Cuando el CaCl₂ se disuelve en agua, se disocia en Ca²⁺ y 2Cl⁻. Cada mol de CaCl₂ produce un mol de iones Ca²⁺ con una carga de +2 y dos moles de iones Cl⁻ con una carga de -1 (total -2). El factor de valencia (n) para CaCl₂ es 2 (basado en la carga del catión Ca²⁺).
Si tienes una solución 0.5 M de CaCl₂:N = 0.5 M × 2 = 1.0 N
Es importante notar que la normalidad es una medida que depende del tipo de reacción en la que la sal va a participar. Sin embargo, para sales que simplemente se disocian en iones, el factor de valencia se basa en la carga total de los iones.

Tabla Comparativa de Unidades de Concentración
Para entender mejor el panorama de la concentración, es útil comparar las diferentes unidades utilizadas:
| Unidad de Concentración | Definición | Uso Común | Ventajas | Desventajas |
|---|---|---|---|---|
| Porcentaje en Masa (% m/m) | (Masa de soluto / Masa de solución) × 100 | Etiquetas de alimentos, soluciones comerciales, mezclas sólidas. | Fácil de calcular y entender; no depende de la temperatura. | No relaciona directamente con la estequiometría de reacciones. |
| Porcentaje en Volumen (% v/v) | (Volumen de soluto / Volumen de solución) × 100 | Soluciones líquidas (ej. alcohol en bebidas). | Sencillo para mezclas líquidas. | Volúmenes no son aditivos, depende de la temperatura. |
| Molaridad (M) | Moles de soluto / Litros de solución | Química general, reacciones estequiométricas, bioquímica. | Relaciona directamente con moles y estequiometría; muy utilizada. | Depende de la temperatura (el volumen cambia). |
| Molalidad (m) | Moles de soluto / Kilogramos de disolvente | Propiedades coligativas, estudios termodinámicos. | No depende de la temperatura; útil en cálculos físicos. | Menos práctica para preparar soluciones volumétricas. |
| Normalidad (N) | Equivalentes de soluto / Litros de solución | Titulaciones ácido-base y redox; algunas aplicaciones analíticas. | Simplifica cálculos estequiométricos de equivalentes. | Definición de 'equivalente' puede ser ambigua; menos usada globalmente. |
Preguntas Frecuentes (FAQs)
¿Es lo mismo sodio que sal?
No, no son lo mismo. El sodio (Na) es un elemento químico, mientras que la sal común es cloruro de sodio (NaCl), un compuesto formado por sodio y cloro. El sodio es un componente de la sal, y representa aproximadamente el 40% de su peso. Es importante diferenciar porque el impacto en la salud se asocia principalmente con la ingesta de sodio.
¿Por qué se usa HNO₃ concentrado en el método Volhard?
El ácido nítrico concentrado (HNO₃) se añade en el método Volhard para acidificar la solución. Esto tiene varios propósitos clave: evita la precipitación de otras sales de plata que no sean cloruro de plata (AgCl) en condiciones neutras o básicas, previene la hidrólisis del indicador férrico que se usa para detectar el punto final, y asegura que el precipitado de tiocianato de plata (AgSCN) que se forma durante la titulación de retroceso sea estable y no se disuelva.
¿Qué es un equivalente químico?
Un equivalente químico es la cantidad de una sustancia que puede reaccionar con, o es equivalente a, un mol de iones hidrógeno (H⁺) en una reacción ácido-base, o un mol de electrones en una reacción de oxidación-reducción. Para una sal, el número de equivalentes por mol se basa en la carga total de los iones que se disocian en solución (por ejemplo, 1 para NaCl, 2 para CaCl₂).
¿Cuál es la principal diferencia entre molaridad y normalidad?
La principal diferencia radica en lo que miden por litro de solución. La molaridad (M) mide los moles de soluto por litro de solución, lo que es útil para expresar la concentración de una sustancia en términos de su cantidad de materia. La normalidad (N), por otro lado, mide los equivalentes de soluto por litro de solución, lo que es particularmente útil en reacciones donde la estequiometría se basa en la transferencia de iones o electrones (ácido-base, redox), ya que un equivalente de una sustancia reacciona con exactamente un equivalente de otra.
¿El factor de conversión 2.54 entre sodio y sal es siempre exacto?
El factor de conversión de 2.54 se basa en las masas atómicas promedio del sodio y el cloro. Es una aproximación muy precisa y ampliamente aceptada para convertir la cantidad de sodio a sal común (cloruro de sodio). Aunque las masas atómicas pueden variar ligeramente según los isótopos, para fines nutricionales y prácticos, este factor se considera suficientemente exacto.
Conclusión
Calcular la concentración de sal es una tarea esencial en múltiples disciplinas, desde la química analítica hasta la nutrición. Hemos explorado métodos precisos como el Volhard para la determinación en laboratorio, y la práctica conversión de sodio a sal para la interpretación de etiquetas alimentarias. Además, hemos profundizado en el concepto de Normalidad, una medida de concentración que, aunque menos común hoy día, sigue siendo valiosa en contextos específicos de la química. La capacidad de comprender y aplicar estos cálculos no solo mejora nuestra precisión en la investigación y la industria, sino que también nos empodera como consumidores para tomar decisiones informadas sobre nuestra salud y bienestar.
Si quieres conocer otros artículos parecidos a Calculando la Concentración de Sal: Guía Completa puedes visitar la categoría Cálculos.