13/05/2023
En el fascinante mundo de la termodinámica y la transferencia de calor, existen dos conceptos fundamentales que a menudo se entrelazan y son cruciales para entender cómo interactúa la energía con la materia: el calor específico y la conductividad térmica. Estos términos no son solo teorías abstractas de la física; tienen aplicaciones prácticas directas en nuestra vida cotidiana, especialmente cuando consideramos la eficiencia energética de nuestros hogares o la funcionalidad de sistemas como la calefacción. Comprender qué son, cómo se miden y cómo influyen en el comportamiento de los materiales nos permitirá tomar decisiones más informadas, desde la selección de un radiador hasta el diseño de un aislamiento eficaz. Acompáñanos en este recorrido para desentrañar estos conceptos y aprender a realizar cálculos esenciales.
- ¿Qué es el Calor Específico?
- ¿Qué es la Conductividad Térmica?
- ¿Cómo se Calcula el Calor Específico de una Mezcla?
- ¿Cómo calcular el Calor de Mezcla (Entalpía de Mezcla)?
- ¿Cómo calcular el Calor Absorbido o Perdido por una Muestra (incluyendo una Mezcla)?
- Impacto de Calor Específico y Conductividad en Sistemas de Calefacción y Aislamiento
- Preguntas Frecuentes (FAQ)
- ¿Qué es el calor específico y por qué es importante?
- ¿Cómo se calcula la cantidad de calor transferida?
- ¿Qué es la conductividad térmica?
- ¿Cuál es la diferencia entre calor específico y conductividad térmica?
- ¿Cómo se calcula el calor específico de una mezcla de gases?
- ¿Qué es el calor de mezcla?
- ¿Por qué son importantes estos conceptos al elegir un sistema de calefacción?
- Conclusión
¿Qué es el Calor Específico?
El calor específico, también conocido como capacidad calorífica específica o capacidad térmica específica, es una propiedad intrínseca de cada sustancia que nos indica la cantidad de energía térmica que se requiere para elevar la temperatura de una unidad de masa de esa sustancia en un grado Celsius (o Kelvin). Imagina que tienes un kilogramo de un material y quieres aumentar su temperatura en un grado; la cantidad de calor que debes suministrar para lograrlo es precisamente su calor específico. Esta propiedad se mide comúnmente en unidades de julios por kilogramo por grado Celsius (J/(kg·°C)) o julios por kilogramo por Kelvin (J/(kg·K)), ya que un cambio de un grado Celsius es equivalente a un cambio de un Kelvin.
La importancia del calor específico radica en su capacidad para determinar cuán 'resistente' es un material a los cambios de temperatura. Un material con un calor específico alto, como el agua, requiere una gran cantidad de energía para cambiar su temperatura. Por el contrario, un material con un calor específico bajo, como muchos metales, se calienta y enfría rápidamente con una menor cantidad de energía.
Ejemplo Práctico: Radiadores y Eficiencia Energética
Para ilustrar la relevancia del calor específico, consideremos el diseño y la eficiencia de un sistema de calefacción. Pensemos en un radiador. La mayoría de los radiadores modernos están fabricados con materiales como el aluminio o el acero. El aluminio, por ejemplo, es un excelente conductor de calor y tiene un calor específico relativamente bajo en comparación con otros materiales aislantes. Esto significa que el aluminio puede absorber y liberar calor de manera eficiente, transmitiendo rápidamente la energía térmica generada por el fluido interno (agua o fluido térmico) hacia la habitación.
Ahora, imaginemos por un momento que un radiador estuviera hecho de madera. La madera posee un calor específico significativamente más alto que el aluminio. Si intentáramos calentar una pieza de madera con la misma cantidad de energía que calienta un radiador de aluminio, la temperatura de la madera aumentaría mucho más lentamente y en menor medida. Esto implicaría que el radiador de madera necesitaría una cantidad de energía considerablemente mayor y un tiempo mucho más prolongado para alcanzar una temperatura que proporcionara confort a la estancia. En la práctica, un radiador de madera sería sumamente ineficiente, ya que la mayor parte de la energía se consumiría intentando elevar la temperatura del propio material en lugar de transferir calor al ambiente.
Este ejemplo subraya la importancia de elegir materiales con un calor específico adecuado para cada aplicación. En sistemas de calefacción, buscamos materiales que se calienten y enfríen con facilidad para una transferencia de calor eficiente. Por otro lado, en aplicaciones de aislamiento, como las paredes de una casa, buscamos materiales con un calor específico alto y baja conductividad térmica para que retengan el calor y eviten su paso.
Cómo Calcular el Calor Específico y la Energía Transferida
La relación fundamental que conecta el calor transferido, la masa de una sustancia, su calor específico y el cambio de temperatura es una de las ecuaciones más utilizadas en termodinámica. Se expresa mediante la fórmula:
Q = m * c * ΔT
Donde:
Q: Representa la cantidad de energía calorífica que ha sido ganada o perdida por la sustancia. Se mide en julios (J), kilojulios (kJ) o a veces en calorías (cal).m: Es la masa de la sustancia en cuestión. Se expresa comúnmente en kilogramos (kg) o gramos (g).c: Es el calor específico de la sustancia. Como mencionamos, sus unidades suelen ser J/(kg·°C) o J/(kg·K).ΔT(Delta T): Indica el cambio de temperatura de la sustancia. Se calcula como la temperatura final menos la temperatura inicial (T_final - T_inicial). Las unidades son grados Celsius (°C) o Kelvin (K).
Esta fórmula nos permite calcular cualquiera de las variables si conocemos las otras tres. Por ejemplo, si queremos saber cuánto calor se necesita para calentar 2 kg de agua de 20°C a 80°C, y sabemos que el calor específico del agua es aproximadamente 4186 J/(kg·°C), el cálculo sería:
Q = 2 kg * 4186 J/(kg·°C) * (80°C - 20°C)
Q = 2 kg * 4186 J/(kg·°C) * 60°C
Q = 502,320 J o 502.32 kJ
Este cálculo es fundamental para diseñar sistemas de climatización, procesos industriales de calentamiento o enfriamiento, y para entender la capacidad de almacenamiento de energía térmica de diferentes materiales.
Tabla de Calor Específico de Materiales Comunes
Para facilitar la comprensión y el uso de estos conceptos, a continuación se presenta una tabla con los valores de calor específico para una variedad de materiales. Es importante recordar que estos valores pueden variar ligeramente dependiendo de la temperatura y la presión, pero son útiles como referencia general.
| Material | Calor Específico J/(kg·K) |
|---|---|
| Aceite vegetal | 2000 |
| Hielo (-10 °C a 0 °C) | 2093 |
| Agua (0 °C a 100 °C) | 4186 |
| Hierro/Acero | 452 |
| Aire | 1012 |
| Hormigón | 880 |
| Alcohol etílico | 2460 |
| Latón | 380 |
| Alcohol metílico | 2549 |
| Litio | 3560 |
| Aluminio | 897 |
| Madera | 420 |
| Amoniaco (líquido) | 4700 |
| Magnesio | 1023 |
| Arena | 290 |
| Mármol | 858 |
| Asfalto | 920 |
| Mercurio | 138 |
| Azufre | 730 |
| Metano (275 K) | 2191 |
| Benceno | 1750 |
| Níquel | 440 |
| Calcio | 650 |
| Nitrógeno | 1040 |
| Cinc | 390 |
| Oro | 129 |
| Cobre | 387 |
| Oxígeno | 918 |
| Diamante | 509 |
| Plata | 236 |
| Dióxido de carbono (gas) | 839 |
| Plomo | 128 |
| Estaño | 210 |
| Potasio | 750 |
| Etilen glicol | 2200 |
| Sodio | 1230 |
| Gasolina | 2220 |
| Tejido humano | 3500 |
| Grafito | 710 |
| Tierra (típica) | 1046 |
| Granito | 790 |
| Vapor de agua (100 oC) | 2009 |
| Helio (gas) | 5300 |
| Vidrio (típico) | 837 |
| Hidrógeno (gas) | 14267 |
¿Qué es la Conductividad Térmica?
Mientras que el calor específico nos dice cuánto calor se necesita para cambiar la temperatura de un material, la conductividad térmica nos indica con qué facilidad un material permite que el calor fluya a través de él. Es una medida de la capacidad de un material para transferir energía térmica desde una región de mayor temperatura a una de menor temperatura. Los materiales con alta conductividad térmica, como los metales, son excelentes conductores de calor, lo que significa que el calor se propaga rápidamente a través de ellos. Por otro lado, los materiales con baja conductividad térmica, como los aislantes (lana de vidrio, poliestireno), son malos conductores de calor y, por lo tanto, excelentes aislantes, ya que dificultan el paso del calor.
El coeficiente de conductividad térmica se denota con la letra griega 'k' o 'λ' y se mide en vatios por metro por Kelvin (W/(m·K)) o vatios por metro por grado Celsius (W/(m·°C)). Un valor alto indica que el material es un buen conductor de calor, mientras que un valor bajo indica que es un buen aislante.
Tabla de Conductividad Térmica de Materiales Comunes
La siguiente tabla muestra la conductividad térmica de varios materiales, lo que permite una comparación rápida de sus propiedades de transferencia de calor.

| Material | Conductividad Térmica W/(m·K) |
|---|---|
| Plata | 406,1 – 418,7 |
| Cobre | 372,1 – 385,3 |
| Oro | 308,2 |
| Aluminio | 209,3 |
| Hierro | 80,2 |
| Acero | 47 – 58 |
| Ladrillo | 0,8 |
| Agua | 0,58 |
| Aire | 0,024 |
Observando la tabla, notamos que el aire tiene una conductividad térmica extremadamente baja. Esta propiedad es ampliamente utilizada en la construcción de edificios mediante la creación de cámaras de aire en paredes y muros, que actúan como un eficaz aislante térmico. Por el contrario, metales como la plata, el cobre y el aluminio son excelentes conductores. El aluminio, en particular, ofrece una relación muy favorable entre su coste y su alta conductividad térmica, lo que lo convierte en un material ideal para la fabricación de componentes que requieren una rápida disipación o transferencia de calor, como los radiadores eléctricos.
Factores que Influyen en la Conductividad Térmica: Modos de Transferencia de Calor
La transferencia de energía térmica, comúnmente conocida como calor, puede ocurrir de tres maneras principales, cada una con sus propias características y relevancia en la conductividad térmica de los materiales:
1. Conducción
La conducción es la transferencia de energía térmica que ocurre a través del contacto directo entre las partículas de dos cuerpos, o entre partículas adyacentes dentro de un mismo cuerpo. En este proceso, las moléculas más energéticas (más calientes) vibran y chocan con las moléculas vecinas menos energéticas, transfiriéndoles parte de su energía cinética. Este fenómeno es predominante en los sólidos, donde las partículas están muy cerca unas de otras y pueden transmitir vibraciones eficientemente. Los metales son excelentes conductores debido a la presencia de electrones libres que pueden moverse y transportar energía rápidamente. Es la principal forma de transferencia de calor en una sartén sobre una llama o a través de la pared de un radiador.
2. Convección
La convección es la transferencia de calor que se produce a través del movimiento de un fluido (líquido o gas). Cuando una parte del fluido se calienta, se vuelve menos densa y asciende, mientras que el fluido más frío y denso desciende para ocupar su lugar. Este ciclo crea corrientes de convección que transportan el calor de un lugar a otro. La convección puede ser natural (por diferencias de densidad, como el aire caliente que sube en una habitación) o forzada (con la ayuda de ventiladores o bombas, como en un sistema de aire acondicionado o una caldera de circulación forzada). Los radiadores transfieren calor al ambiente en gran medida por convección, calentando el aire circundante que luego se eleva y distribuye el calor por la estancia.
3. Radiación
La radiación térmica es la transferencia de calor mediante ondas electromagnéticas (como la luz infrarroja), sin necesidad de un medio material para su propagación. Todos los cuerpos con una temperatura superior al cero absoluto emiten radiación térmica. Cuanto mayor es la temperatura de un cuerpo, mayor es la cantidad de energía radiada. La radiación es cómo el calor del sol llega a la Tierra o cómo sentimos el calor de una fogata o de un radiador a distancia. Los radiadores no solo calientan el aire por convección, sino que también emiten calor directamente a través de radiación infrarroja, calentando objetos y personas en su camino.
La interacción de estos tres modos de transferencia de calor es crucial para el diseño y la eficiencia de cualquier sistema térmico, desde un simple termostato hasta complejos sistemas de climatización industrial.
¿Cómo se Calcula el Calor Específico de una Mezcla?
La pregunta sobre cómo calcular el calor específico de una mezcla es compleja, ya que depende del estado de agregación de la mezcla (gaseosa, líquida, sólida) y de la naturaleza de sus componentes. La información proporcionada se centra específicamente en la relación de calor específico para mezclas de gases y en el calor de mezcla (entalpía de mezcla), que son conceptos relacionados pero distintos del calor específico de la mezcla.
La Relación de Calor Específico (γ) para Mezclas de Gases
Para una mezcla de gases, la relación de calor específico, denotada por la letra griega gamma (γ), es un parámetro importante en la termodinámica, especialmente en procesos adiabáticos (sin transferencia de calor). Esta relación se define como el cociente entre el calor específico a presión constante (Cp) y el calor específico a volumen constante (Cv):
γ = Cp / Cv
Donde:
Cp: Es el calor específico de la mezcla a presión constante. Esto significa la cantidad de calor necesaria para elevar la temperatura de una unidad de masa de la mezcla en un grado, manteniendo la presión constante.Cv: Es el calor específico de la mezcla a volumen constante. Similarmente, es la cantidad de calor necesaria para elevar la temperatura de una unidad de masa de la mezcla en un grado, manteniendo el volumen constante.
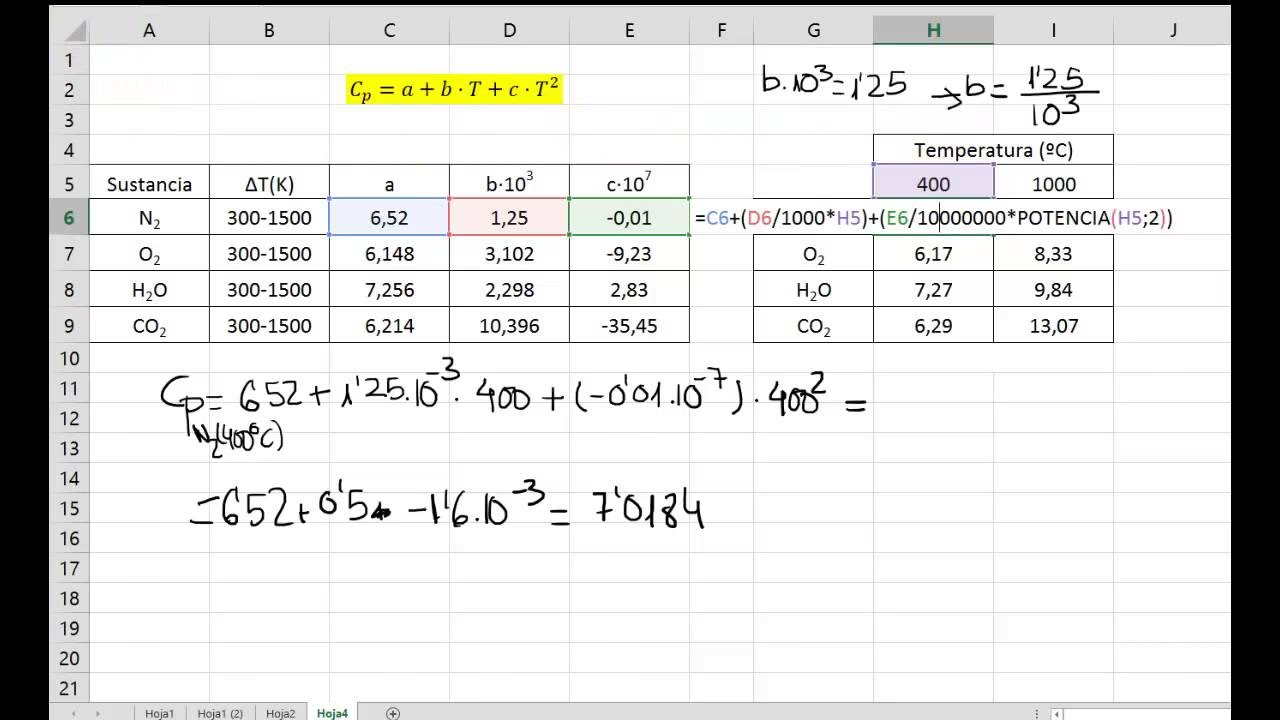
Para calcular Cp y Cv de una mezcla de gases, generalmente se utilizan las fracciones molares de cada componente y sus respectivos calores específicos individuales a presión y volumen constante. Por ejemplo, para una mezcla de gases ideales, el calor específico a presión constante de la mezcla (Cp_mezcla) se puede calcular como una media ponderada de los calores específicos molares de los componentes puros a presión constante, basándose en sus fracciones molares:
Cp_mezcla = Σ (xi * Cpi)
Donde xi es la fracción molar del componente i y Cpi es el calor específico molar a presión constante del componente i. De manera similar, se puede calcular Cv_mezcla. Una vez obtenidos Cp_mezcla y Cv_mezcla, se puede determinar γ para la mezcla de gases.
Es importante destacar que esta fórmula y consideración se aplican específicamente a la relación de calores específicos de gases. Para mezclas de líquidos o sólidos, el cálculo del calor específico de la mezcla suele involucrar una ponderación de los calores específicos de los componentes puros basada en sus fracciones másicas o volumétricas, pero la información proporcionada no detalla estas fórmulas específicas para otros estados de la materia.
¿Cómo calcular el Calor de Mezcla (Entalpía de Mezcla)?
El calor de mezcla, o entalpía de mezcla (ΔH_mix), es el cambio de entalpía que ocurre cuando se mezclan dos o más sustancias a una temperatura y presión constantes. Este valor es crucial para entender las interacciones entre los componentes de una solución y si el proceso de mezcla es exotérmico (libera calor) o endotérmico (absorbe calor).
Soluciones Ideales
Para una solución ideal, se asume que no hay interacciones energéticas entre las diferentes moléculas de los componentes más allá de las que ya existen en los componentes puros. En este caso, la entalpía de la solución (H) es simplemente la suma ponderada de las entalpías molares de los componentes puros (H_A, H_B) multiplicadas por sus respectivas fracciones molares (x_A, x_B):
H = x_A * H_A + x_B * H_B
En una solución ideal, el calor de mezcla (ΔH_mix) es cero, lo que significa que no hay liberación ni absorción neta de calor cuando los componentes se mezclan.

Soluciones No Ideales
Sin embargo, la mayoría de las soluciones reales son no ideales. Esto significa que existen interacciones entre las moléculas de los diferentes componentes que son diferentes a las interacciones entre las moléculas del mismo componente. Estas interacciones adicionales (o la falta de ellas) resultan en un cambio de entalpía durante la mezcla. Para una solución binaria no ideal, la entalpía de la solución se puede representar como:
H = x_A * H_A + x_B * H_B + α * x_A * x_B
Donde α (alfa) es un parámetro que cuantifica la desviación de la idealidad. Este parámetro α es empírico y depende de la naturaleza de los componentes y de la temperatura.
El calor de mezcla (ΔH_mix) se define entonces como la diferencia entre la entalpía de la solución no ideal y la entalpía que tendría si fuera una solución ideal:
ΔH_mix = H – (x_A * H_A + x_B * H_B)
Sustituyendo la expresión para H en la ecuación anterior, obtenemos:
ΔH_mix = α * x_A * x_B
Este ΔH_mix también se conoce como la entalpía en exceso (H^E), lo que resalta que es la parte de la entalpía que va más allá del comportamiento ideal. Un ΔH_mix positivo indica que la mezcla es endotérmica (absorbe calor), mientras que un ΔH_mix negativo indica que es exotérmica (libera calor).
Ley de Raoult Modificada
En el contexto de soluciones no ideales y el equilibrio vapor-líquido, la Ley de Raoult Modificada incorpora el concepto de coeficiente de actividad (γi) para tener en cuenta las desviaciones de la idealidad. Esta ley es fundamental para predecir las presiones de vapor de los componentes en una mezcla y, por extensión, el comportamiento de ebullición y condensación de las mezclas.
x_i * γ_i * P_i^(sat) = y_i * P
Donde:
x_i: Es la fracción molar del componenteien la fase líquida.γ_i(gamma sub i): Es el coeficiente de actividad del componentei. Este factor corrige la presión de vapor ideal predicha por la Ley de Raoult para soluciones no ideales. Unγ_imayor que 1 indica una desviación positiva (interacciones más débiles entre diferentes moléculas que entre iguales), mientras que unγ_imenor que 1 indica una desviación negativa (interacciones más fuertes).P_i^(sat): Es la presión de saturación (o presión de vapor puro) del componenteia la temperatura dada.y_i: Es la fracción molar del componenteien la fase de vapor.P: Es la presión total del sistema.
La Ley de Raoult Modificada, junto con el concepto de entalpía de mezcla, es esencial para el diseño de procesos de separación, como la destilación, y para comprender el comportamiento termodinámico de una amplia gama de soluciones químicas e industriales.
¿Cómo calcular el Calor Absorbido o Perdido por una Muestra (incluyendo una Mezcla)?
Independientemente de si se trata de una sustancia pura o de una mezcla, la cantidad de calor ganado o perdido por una muestra (q) cuando su temperatura cambia se calcula utilizando la misma ecuación fundamental que vimos para el calor específico:
q = m * c * ΔT
Aquí, m es la masa de la muestra, c es el calor específico de la muestra, y ΔT es el cambio de temperatura. Es crucial entender que para aplicar esta fórmula a una mezcla, necesitamos conocer el calor específico de esa mezcla específica. Si la mezcla es homogénea y su calor específico ya ha sido determinado experimentalmente o calculado a partir de modelos (como en el caso de la ponderación de calores específicos de componentes para líquidos o sólidos, si se dispusiera de esa información), entonces la aplicación de esta fórmula es directa.
Por ejemplo, si tenemos una mezcla líquida con una masa conocida y su calor específico promedio ha sido determinado, podemos calcular fácilmente cuánto calor se necesita para elevar su temperatura. Si la temperatura final es mayor que la inicial (ΔT es positivo), la muestra ha ganado calor (q es positivo). Si la temperatura final es menor que la inicial (ΔT es negativo), la muestra ha perdido calor (q es negativo).
Esta ecuación es la piedra angular para realizar cálculos de balance energético en una multitud de aplicaciones, desde experimentos de laboratorio hasta el dimensionamiento de sistemas de calefacción y refrigeración donde se busca controlar la temperatura de fluidos o materiales compuestos.
Impacto de Calor Específico y Conductividad en Sistemas de Calefacción y Aislamiento
La elección de materiales para sistemas de calefacción y aislamiento es una aplicación directa y crítica de los conceptos de calor específico y conductividad térmica. Un diseño óptimo busca maximizar la transferencia de calor donde se desea calentar y minimizarla donde se busca aislar.
En el caso de los radiadores, como los de aluminio, su alta conductividad térmica asegura que el calor generado por el fluido interno se transfiera rápidamente a la superficie exterior del radiador y de ahí al ambiente. Su calor específico, si bien no es el más bajo, permite que el material se caliente de manera eficiente. Los fabricantes, como Rointe, diseñan radiadores eléctricos que no solo son estéticos, sino también altamente eficientes, aprovechando las propiedades térmicas del aluminio y la combinación de convección y radiación para distribuir el calor de manera efectiva.
Por otro lado, para el aislamiento en edificios, se prefieren materiales con baja conductividad térmica y, a menudo, un calor específico relativamente alto. Materiales como la lana mineral, el poliestireno expandido o las cámaras de aire aprovechan su baja conductividad para crear una barrera que ralentiza la transferencia de calor entre el interior y el exterior, manteniendo la temperatura deseada con un menor consumo de energía. La capacidad del aire para ser un excelente aislante es la razón por la que las ventanas de doble acristalamiento y las paredes con cámaras de aire son tan efectivas.

En resumen, una comprensión profunda de estas propiedades térmicas es indispensable para la ingeniería de sistemas térmicos, la construcción sostenible y cualquier aplicación que involucre el control y la gestión de la energía calorífica.
Preguntas Frecuentes (FAQ)
¿Qué es el calor específico y por qué es importante?
El calor específico es la cantidad de calor necesaria para elevar la temperatura de una unidad de masa de una sustancia en un grado. Es importante porque determina la capacidad de un material para almacenar o liberar energía térmica, influyendo directamente en la eficiencia de procesos de calentamiento, enfriamiento y aislamiento.
¿Cómo se calcula la cantidad de calor transferida?
La cantidad de calor (Q) ganada o perdida por una sustancia se calcula con la fórmula Q = m * c * ΔT, donde m es la masa, c es el calor específico y ΔT es el cambio de temperatura.
¿Qué es la conductividad térmica?
La conductividad térmica es una propiedad que mide la capacidad de un material para transferir calor a través de sí mismo. Los materiales con alta conductividad son buenos conductores de calor, mientras que los de baja conductividad son buenos aislantes.
¿Cuál es la diferencia entre calor específico y conductividad térmica?
El calor específico indica cuánto calor se necesita para cambiar la temperatura de un material (su capacidad de almacenar calor), mientras que la conductividad térmica indica con qué rapidez o facilidad el calor se mueve a través de un material (su capacidad de conducir calor).
¿Cómo se calcula el calor específico de una mezcla de gases?
La información proporcionada se refiere a la relación de calor específico (γ) para una mezcla de gases, que se calcula como el cociente entre el calor específico a presión constante (Cp) y el calor específico a volumen constante (Cv) de la mezcla (γ = Cp / Cv). Los valores de Cp y Cv para la mezcla se obtienen típicamente como promedios ponderados de los componentes individuales.
¿Qué es el calor de mezcla?
El calor de mezcla (o entalpía de mezcla, ΔH_mix) es el cambio de energía que ocurre cuando dos o más sustancias se mezclan para formar una solución. Para soluciones no ideales, este valor puede ser positivo (endotérmico) o negativo (exotérmico), indicando la naturaleza de las interacciones moleculares.
¿Por qué son importantes estos conceptos al elegir un sistema de calefacción?
Son fundamentales para elegir materiales eficientes. Un radiador debe estar hecho de un material con alta conductividad térmica (como el aluminio) para transferir calor rápidamente. El aislamiento debe usar materiales con baja conductividad térmica (como el aire o espumas) para evitar la pérdida de calor y mantener la eficiencia energética de la vivienda.
Conclusión
El calor específico y la conductividad térmica son pilares fundamentales en la comprensión de cómo la energía térmica interactúa con los materiales. Desde la elección del material para un radiador que nos brinde calor en invierno, hasta el diseño de un aislamiento eficiente que nos proteja del frío o del calor excesivo, estos conceptos guían las decisiones de ingeniería y diseño. La capacidad de calcular la energía transferida y de comprender el comportamiento térmico de las mezclas nos empodera para crear sistemas más eficientes, sostenibles y confortables. Dominar estos principios no solo enriquece nuestro conocimiento de la física, sino que también nos proporciona herramientas prácticas para mejorar nuestro entorno y optimizar el uso de la energía.
Si quieres conocer otros artículos parecidos a Cálculo de Calor Específico y Conductividad Térmica puedes visitar la categoría Cálculos.

