20/04/2024
En el fascinante mundo de la química y la ciencia de los materiales, los sólidos se organizan en patrones tridimensionales repetitivos conocidos como estructuras cristalinas. La unidad fundamental de esta repetición es la celda unitaria, una pequeña porción que, al replicarse en todas direcciones, construye todo el cristal. Comprender y calcular las dimensiones de esta celda unitaria es crucial, ya que estas propiedades microscópicas determinan muchas de las características macroscópicas de un material, desde su densidad hasta su conductividad. ¿Alguna vez te has preguntado cómo los científicos determinan el tamaño de los átomos o cómo se empaquetan en un sólido? La respuesta radica en la celda unitaria.
Este artículo te sumergirá en los métodos para calcular la longitud de una celda unitaria, explorando las relaciones matemáticas entre el tamaño de los átomos y la geometría de su empaquetamiento. Abordaremos las estructuras metálicas más comunes y también nos adentraremos en la complejidad de las celdas unitarias iónicas, proporcionando ejemplos claros y explicaciones detalladas para que domines este concepto fundamental.
- Cómo Calcular la Longitud de una Celda Unitaria en Metales
- Tabla Comparativa de Celdas Unitarias Metálicas
- Cálculo de la Longitud de Celdas Unitarias Iónicas
- Cómo Calcular el Número de Átomos en una Celda Unitaria
- ¿Cuál es la longitud del borde de la celda unitaria de la plata?
- Preguntas Frecuentes sobre Celdas Unitarias
Cómo Calcular la Longitud de una Celda Unitaria en Metales
La longitud del lado de una celda unitaria cúbica, a menudo denotada como 'l' o 'a', depende directamente del radio atómico (r) de los átomos que la componen y de la forma en que estos átomos están dispuestos dentro de la celda. Las relaciones matemáticas se derivan generalmente utilizando el teorema de Pitágoras, ya que las celdas cúbicas presentan ángulos rectos y diagonales que forman triángulos rectángulos.
Celda Cúbica Simple (SC)
En una celda unitaria cúbica simple, los átomos se encuentran en cada una de las ocho esquinas del cubo. Los átomos de las esquinas adyacentes están en contacto físico a lo largo de las aristas de la celda. Esto significa que la longitud de una arista es igual a dos veces el radio del átomo.
- Descripción: Átomos en las esquinas, en contacto a lo largo de los bordes.
- Relación:
l = 2r - Ejemplo: El polonio alfa (α-Po) cristaliza en una celda unitaria cúbica simple. Si la longitud del borde de su celda unitaria es de 336 pm, entonces el radio de un átomo de polonio es:
r = l / 2 = 336 pm / 2 = 168 pm
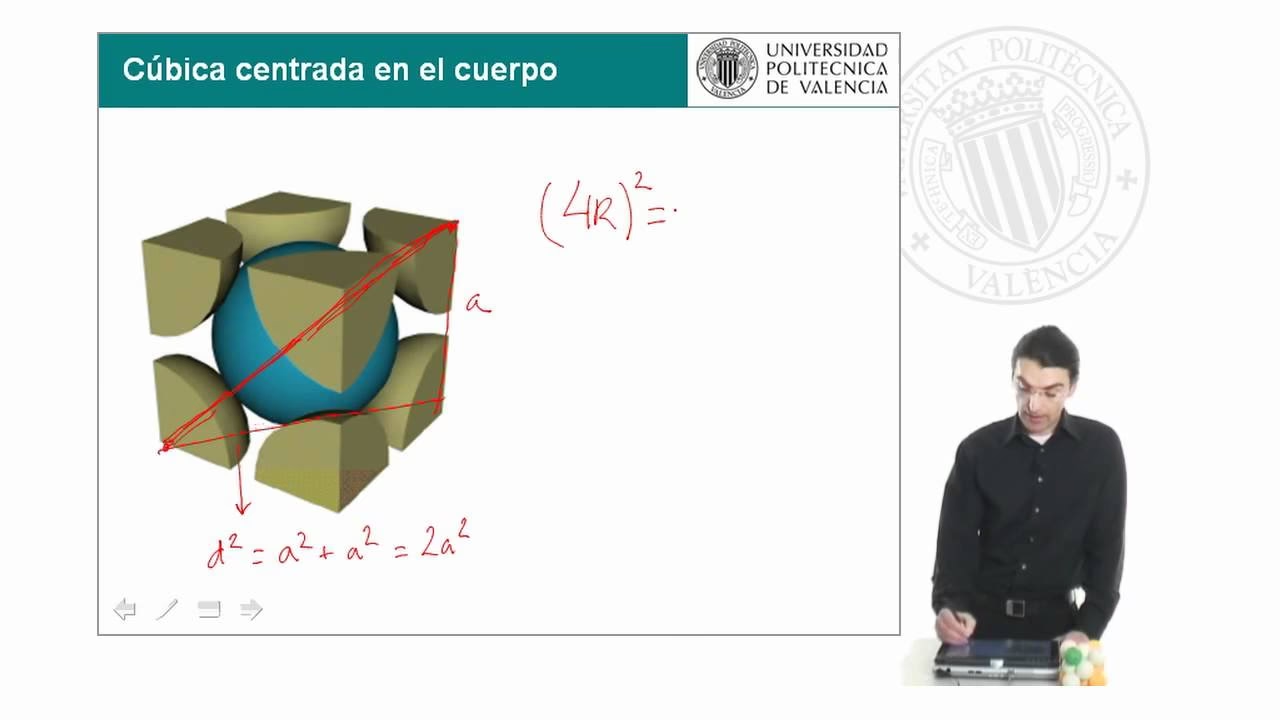
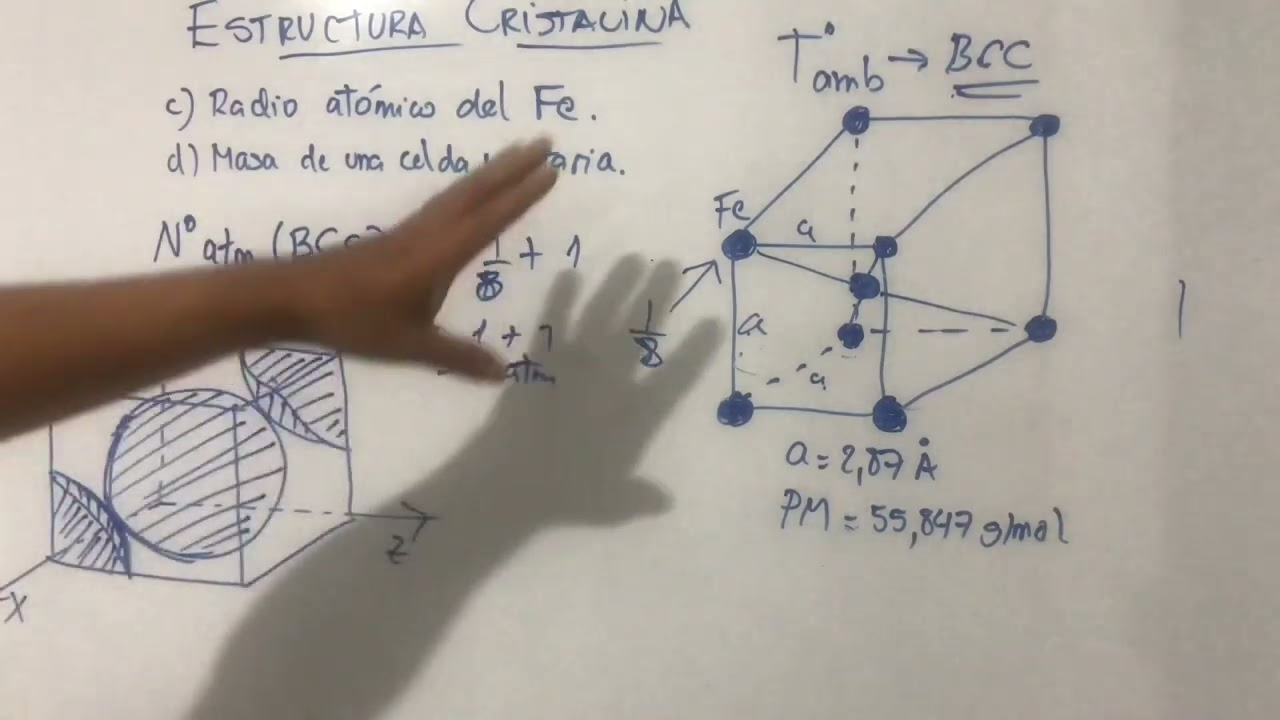
Celda Cúbica Centrada en el Cuerpo (BCC)
En una celda cúbica centrada en el cuerpo (BCC), además de los átomos en las esquinas, hay un átomo adicional en el centro exacto del cubo. En esta estructura, los átomos de las esquinas no están en contacto entre sí, pero sí lo están con el átomo central del cuerpo. El contacto se produce a lo largo de la diagonal del cuerpo de la celda unitaria.
- Descripción: Átomos en las esquinas y uno en el centro del cuerpo, en contacto a lo largo de la diagonal del cuerpo.
- Derivación:
Primero, consideramos la diagonal de una cara (d). Por el teorema de Pitágoras:
d² = l² + l² = 2l²Luego, consideramos la diagonal del cuerpo (h), que forma un triángulo rectángulo con una arista (l) y la diagonal de la cara (d):
h² = l² + d²Sustituyendo d²:
h² = l² + 2l² = 3l²En una estructura BCC, la diagonal del cuerpo (h) está compuesta por cuatro radios atómicos (un radio de cada átomo de la esquina y dos radios, es decir, un diámetro, del átomo central):
h = 4rIgualando:
(4r)² = 3l²16r² = 3l²Relación:
l = (4r) / sqrt(3)ol = 4r / 1.732
Celda Cúbica Centrada en la Cara (FCC)
En una celda cúbica centrada en la cara (FCC), los átomos se encuentran en las ocho esquinas del cubo y en el centro de cada una de sus seis caras. En esta configuración, los átomos de las esquinas no están en contacto entre sí, pero sí lo están con los átomos de las caras adyacentes. El contacto ocurre a lo largo de la diagonal de la cara del cubo.
- Descripción: Átomos en las esquinas y en los centros de las caras, en contacto a lo largo de la diagonal de la cara.
- Derivación:
Consideramos la diagonal de una cara (d), que forma un triángulo rectángulo con dos aristas (l) de la celda unitaria:
d² = l² + l² = 2l²En una estructura FCC, la diagonal de la cara (d) está compuesta por cuatro radios atómicos (un radio de cada átomo de la esquina y dos radios, es decir, un diámetro, del átomo central de la cara):
d = 4rIgualando:
(4r)² = 2l²16r² = 2l²Relación:
l = sqrt(8)rol = 2 * sqrt(2) * rol = 2.828r - Ejemplo: El calcio (Ca) cristaliza en una estructura cúbica centrada en la cara con una longitud de borde de 558.8 pm. Para encontrar el radio atómico del Ca:
(4r)² = 2 * (558.8 pm)²16r² = 2 * 312257.44 pm²16r² = 624514.88 pm²r² = 39032.18 pm²r = sqrt(39032.18) pm ≈ 197.56 pm
Tabla Comparativa de Celdas Unitarias Metálicas
Aquí se resumen las características clave de las celdas unitarias metálicas cúbicas:
| Tipo de Celda Unitaria | Átomos por Celda Unitaria | Número de Coordinación | Relación entre Longitud del Borde (l) y Radio Atómico (r) | Eficiencia de Empaquetamiento (Volumen Ocupado) |
|---|---|---|---|---|
| Cúbica Simple (SC) | 1 | 6 | l = 2r | 52% |
| Cúbica Centrada en el Cuerpo (BCC) | 2 | 8 | l = 4r / sqrt(3) | 68% |
| Cúbica Centrada en la Cara (FCC) | 4 | 12 | l = sqrt(8)r | 74% |
Cálculo de la Longitud de Celdas Unitarias Iónicas
Las celdas unitarias iónicas son más complejas que las metálicas, ya que involucran dos o más tipos de iones (cationes y aniones) con diferentes tamaños. El cálculo de la longitud del borde de la celda unitaria en compuestos iónicos requiere considerar los radios de ambos iones y su disposición específica. Se asume que los iones son esferas perfectas y que están en contacto.
Estructura tipo Cloruro de Cesio (CsCl)
En la estructura del cloruro de cesio, los iones cloruro (Cl-) forman una red cúbica simple, y los iones cesio (Cs+) ocupan los sitios intersticiales cúbicos al 100%. Esta estructura es análoga a una celda cúbica centrada en el cuerpo en términos de la relación geométrica, aunque los átomos no son idénticos.
- Descripción: Iones de diferente tamaño, donde el ión más pequeño (Cs+) se sitúa en el centro de un cubo formado por los iones más grandes (Cl-). Los iones están en contacto a lo largo de la diagonal del cuerpo.
- Derivación: La diagonal del cuerpo (h) está formada por dos radios de aniones y dos radios de cationes (es decir, el radio del ión de la esquina más el diámetro del ión central, más el radio del ión de la esquina opuesta).
h = 2r_anion + 2r_cation
Utilizando la misma relación de la celda BCC:
h² = 3l²
Por lo tanto:
(2r_anion + 2r_cation)² = 3l²
Relación:l = (2r_anion + 2r_cation) / sqrt(3)
Estructura tipo Cloruro de Litio (LiCl)
En la estructura del cloruro de litio, los iones cloruro (Cl-) forman una red cúbica centrada en la cara (FCC), y los iones litio (Li+) ocupan los sitios intersticiales octaédricos al 100%. Los iones de litio son lo suficientemente pequeños como para que los iones de cloruro de las esquinas estén en contacto con los iones de cloruro de las caras.
- Descripción: Iones de diferente tamaño, donde los aniones (Cl-) forman una red FCC, y los cationes (Li+) ocupan los agujeros octaédricos. Los aniones están en contacto a lo largo de la diagonal de la cara.
- Derivación: La diagonal de la cara (d) está formada por cuatro radios del ión de la esquina (el anión).
- Ejemplo: La longitud del borde de la celda unitaria del LiCl es de 0.514 nm. Suponiendo que los iones cloruro están en contacto, el radio iónico del cloruro es:
d = 4r_anion
Utilizando la misma relación de la celda FCC:
d² = 2l²
Por lo tanto:
(4r_anion)² = 2l²
16r_anion² = 2l²
Relación:l = sqrt(8)r_anion o l = 2 * sqrt(2) * r_anion
l = sqrt(8) * r_Cl-
0.514 nm = sqrt(8) * r_Cl-
r_Cl- = 0.514 nm / sqrt(8) ≈ 0.182 nm
Cómo Calcular el Número de Átomos en una Celda Unitaria
Para determinar la fórmula de un compuesto a partir de su celda unitaria, es esencial saber cuántos átomos o iones completos contiene la celda unitaria. Los átomos que se encuentran en las esquinas, bordes o caras son compartidos por celdas unitarias adyacentes, por lo que solo una fracción de ellos pertenece a una celda unitaria específica.
- Un átomo en una esquina: Contribuye 1/8 a la celda unitaria.
- Un átomo en un borde: Contribuye 1/4 a la celda unitaria.
- Un átomo en una cara: Contribuye 1/2 a la celda unitaria.
- Un átomo en el cuerpo (centro): Contribuye 1 a la celda unitaria.
Para calcular el número total de átomos en una celda unitaria, se suman las contribuciones de todos los átomos presentes.
Ejemplo: Determinar la cantidad de átomos en una celda unitaria de NaCl.
La estructura del NaCl es FCC para los iones Cl- (aniones) y los iones Na+ (cationes) ocupan los agujeros octaédricos. Observando la celda unitaria:
- Iones Cl- (aniones):
- 8 en las esquinas:
8 * (1/8) = 1ión Cl- - 6 en los centros de las caras:
6 * (1/2) = 3iones Cl- - Total de iones Cl- =
1 + 3 = 4iones Cl-
- 8 en las esquinas:
- Iones Na+ (cationes):
- 12 en los bordes:
12 * (1/4) = 3iones Na+ - 1 en el centro del cuerpo:
1 * (1) = 1ión Na+ - Total de iones Na+ =
3 + 1 = 4iones Na+
- 12 en los bordes:
Por lo tanto, una celda unitaria de NaCl contiene 4 iones Na+ y 4 iones Cl-, lo que confirma la estequiometría 1:1 de la fórmula NaCl.
¿Cuál es la longitud del borde de la celda unitaria de la plata?
La plata (Ag) es un metal conocido por su alta conductividad eléctrica y térmica. Cristaliza en una estructura cúbica centrada en la cara (FCC). Según las mediciones cristalográficas, la longitud del borde de su celda unitaria es de 409 pm (picómetros).
Utilizando la relación para una estructura FCC que derivamos anteriormente (l = sqrt(8)r o l = 2 * sqrt(2) * r), podemos calcular el radio atómico de la plata:
409 pm = sqrt(8) * r_Ag
r_Ag = 409 pm / sqrt(8)
r_Ag = 409 pm / 2.8284
r_Ag ≈ 144.5 pm
Además de la longitud del borde y el radio atómico, podemos calcular la densidad de la plata. Una celda unitaria FCC contiene 4 átomos (como se explicó en la sección de conteo de átomos).

- Masa de la celda unitaria de Ag:
- Volumen de la celda unitaria de Ag:
- Densidad de Ag:
Masa atómica de Ag ≈ 107.87 g/mol
Número de Avogadro = 6.022 x 1023 átomos/mol
Masa = 4 átomos Ag * (1 mol Ag / 6.022 x 10^23 átomos) * (107.87 g / 1 mol Ag)
Masa ≈ 7.161 x 10^-22 g
Convertimos la longitud del borde a cm: 409 pm = 409 x 10^-12 m = 409 x 10^-10 cm
V = l³ = (409 x 10^-10 cm)³
V ≈ 6.830 x 10^-23 cm³
Densidad = Masa / Volumen
Densidad = (7.161 x 10^-22 g) / (6.830 x 10^-23 cm³)
Densidad ≈ 10.48 g/cm³
Este valor calculado se aproxima muy bien a la densidad experimental de la plata (alrededor de 10.49 g/cm³), lo que valida la estructura FCC y la longitud del borde.
Preguntas Frecuentes sobre Celdas Unitarias
¿Qué es una celda unitaria?
Una celda unitaria es la unidad de repetición más pequeña y básica de un sólido cristalino. Es el 'ladrillo' fundamental que, al repetirse en tres dimensiones, construye la estructura cristalina completa del material. Definir una celda unitaria es crucial para describir la disposición atómica de un cristal.
¿Por qué existen diferentes tipos de celdas unitarias?
Los diferentes tipos de celdas unitarias (como cúbica simple, BCC, FCC, etc.) surgen de las distintas formas en que los átomos o iones pueden empaquetarse para maximizar las interacciones atractivas y minimizar la energía total. La geometría y la eficiencia de empaquetamiento varían entre ellas, lo que lleva a propiedades materiales diversas. Existen catorce tipos de celdas unitarias, conocidos como redes de Bravais, agrupadas en siete sistemas cristalinos.
¿Qué es el número de coordinación en una celda unitaria?
El número de coordinación de un átomo o ión en una estructura cristalina es el número de otros átomos o iones con los que está en contacto directo. Es una medida de cuán densamente empaquetado está el cristal. Por ejemplo, en una celda FCC, cada átomo tiene un número de coordinación de 12, lo que indica un empaquetamiento muy eficiente.
¿Cómo se determinan los radios iónicos a partir de las celdas unitarias?
Los radios iónicos se pueden estimar a partir de la longitud del borde de la celda unitaria y la geometría de la red, asumiendo que los iones se comportan como esferas perfectas que están en contacto. Para compuestos iónicos, se suelen considerar los radios de los cationes y aniones, y su disposición en los huecos (tetraédricos, octaédricos o cúbicos) de la red aniónica o catiónica. Aunque estos valores son aproximados, son útiles para comprender la estructura y propiedades de los compuestos iónicos.
¿Qué importancia tiene la longitud de la celda unitaria en la ciencia de materiales?
La longitud de la celda unitaria es fundamental para calcular propiedades como la densidad del material, que es una propiedad macroscópica directamente relacionada con la masa contenida en el volumen de la celda unitaria. También influye en propiedades mecánicas, eléctricas y ópticas, ya que la distancia entre átomos afecta cómo interactúan entre sí y con el entorno.
Si quieres conocer otros artículos parecidos a Calculando la Longitud de Celdas Unitarias puedes visitar la categoría Cálculos.
