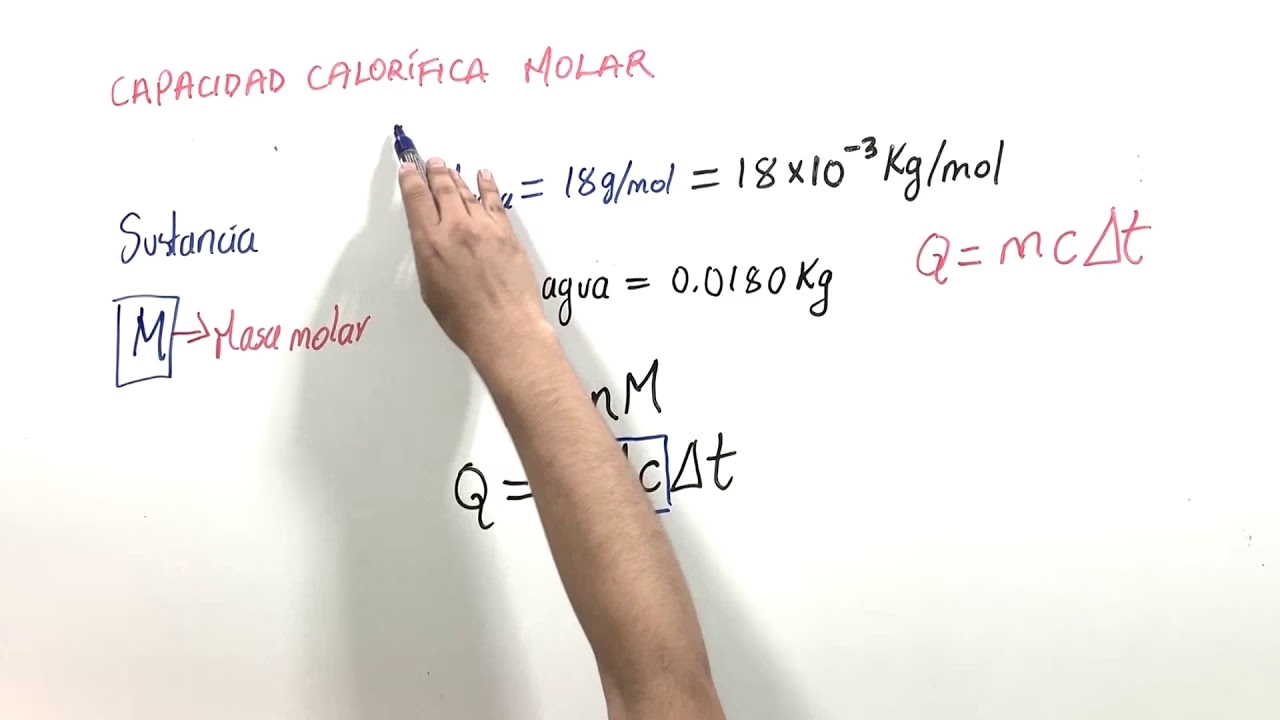15/01/2026
¿Alguna vez te has preguntado por qué, en un día soleado en la playa, la arena está abrasadora mientras el agua del mar se mantiene sorprendentemente fresca? Este fenómeno, tan común en nuestra experiencia diaria, es un punto de partida excelente para explorar un concepto fundamental en la física y la química: la capacidad de las sustancias para absorber y retener calor. Aunque el sol irradia la misma cantidad de energía sobre ambos, la arena y el agua reaccionan de manera diferente. Esta disparidad nos lleva directamente a la idea de la capacidad calorífica específica, y más allá, al concepto de calor molar específico, una medida crucial para entender cómo la materia interactúa con la energía térmica a nivel de sus constituyentes fundamentales.

Cuando aplicamos calor a un elemento sólido o líquido, su temperatura suele aumentar. Sin embargo, si aplicamos la misma cantidad de calor a dos tipos distintos de sólidos, el aumento de temperatura en cada uno puede ser diferente. Esto nos indica que la respuesta térmica de un material es intrínseca a su composición. Esta propiedad se conoce como capacidad calorífica específica, y es la base para comprender el calor molar.
- ¿Qué es la Capacidad Calorífica Específica?
- Del Gramo al Mol: El Calor Molar Específico
- Capacidad Calorífica a Volumen Constante (Cv) y a Presión Constante (Cp)
- Importancia y Aplicaciones del Calor Específico y Molar
- Calor Molar de Fusión (ΔHfus)
- Calor Molar de Combustión
- Comparativa: Capacidad Calorífica Específica vs. Capacidad Calorífica Molar
- Preguntas Frecuentes (FAQ)
- Conclusión
¿Qué es la Capacidad Calorífica Específica?
En términos sencillos, la capacidad calorífica específica de un sólido o líquido es la cantidad de calor necesaria para elevar la temperatura de una unidad de masa de la sustancia en un grado Celsius (o Kelvin). Se simboliza con la letra 'c' o 'C' (minúscula en algunos contextos, mayúscula en otros, aunque para molar se usa más la mayúscula). En el Sistema Internacional (S.I.), su unidad de medida es julios por kilogramo y por Kelvin (J kg⁻¹ K⁻¹). En el sistema CGS, se mide en calorías por gramo y por grado Celsius (cal g⁻¹ °C⁻¹).
Si la cantidad de calor 'Q' necesaria para elevar la temperatura de una masa 'm' a través de una diferencia de temperatura '∆T' es conocida, la fórmula de la capacidad calorífica específica es la siguiente:
c = Q / (m * ∆T)
O, de manera equivalente, para calcular el calor absorbido o liberado:
Q = m * c * ∆T
Esta fórmula es fundamental para cuantificar cómo el calor interactúa con la masa de una sustancia, proporcionando una comprensión básica de las diferencias térmicas que observamos en nuestro entorno.
Del Gramo al Mol: El Calor Molar Específico
Mientras que la capacidad calorífica específica se refiere a la unidad de masa (generalmente kilogramos o gramos), el calor molar específico (o capacidad calorífica molar) lleva esta idea un paso más allá, enfocándose en la cantidad de sustancia a nivel molecular. Se define como la cantidad de calor necesaria para aumentar la temperatura de un mol de una sustancia (sólido o líquido) en un Kelvin (o un grado Celsius).
Se simboliza con la letra 'C' (mayúscula) y su unidad de medida en el S.I. es julios por mol y por Kelvin (J mol⁻¹ K⁻¹). Por lo tanto, para elevar la temperatura de un mol de sólido a través de una diferencia de temperatura ∆T, se requeriría una cantidad de calor 'Q' igual a:
Q = n * C * ∆T
Donde 'n' es el número de moles de la sustancia. Cuando hablamos de la capacidad calorífica molar de una sustancia, nos referimos a la cantidad de calor que necesitamos entregar para elevar la temperatura de una molécula gramo (un mol) de la sustancia en un grado Celsius. Esto es particularmente útil en química y física cuando se trabaja con reacciones y procesos a nivel molecular, ya que el mol es una unidad que directamente relaciona la masa con el número de partículas.
La capacidad calorífica específica del agua, por ejemplo, se considera uno (1 cal g⁻¹ °C⁻¹ o 4.184 J g⁻¹ °C⁻¹). Esto se debe a que la unidad de calor (la caloría) se definió históricamente utilizando el agua como referencia. La alta capacidad calorífica del agua es la razón principal por la que modera las temperaturas en las regiones costeras y es esencial para la vida en la Tierra.

Capacidad Calorífica a Volumen Constante (Cv) y a Presión Constante (Cp)
La forma en que se calienta una sustancia, especialmente un gas, puede influir significativamente en la cantidad de calor necesaria para elevar su temperatura. Para sólidos y líquidos, la expansión térmica es mínima, por lo que la diferencia entre calentar a volumen constante o a presión constante es generalmente despreciable. Sin embargo, para los gases, esta distinción es crucial.
- Capacidad Calorífica a Volumen Constante (Cv): Cuando un gas se calienta en un recipiente cerrado que impide su expansión (es decir, el volumen permanece constante), todo el calor suministrado se utiliza para aumentar la energía interna del gas, lo que se manifiesta como un aumento de temperatura. No se realiza trabajo sobre el entorno.
- Capacidad Calorífica a Presión Constante (Cp): Cuando un gas se calienta permitiéndole expandirse libremente para mantener la presión constante (por ejemplo, en un cilindro con un pistón móvil), parte del calor suministrado se utiliza para aumentar la energía interna, y otra parte se convierte en trabajo realizado por el gas sobre el entorno (al expandirse). Por lo tanto, se necesita más calor para lograr el mismo aumento de temperatura a presión constante que a volumen constante.
Esta diferencia lleva a la importante relación para un gas ideal:
Cp – Cv = nR
Donde 'n' es la cantidad de sustancia en moles, y 'R' es la constante de los gases ideales (aproximadamente 8.314 J mol⁻¹ K⁻¹). Esta ecuación ilustra que la capacidad calorífica de un gas no es un valor único, sino que depende de las condiciones bajo las cuales se suministra el calor. En el caso de un gas, la capacidad calorífica puede tener un rango infinito de valores si no se mantiene constante la presión o el volumen.
Importancia y Aplicaciones del Calor Específico y Molar
Comprender la capacidad calorífica, tanto específica como molar, tiene numerosas aplicaciones prácticas en nuestra vida cotidiana y en diversas industrias:
- Utensilios de Cocina: Los fondos de sartenes y ollas suelen estar hechos de materiales con baja capacidad calorífica, como el aluminio o el cobre pulido. Esto permite que se calienten rápidamente, transmitiendo el calor a los alimentos de manera eficiente. Por el contrario, los mangos de estos utensilios están hechos de materiales con alta capacidad calorífica (como plásticos o madera) para aislar el calor y proteger nuestras manos, evitando quemaduras.
- Aislamiento: Los materiales con alta capacidad calorífica son excelentes aislantes. La madera, por ejemplo, es un buen aislante térmico debido a su capacidad para absorber y liberar calor lentamente. Por eso, las casas de madera son adecuadas tanto para climas cálidos como fríos, ya que ayudan a mantener una temperatura interior más estable.
- Regulación Climática: La alta capacidad calorífica del agua es fundamental para la regulación del clima global. Grandes masas de agua, como los océanos, absorben enormes cantidades de calor durante el día o el verano y lo liberan lentamente durante la noche o el invierno, moderando así las temperaturas de las regiones costeras. Es por esto que el agua de una piscina se siente relativamente fresca en comparación con la temperatura ambiente, ya que necesita absorber una gran cantidad de calor para que su temperatura aumente significativamente.
- Ingeniería y Materiales: En ingeniería, el conocimiento de estas propiedades es crucial para el diseño de sistemas de enfriamiento, intercambiadores de calor, motores, y en la selección de materiales para diversas aplicaciones donde la gestión térmica es clave.
Calor Molar de Fusión (ΔHfus)
El calor molar de fusión es un concepto relacionado pero distinto, que se refiere a los cambios de estado de la materia. Es el cambio de entalpía (o calor) que se requiere para que un mol de una sustancia pase del estado sólido al estado líquido a su temperatura de fusión, sin que haya un cambio de temperatura. Es un proceso endotérmico, lo que significa que la sustancia absorbe calor del entorno para llevar a cabo la fusión.
Todos los sólidos absorben calor al fundirse para convertirse en líquidos. Este calor absorbido se utiliza para romper los enlaces intermoleculares en la estructura cristalina del sólido y reorganizarlos en la estructura más desordenada del líquido, en lugar de aumentar la energía cinética de las moléculas (que se manifestaría como un aumento de temperatura).
Para calcular el calor molar de fusión, primero se convierte la masa de la muestra a moles y luego se multiplica por el valor de ΔHfus (generalmente en kJ/mol) para la sustancia en cuestión. Por ejemplo, el calor molar de fusión del agua es de aproximadamente 6.01 kJ/mol. Esto significa que se necesitan 6.01 kilojulios de energía para fundir un mol de hielo a 0°C y convertirlo en un mol de agua líquida a 0°C.
Calor Molar de Combustión
Aunque no se detalló en la información original, es importante mencionar que existe un concepto análogo para las reacciones de combustión: el calor molar de combustión. Se define como la cantidad de calor liberada cuando un mol de una sustancia reacciona completamente con oxígeno en una reacción de combustión. Las reacciones de combustión son exotérmicas, lo que significa que liberan energía en forma de calor. Este valor es crucial en el estudio de combustibles y en la ingeniería de motores, ya que indica la eficiencia energética de una sustancia.

Comparativa: Capacidad Calorífica Específica vs. Capacidad Calorífica Molar
Para clarificar las diferencias, presentamos la siguiente tabla comparativa:
| Característica | Capacidad Calorífica Específica (c) | Capacidad Calorífica Molar (C) |
|---|---|---|
| Definición | Calor para elevar 1 unidad de masa en 1 K/°C | Calor para elevar 1 mol en 1 K/°C |
| Unidades S.I. | J kg⁻¹ K⁻¹ (o J g⁻¹ K⁻¹) | J mol⁻¹ K⁻¹ |
| Dependencia | De la masa y la naturaleza de la sustancia | De la cantidad de sustancia (moles) y su naturaleza |
| Aplicación principal | Cálculos de transferencia de calor en ingeniería, termodinámica | Cálculos en química, reacciones a nivel molecular, termodinámica |
| Relación | c = C / Masa Molar | C = c * Masa Molar |
Preguntas Frecuentes (FAQ)
Aquí respondemos algunas de las preguntas más comunes sobre el calor molar y conceptos relacionados:
¿Cuál es la principal diferencia entre capacidad calorífica y calor molar?
La capacidad calorífica (o calor específico) se refiere a la cantidad de calor necesaria para elevar la temperatura de una unidad de masa (ej., 1 gramo o 1 kilogramo) de una sustancia en un grado. El calor molar, en cambio, se refiere a la cantidad de calor necesaria para elevar la temperatura de un mol de una sustancia en un grado. La diferencia radica en la unidad de cantidad de sustancia utilizada (masa vs. moles).
¿Por qué el agua tiene una capacidad calorífica tan alta?
El agua tiene una capacidad calorífica muy alta debido a los fuertes enlaces de hidrógeno entre sus moléculas. Se necesita una gran cantidad de energía para romper estos enlaces antes de que la energía cinética de las moléculas pueda aumentar significativamente, lo que se traduce en un aumento de temperatura.
¿Cómo se mide el calor molar en un laboratorio?
El calor molar se mide experimentalmente utilizando un calorímetro. Este dispositivo permite medir el cambio de temperatura de una sustancia cuando se le añade o se le quita una cantidad conocida de calor. A partir de estas mediciones y conociendo la masa molar de la sustancia, se puede calcular su calor molar.
¿El calor molar es siempre positivo?
El calor molar específico (o capacidad calorífica molar) es siempre positivo, ya que se necesita una entrada de energía (calor) para aumentar la temperatura de una sustancia. Sin embargo, los calores molares de reacción (como el calor molar de combustión) pueden ser negativos, indicando que se libera calor, o positivos (como el calor molar de fusión), indicando que se absorbe calor.
¿Qué significa que una sustancia tiene un calor molar alto?
Una sustancia con un calor molar alto significa que requiere una gran cantidad de energía térmica para que su temperatura cambie significativamente. Estas sustancias son buenos aislantes térmicos o pueden almacenar grandes cantidades de energía sin un gran aumento de temperatura, como el agua.
Conclusión
La capacidad calorífica molar de una sustancia química se define como la cantidad de energía que debe suministrarse en forma de calor a un mol de la sustancia para producir un aumento de una unidad en su temperatura. Es, en esencia, la capacidad calorífica de una muestra de la sustancia dividida por la cantidad de sustancia en la muestra, o alternativamente, la capacidad calorífica específica de la sustancia multiplicada por su masa molar. Comprender el calor molar es fundamental para predecir y controlar los cambios de temperatura en diversos sistemas, desde el diseño de materiales hasta la comprensión de los fenómenos naturales. Revela cómo las propiedades intrínsecas de la materia a nivel molecular dictan su respuesta a la energía térmica, siendo una herramienta indispensable en campos como la química, la física, la ingeniería y las ciencias ambientales. La próxima vez que estés en la playa, recordarás que la diferencia en la temperatura entre la arena y el agua es un testimonio elocuente del poder del calor molar.
Si quieres conocer otros artículos parecidos a ¿Qué es el Calor Molar? Una Guía Completa puedes visitar la categoría Física.