02/04/2026
La presión de vapor es una propiedad física crucial que describe la tendencia de una sustancia a pasar del estado líquido o sólido al estado gaseoso. Su conocimiento es fundamental en una amplia gama de campos, desde la química y la física hasta la ingeniería de procesos y la meteorología. Comprender cómo calcularla a partir de la temperatura es una habilidad invaluable para ingenieros, científicos y estudiantes por igual. Este artículo desglosará los métodos más comunes y las ecuaciones clave utilizadas para determinar la presión de vapor cuando se conoce la temperatura, y explorará conceptos relacionados como el calor latente de vaporización.

- Entendiendo la Presión de Vapor
- Métodos para Calcular la Presión de Vapor a partir de la Temperatura
- Derivando el Calor Latente de Vaporización (ΔH) de una Ecuación de Presión de Vapor
- Paso 1: Convertir la Ecuación a Logaritmo Natural (ln)
- Paso 2: Diferenciar la Ecuación con Respecto a T
- Paso 3: Relacionar la Derivada con el Calor Latente (Clausius-Clapeyron)
- Paso 4: Igualar las Expresiones y Resolver para ΔH_vap
- Paso 5: Calcular ΔH_vap a una Temperatura Específica (Ejemplo a T = 80 K)
- Importancia Industrial de la Presión de Vapor y el Calor Latente
- Tabla Comparativa de Métodos de Cálculo
- Preguntas Frecuentes (FAQs)
- Conclusión
Entendiendo la Presión de Vapor
Antes de sumergirnos en los cálculos, es vital comprender qué representa la presión de vapor. Imagina un líquido en un recipiente cerrado. Las moléculas en la superficie del líquido tienen suficiente energía para escapar y convertirse en gas. Este gas ejerce una presión sobre las paredes del recipiente. Con el tiempo, se alcanza un equilibrio dinámico donde la velocidad de evaporación es igual a la velocidad de condensación. La presión que ejerce el vapor en este equilibrio se conoce como presión de vapor saturada o simplemente presión de vapor.
La presión de vapor es fuertemente dependiente de la temperatura: a mayor temperatura, más moléculas tienen la energía necesaria para escapar, lo que resulta en una mayor presión de vapor. Cada sustancia pura tiene una curva de presión de vapor característica que define su comportamiento en función de la temperatura.
Métodos para Calcular la Presión de Vapor a partir de la Temperatura
Existen varias aproximaciones para determinar la presión de vapor de una sustancia a una temperatura dada. Estas van desde el uso de ecuaciones empíricas hasta relaciones termodinámicas fundamentales.
1. Uso de Ecuaciones Empíricas Específicas
Muchas sustancias tienen ecuaciones de presión de vapor que han sido determinadas experimentalmente y ajustadas a una forma matemática particular. La ecuación proporcionada en el problema es un ejemplo de ello:
log10P = 3.54595 − 313.7/T + 1.40655*log10T
Donde P es la presión de vapor y T es la temperatura (generalmente en Kelvin). Para calcular la presión de vapor con esta ecuación, simplemente necesitas sustituir el valor de la temperatura (T) y resolver para P. Es importante asegurarse de que la temperatura se ingresa en las unidades correctas, que en este caso, por la forma de la ecuación, es muy probable que sean Kelvin.
Ejemplo de Cálculo Directo:
Supongamos que deseamos calcular la presión de vapor utilizando la ecuación dada a una temperatura de 80 K.
log10P = 3.54595 − 313.7/80 + 1.40655*log10(80)
Primero, calculamos los términos:
313.7/80 = 3.92125log10(80) ≈ 1.903091.40655 * 1.90309 ≈ 2.6766
Ahora, sustituimos estos valores en la ecuación:
log10P = 3.54595 − 3.92125 + 2.6766
log10P = 2.3013
Para encontrar P, tomamos 10 elevado a la potencia de este resultado:
P = 10^(2.3013)
P ≈ 200.1 mmHg (Asumiendo que la ecuación está calibrada para mmHg, una unidad común para presión de vapor en ciertas aplicaciones).
Este ejemplo demuestra que, cuando se dispone de una ecuación empírica, el cálculo de la presión de vapor es un proceso de sustitución directa.
2. La Ecuación de Antoine
Una de las ecuaciones empíricas más ampliamente utilizadas para la presión de vapor es la Ecuación de Antoine. Su forma general es:
log10P = A − B / (C + T)
Donde P es la presión de vapor, T es la temperatura (a menudo en grados Celsius o Kelvin, dependiendo de los coeficientes), y A, B, C son constantes específicas para cada sustancia. Estas constantes se obtienen experimentalmente y se tabulan para miles de compuestos. La ecuación de Antoine es precisa en un rango de temperatura limitado, pero es muy popular debido a su simplicidad y buena precisión dentro de esos rangos.
Ventajas de la Ecuación de Antoine:
- Fácil de usar y aplicar.
- Coeficientes disponibles para una vasta cantidad de sustancias.
- Buena precisión en el rango de temperatura aplicable.
Limitaciones:
- No es válida para todo el rango de temperaturas, especialmente cerca del punto crítico o del punto triple.
- Los coeficientes son específicos para el rango de temperatura y las unidades de presión y temperatura.
3. La Ecuación de Clausius-Clapeyron
La Ecuación de Clausius-Clapeyron es una relación termodinámica fundamental que describe la relación entre la presión de vapor y la temperatura. Es especialmente útil cuando se conocen dos puntos de presión-temperatura o cuando se conoce el calor latente de vaporización.
La forma diferencial de la ecuación es:
d(lnP)/dT = ΔH_vap / (R * T^2)
Donde:
Pes la presión de vapor.Tes la temperatura absoluta (en Kelvin).ΔH_vapes el calor molar latente de vaporización (se asume constante en su forma integrada simplificada).Res la constante de los gases ideales.
Si se integra esta ecuación asumiendo que ΔH_vap es constante en un rango de temperatura, se obtiene una forma lineal:
ln(P2/P1) = - (ΔH_vap / R) * (1/T2 - 1/T1)
Esta forma permite calcular la presión de vapor (P2) a una nueva temperatura (T2) si se conoce la presión de vapor (P1) a una temperatura de referencia (T1) y el calor latente de vaporización. Alternativamente, si se tienen múltiples puntos de datos (P, T), se puede graficar ln(P) contra 1/T para obtener una línea recta cuya pendiente es -ΔH_vap/R, permitiendo calcular el calor latente.
Derivando el Calor Latente de Vaporización (ΔH) de una Ecuación de Presión de Vapor
Aunque el objetivo principal es calcular la presión de vapor a partir de la temperatura, las ecuaciones empíricas de presión de vapor, como la que se nos dio, también pueden usarse para derivar otras propiedades termodinámicas importantes, como el calor latente de vaporización (ΔH_vap). Este es el proceso inverso al que a menudo se usa para construir la ecuación de Clausius-Clapeyron a partir de datos experimentales.
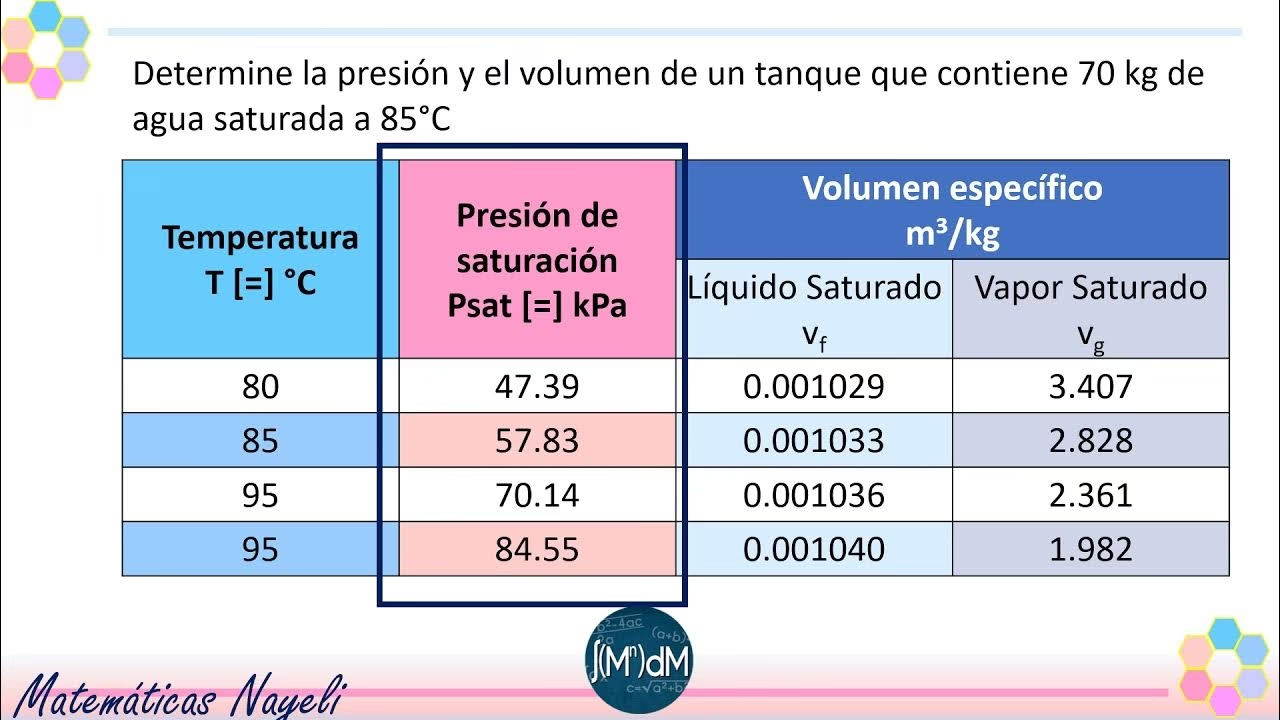
Retomemos la ecuación proporcionada:
log10P = 3.54595 − 313.7/T + 1.40655*log10T
Paso 1: Convertir la Ecuación a Logaritmo Natural (ln)
La ecuación de Clausius-Clapeyron utiliza el logaritmo natural (ln). Sabemos que log10X = lnX / 2.303, por lo tanto, lnX = 2.303 * log10X. Multiplicamos toda la ecuación por 2.303 para convertirla a lnP:
lnP = 2.303 * (3.54595 − 313.7/T + 1.40655*log10T)
lnP = (3.54595 * 2.303) − (313.7 * 2.303)/T + (1.40655 * 2.303)*log10T
Calculando los productos:
3.54595 * 2.303 ≈ 8.1666313.7 * 2.303 ≈ 722.401.40655 * 2.303 ≈ 3.2392
Y reemplazando 2.303*log10T con lnT:
lnP = 8.1666 − 722.40/T + 3.2392*lnT
Paso 2: Diferenciar la Ecuación con Respecto a T
Ahora, diferenciamos ambos lados de la ecuación con respecto a la temperatura (T):
d(lnP)/dT = d/dT (8.1666 − 722.40/T + 3.2392*lnT)
Recordemos que d/dT (constante) = 0, d/dT (K/T) = -K/T^2 (por lo que d/dT (-K/T) = K/T^2) y d/dT (lnT) = 1/T.
Aplicando esto:
d(lnP)/dT = 0 − (-722.40/T^2) + 3.2392*(1/T)
d(lnP)/dT = 722.40/T^2 + 3.2392/T
Paso 3: Relacionar la Derivada con el Calor Latente (Clausius-Clapeyron)
Según la ecuación de Clausius-Clapeyron (en su forma diferencial), sabemos que:
d(lnP)/dT = ΔH_vap / (R * T^2)
Donde R es la constante de los gases ideales.
Paso 4: Igualar las Expresiones y Resolver para ΔH_vap
Ahora igualamos las dos expresiones para d(lnP)/dT:
ΔH_vap / (R * T^2) = 722.40/T^2 + 3.2392/T
Para despejar ΔH_vap, multiplicamos ambos lados por R * T^2:
ΔH_vap = R * T^2 * (722.40/T^2 + 3.2392/T)
Distribuimos R * T^2:
ΔH_vap = R * (722.40 * T^2/T^2 + 3.2392 * T^2/T)
ΔH_vap = R * (722.40 + 3.2392 * T)
Esta es la expresión para el calor molar latente de vaporización (ΔH_vap) como función de la temperatura (T) para la sustancia descrita por la ecuación de presión de vapor original. Es importante notar que, a diferencia de la suposición simplificada en la integración de Clausius-Clapeyron, esta derivación permite que ΔH_vap varíe con la temperatura, lo cual es más realista.
Paso 5: Calcular ΔH_vap a una Temperatura Específica (Ejemplo a T = 80 K)
Asumiendo que R = 1.987 cal/(mol·K) (un valor común para la constante de los gases en unidades calóricas), y para T = 80 K:
ΔH_vap = 1.987 * (722.40 + 3.2392 * 80)
Calculamos el término dentro del paréntesis:
3.2392 * 80 ≈ 259.136722.40 + 259.136 ≈ 981.536
Ahora, multiplicamos por R:
ΔH_vap = 1.987 * 981.536
ΔH_vap ≈ 1950.4 cal/mol
Es fundamental comprender que el valor del calor latente de vaporización (ΔH_vap) no siempre es constante y puede variar con la temperatura, como se observa en la expresión derivada. Las ecuaciones simplificadas de Clausius-Clapeyron a menudo asumen un ΔH_vap constante para facilitar los cálculos, lo cual es una aproximación válida en rangos de temperatura pequeños.
Importancia Industrial de la Presión de Vapor y el Calor Latente
En el ámbito industrial, especialmente en plantas de procesamiento, la gestión de la presión y la temperatura del vapor es crítica. El vapor se utiliza para calefacción, generación de energía y como medio de reacción. La comprensión de la presión de vapor y el calor latente de vaporización es esencial por varias razones:
- Diseño de Equipos: Recipientes a presión, intercambiadores de calor y tuberías deben diseñarse para soportar las presiones y temperaturas máximas esperadas. El conocimiento de la presión de vapor a diferentes temperaturas es vital para garantizar la seguridad y eficiencia.
- Eficiencia Energética: El calor latente de vaporización representa la energía necesaria para cambiar de fase. En procesos donde el vapor condensa (libera calor latente) o se evapora (absorbe calor latente), conocer este valor permite calcular las necesidades energéticas y optimizar el consumo. El vapor saturado, por ejemplo, es preferido en intercambiadores de calor debido a su alta transferencia de calor latente, mientras que el vapor sobrecalentado es más adecuado para turbinas donde se busca evitar la condensación prematura.
- Control de Procesos: En las plantas, la temperatura del vapor se monitorea continuamente. Si bien en los niveles más altos (como las estaciones de reducción de presión) se controla la temperatura, en los niveles inferiores, a menudo se controla la presión y se permite que la temperatura se ajuste. Las estaciones de desobrecalentamiento pueden añadir agua para reducir el sobrecalentamiento y mantener el vapor dentro de las especificaciones de las tuberías y los equipos, evitando problemas como la superación de los límites de temperatura de los materiales o la reducción de la eficiencia de transferencia de calor en los intercambiadores.
- Prevención de Problemas: Un control inadecuado puede llevar a la condensación indeseada (formación de condensado) o, por el contrario, a un sobrecalentamiento excesivo que puede dañar el equipo o reducir la eficiencia de transferencia de calor. La meta es a menudo tener solo el sobrecalentamiento suficiente para asegurar que el vapor permanezca seco hasta su punto de uso.
Tabla Comparativa de Métodos de Cálculo
Para una mejor comprensión, la siguiente tabla resume las características principales de los métodos de cálculo de presión de vapor discutidos:
| Método | Descripción | Ventajas | Limitaciones | Aplicación Típica |
|---|---|---|---|---|
Ecuaciones Empíricas Específicas (Ej. log10P = A - B/T + C*log10T) | Fórmulas derivadas de datos experimentales, únicas para cada sustancia. | Alta precisión dentro de su rango de validez; cálculo directo. | Válidas solo para la sustancia y rango específico; no siempre disponibles. | Cálculos precisos para sustancias bien caracterizadas. |
Ecuación de Antoine (log10P = A - B / (C + T)) | Empírica, ampliamente tabulada con coeficientes A, B, C para muchas sustancias. | Amplia disponibilidad de coeficientes; relativamente simple y precisa. | Precisa solo en rangos de temperatura específicos; no aplica cerca de puntos críticos. | Estimaciones rápidas y fiables en ingeniería química. |
| Ecuación de Clausius-Clapeyron (Forma Integrada) | Basada en termodinámica; relaciona P y T con el calor latente de vaporización. | Fundamento teórico sólido; útil para estimar P a T diferentes si se conoce ΔH_vap. | Asume ΔH_vap constante (simplificación); requiere un punto de referencia (P1, T1). | Estimaciones cuando hay datos limitados o para comprender el comportamiento fundamental. |
| Tablas de Vapor / Software Termodinámico | Datos tabulados o algoritmos complejos que integran múltiples propiedades. | Muy alta precisión; cubren amplios rangos; incluyen otras propiedades. | Requiere acceso a tablas/software; no es un "cálculo manual" directo por ecuación. | Diseño de plantas, simulaciones de procesos, operaciones industriales. |
Preguntas Frecuentes (FAQs)
¿Por qué es tan importante calcular la presión de vapor?
La presión de vapor es fundamental para entender y predecir el comportamiento de las sustancias en diferentes condiciones. Es crucial en el diseño de equipos (como bombas, compresores, intercambiadores de calor), en la seguridad industrial (riesgo de explosiones, inflamabilidad), en la separación de mezclas (destilación), y en fenómenos naturales (ciclo del agua, meteorología).
¿Qué factores afectan la presión de vapor de una sustancia?
El factor más significativo es la temperatura: a mayor temperatura, mayor presión de vapor. Otros factores incluyen la naturaleza de la sustancia (fuerzas intermoleculares), la presencia de solutos (presión de vapor de soluciones es menor que la del solvente puro) y, en menor medida, la presión externa total (aunque esto es más relevante para la ebullición que para la presión de vapor intrínseca).
¿Cuándo se debe usar vapor sobrecalentado y cuándo vapor saturado en una planta?
El vapor saturado, que coexiste con el agua líquida a la misma temperatura y presión, es ideal para procesos de calentamiento (como en intercambiadores de calor) porque libera una gran cantidad de calor latente de vaporización al condensarse, lo que resulta en una transferencia de calor muy eficiente a temperatura constante. El vapor sobrecalentado, que está a una temperatura superior a su punto de saturación para una presión dada, se utiliza comúnmente para accionar turbinas o en procesos donde la condensación es indeseable, ya que contiene solo calor sensible y mantiene su estado gaseoso por más tiempo.
¿Puedo usar la ecuación empírica dada para cualquier sustancia?
No. Las ecuaciones empíricas como la proporcionada (log10P = 3.54595 − 313.7/T + 1.40655*log10T) o la ecuación de Antoine tienen coeficientes que son específicos para una sustancia en particular y a menudo para un rango de temperatura determinado. Utilizar los coeficientes de una sustancia para otra o fuera de su rango de validez resultará en cálculos incorrectos. Es crucial consultar fuentes fiables para obtener los coeficientes correctos para la sustancia de interés.
¿Cómo se manejan las unidades en estas ecuaciones?
Es vital prestar extrema atención a las unidades. Las constantes en las ecuaciones empíricas están definidas para unidades específicas de presión (por ejemplo, mmHg, kPa, bar) y temperatura (Kelvin o Celsius). Si la ecuación requiere Kelvin, siempre convierta la temperatura a Kelvin. Si los coeficientes de Antoine están dados para presión en mmHg y temperatura en °C, use esas unidades. El uso inconsistente de unidades es una fuente común de errores en estos cálculos.
¿Qué es la "política de cookies" o "redes sociales" en este contexto?
Estos términos no tienen ninguna relación directa con el cálculo de la presión de vapor o los conceptos termodinámicos discutidos en este artículo. Son elementos de la infraestructura web o de negocios que no son relevantes para el contenido técnico.
Conclusión
El cálculo de la presión de vapor a partir de la temperatura es una habilidad esencial en muchas disciplinas científicas y de ingeniería. Ya sea utilizando ecuaciones empíricas directas, la versátil ecuación de Antoine, o las relaciones termodinámicas de Clausius-Clapeyron, la clave reside en entender los principios subyacentes y aplicar las fórmulas correctamente con las unidades adecuadas. Además, la capacidad de derivar propiedades como el calor latente de vaporización a partir de estas ecuaciones enriquece nuestra comprensión del comportamiento de las sustancias y su aplicación en procesos industriales, donde la gestión precisa de las propiedades del vapor es crucial para la eficiencia y la seguridad. Dominar estos cálculos no solo facilita la resolución de problemas teóricos, sino que también equipa a los profesionales con las herramientas necesarias para optimizar operaciones en el mundo real.
Si quieres conocer otros artículos parecidos a Calculando la Presión de Vapor: Guía Completa puedes visitar la categoría Cálculos.
