30/12/2024
La atmósfera que nos rodea es una mezcla compleja de gases, y uno de sus componentes más dinámicos y esenciales es el vapor de agua. Aunque a menudo invisible, su presencia y concentración tienen un impacto profundo en nuestro clima, en la forma en que cocinamos nuestros alimentos e incluso en procesos industriales. Comprender y calcular la presión de vapor saturado del agua es fundamental para diversas disciplinas, desde la meteorología hasta la ingeniería. En este artículo, desglosaremos qué es exactamente la presión de vapor, por qué alcanza un punto de saturación y cómo podemos calcularla utilizando ecuaciones científicamente probadas y aproximaciones prácticas.
- ¿Qué es la Presión de Vapor Saturado?
- La Relación Fundamental: Temperatura y Presión de Vapor
- El Corazón del Cálculo: La Ecuación de Clausius-Clapeyron
- Una Alternativa Práctica: La Fórmula de Tetens
- Fenómenos Relacionados con la Presión de Vapor
- Cálculos de Alta Precisión: Más Allá de las Aproximaciones
- Preguntas Frecuentes (FAQ)
¿Qué es la Presión de Vapor Saturado?
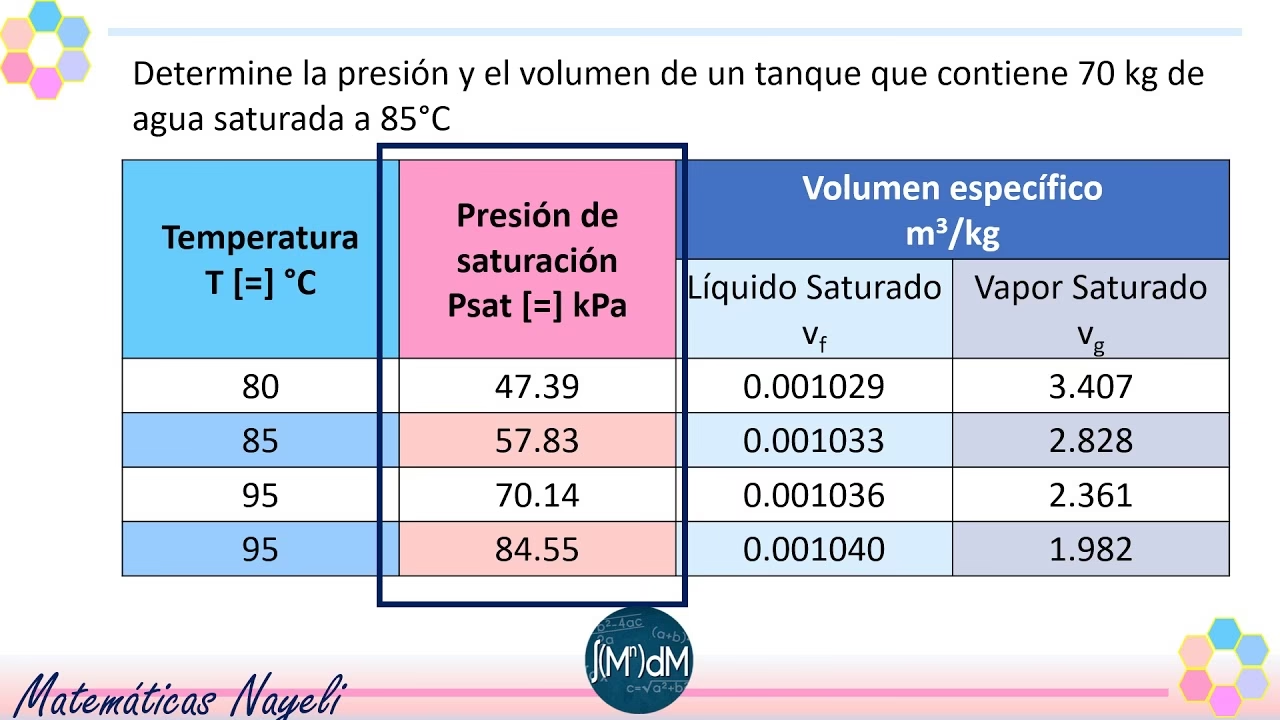
Para entender la presión de vapor saturado, primero debemos diferenciar entre la presión total y la presión parcial. La presión atmosférica total es la suma de las presiones parciales de todos los gases que la componen. Para el vapor de agua, esta presión parcial se denomina simplemente "presión de vapor", denotada como 'e', y se mide comúnmente en kilopascales (kPa).
Los gases en el aire pueden mezclarse en cualquier proporción relativa. Sin embargo, para el vapor de agua, existe una concentración crítica, conocida como humedad de saturación. Cuando la concentración de vapor de agua en el aire supera este valor crítico, el vapor de agua comienza a condensarse más rápidamente de lo que se evapora. Este proceso reduce la concentración de vapor de agua hasta que regresa a ese valor crítico. En este punto, se dice que el aire está saturado, y el vapor de agua se encuentra en equilibrio con el agua líquida. A esta presión de vapor en equilibrio sobre agua pura con una superficie plana la llamamos "presión de vapor saturado", y la representamos como 'es'.
Es frecuente que el aire contenga menos vapor de agua que el valor crítico, en cuyo caso se dice que está insaturado (e < es). Por otro lado, es raro que la presión de vapor supere el valor de saturación en más del 1%. Cuando el aire tiene e > es, se considera sobresaturado. El aire sobresaturado puede ocurrir como una condición transitoria mientras el exceso de vapor de agua se condensa en superficies disponibles, como las partículas de polvo llamadas núcleos de condensación de nubes. Sin embargo, la condensación para formar gotas de nubes ocurre casi instantáneamente.
La Relación Fundamental: Temperatura y Presión de Vapor
Durante el estado de equilibrio (es decir, en la saturación), existe un balance dinámico entre la tasa de evaporación desde el líquido y la tasa de condensación del vapor. La temperatura del agua líquida es el factor principal que controla la tasa de evaporación, mientras que la humedad (la concentración de vapor de agua en el aire) controla la tasa de condensación.
Temperaturas más cálidas del líquido provocan mayores tasas de evaporación, lo que permite que la humedad en el aire aumente hasta que se alcance un nuevo equilibrio. Lo contrario ocurre con temperaturas más frías. Si las temperaturas del aire y del agua líquida son iguales, podemos concluir que el aire más frío tiene una capacidad menor para retener vapor de agua que el aire más cálido. Esta es una observación crucial que explica muchos fenómenos meteorológicos, como la formación de rocío y nubes al enfriarse el aire.
El Corazón del Cálculo: La Ecuación de Clausius-Clapeyron
La relación entre la presión de vapor saturado y la temperatura es una piedra angular en la termodinámica atmosférica. Esta relación se aproxima muy bien mediante la famosa ecuación de Clausius-Clapeyron:
es ≈ eo ⋅ exp [ (L / ℛv) ⋅ (1/To − 1/T) ]
Donde:
- es es la presión de vapor saturado que deseamos calcular (en kPa).
- eo es una presión de vapor de referencia, con un valor de 0.6113 kPa.
- T es la temperatura del aire o del agua, expresada en Kelvin.
- To es una temperatura de referencia, fijada en 273.15 K (0 °C).
- ℛv es la constante de los gases para el vapor de agua, igual a 461 J⋅K−1⋅kg−1.
- L es el parámetro de calor latente. Este valor cambia dependiendo de si la saturación ocurre sobre agua líquida o sobre hielo:
- Para agua líquida (calor latente de vaporización, Lv): Lv = 2.5x106 J⋅kg−1. Esto da una relación Lv/ℛv = 5423 K.
- Para hielo (calor latente de deposición, Ld): Ld = 2.83x106 J⋅kg−1. Esto da una relación Ld/ℛv = 6139 K.
Es crucial recordar que las temperaturas en esta ecuación deben estar en Kelvin. Para convertir grados Celsius a Kelvin, simplemente sume 273.15.
Ejemplo de Aplicación de la Ecuación de Clausius-Clapeyron
Calculemos la presión de vapor saturado del aire a una temperatura de 30°C sobre agua líquida.
Datos:
- T = 30°C. Convertimos a Kelvin: T = 30 + 273.15 = 303.15 K.
- Para agua líquida, Lv/ℛv = 5423 K.
- To = 273.15 K.
- eo = 0.6113 kPa.
Aplicamos la ecuación (4.1a):
es = (0.6113 kPa) ⋅ exp [ (5423 K) ⋅ (1/273.15 K − 1/303.15 K) ]
Primero, calculamos la parte dentro del paréntesis:
(1/273.15) − (1/303.15) ≈ 0.0036611 − 0.0032986 ≈ 0.0003625 K−1
Luego, multiplicamos por Lv/ℛv:
5423 K ⋅ 0.0003625 K−1 ≈ 1.96473
Ahora, calculamos el exponencial:
exp(1.96473) ≈ 7.133
Finalmente, multiplicamos por eo:
es = 0.6113 kPa ⋅ 7.133 ≈ 4.36 kPa
Así, la presión de vapor saturado a 30°C es aproximadamente 4.36 kPa. Esto significa que, a saturación para esta temperatura, la presión parcial del vapor de agua es solo alrededor del 4.3% de la presión atmosférica total (considerando una presión atmosférica estándar de ~101.3 kPa).
Una Alternativa Práctica: La Fórmula de Tetens
Aunque la ecuación de Clausius-Clapeyron es fundamental, el parámetro de calor latente L varía ligeramente con la temperatura. Para tener esto en cuenta y ofrecer una formulación a menudo más conveniente para cálculos directos, se ha sugerido una aproximación diferente conocida como la Fórmula de Tetens para la presión de vapor saturado (es) en función de la temperatura (T, en Kelvin):
es = eo ⋅ exp [ (b ⋅ (T − T1)) / (T − T2) ]
Donde:
- es es la presión de vapor saturado (en kPa).
- eo = 0.6113 kPa.
- b = 17.2694.
- T1 = 273.15 K.
- T2 = 35.86 K.
La Fórmula de Tetens es una aproximación empírica que se ha demostrado muy precisa para un rango común de temperaturas. Las diferencias entre los valores de presión de vapor obtenidos con la Fórmula de Tetens y la ecuación de Clausius-Clapeyron son generalmente muy pequeñas, a menudo menores que otras incertidumbres en las mediciones de temperatura o humedad. Por lo tanto, se puede utilizar cualquiera de las dos ecuaciones con confianza para la mayoría de las aplicaciones prácticas.
Comparación de Fórmulas para la Presión de Vapor Saturado
Para ayudar a visualizar las diferencias y similitudes, aquí hay una tabla comparativa entre las dos principales fórmulas que hemos discutido:
| Característica | Ecuación de Clausius-Clapeyron | Fórmula de Tetens |
|---|---|---|
| Base | Derivación termodinámica fundamental (aproximada) | Empírica, ajustada a datos experimentales |
| Fórmula | es ≈ eo ⋅ exp [ (L/ℛv) ⋅ (1/To − 1/T) ] | es = eo ⋅ exp [ (b ⋅ (T − T1)) / (T − T2) ] |
| Parámetros clave | L (calor latente), ℛv (constante de los gases) | b, T1, T2 (constantes empíricas) |
| Aplicabilidad | Sobre agua líquida o hielo (cambiando L) | Principalmente sobre agua líquida |
| Precisión | Muy buena aproximación, base teórica sólida | Muy buena aproximación en rangos comunes, práctica |
| Uso común | Estudios teóricos, modelado atmosférico | Aplicaciones prácticas, cálculos rápidos |
Fenómenos Relacionados con la Presión de Vapor
Agua Sobreenfriada
En la atmósfera, es posible que el agua líquida permanezca sin congelar a temperaturas muy por debajo de 0°C, incluso hasta -40°C. Esta agua fría y no congelada se conoce como agua sobreenfriada. Las ecuaciones de presión de vapor saturado, como la de Clausius-Clapeyron, también pueden calcular la presión de vapor sobre superficies de hielo. Curiosamente, existe una diferencia notable entre los valores de saturación de vapor de agua sobre agua líquida sobreenfriada y sobre hielo a la misma temperatura, lo que tiene implicaciones importantes para la formación de nubes y precipitaciones en atmósferas frías.
Punto de Rocío
La ecuación de Clausius-Clapeyron no solo describe la presión de vapor saturado, sino que también puede describir la relación entre la presión de vapor real (insaturada) 'e' y la temperatura del punto de rocío (Td), que es la temperatura a la cual el aire se saturaría si se enfriara sin cambiar su contenido de humedad:
e = eo ⋅ exp [ (L / ℛv) ⋅ (1/To − 1/Td) ]
Donde Td es la temperatura del punto de rocío. Esta fórmula es vital para los higrómetros y para predecir la condensación y la formación de niebla.
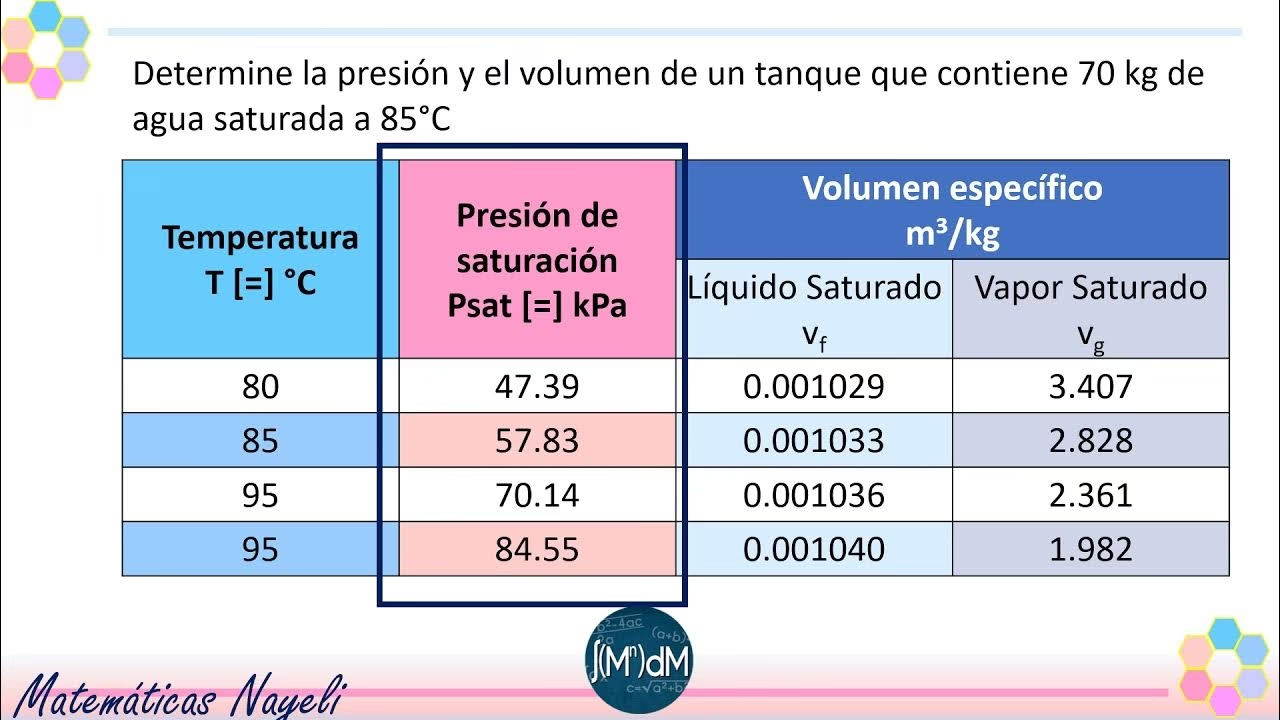
Punto de Ebullición y Altitud
Un líquido hierve cuando su presión de vapor saturado (es) iguala la presión ambiente (P) de la atmósfera circundante: P = es. Dado que la presión atmosférica disminuye exponencialmente con el aumento de la altitud, esto tiene una consecuencia directa sobre el punto de ebullición del agua.
A medida que ascendemos, la presión atmosférica es menor, lo que significa que el agua necesita alcanzar una presión de vapor saturado más baja para igualar la presión ambiente y, por lo tanto, hierve a una temperatura más baja. Por ejemplo, el punto de ebullición del agua disminuye aproximadamente 3.4°C por cada kilómetro de altitud. A 2 km de altitud, el agua hierve a unos 93.2°C, en lugar de los 100°C a nivel del mar.
Esto tiene implicaciones prácticas significativas para la cocina. Para ablandar verduras a la ternura deseada o preparar carnes al punto correcto, los alimentos deben cocinarse a una cierta temperatura durante una duración específica. Temperaturas de cocción ligeramente más bajas deben compensarse con tiempos de cocción ligeramente más largos. Por lo tanto, en altitudes elevadas, necesitará cocinar los alimentos hervidos durante más tiempo, ya que el agua hierve a una temperatura inferior.
Cálculos de Alta Precisión: Más Allá de las Aproximaciones
Si bien las ecuaciones de Clausius-Clapeyron y Tetens son excelentes aproximaciones, para aplicaciones científicas y de ingeniería que requieren la máxima precisión, como el establecimiento de estándares de humedad, la calibración de higrómetros o la tecnología de energía de vapor, se utilizan formulaciones más complejas. Estas formulaciones se basan en datos calorimétricos precisos y en la consideración de cómo el vapor de agua se desvía del comportamiento de un gas ideal.
Investigadores como H. F. Stimson, y las formulaciones de Goff y Gratch, han dedicado esfuerzos significativos a obtener mediciones extremadamente precisas de la presión de vapor del agua. Estas formulaciones de alta precisión (como las ecuaciones 16, 17 y 18 mencionadas en la literatura científica) parten de una versión modificada de la ecuación de Clausius-Clapeyron e incorporan "coeficientes viriales" para tener en cuenta las interacciones moleculares del vapor de agua. El proceso implica integraciones complejas y el ajuste de polinomios a vastos conjuntos de datos experimentales, resultando en ecuaciones con múltiples coeficientes ajustados para proporcionar una concordancia de hasta unas pocas partes por millón con las mediciones más precisas. Aunque estas ecuaciones son computacionalmente más intensivas, su exactitud es indispensable en campos donde la más mínima variación puede tener consecuencias críticas.
Preguntas Frecuentes (FAQ)
¿Por qué es importante calcular la presión de vapor saturado del agua?
Es crucial para entender y predecir fenómenos meteorológicos como la formación de nubes, niebla y precipitaciones. También es vital en ingeniería para el diseño de sistemas de aire acondicionado, procesos industriales que involucran vapor, y en la ciencia para la calibración de instrumentos de humedad y estudios termodinámicos.
¿Cuál es la diferencia entre vapor de agua y humedad?
El vapor de agua es el agua en su estado gaseoso. La humedad se refiere a la cantidad de vapor de agua presente en el aire. La presión de vapor es una medida de esa cantidad, mientras que la presión de vapor saturado es la cantidad máxima de vapor de agua que el aire puede contener a una temperatura dada antes de que comience a condensarse.
¿Qué factores afectan la presión de vapor saturado?
El factor más significativo que afecta la presión de vapor saturado es la temperatura. A temperaturas más altas, las moléculas de agua tienen más energía y pueden escapar más fácilmente de la superficie líquida, lo que resulta en una mayor presión de vapor saturado.
¿Se puede calcular la presión de vapor para el hielo?
Sí, la ecuación de Clausius-Clapeyron (y otras más avanzadas) pueden utilizarse para calcular la presión de vapor saturado sobre una superficie de hielo. La principal diferencia es el valor del calor latente utilizado en la ecuación, que es el calor latente de deposición para el hielo en lugar del calor latente de vaporización para el agua líquida.
¿Cómo se relaciona la presión de vapor con el clima?
La presión de vapor es un componente clave del ciclo del agua. Determina la cantidad de humedad en el aire, lo que influye directamente en la formación de nubes, la precipitación y la transferencia de calor en la atmósfera. Un aire más cálido puede contener más vapor de agua, y cuando este aire se enfría, el exceso de vapor se condensa, liberando calor latente y contribuyendo a la energía de los sistemas climáticos.
En resumen, el cálculo de la presión de vapor saturado del agua es una herramienta poderosa para comprender la interacción entre el agua y la atmósfera. Desde las aproximaciones fundamentales de Clausius-Clapeyron y Tetens hasta las formulaciones de alta precisión utilizadas en la investigación avanzada, cada método ofrece una ventana a la forma en que la temperatura y la humedad dan forma a nuestro mundo. Ya sea que esté prediciendo el clima, diseñando un sistema de humidificación o simplemente cocinando a gran altitud, la comprensión de estos principios es invaluable.
Si quieres conocer otros artículos parecidos a Calculando la Presión de Vapor Saturado del Agua puedes visitar la categoría Calculadoras.

