10/05/2026
Las máquinas térmicas son dispositivos ingeniosos que transforman la energía calorífica en trabajo mecánico, una proeza que ha impulsado gran parte de nuestra civilización, desde los motores de un automóvil hasta las vastas centrales eléctricas que iluminan nuestras ciudades. Comprender cómo se calcula su potencia y, más importante aún, su eficiencia, es fundamental para optimizar su rendimiento y abordar los desafíos energéticos actuales. En este artículo, desentrañaremos los principios que rigen estas máquinas, desde sus componentes básicos hasta el ideal teórico del Ciclo de Carnot, explorando cómo la física establece los límites de lo que es posible transformar.
¿Qué es una Máquina Térmica y Cómo Funciona?
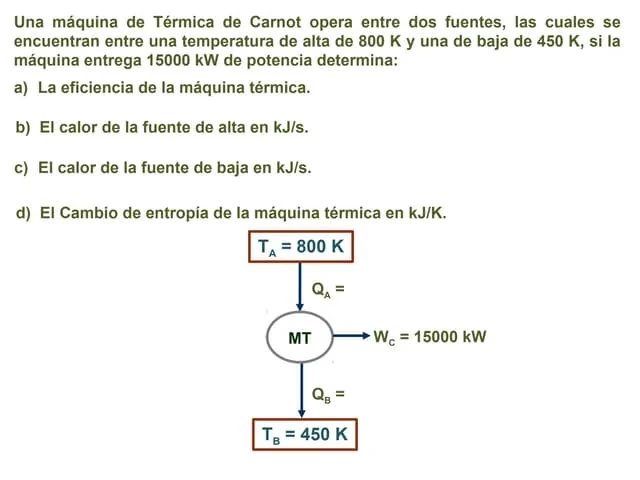
En esencia, una máquina térmica es un sistema diseñado para extraer calor de una fuente de alta temperatura, conocida como reservorio caliente, utilizar una parte de esa energía para realizar un trabajo útil y desechar el calor restante en un reservorio de baja temperatura, denominado reservorio frío o disipador de calor. Imagina una locomotora de vapor antigua: el carbón calienta el agua (reservorio caliente), el vapor generado mueve los pistones (trabajo mecánico), y el vapor condensado o el calor residual se libera a la atmósfera (reservorio frío).
Los componentes clave de una máquina térmica incluyen:
- Fuente de Calor (Reservorio Caliente): Suministra el calor (Qh) a una temperatura Th.
- Sustancia de Trabajo: Un fluido (como gas o vapor) que experimenta cambios de estado y volumen para realizar trabajo.
- Disipador de Calor (Reservorio Frío): Recibe el calor (Qc) a una temperatura Tc.
- Mecanismo de Trabajo: Los componentes que convierten la energía de la sustancia de trabajo en trabajo mecánico (ej., pistones, turbinas).
El funcionamiento de una máquina térmica se basa en un proceso cíclico. Esto significa que la sustancia de trabajo regresa a su estado inicial después de cada ciclo. Según la Primera Ley de la Termodinámica, que es una declaración de la conservación de la energía, la variación de la energía interna de un sistema en un ciclo completo es cero (ΔEint = 0). Esto implica que el trabajo neto (W) realizado por la máquina es igual a la diferencia entre el calor absorbido del reservorio caliente (Qh) y el calor cedido al reservorio frío (Qc):
W = Qh - Qc
Esta ecuación es fundamental para entender el balance energético de cualquier máquina térmica.
La Eficiencia de una Máquina Térmica: ¿Cuánto Podemos Aprovechar?
La eficiencia (e) es la medida más crítica del rendimiento de una máquina térmica. Nos dice qué porcentaje del calor absorbido del reservorio caliente se convierte realmente en trabajo útil. Se define como la relación entre el trabajo producido (lo que "sacamos") y el calor absorbido (lo que "metemos") en cada ciclo:
e = W / Qh
Sustituyendo la expresión de W de la Primera Ley (W = Qh - Qc), obtenemos otra forma de calcular la eficiencia:
e = (Qh - Qc) / Qh = 1 - Qc / Qh
Por ejemplo, si una máquina absorbe 100 unidades de calor y realiza 30 unidades de trabajo, su eficiencia es del 30%. El 70% restante se desecha como calor residual al reservorio frío. Es importante destacar que, debido a la Segunda Ley de la Termodinámica, ninguna máquina térmica puede tener una eficiencia del 100%. Siempre habrá una cantidad de calor que deba ser desechada.
El Ciclo de Carnot: El Estándar de Oro de la Eficiencia
El Ciclo de Carnot es un ciclo termodinámico ideal y reversible que representa el límite superior teórico de la eficiencia para cualquier máquina térmica que opere entre dos temperaturas dadas. Fue propuesto por Sadi Carnot en 1824 y es crucial para comprender los límites fundamentales de la conversión de energía térmica en trabajo.
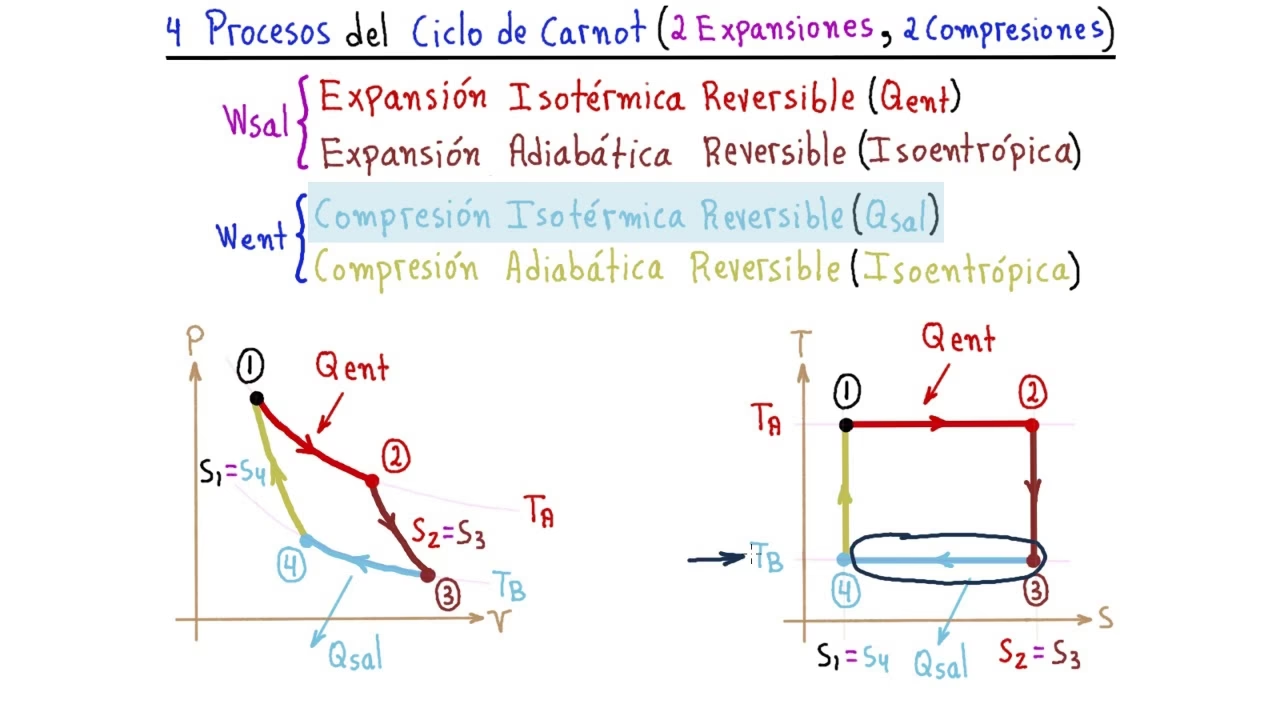
Este ciclo consta de cuatro procesos reversibles:
- Expansión Isoterma (A → B): La sustancia de trabajo absorbe calor (Qh) del reservorio caliente (a temperatura Th) y se expande, realizando trabajo. La temperatura se mantiene constante, por lo que la energía interna no cambia (ΔU = 0). Todo el calor absorbido se convierte en trabajo. La entropía del sistema aumenta.
- Expansión Adiabática (B → C): La sustancia de trabajo se aísla térmicamente y continúa expandiéndose. Al no haber intercambio de calor (Q = 0), la sustancia se enfría y su energía interna disminuye, realizando trabajo. La entropía se mantiene constante.
- Compresión Isoterma (C → D): La sustancia de trabajo se pone en contacto con el reservorio frío (a temperatura Tc) y se comprime, cediendo calor (Qc) a este. La temperatura se mantiene constante, por lo que la energía interna no cambia (ΔU = 0). Se realiza trabajo sobre el sistema. La entropía del sistema disminuye.
- Compresión Adiabática (D → A): La sustancia de trabajo se aísla térmicamente y se comprime hasta su estado inicial. Al no haber intercambio de calor (Q = 0), la sustancia se calienta, su energía interna aumenta, y se realiza trabajo sobre el sistema. La entropía se mantiene constante.
Para un gas ideal que sigue el Ciclo de Carnot, la eficiencia (η) se puede expresar de manera sorprendentemente simple, dependiendo solo de las temperaturas absolutas (en Kelvin) de los reservorios caliente (Th) y frío (Tc):
ηCarnot = 1 - Tc / Th
Esta es la Fórmula de Carnot. Cuanto mayor sea la diferencia de temperatura entre los reservorios, mayor será la eficiencia máxima posible. Si Tc fuera 0 K (cero absoluto), la eficiencia sería del 100%, pero el cero absoluto es inalcanzable.
Teoremas de Carnot: Implicaciones Fundamentales
Los teoremas de Carnot establecen dos principios cruciales sobre el rendimiento de las máquinas térmicas:
- Primer Teorema: Ninguna máquina térmica real que opere entre dos reservorios de calor dados puede tener una eficiencia mayor que una máquina de Carnot que opere entre los mismos reservorios. Esto significa que el ciclo de Carnot establece un límite superior inquebrantable para la eficiencia.
- Segundo Teorema: Todas las máquinas de Carnot (o máquinas térmicas reversibles) que operan entre los mismos dos reservorios de calor tienen la misma eficiencia, independientemente de la sustancia de trabajo o de los detalles de su construcción. Esto subraya que la eficiencia máxima solo depende de las temperaturas de los reservorios.
Cálculo de la Potencia de una Máquina Térmica
Mientras que la eficiencia nos dice qué tan bien una máquina convierte el calor en trabajo, la potencia (P) nos indica la rapidez con la que lo hace. La potencia es el trabajo realizado por unidad de tiempo. Si W es el trabajo realizado por la máquina en un ciclo y Δt es el tiempo que tarda en completar ese ciclo, entonces la potencia promedio es:
P = W / Δt
Para calcular la potencia, primero necesitamos determinar el trabajo realizado por ciclo (W) y luego dividirlo por la duración de ese ciclo. Si conocemos la eficiencia (e) de la máquina y el calor absorbido por ciclo (Qh), podemos usar la relación W = e * Qh. Así, la potencia también se puede expresar como:
P = (e * Qh) / Δt
O, si conocemos la tasa de absorción de calor (potencia térmica de entrada, Q̇h = Qh / Δt):
P = e * Q̇h
Esto significa que una máquina puede tener una alta eficiencia (e) pero una baja potencia si realiza poco trabajo por ciclo o si sus ciclos son muy lentos. Por el contrario, una máquina puede tener una eficiencia moderada pero una alta potencia si procesa grandes cantidades de calor rápidamente.
¿Cómo se calcula Qh (Calor Absorbido)?
Para una máquina térmica general, Qh es simplemente la cantidad total de calor que la sustancia de trabajo absorbe del reservorio caliente durante un ciclo. En el contexto del ciclo de Carnot con un gas ideal, Qh ocurre durante la expansión isoterma (A → B) y se calcula como:
Qh = n R Th ln(VB / VA)
Donde:
- n es el número de moles del gas.
- R es la constante de los gases ideales.
- Th es la temperatura del reservorio caliente (en Kelvin).
- VB es el volumen final de la expansión isoterma.
- VA es el volumen inicial de la expansión isoterma.
Para máquinas reales, el calor Qh se mide o se calcula a partir de las propiedades del combustible y el flujo másico. Por ejemplo, en una central eléctrica, Qh estaría relacionado con la energía liberada por la combustión de carbón o gas, o por la fisión nuclear, que luego se transfiere al vapor de agua.
Máquinas Térmicas Reales vs. Ideales
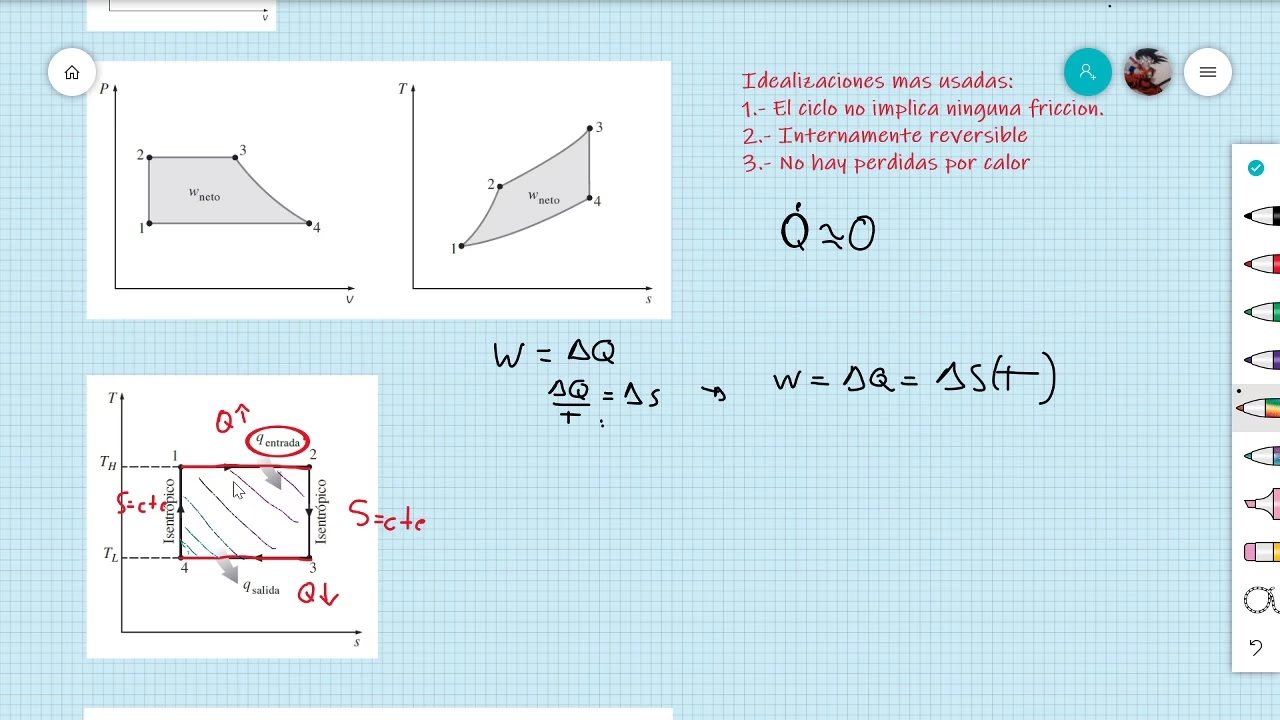
Es crucial entender que el Ciclo de Carnot es un modelo ideal. Las máquinas térmicas reales siempre operan con una eficiencia menor que la predicha por la Fórmula de Carnot. Esto se debe a las irreversibilidades inherentes a cualquier proceso real:
- Fricción: Las partes móviles de una máquina generan fricción, lo que disipa energía en forma de calor y reduce el trabajo útil.
- Transferencia de Calor a Través de Diferencias Finitas de Temperatura: En un ciclo real, la transferencia de calor no ocurre de manera isotérmica perfecta; siempre hay un gradiente de temperatura, lo que aumenta la entropía y reduce la eficiencia.
- Pérdidas de Calor al Entorno: Las máquinas no están perfectamente aisladas, lo que resulta en pérdidas de calor al ambiente que no contribuyen al trabajo.
- Procesos no Cuasiestáticos: Los procesos en las máquinas reales ocurren a velocidades finitas, lo que significa que el sistema no está siempre en equilibrio termodinámico, generando irreversibilidades.
- Propiedades No Ideales de la Sustancia de Trabajo: Los gases y fluidos reales no siempre se comportan como gases ideales, lo que introduce desviaciones de las ecuaciones teóricas.
Estos factores hacen que el trabajo real (Wreal) sea siempre menor que el trabajo ideal (Wideal) para la misma cantidad de calor absorbido, o que el calor cedido (Qc,real) sea mayor. Por lo tanto, la eficiencia real (ereal) es siempre menor que la eficiencia de Carnot (ηCarnot):
ereal < ηCarnot
Tabla Comparativa: Ciclo de Carnot vs. Máquina Térmica Real
| Característica | Ciclo de Carnot (Ideal) | Máquina Térmica Real |
|---|---|---|
| Reversibilidad | Completamente reversible | Irreversible (debido a fricción, transferencia de calor finita, etc.) |
| Eficiencia | Máxima posible (η = 1 - Tc/Th) | Siempre menor que la de Carnot (e < ηCarnot) |
| Transferencia de Calor | Isotérmica (a Th y Tc) y Adiabática | Con gradientes de temperatura, pérdidas al entorno |
| Fricción | Nula | Presente en componentes móviles |
| Realidad Práctica | Teórico, no construible en la práctica | Dispositivos funcionales (motores, turbinas, etc.) |
Preguntas Frecuentes sobre Máquinas Térmicas
¿Por qué la eficiencia de una máquina térmica nunca es del 100%?
La eficiencia de una máquina térmica nunca puede ser del 100% debido a la Segunda Ley de la Termodinámica. Esta ley establece que es imposible construir una máquina que opere en un ciclo y cuyo único efecto sea la absorción de calor de un reservorio y la producción equivalente de trabajo. Siempre debe haber una expulsión de calor a un reservorio frío. En otras palabras, la energía térmica no puede convertirse completamente en trabajo sin que parte de ella se disipe como calor residual.
¿Qué es un reservorio térmico?
Un reservorio térmico (o fuente de calor/sumidero de calor) es un cuerpo de masa tan grande que puede absorber o ceder una cantidad arbitraria de calor sin que su temperatura cambie apreciablemente. Ejemplos de reservorios calientes son una caldera en una central eléctrica, el sol o una reacción nuclear. Ejemplos de reservorios fríos son la atmósfera, un río o un lago.
¿Se puede usar cualquier sustancia como "sustancia de trabajo"?
Teóricamente, sí, cualquier sustancia que pueda sufrir cambios de estado o volumen en respuesta a la absorción y liberación de calor puede usarse como sustancia de trabajo. Sin embargo, en la práctica, se eligen sustancias con propiedades termodinámicas específicas que optimizan el rendimiento y la viabilidad de la máquina, como el agua (vapor) en las turbinas, mezclas de aire y combustible en motores de combustión interna, o refrigerantes en bombas de calor.

¿Cómo se mide la temperatura para la fórmula de Carnot?
Las temperaturas Th y Tc en la fórmula de Carnot (η = 1 - Tc / Th) deben expresarse en una escala de temperatura absoluta, como la escala Kelvin (K). Es incorrecto usar grados Celsius o Fahrenheit, ya que estas escalas tienen puntos cero arbitrarios que distorsionan la relación. La escala Kelvin se basa en el cero absoluto, donde la energía térmica es mínima.
¿Qué diferencia hay entre potencia y eficiencia?
La eficiencia es una medida de la calidad de la conversión de energía: qué proporción del calor de entrada se convierte en trabajo útil. Es una proporción sin unidades (o en porcentaje). La potencia, por otro lado, es una medida de la tasa a la que se realiza el trabajo, es decir, la cantidad de trabajo por unidad de tiempo. Se mide en vatios (W) o caballos de fuerza (hp). Una máquina puede ser muy eficiente pero lenta (baja potencia), o muy potente pero poco eficiente, aunque el objetivo de la ingeniería es lograr un equilibrio óptimo entre ambas.
En resumen, las máquinas térmicas son pilares de nuestra infraestructura energética. Aunque el ideal del Ciclo de Carnot nos muestra la máxima eficiencia teórica, las máquinas reales enfrentan limitaciones debido a las irreversibilidades. Comprender estos principios nos permite diseñar sistemas más eficientes y potentes, avanzando hacia un futuro energético más sostenible.
Si quieres conocer otros artículos parecidos a Cómo Calcular la Potencia de una Máquina Térmica puedes visitar la categoría Cálculos.
