24/09/2025
El pH es un concepto fundamental en la química que nos permite clasificar las soluciones como ácidas, básicas o neutras. Sin embargo, su influencia se extiende mucho más allá de una simple etiqueta, jugando un papel crítico en fenómenos complejos a escala nanométrica. Aunque comúnmente se asocia con la acidez o alcalinidad de una sustancia, recientes investigaciones revelan su impacto sorprendente en la dinámica y el comportamiento de las nanopartículas en entornos acuosos. Este artículo explorará la relación entre el pH y la movilidad de las nanogotas, desentrañando por qué, en algunos casos, un cambio en el pH puede alterar drásticamente su movimiento sin modificar su carga superficial, un hallazgo que desafía las explicaciones clásicas y nos invita a reconsiderar nuestra comprensión de las interacciones moleculares.
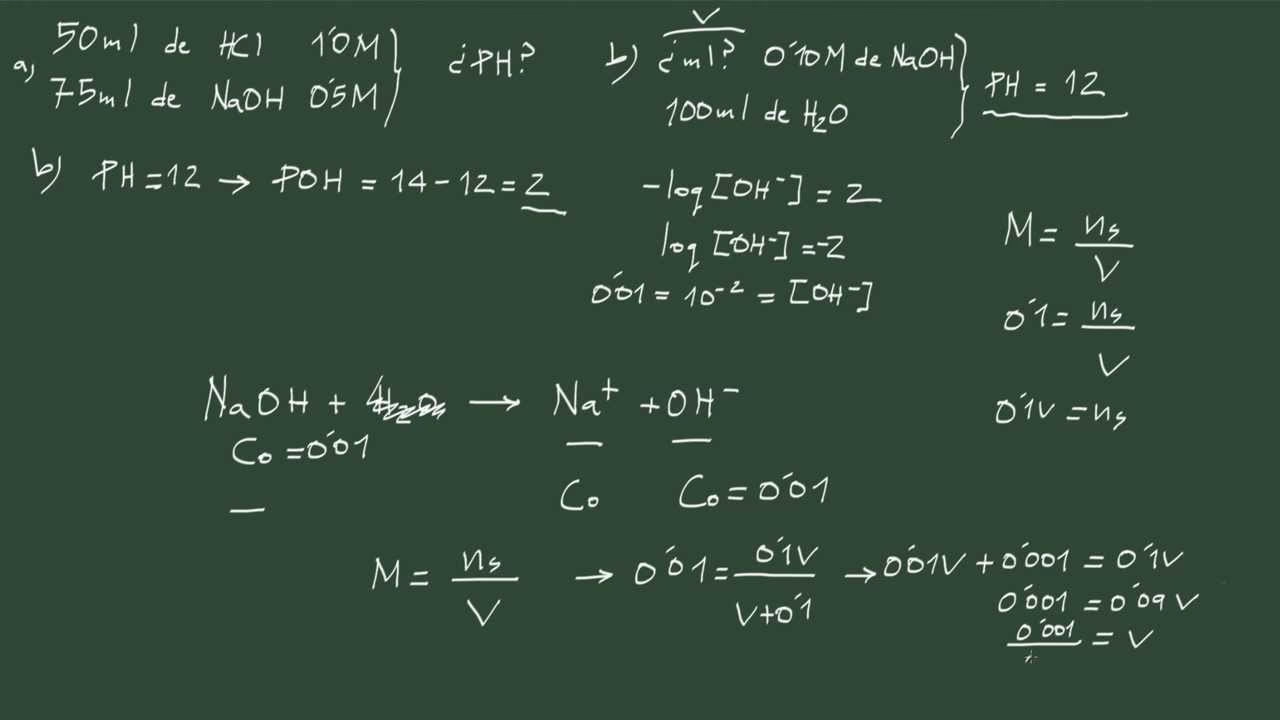
Entendiendo el pH: Conceptos Básicos y Cálculo
Antes de sumergirnos en las complejidades de la nanodinámica, es esencial refrescar los fundamentos del pH. El pH es una medida de la concentración de iones de hidrógeno (H+) en una solución acuosa, indicando su grado de acidez o basicidad. La escala de pH va de 0 a 14: un valor de 7 es neutro, valores menores a 7 indican acidez, y valores mayores a 7 indican basicidad (alcalinidad).
La relación entre el pH y la concentración de iones de hidrógeno se define mediante la siguiente fórmula:
pH = -log₁₀[H+]
Donde [H+] representa la concentración molar de iones de hidrógeno en moles por litro (M). Es importante recordar que esta concentración se refiere a la molaridad. Si se proporciona la concentración en otras unidades, como porcentaje en masa o molalidad, debe convertirse a molaridad antes de aplicar la fórmula.
De manera inversa, si conocemos el pH de una solución y queremos determinar la concentración de iones de hidrógeno, podemos usar la siguiente relación:
[H+] = 10⁻pH
Además, el pH está intrínsecamente relacionado con el pOH (medida de la concentración de iones hidróxido, OH-) en soluciones acuosas a 25°C, mediante la constante de disociación del agua (Kw = 1x10⁻¹⁴):
pH + pOH = 14
Esta última relación es particularmente útil cuando se trabaja con soluciones básicas, ya que a menudo se calcula primero el pOH a partir de la concentración de OH- y luego se deriva el pH.
Ejemplos de Cálculo de pH
Para ilustrar cómo se realizan estos cálculos, consideremos algunos ejemplos prácticos:
- Ejemplo 1: Calcular el pH dada la [H+]
Si la concentración de iones de hidrógeno es[H+] = 1.4 x 10⁻⁵ M, el pH se calcula como:pH = -log₁₀(1.4 x 10⁻⁵) = 4.85 - Ejemplo 2: Calcular [H+] dado el pH
Si el pH de una solución es8.5, la concentración de iones de hidrógeno es:[H+] = 10⁻⁸.⁵ = 3.2 x 10⁻⁹ M - Ejemplo 3: pH de una solución de ácido fuerte
Calcular el pH de una solución de0.03 Mde ácido clorhídrico (HCl). Dado que el HCl es un ácido fuerte, se disocia completamente en agua en una proporción 1:1, lo que significa que[H+] = 0.03 M.pH = -log₁₀(0.03) = 1.52
Al realizar estos cálculos, siempre es recomendable verificar que el resultado tenga sentido: un pH bajo (entre 1 y 3) para ácidos fuertes y un pH alto (entre 11 y 13) para bases fuertes. Aunque teóricamente es posible, en la práctica los valores de pH suelen encontrarse entre 0 y 14.
pH y la Movilidad Electrocinética de Nanogotas
La movilidad electrocinética de partículas pequeñas en un líquido, como las nanogotas de aceite en agua, es un fenómeno crucial en campos como la ciencia de materiales, la biología y la medicina. Cuando estas gotas se exponen a un campo electrostático, se mueven hacia un electrodo con una velocidad determinada, lo que se describe por su movilidad (μ = v/E). Esta movilidad se convierte clásicamente en un potencial zeta (ζ-potential), interpretado como el potencial electrostático cercano a la superficie de la partícula debido a la presencia de iones o grupos cargados.
Un estudio con nanogotas de hexadecano en agua reveló un comportamiento fascinante: al reemplazar iones Cl- por iones OH- (es decir, aumentar el pH de neutro a 11), la magnitud de la movilidad y el potencial zeta de las gotas aumentaron significativamente (aproximadamente 2.2 veces). Este aumento drástico de la movilidad, dependiente del pH, concuerda con experimentos previos que mostraban un incremento del potencial zeta al aumentar el pH.
La Sorprendente Verdad: Carga Superficial Independiente del pH
A pesar del notable aumento en la movilidad y el potencial zeta con el pH, la investigación ha revelado un hallazgo contraintuitivo: la carga superficial real de las nanogotas de aceite permanece prácticamente inalterada. Esto se determinó utilizando métodos ópticos avanzados como la Dispersión de Segundo Armónico (SHS) y la Espectroscopia de Dispersión de Frecuencia de Suma Vibracional (SFS).
El SHS es una técnica extremadamente sensible a las interfaces, capaz de detectar moléculas orientadas anisotrópicamente, como las moléculas de agua en la superficie de una gota. Mediante SHS, se determinó que el potencial superficial (Φ₀) de las gotas de aceite no cambiaba cuando se aumentaba el pH de neutro a 11 (reemplazando NaCl por NaOH). Las mediciones de SHS para las gotas en soluciones de NaCl y NaOH fueron indistinguibles, lo que indica que las propiedades interfaciales, incluyendo la densidad de carga superficial, no se modifican con el pH.
De manera similar, la espectroscopia SFS, que es sensible a la estructura de los enlaces de hidrógeno y a la conformación de las cadenas de hidrocarburos en la interfaz, mostró que la red de enlaces de hidrógeno interfacial y la cantidad de transferencia de carga entre el agua y el aceite tampoco dependían del pH. Los espectros de SFS en las regiones de estiramiento O-D (agua interfacial) y C-H (aceite interfacial) fueron idénticos para soluciones con pH neutro y pH 11. Esto sugiere que los iones OH- y Cl- tienen un impacto idéntico en la red de enlaces de hidrógeno interfacial y que no hay diferencias inducidas por el pH en esta estructura.
Estos resultados desafían la explicación tradicional de que un cambio drástico en la movilidad/potencial zeta se deriva de cambios en la densidad de carga iónica superficial o en la distribución de iones en la doble capa eléctrica. Si la carga superficial no cambia, ¿qué explica el aumento de la movilidad?
El Mecanismo Clave: Polarización Electrónica y el Efecto Grotthuss
La explicación a esta aparente paradoja reside en las propiedades electrónicas y la dinámica de transporte de carga en la solución a granel, más que en la superficie de la gota. La investigación sugiere que dos factores principales contribuyen al aumento de la movilidad sin un cambio en la carga superficial:
1. Polarización Electrónica Inducida por Campo Eléctrico
A nivel cuántico, un campo eléctrico externo induce una polarización electrónica significativa en las moléculas hidrofóbicas en el agua. Simulaciones de dinámica molecular ab initio (AIMD) mostraron que un campo eléctrico aplicado provoca una asimetría considerable en el potencial eléctrico a través de una molécula hidrofóbica (como el neopentano), lo que resulta en una polarización electrónica. Esta polarización, que no está incluida en las descripciones clásicas del flujo hidrodinámico, puede generar un gradiente de energía y, por lo tanto, una fuerza que impulsa el movimiento de la molécula.
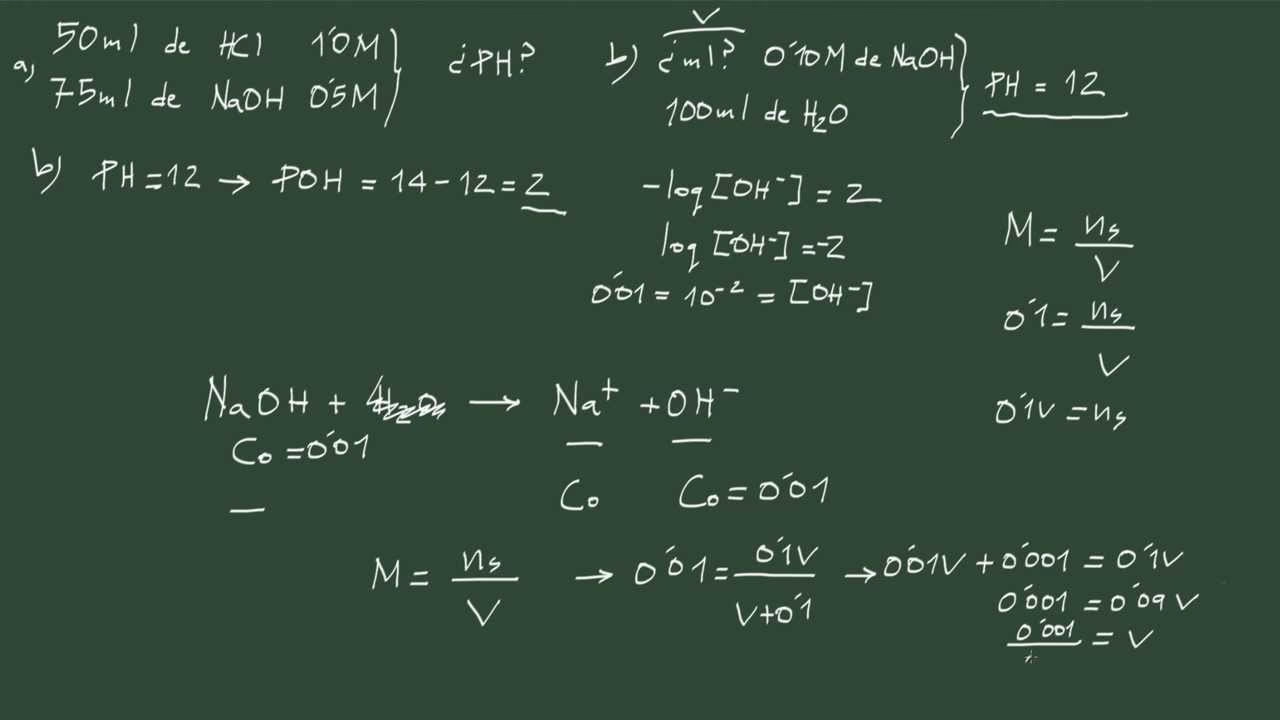
La interacción entre las fluctuaciones de polarización y el campo eléctrico externo genera corrientes locales y realiza trabajo electrodinámico, lo que explica la deriva de las moléculas hidrofóbicas. Las simulaciones lograron predecir una movilidad y un potencial zeta para el neopentano que están en buena concordancia con los valores experimentales observados para las nanogotas de aceite.
2. El Mecanismo de Grotthuss y la Conducción de Carga en Soluciones Básicas
La diferencia fundamental en la movilidad de las gotas entre soluciones salinas y básicas se atribuye al mecanismo de transporte de carga de los iones OH- en comparación con los iones Cl-. Los iones Cl- se hidratan simétricamente y se mueven por flujo hidrodinámico. En contraste, los iones OH- están solvatados asimétricamente y actúan como defectos topológicos en la red de enlaces de hidrógeno del agua. Gracias a esta estructura, la red de enlaces de hidrógeno se convierte en un conducto mucho más eficiente para el transporte de carga a través del mecanismo de Grotthuss.
El mecanismo de Grotthuss implica que los protones se mueven a través de la red de enlaces de hidrógeno mediante la interconversión de enlaces covalentes y enlaces de hidrógeno, lo que permite una transferencia de carga mucho más rápida que el movimiento físico de los iones. Como resultado, las soluciones diluidas de OH- conducen la carga aproximadamente el doble de rápido que las soluciones diluidas de Cl-, incluso si la constante dieléctrica y la viscosidad de ambas soluciones son idénticas.
Cuando se aplica un campo electrostático, la densidad de corriente es proporcional a la conductividad de la solución. Dado que las soluciones básicas (con OH-) son más conductoras debido al mecanismo de Grotthuss, la polarización de la solución a granel es mayor. Esta mayor polarización de la solución, combinada con la polarización electrónica inducida en las propias nanogotas, resulta en una fuerza electrodinámica neta más grande sobre las cargas negativas de la gota, lo que lleva a una mayor movilidad. Es decir, si las cargas en el medio se mueven el doble de rápido, la gota también lo hace.
Implicaciones y Futuras Investigaciones
Este descubrimiento de que la movilidad de las nanogotas de aceite es significativamente influenciada por el pH, no por cambios en la carga superficial sino por las propiedades de polarización electrónica y el transporte de carga del medio circundante (especialmente el mecanismo de Grotthuss), tiene profundas implicaciones. Desafía las interpretaciones clásicas del potencial zeta y abre nuevas vías para comprender y manipular el comportamiento de las nanopartículas en diversos entornos. La capacidad de controlar la movilidad de las nanopartículas sin alterar su química superficial podría ser crucial para aplicaciones en la administración de fármacos, la catálisis, la nanofabricación y la separación de materiales. Se requiere más investigación para desentrañar completamente los mecanismos moleculares exactos por los cuales el mecanismo de Grotthuss facilita un movimiento más rápido de las nanogotas de aceite.
Preguntas Frecuentes
Aquí abordamos algunas preguntas comunes para consolidar la comprensión de estos conceptos:
¿Qué es el pH y por qué es importante?
El pH es una escala logarítmica que mide la acidez o basicidad de una solución acuosa, basada en la concentración de iones de hidrógeno. Es crucial en química, biología y diversas industrias porque influye en la velocidad de las reacciones químicas, la solubilidad de las sustancias, la estabilidad de las proteínas y el comportamiento de los materiales, incluyendo las nanopartículas.
¿Cómo se calcula el valor del pH?
El pH se calcula tomando el logaritmo negativo en base 10 de la concentración molar de iones de hidrógeno ([H+]). La fórmula es pH = -log₁₀[H+]. Para concentraciones dadas en otras unidades, primero se deben convertir a molaridad (moles por litro).
¿El pH se relaciona con la densidad de una solución?
Aunque el texto proporcionado no establece una relación directa entre el pH y la densidad en el contexto de la movilidad de las nanogotas, es importante señalar que el pH puede afectar indirectamente la densidad de una solución. Por ejemplo, al añadir un ácido o una base a una solución, se introduce una nueva cantidad de soluto (iones H+, OH-, o las especies que los generan, como NaCl o NaOH). Estos solutos tienen masa y volumen, y su concentración puede cambiar la densidad total de la solución. Sin embargo, en el estudio científico discutido, el enfoque principal está en las interacciones electrónicas y la dinámica de transporte de carga, no en los cambios macroscópicos de densidad como el factor dominante para la movilidad observada.
¿Por qué la movilidad de las nanogotas depende del pH si su carga superficial no cambia?
La investigación actual sugiere que la dependencia de la movilidad del pH no se debe a un cambio en la densidad de carga iónica en la superficie de la gota. En cambio, se atribuye a dos factores principales: la polarización electrónica inducida por el campo eléctrico en las propias nanogotas y, más significativamente, las propiedades de transporte de carga de la solución a granel. En soluciones básicas, los iones hidróxido (OH-) utilizan el mecanismo de Grotthuss para una transferencia de carga mucho más eficiente a través de la red de enlaces de hidrógeno del agua, lo que hace que la solución sea más conductora. Esta mayor conductividad y polarización del medio circundante, combinada con la polarización de la gota, resulta en una fuerza electrodinámica mayor sobre la gota, aumentando su movilidad.
¿Qué es el mecanismo de Grotthuss?
El mecanismo de Grotthuss es un proceso de transporte de protones en soluciones acuosas (y otras redes de enlaces de hidrógeno) donde los protones se mueven a través de la red de enlaces de hidrógeno del agua mediante una serie de saltos y reordenamientos de enlaces covalentes y de hidrógeno, en lugar del movimiento físico de iones individuales. Este mecanismo permite una conductividad protónica excepcionalmente rápida, especialmente relevante para iones como el OH- y el H+.
Si quieres conocer otros artículos parecidos a pH y la Fascinante Danza de las Nanopartículas puedes visitar la categoría Química.
