09/04/2025
El pH, una medida aparentemente simple, es en realidad un indicador fundamental que nos revela la acidez o alcalinidad de una sustancia. Desde la calidad del agua que bebemos o utilizamos en la industria, hasta la salud de las plantas en nuestro jardín, comprender y medir el pH es de vital importancia. Pero, ¿qué es exactamente el pH y cómo podemos desentrañar este valor que influye en tantos aspectos de nuestro día a día?
En este artículo, exploraremos a fondo el concepto de pH, su fórmula matemática, los métodos profesionales y las ingeniosas técnicas caseras para determinarlo. Prepárate para descubrir por qué esta medida es tan crucial y cómo puedes aplicarla en diferentes contextos, garantizando así un equilibrio óptimo en tus procesos y en tu entorno natural.

¿Qué es el pH? El Potencial de Hidrógeno Desvelado
El término pH es la abreviatura de Potencial de Hidrógeno, y como su nombre lo indica, es una medida que nos permite cuantificar el grado de acidez o alcalinidad (también conocida como basicidad) de una disolución. Su importancia radica en que nos indica la concentración de hidrogeniones en dicha disolución. Pero, ¿qué es un hidrogenión?
Un hidrogenión no es más que un ion positivo de Hidrógeno, una partícula diminuta de Hidrógeno con una carga eléctrica positiva. Cuantos más de estos 'cachitos con carga positiva' de Hidrógeno existan en una disolución, más ácida será. Por el contrario, si la actividad o concentración de estos iones de hidrógeno es baja, la disolución tenderá a ser alcalina.
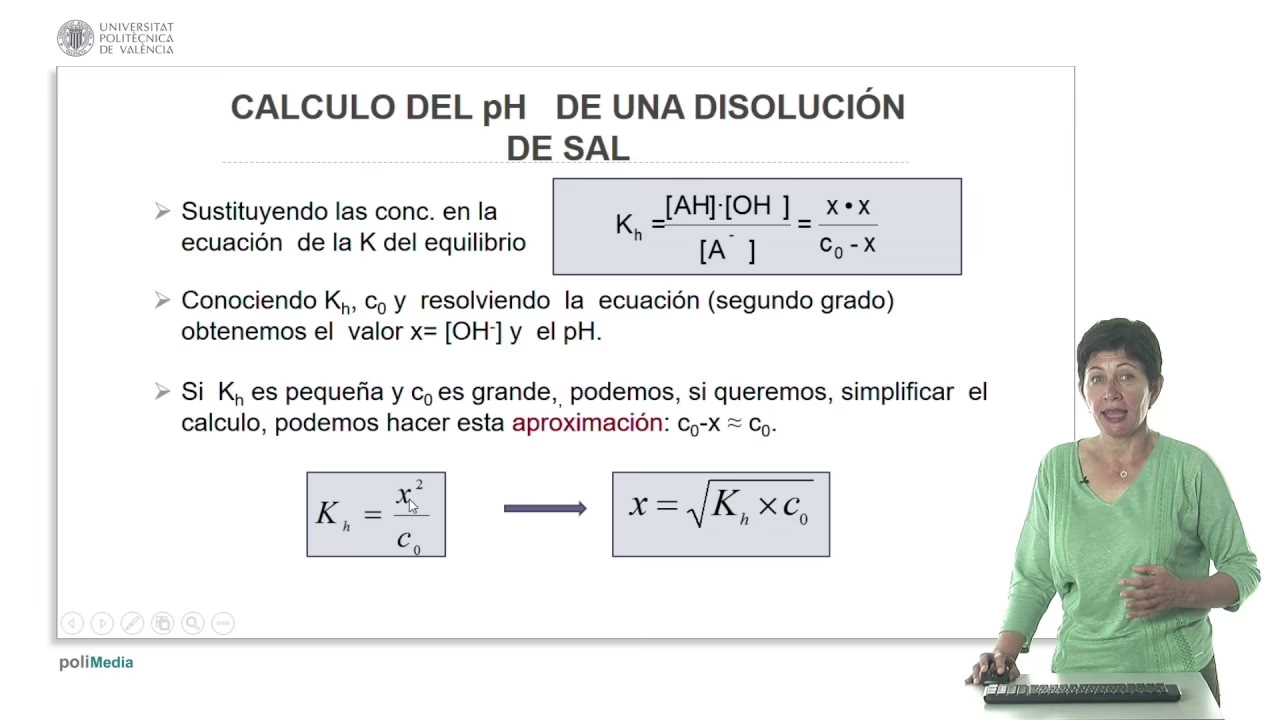
La relación entre la concentración de hidrogeniones y el pH no es lineal, sino logarítmica. Esto significa que un pequeño cambio en el valor del pH representa un cambio significativo en la concentración de los iones de hidrógeno. La fórmula matemática universalmente aceptada para calcular el pH es:
pH = –log[aH+]
Donde 'aH+' representa la actividad de los iones de hidrógeno. En términos más sencillos, es el logaritmo negativo en base 10 de la concentración de iones de hidrógeno. Esta fórmula nos permite traducir una amplia gama de concentraciones de iones de hidrógeno en una escala manejable y fácil de interpretar.
La Escala de pH: Un Vistazo Rápido
Para facilitar la interpretación, el pH se mide normalmente en una escala que va del 1 al 14. Esta escala nos permite clasificar las disoluciones de la siguiente manera:
- Valores entre 1 y menos de 7: Indican una disolución ácida. Cuanto más cerca del 1, más ácida es la sustancia. Ejemplos comunes incluyen el jugo de limón (pH ~2) o el ácido de batería (pH ~1).
- Valor de 7: Representa una disolución neutra. El ejemplo más conocido es el agua pura a 25°C, que tiene un pH de 7. Esto significa que la concentración de iones de hidrógeno es igual a la de iones hidroxilo.
- Valores entre más de 7 y 14: Indican una disolución alcalina o básica. Cuanto más cerca del 14, más alcalina es la sustancia. Ejemplos incluyen el bicarbonato de sodio (pH ~8.5) o la lejía (pH ~13).
Comprender esta escala es fundamental para interpretar las mediciones de pH y tomar decisiones informadas en diversos campos.
Métodos Profesionales para Medir el pH
La medición precisa del pH es crucial en numerosos entornos industriales y de investigación. Para ello, se utilizan instrumentos y reactivos específicos que garantizan resultados fiables.

El pH-metro: Precisión en sus Manos
El pH-metro es el instrumento estándar para la medición precisa del pH. Se trata de un potenciómetro que mide la diferencia de potencial eléctrico entre dos electrodos sumergidos en la disolución a analizar. Un sistema típico de dos electrodos consiste en:
- Electrodo de vidrio: Este electrodo contiene una solución ácida de referencia y es sensible a la actividad de los hidrogeniones en la muestra. Su membrana de vidrio ultra fina reacciona a la concentración de iones H+, generando una pequeña carga eléctrica.
- Electrodo de referencia: Generalmente de plata o cloruro de plata, este electrodo mantiene un potencial constante, sirviendo como punto de comparación.
Cuando ambos electrodos se sumergen en el agua o la disolución, se produce una fuerza eléctrica (un voltaje) entre el ácido del electrodo de vidrio y la disolución de la muestra. Esta fuerza eléctrica, o diferencia de potencial, es directamente proporcional al pH de la muestra y es lo que el pH-metro mide. El dispositivo convierte esta señal eléctrica en un valor de pH numérico que se muestra en una pantalla digital. Los pH-metros ofrecen una alta precisión y son indispensables en laboratorios, industrias y cualquier aplicación donde la exactitud del pH sea crítica.
Reactivos de pH: Simplicidad y Eficacia
Para mediciones menos exigentes en cuanto a precisión, pero igualmente útiles y sencillas, se emplean los reactivos de pH. Estos se presentan comúnmente en dos formatos:
- Tiras de pH: Son pequeñas tiras de papel impregnadas con indicadores químicos que cambian de color según el pH de la disolución. El procedimiento es muy simple: se sumerge la tira en la muestra de agua (o se coloca en contacto con la superficie de la muestra si es un suelo húmedo) y se espera unos segundos. El color que adquiere la tira se compara con una tabla de colores incluida en el empaque, lo que permite determinar el rango de pH. Son ideales para pruebas rápidas y de campo.
- Gotas de pH: Similar a las tiras, pero en formato líquido. Se añaden unas pocas gotas del reactivo a una pequeña muestra de la disolución. El líquido de la muestra cambiará de color, y este color se compara con una carta de colores para determinar el pH. Son muy fáciles de usar y también proporcionan una indicación rápida de si una sustancia es ácida, alcalina o neutra.
Ambos métodos son económicos, portátiles y excelentes para usuarios que se inician en la medición del pH o que necesitan una estimación rápida sin la necesidad de la alta precisión de un pH-metro.
¿Por Qué es Crucial Medir el pH?
La medición del pH es una de las determinaciones más comunes y fundamentales en una vasta gama de procesos y aplicaciones. Su importancia radica en que el pH afecta directamente la solubilidad, la disponibilidad de nutrientes, la toxicidad de ciertos compuestos, la actividad enzimática y la estabilidad de muchas sustancias. Aquí destacamos algunas de las razones principales y campos de aplicación:
- Procesos Industriales: En la fabricación de productos químicos, farmacéuticos, textiles o papel, el control preciso del pH es vital para la eficiencia de las reacciones químicas, la calidad del producto final y la prevención de la corrosión de los equipos. Un pH inadecuado puede resultar en productos de baja calidad o incluso en fallos de producción.
- Procesamiento de Alimentos y Bebidas: El pH influye en el sabor, la textura, la conservación y la seguridad alimentaria. Por ejemplo, en la elaboración de quesos, cervezas o productos lácteos, el pH es monitoreado constantemente para asegurar la fermentación adecuada y prevenir el crecimiento de microorganismos indeseados.
- Agricultura y Horticultura: El pH del suelo es un factor determinante para la disponibilidad de nutrientes para las plantas. Cada especie vegetal tiene un rango de pH óptimo en el que puede absorber mejor los minerales. Un suelo demasiado ácido o alcalino puede bloquear la absorción de nutrientes esenciales, afectando el crecimiento y la productividad de los cultivos. La medición del pH del suelo permite a los agricultores y jardineros ajustar las condiciones para maximizar el rendimiento.
- Acuicultura y Acuarios: En la cría de peces y otros organismos acuáticos, el pH del agua es crítico para su salud y supervivencia. Variaciones extremas pueden ser letales. Un monitoreo constante asegura un ambiente acuático estable y adecuado para las especies.
- Tratamiento de Aguas Residuales: El pH es un parámetro clave en las plantas de tratamiento de aguas. Ajustar el pH ayuda a optimizar los procesos de coagulación, floculación y desinfección, asegurando que el agua tratada cumpla con las normativas ambientales antes de ser descargada.
- Medicina y Salud: El pH de la sangre y otros fluidos corporales es estrictamente regulado. Desequilibrios en el pH pueden indicar problemas de salud significativos. En laboratorios clínicos, la medición del pH es una herramienta diagnóstica esencial.
En resumen, el control del pH no es solo una medida técnica, sino una práctica esencial para garantizar la calidad, la seguridad y la eficiencia en una multitud de aplicaciones, desde la escala industrial hasta el cuidado de nuestro hogar y jardín.
Medición del pH en Casa: Soluciones Prácticas y Sencillas
Aunque los métodos profesionales ofrecen una precisión inigualable, no siempre son necesarios, especialmente cuando se trata de aplicaciones domésticas como el cuidado del jardín. Conocer el pH del suelo de tus plantas es esencial para asegurar que estas reciban los minerales que necesitan para prosperar. Afortunadamente, existen formas sencillas y económicas de estimar el pH de tu suelo sin necesidad de equipos especializados. Es importante recordar que estos métodos caseros no te brindarán un número exacto de pH, sino una indicación general de si tu suelo es ácido, alcalino o neutro.
Un suelo con un pH superior a 7.0 es alcalino, mientras que uno con un pH inferior a 7.0 es ácido. Si bien algunas plantas se adaptan mejor a condiciones específicas, un pH cercano a 7.0 (neutro) suele ser el ideal para la mayoría de las especies, ya que permite una óptima disponibilidad de nutrientes. Si tu suelo es demasiado alcalino o ácido, puedes tomar medidas para ajustarlo, como la adición de material orgánico como compost casero, que tiende a regular el pH hacia la neutralidad.
Método del Vinagre y el Bicarbonato de Sodio
Este método es una forma ingeniosa y divertida de determinar la tendencia de pH de tu suelo. Necesitarás vinagre blanco (ácido) y bicarbonato de sodio (alcalino).
- Recolección de Muestras: Toma pequeñas muestras de tierra de diferentes partes de tu jardín, ya que el pH puede variar. Coloca aproximadamente una taza de tierra de cada área.
- Prueba de Alcalinidad (con Vinagre): De la primera muestra de tierra, toma dos cucharadas y colócalas en un recipiente separado. Agrégale aproximadamente media taza de vinagre blanco.
- Observación: Si la mezcla reacciona produciendo burbujas o efervescencia, esto indica que tu suelo es alcalino. La reacción se debe a la presencia de carbonatos en el suelo, que reaccionan con el ácido del vinagre. Un suelo que burbujea con vinagre suele tener un pH entre 7 y 8.
- Prueba de Acidez (con Bicarbonato): Si la primera prueba con vinagre no produce burbujas, tu suelo no es alcalino. Procede entonces con la segunda prueba: toma otras dos cucharadas de la misma muestra de tierra y colócalas en un recipiente diferente. Añade agua destilada (importante que sea destilada para no introducir otros iones que alteren la prueba) hasta que la tierra se convierta en una pasta fangosa. Luego, agrega media taza de bicarbonato de sodio.
- Observación: Si esta mezcla burbujea, significa que tu suelo es ácido. La reacción se produce porque el bicarbonato de sodio, una base, reacciona con los ácidos presentes en el suelo. Un suelo que burbujea con bicarbonato de sodio suele tener un pH entre 5 y 6.
- Suelo Neutro: Si tu muestra de tierra no reacciona ni con el vinagre ni con el bicarbonato de sodio, ¡felicidades! Tienes un suelo con un pH neutral, lo cual es ideal para la mayoría de las plantas.
El Método de la Col Roja: Un Indicador Natural
La col roja (también conocida como repollo morado o col lombarda) contiene pigmentos naturales llamados antocianinas, que cambian de color según el pH del medio. Es un excelente indicador natural.
- Preparar el Indicador: Corta una taza de col roja en trozos pequeños. Colócalos en una cacerola con dos tazas de agua destilada. Cocina a fuego lento durante unos 5 minutos hasta que el agua adquiera un color azulado o púrpura intenso.
- Enfriar y Colar: Retira del fuego y deja reposar la mezcla durante al menos media hora para que los pigmentos se liberen completamente. Luego, cuela el líquido, desechando los trozos de col. El líquido resultante será tu indicador de pH casero, con un pH neutral de 7.
- Probar el Suelo: Toma una muestra de tierra de tu jardín y colócala en un frasco o recipiente transparente. Sobre esta muestra, vierte el agua de col preparada.
- Mezclar y Observar: Mezcla bien la tierra con el agua de col y deja reposar durante unos minutos.
- Interpretación de Colores:
- Si el agua se vuelve de color rosa o rojo, tu suelo es ácido. Cuanto más intenso el rosa, más ácido es.
- Si el agua se torna de color azul verdoso o verde, tu suelo es alcalino. Un verde más intenso indica una mayor alcalinidad.
- Si el color permanece azul o púrpura (el color original del indicador), tu suelo es neutro.
Estos métodos caseros son herramientas valiosas para tener una idea general del pH de tu suelo, permitiéndote tomar decisiones informadas sobre cómo cuidarlo y qué plantas son las más adecuadas para él.
Tabla Comparativa: Métodos de Medición de pH
Para resumir las diferencias entre los métodos profesionales y caseros, la siguiente tabla ofrece un vistazo rápido a sus características principales:
+-----------------------+---------------------+---------------------+-------------------------+ | Característica | pH-metro | Tiras/Gotas de pH | Métodos Caseros | +-----------------------+---------------------+---------------------+-------------------------+ | Precisión | Muy alta (numérica) | Media (rango) | Baja (indicación gral.) | | Costo | Alto | Bajo | Muy bajo | | Complejidad de Uso | Media (calibración) | Muy baja | Baja | | Aplicaciones Típicas | Laboratorio, Ind. | Campo, Acuarios | Jardinería, Educación | | Resultado | Valor numérico exacto| Rango de color | Acidez/Alcalinidad | +-----------------------+---------------------+---------------------+-------------------------+
Preguntas Frecuentes sobre el pH
- ¿El pH del agua potable es importante?
- Sí, el pH del agua potable es importante tanto para la salud como para la durabilidad de las tuberías. Un pH muy bajo (ácido) puede corroer las tuberías y liberar metales, mientras que un pH muy alto (alcalino) puede causar incrustaciones. La mayoría de las normativas establecen un rango de pH seguro para el agua potable, generalmente entre 6.5 y 8.5.
- ¿Puede cambiar el pH de una solución con el tiempo?
- Sí, el pH de una solución puede cambiar debido a varios factores, como la absorción de dióxido de carbono del aire (que forma ácido carbónico), la actividad microbiana, la evaporación de volátiles o reacciones químicas internas. Por eso, en aplicaciones críticas, el pH se monitorea continuamente.
- ¿Qué es un amortiguador de pH o solución buffer?
- Una solución amortiguadora (o buffer) es una mezcla de un ácido débil y su base conjugada, o una base débil y su ácido conjugado. Tienen la capacidad de resistir cambios significativos en el pH cuando se les añaden pequeñas cantidades de un ácido o una base. Son esenciales en biología, química y procesos industriales para mantener el pH estable.
- ¿Es seguro tocar ácidos o bases?
- No. Muchas soluciones ácidas o básicas concentradas son corrosivas y pueden causar quemaduras graves en la piel y los ojos. Siempre se deben usar equipos de protección personal (guantes, gafas de seguridad, bata de laboratorio) al manipular cualquier sustancia con pH extremo. Las soluciones caseras utilizadas en los métodos de prueba (vinagre, bicarbonato, col roja) son generalmente seguras, pero siempre es prudente manejarlas con cuidado.
En resumen, el pH es mucho más que un simple número; es un indicador dinámico y crucial que nos permite comprender y controlar el equilibrio químico en una multitud de sistemas, desde la compleja química de nuestro cuerpo hasta la simplicidad de un jardín en casa. Ya sea con la precisión de un pH-metro o la simplicidad de la col roja, la capacidad de medir el pH nos empodera para tomar decisiones informadas y mantener un entorno óptimo.
Si quieres conocer otros artículos parecidos a Descifrando el pH: Medición y Cálculo Esencial puedes visitar la categoría Cálculos.