30/09/2025
El universo en su escala más pequeña es un lugar de asombrosa complejidad y orden. Para comprender cómo se estructuran los átomos y, por ende, cómo interactúa la materia, los científicos han desarrollado un marco teórico basado en los números cuánticos. Estos números no son meras abstracciones; son las coordenadas que nos permiten mapear la improbable danza de los electrones alrededor del núcleo atómico. Son la clave para entender por qué los elementos se comportan como lo hacen y cómo se forman los enlaces químicos.

En el corazón de esta descripción cuántica se encuentran conceptos fundamentales como los niveles y subniveles de energía, que definen las regiones donde es más probable encontrar un electrón. Acompáñanos en este viaje para desvelar qué son estos niveles y subniveles y cómo los números cuánticos nos permiten descifrarlos.
- El Número Cuántico Principal (n): Los Niveles de Energía
- El Número Cuántico Secundario (l): La Forma de los Subniveles
- La Relación entre Nivel y Subnivel: La Arquitectura Atómica
- Cálculo del Número de Orbitals y Electrones
- Preguntas Frecuentes sobre Niveles y Subniveles Cuánticos
- ¿Qué son los números cuánticos y por qué son importantes?
- ¿Cómo se relaciona el número cuántico principal (n) con los niveles de energía?
- ¿Qué número cuántico determina la forma del orbital o subnivel?
- ¿Cuántos subniveles puede tener un nivel de energía dado?
- ¿Cuál es la diferencia fundamental entre un nivel y un subnivel de energía?
- Conclusión
El Número Cuántico Principal (n): Los Niveles de Energía
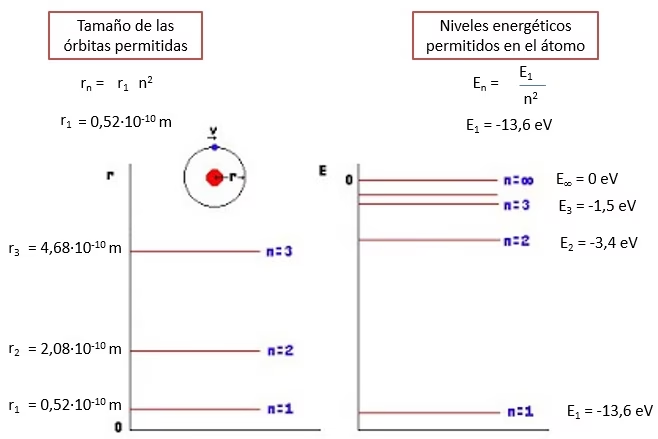
El primer y más fundamental de los números cuánticos es el número cuántico principal, denotado por la letra n. Este número es el equivalente cuántico del número de piso en un edificio: determina el nivel de energía general de un electrón y, consecuentemente, su distancia promedio al núcleo atómico. Cuanto mayor sea el valor de 'n', mayor será la energía del electrón y más lejos se encontrará, en promedio, del núcleo.
Los valores posibles para 'n' son números enteros positivos: 1, 2, 3, 4, y así sucesivamente. Cada valor de 'n' representa una capa o nivel de energía distinto. Por ejemplo:
- Cuando n=1, el nivel de energía está más cerca del núcleo y los electrones tienen la energía más baja posible (estado fundamental).
- Cuando n=4, el nivel de energía está más alejado del núcleo, y los electrones en este nivel poseen una energía significativamente mayor. Además, a medida que 'n' aumenta, el nivel de energía se vuelve más complejo, conteniendo múltiples subniveles, como veremos a continuación (4s, 4p, 4d, 4f).
El número cuántico principal no solo nos da una idea de la energía y la distancia, sino que también influye en el tamaño de la nube electrónica, es decir, el espacio que ocupa el electrón. Un 'n' más grande implica una nube electrónica más grande y difusa.
El Número Cuántico Secundario (l): La Forma de los Subniveles
Mientras que 'n' nos dice en qué 'piso' de energía se encuentra el electrón, el número cuántico secundario, denotado por la letra l, nos revela la 'forma' de la 'habitación' dentro de ese piso. Este número es crucial porque determina la forma geométrica del orbital o subnivel de energía en el que se encuentra el electrón.
Los valores de 'l' dependen directamente del valor de 'n'. Para un valor dado de 'n', 'l' puede tomar cualquier valor entero desde 0 hasta (n-1). A cada valor de 'l' se le asigna una letra específica para designar el tipo de subnivel:
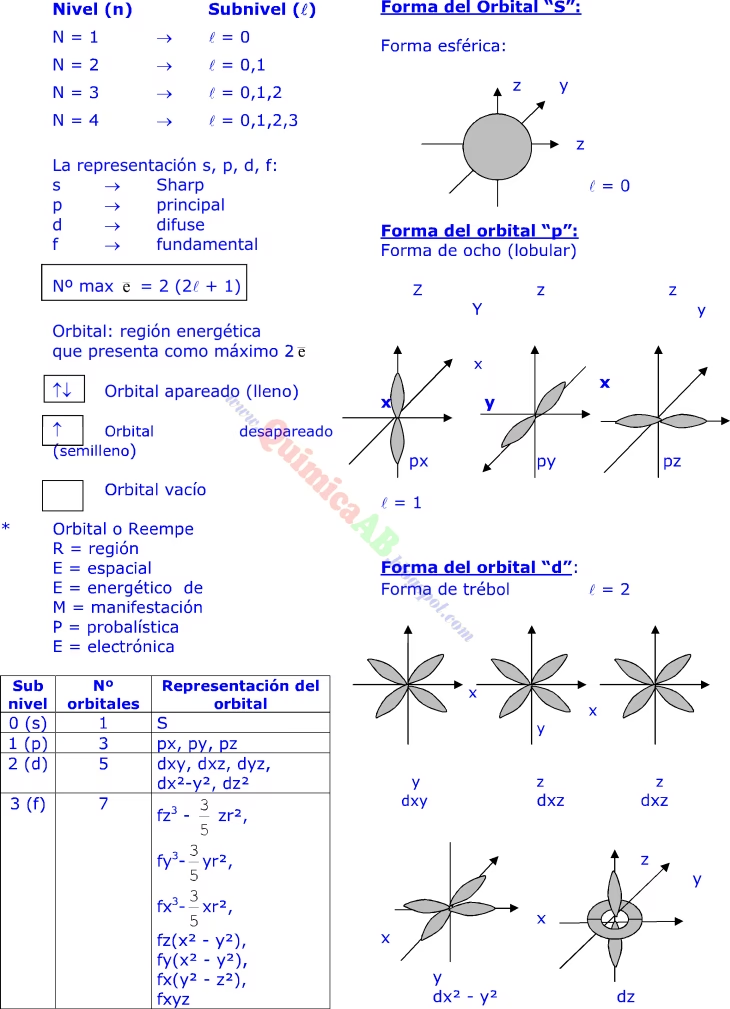
- l = 0: Corresponde al subnivel 's'. Los orbitales 's' tienen una forma esférica.
- l = 1: Corresponde al subnivel 'p'. Los orbitales 'p' tienen una forma de mancuerna o lóbulo doble.
- l = 2: Corresponde al subnivel 'd'. Los orbitales 'd' tienen formas más complejas, generalmente de cuatro lóbulos o una mancuerna con un 'donut' alrededor.
- l = 3: Corresponde al subnivel 'f'. Los orbitales 'f' tienen formas aún más intrincadas y multilobuladas.
Es importante recalcar que el número cuántico secundario es el que directamente determina el subnivel. Sin él, solo sabríamos el nivel general de energía, pero no la particular región espacial donde el electrón se mueve con mayor probabilidad.

La Relación entre Nivel y Subnivel: La Arquitectura Atómica
La combinación de 'n' y 'l' nos da una imagen más completa de la ubicación y el comportamiento de un electrón. Cada nivel de energía 'n' contiene un cierto número de subniveles 'l'. La cantidad de subniveles posibles en un nivel dado es igual a 'n'.
Veamos algunos ejemplos para entender esta relación:
- Para n = 1: El único valor posible para 'l' es 0 (n-1 = 1-1 = 0). Esto significa que el primer nivel de energía (n=1) solo tiene un subnivel, el subnivel '1s'.
- Para n = 2: Los valores posibles para 'l' son 0 y 1. Esto implica que el segundo nivel de energía (n=2) tiene dos subniveles: el subnivel '2s' (l=0) y el subnivel '2p' (l=1).
- Para n = 3: Los valores posibles para 'l' son 0, 1 y 2. Por lo tanto, el tercer nivel de energía (n=3) tiene tres subniveles: el '3s' (l=0), el '3p' (l=1) y el '3d' (l=2).
- Para n = 4: Los valores posibles para 'l' son 0, 1, 2 y 3. Así, el cuarto nivel de energía (n=4) tiene cuatro subniveles: el '4s' (l=0), el '4p' (l=1), el '4d' (l=2) y el '4f' (l=3).
Esta jerarquía de niveles y subniveles es fundamental para entender la configuración electrónica de los átomos y, por extensión, las propiedades periódicas de los elementos en la tabla periódica.
Cálculo del Número de Orbitals y Electrones
Dentro de cada subnivel, existen uno o más orbitales. Un orbital se puede definir como la región del espacio alrededor del núcleo donde la probabilidad de encontrar un electrón es máxima. El número de orbitales dentro de un subnivel específico depende de un tercer número cuántico, el número cuántico magnético (ml), que no es el foco principal de este artículo, pero es importante mencionarlo para el cálculo total.
Para simplificar, podemos calcular el número total de orbitales posibles en un nivel de energía dado (n) utilizando una fórmula sencilla:
Número de orbitales = n2
Por ejemplo:
- Si n=1, hay 12 = 1 orbital (el orbital 1s).
- Si n=2, hay 22 = 4 orbitales (un 2s y tres 2p).
- Si n=3, hay 32 = 9 orbitales (un 3s, tres 3p y cinco 3d).
Dado que cada orbital puede albergar un máximo de dos electrones (principio de exclusión de Pauli, que también requiere un cuarto número cuántico, el número cuántico de espín), podemos determinar el número máximo de electrones que un nivel de energía puede contener con la fórmula:
Número máximo de electrones = 2n2
Por ejemplo:
- Para n=1, el número máximo de electrones es 2(1)2 = 2 electrones.
- Para n=2, el número máximo de electrones es 2(2)2 = 8 electrones.
- Para n=3, el número máximo de electrones es 2(3)2 = 18 electrones.
Tabla Comparativa de Niveles y Subniveles
La siguiente tabla resume la relación entre el número cuántico principal (n), los valores posibles del número cuántico secundario (l), los subniveles resultantes, el número de orbitales por subnivel, y el total de orbitales y electrones por nivel.
| n (Nivel de Energía) | Valores de l (Subniveles) | Designación del Subnivel | Forma del Orbital | Número de Orbitales por Subnivel | Total de Orbitales por Nivel (n2) | Máx. Electrones por Nivel (2n2) |
|---|---|---|---|---|---|---|
| 1 | 0 | 1s | Esférica | 1 | 1 | 2 |
| 2 | 0 | 2s | Esférica | 1 | 4 | 8 |
| 1 | 2p | Mancuerna | 3 | |||
| 3 | 0 | 3s | Esférica | 1 | 9 | 18 |
| 1 | 3p | Mancuerna | 3 | |||
| 2 | 3d | Compleja | 5 | |||
| 4 | 0 | 4s | Esférica | 1 | 16 | 32 |
| 1 | 4p | Mancuerna | 3 | |||
| 2 | 4d | Compleja | 5 | |||
| 3 | 4f | Muy compleja | 7 |
Preguntas Frecuentes sobre Niveles y Subniveles Cuánticos
¿Qué son los números cuánticos y por qué son importantes?
Los números cuánticos son un conjunto de valores numéricos que describen el estado de energía de un electrón en un átomo. Son fundamentales porque especifican la ubicación probable de un electrón, su energía, la forma de la región espacial que ocupa (orbital) y su orientación en el espacio. Sin ellos, sería imposible entender la estructura atómica, la tabla periódica y la forma en que los átomos interactúan para formar moléculas.
¿Cómo se relaciona el número cuántico principal (n) con los niveles de energía?
El número cuántico principal (n) determina directamente el nivel de energía general del electrón. Un valor de 'n' más alto indica un nivel de energía superior y, consecuentemente, que el electrón se encuentra, en promedio, más lejos del núcleo. Es el principal factor que influye en la energía total del electrón.
¿Qué número cuántico determina la forma del orbital o subnivel?
El número cuántico secundario (l), también conocido como número cuántico azimutal o de momento angular, es el que determina la forma geométrica del orbital o subnivel de energía. Los valores de 'l' (0, 1, 2, 3...) corresponden a las formas 's' (esférica), 'p' (mancuerna), 'd' (compleja) y 'f' (muy compleja), respectivamente.
¿Cuántos subniveles puede tener un nivel de energía dado?
Un nivel de energía dado por el número cuántico principal 'n' puede tener 'n' subniveles diferentes. Por ejemplo, si n=1, solo hay 1 subnivel (1s). Si n=3, hay 3 subniveles (3s, 3p, 3d). Esto se debe a que 'l' puede tomar valores desde 0 hasta (n-1), lo que resulta en 'n' posibles valores para 'l'.
¿Cuál es la diferencia fundamental entre un nivel y un subnivel de energía?
Un nivel de energía (determinado por 'n') es una capa principal que agrupa electrones con energías similares y distancias promedio al núcleo. Dentro de cada nivel, existen uno o más subniveles (determinados por 'l'), que son divisiones más específicas del nivel de energía. Los subniveles describen las diferentes formas espaciales (orbitales) que los electrones pueden adoptar dentro de esa capa principal. Piénsalo como un edificio (nivel) que tiene diferentes tipos de apartamentos (subniveles) dentro de cada piso.
Conclusión
Comprender los niveles y subniveles de energía, definidos por los números cuánticos principal (n) y secundario (l), es esencial para desentrañar la organización interna de los átomos. Estos números nos proporcionan un mapa preciso de dónde se encuentran los electrones y cómo se mueven, revelando la fascinante arquitectura que subyace a toda la materia. Desde la esférica simplicidad de un orbital 's' hasta la compleja elegancia de un 'f', cada subnivel juega un papel crucial en la determinación de las propiedades químicas de los elementos. Al dominar estos conceptos, abrimos una ventana a la mecánica cuántica y a la forma en que el universo se construye a sí mismo, electrón por electrón.
Si quieres conocer otros artículos parecidos a Descifrando Niveles y Subniveles Cuánticos puedes visitar la categoría Cálculos.