10/02/2025
En el vasto universo de la física, el electrón se erige como una de las partículas subatómicas más fundamentales y omnipresentes. Como componente esencial de cada átomo, su masa, aunque increíblemente pequeña, desempeña un papel trascendental en la determinación de las propiedades de la materia, desde la forma en que los elementos interactúan químicamente hasta cómo funciona la electricidad. Pero, ¿alguna vez te has preguntado cómo se calcula o, más precisamente, cómo se determina la masa de algo tan diminuto e imperceptible a simple vista? En este artículo, exploraremos en profundidad la masa del electrón: su valor preciso, los ingeniosos experimentos que la revelaron y su profunda importancia en diversas ramas de la ciencia y la tecnología.

- ¿Qué es la Masa del Electrón?
- El Valor de la Masa del Electrón y sus Unidades
- La Fascinante Historia de su Determinación
- Métodos Modernos para la Medición Precisa
- Masa en Reposo vs. Masa Relativista
- La Importancia Fundamental de la Masa del Electrón
- Relación con Otras Constantes Físicas
- Preguntas Frecuentes (FAQs)
- Conclusión
¿Qué es la Masa del Electrón?
La masa del electrón, o más específicamente, la masa en reposo del electrón (me), es una de las constantes físicas fundamentales del universo. Se define como la masa de un electrón cuando está en reposo, es decir, sin movimiento relativo a un observador. Este concepto de “masa en reposo” es crucial porque, según la Teoría Especial de la Relatividad de Einstein, la masa de un objeto puede variar con su velocidad. Sin embargo, la masa en reposo es una propiedad intrínseca e invariable de la partícula.
El electrón fue descubierto a finales del siglo XIX por J.J. Thomson. Estas partículas subatómicas, con carga negativa, orbitan el núcleo de un átomo y son las responsables de fenómenos tan diversos como la conductividad eléctrica y las reacciones químicas. Dada su ubicuidad y su rol central, conocer su masa con precisión es vital para la física atómica, la química y la electrónica.
El Valor de la Masa del Electrón y sus Unidades
El valor de la masa en reposo del electrón es extraordinariamente pequeño. Su valor aceptado internacionalmente es de aproximadamente 9.109 × 10-31 kilogramos. Sin embargo, este valor puede expresarse en varias unidades, dependiendo del contexto científico, lo que facilita su uso en diferentes cálculos. A continuación, presentamos una tabla con los valores de la masa del electrón en diversas unidades:
| Unidad | Valor de la Masa del Electrón |
|---|---|
| Kilogramos (kg) | 9.10938356(11) × 10-31 kg |
| Gramos (g) | 9.10938356(11) × 10-28 gramos |
| Unidad de Masa Atómica (amu) | 5.48579909070(16) × 10-4 amu |
| Megaelectronvoltios por velocidad de la luz al cuadrado (MeV/c²) | 0.5109989461(31) MeV/c² |
La unidad MeV/c² es particularmente común en física de partículas, ya que la energía y la masa están interrelacionadas por la famosa ecuación de Einstein E=mc².
La Fascinante Historia de su Determinación
La determinación de la masa del electrón no fue una tarea sencilla y requirió de una serie de experimentos ingeniosos que marcaron hitos en la física. Aquí te contamos cómo se logró:
1. Determinación de la Relación Carga-Masa (e/m) por J.J. Thomson (1897)
El primer paso crucial fue dado por J.J. Thomson. En 1897, Thomson realizó experimentos con rayos catódicos (que más tarde se identificarían como haces de electrones). Al someter estos rayos a campos eléctricos y magnéticos perpendiculares entre sí, observó la deflexión de las partículas. Midiendo esta deflexión, Thomson pudo determinar la relación entre la carga (e) y la masa (m) de los electrones. Descubrió que esta relación era constante, independientemente del material del que provenían los electrones, lo que sugería la existencia de una partícula fundamental. El valor obtenido para e/m fue de aproximadamente 1.76 × 1011 C/kg.

2. Medición de la Carga del Electrón (e) por Robert Millikan (1909)
Una década después, en 1909, el físico estadounidense Robert A. Millikan llevó a cabo el famoso experimento de la gota de aceite. En este experimento, Millikan observó el movimiento de pequeñas gotas de aceite cargadas eléctricamente entre dos placas metálicas. Al equilibrar la fuerza gravitatoria sobre las gotas con la fuerza eléctrica, pudo determinar la carga de un solo electrón. El valor que obtuvo para la carga elemental (e) fue de aproximadamente 1.60 × 10-19 C (Coulomb).
3. Cálculo Final de la Masa del Electrón (m)
Con los valores de la relación carga-masa (e/m) de Thomson y la carga del electrón (e) de Millikan, la masa del electrón pudo ser finalmente calculada mediante una simple división:
Masa del electrón (m) = Carga (e) / (Relación Carga/Masa (e/m))
m = (1.60 × 10-19 C) / (1.76 × 1011 C/kg) ≈ 9.1 × 10-31 kg
Este enfoque combinado permitió la primera determinación precisa de la masa de una partícula subatómica, abriendo las puertas a una nueva era en la física.
Métodos Modernos para la Medición Precisa
Desde los experimentos pioneros de Thomson y Millikan, la tecnología ha avanzado enormemente, permitiendo mediciones aún más precisas de la masa del electrón. Los métodos actuales se basan en principios físicos sofisticados:
- Trampa de Penning: Este método implica atrapar un solo electrón en un campo eléctrico y magnético. Al medir su movimiento y las frecuencias de resonancia, se puede determinar su masa con una precisión excepcional. Las trampas de Penning son herramientas fundamentales en la física de precisión.
- Medición de la Frecuencia Ciclotrónica: Utilizando un campo magnético para acelerar electrones, se mide la frecuencia de su movimiento circular. Esta frecuencia, conocida como frecuencia ciclotrónica, está directamente relacionada con la carga y la masa del electrón, permitiendo calcular su masa con gran exactitud.
- Difracción de Electrones: Aunque menos directo para la masa en sí, este método implica disparar electrones a un blanco cristalino y medir el patrón de difracción. La forma en que los electrones interactúan con la red cristalina depende de su masa y energía, lo que puede utilizarse en el contexto de mediciones de precisión.
- Medición del Momento Magnético Anómalo del Electrón: Esta es una de las mediciones más precisas en física. Implica medir la pequeña desviación del momento magnético del electrón de lo predicho por la electrodinámica cuántica. Esta desviación es extremadamente sensible a la masa del electrón y otras constantes fundamentales.
Cada uno de estos métodos tiene sus propias fortalezas y limitaciones, pero en conjunto, han establecido la masa del electrón como una constante con un altísimo grado de precisión.
Masa en Reposo vs. Masa Relativista
Es importante aclarar la distinción entre la “masa en reposo” (me) y la “masa relativista”. Como mencionamos, la masa en reposo es una constante intrínseca e invariable del electrón. Sin embargo, la Teoría Especial de la Relatividad de Einstein establece que la masa de un objeto aumenta a medida que su velocidad se acerca a la velocidad de la luz. Esta “masa relativista” se calcula mediante la fórmula:
mrelativista = γ * me
Donde γ (gamma) es el factor de Lorentz, dado por γ = 1 / √(1 - v²/c²), siendo 'v' la velocidad del electrón y 'c' la velocidad de la luz. Para electrones acelerados a voltajes muy altos (por ejemplo, por encima de 100 kV), esta corrección se vuelve sustancial. La mayoría de las mediciones prácticas se realizan con electrones en movimiento, por lo que es fundamental considerar el factor relativista si la velocidad es significativa. No obstante, cuando hablamos de “la masa del electrón” como una constante fundamental, nos referimos siempre a su masa en reposo, que es independiente de la velocidad y del marco de referencia.

La Importancia Fundamental de la Masa del Electrón
La masa del electrón, a pesar de su diminuto tamaño, tiene implicaciones profundas y amplias en diversas áreas de la ciencia y la tecnología:
- Física Atómica: La masa del electrón es un factor crucial en la determinación de la estructura y propiedades de los átomos. Influye directamente en las energías de los orbitales electrónicos, la estabilidad de los núcleos atómicos y los espectros de emisión y absorción de la luz por los átomos.
- Química: En química, la masa del electrón es esencial para comprender las propiedades químicas de los elementos y su reactividad con otros elementos. Las interacciones electrónicas, que dependen de la masa de los electrones, son la base de los enlaces químicos y las reacciones.
- Electrónica: En el campo de la electrónica, la masa del electrón es fundamental para entender el comportamiento de los electrones en los circuitos eléctricos y en el diseño de dispositivos electrónicos como transistores, diodos y microchips. La movilidad de los electrones en los materiales semiconductores, por ejemplo, está directamente relacionada con su masa.
- Física de Altas Energías: En la física de partículas, la masa del electrón es importante para entender las interacciones de los electrones con otras partículas y para explorar las propiedades de los bloques de construcción fundamentales de la materia.
- Astrofísica: La masa del electrón juega un papel en la determinación de las propiedades del plasma (un estado de la materia donde los electrones están separados de los núcleos) y el comportamiento de las estrellas, como las enanas blancas, cuya estabilidad depende de la presión de degeneración de los electrones.
En resumen, la masa del electrón es un parámetro fundamental que tiene una amplia gama de aplicaciones y es indispensable para la comprensión de casi todos los fenómenos en el microcosmos y sus efectos en el macrocosmos.
Relación con Otras Constantes Físicas
La masa del electrón no existe en aislamiento; está intrínsecamente ligada a otras constantes fundamentales de la física, como la constante de Avogadro (NA) y la unidad de masa atómica (mu). Por ejemplo, antes de que la constante de Avogadro fuera redefinida en 2019, su valor se podía calcular utilizando la masa del electrón y la masa atómica relativa del electrón. De manera similar, la unidad de masa atómica se puede expresar en términos de la masa del electrón y su masa atómica relativa.
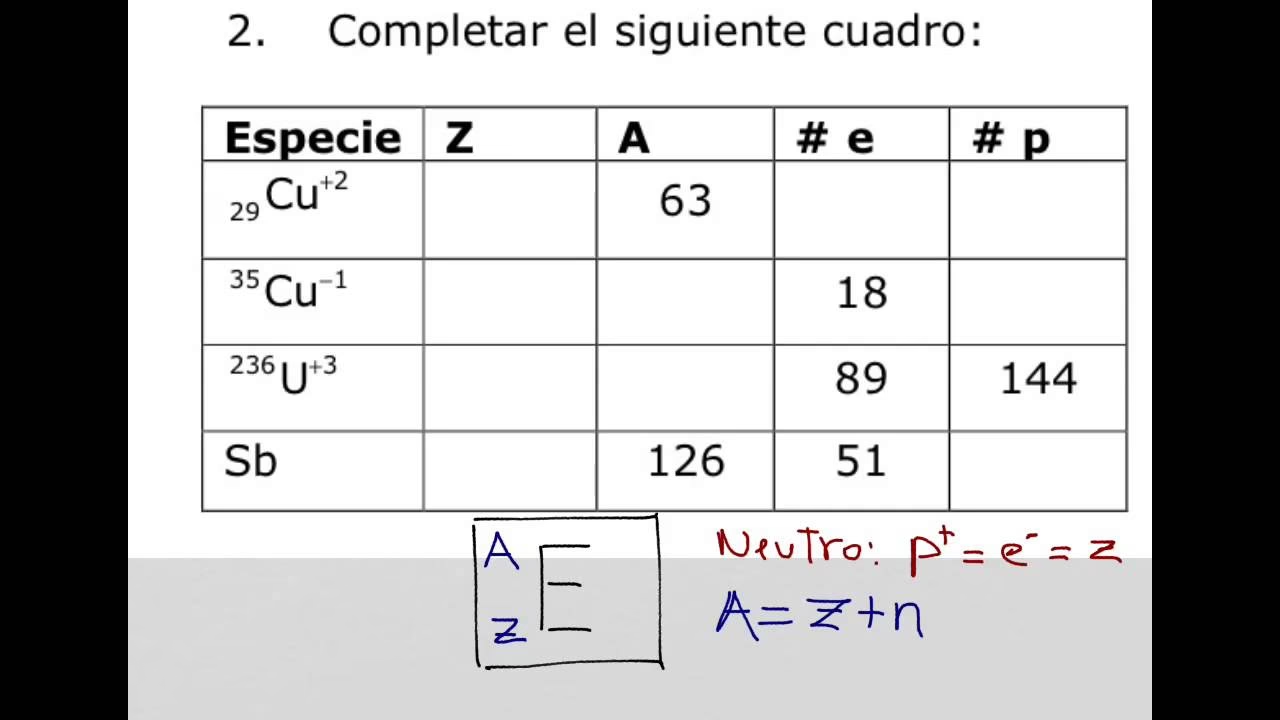
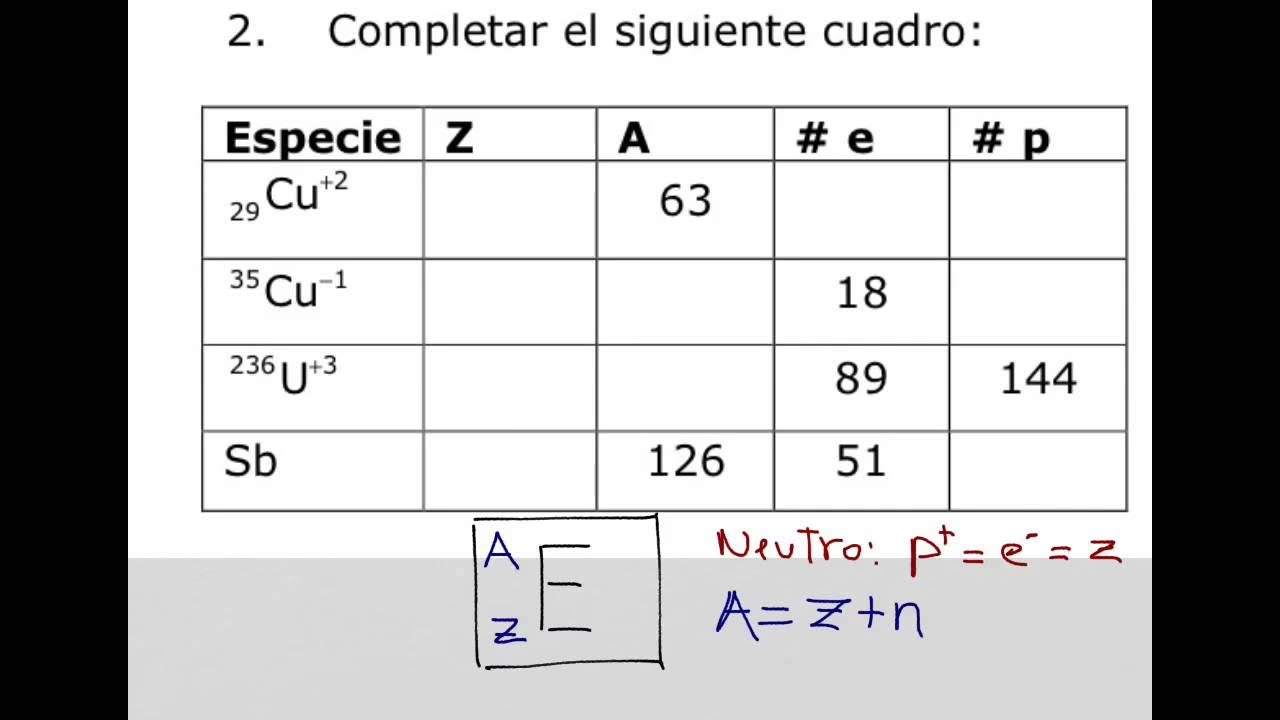
Un ejemplo práctico de esta interconexión se ve en el cálculo de las masas atómicas relativas de los átomos neutros. Aunque las mediciones suelen hacerse en iones (átomos con electrones faltantes o en exceso), para obtener la masa de un átomo neutro, es necesario añadir la masa de los electrones que le corresponden y corregir por la energía de enlace de esos electrones. La fórmula general para un núclido X de número atómico Z es:
Ar(X) = Ar(XZ+) + Z * Ar(e) - Eb / (muc²)
Donde Ar(X) es la masa atómica relativa del átomo neutro, Ar(XZ+) es la masa atómica relativa del ion, Z es el número de electrones, Ar(e) es la masa atómica relativa del electrón, Eb es la energía de enlace de los electrones y muc² es la equivalencia energética de la unidad de masa atómica. Las correcciones por la masa de los electrones y la energía de enlace son pequeñas pero cruciales para la precisión.
Preguntas Frecuentes (FAQs)
¿La masa del electrón cambia?
La masa en reposo del electrón es considerada una constante fundamental de la naturaleza y no cambia con el tiempo ni bajo diferentes condiciones. Sin embargo, su masa “efectiva” puede variar en el contexto de materiales (como semiconductores) debido a las interacciones con el entorno cristalino, y su masa “relativista” aumenta con la velocidad, como se explicó anteriormente.
¿Es la masa del electrón más pequeña que la de un protón?
Sí, la masa del electrón es significativamente más pequeña que la masa de un protón. La masa de un protón es aproximadamente 1,836 veces mayor que la masa de un electrón. Esta gran diferencia de masa es una de las razones por las que los electrones orbitan el núcleo atómico (compuesto por protones y neutrones), que es mucho más masivo y denso.
¿La masa del electrón se ve afectada por campos electromagnéticos?
La masa en reposo intrínseca de un electrón no se ve directamente afectada por campos electromagnéticos. Sin embargo, los campos electromagnéticos ejercen fuerzas sobre los electrones cargados, alterando su trayectoria y energía. En el contexto de la masa relativista, la energía adquirida por el electrón en un campo (y por lo tanto su velocidad) sí contribuye a su masa relativista aparente.
¿Qué significa el “(11)” o “(31)” en los valores de la masa del electrón?
Estos números entre paréntesis, como en 9.10938356(11) × 10-31 kg, representan la incertidumbre estándar en los últimos dígitos del valor. Por ejemplo, (11) significa que la incertidumbre es de ±0.00000011 en los dos últimos dígitos mostrados.
Conclusión
La masa del electrón, aunque una cantidad minúscula, es un pilar fundamental de nuestro entendimiento del universo. Desde su descubrimiento y determinación a través de experimentos históricos hasta su medición con una precisión asombrosa en la actualidad, el electrón ha sido y sigue siendo un objeto de estudio fascinante. Su valor constante es vital para desentrañar los misterios de la materia a nivel atómico y subatómico, impulsando avances en campos tan diversos como la química, la electrónica y la astrofísica. Comprender cómo se calcula y la importancia de esta diminuta partícula nos permite apreciar la profundidad y la interconexión de las leyes que rigen nuestro cosmos.
Si quieres conocer otros artículos parecidos a ¿Cómo se Calcula la Masa de un Electrón? puedes visitar la categoría Física.