17/01/2022
Desde los albores de la física moderna, la luz ha sido una ventana para comprender la estructura de la materia. Cuando la luz emitida por gases excitados, como el hidrógeno, se descompone a través de un prisma, no produce un arcoíris continuo, sino una serie de líneas brillantes y discretas. Este fenómeno, conocido como espectro de emisión, fue un enigma durante mucho tiempo, hasta que un maestro de escuela suizo llamado Johann Jakob Balmer encontró una notable regularidad en las líneas visibles del espectro del hidrógeno en 1885. Su descubrimiento no solo proporcionó una fórmula empírica para estas longitudes de onda, sino que también sentó las bases para el desarrollo posterior de la teoría cuántica del átomo.
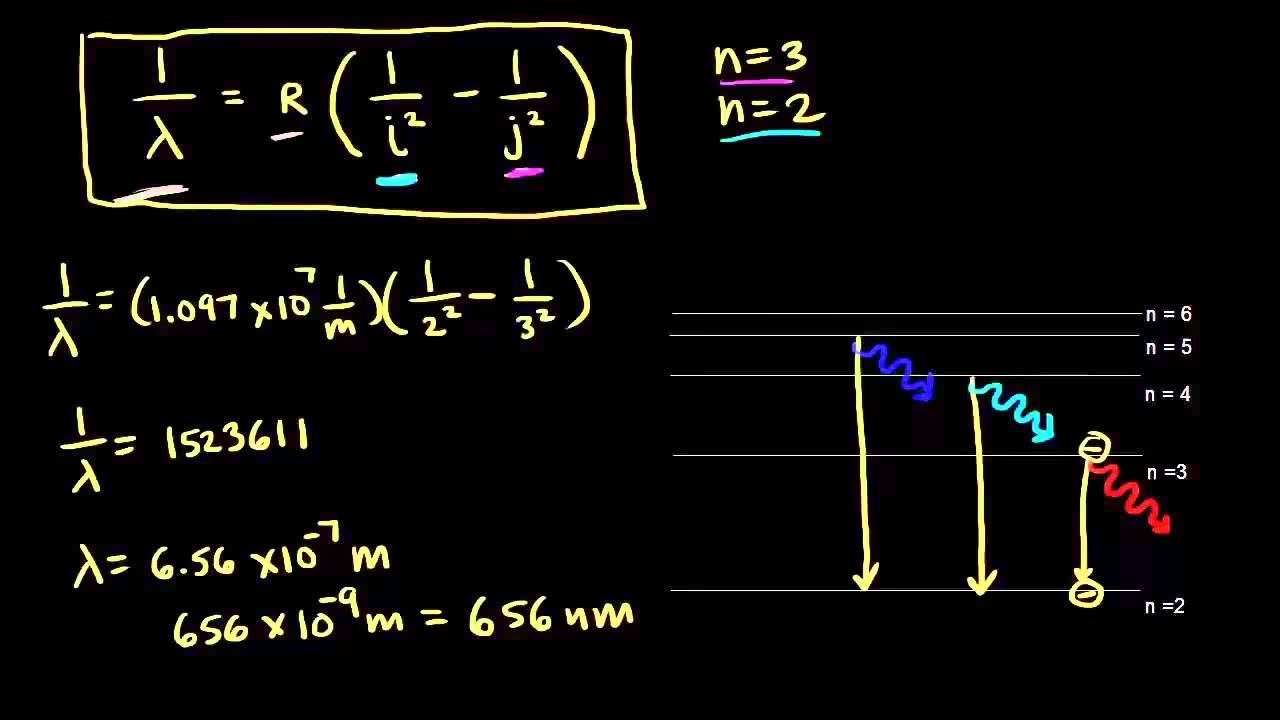
La serie de Balmer es un conjunto específico de líneas espectrales que se observan en el espectro de emisión del átomo de hidrógeno. Estas líneas se generan cuando un electrón en un átomo de hidrógeno realiza una transición desde un nivel de energía superior a un nivel de energía específico: el segundo nivel de energía, denotado como n=2. Lo más fascinante de la serie de Balmer es que sus transiciones caen dentro del rango de la luz visible, lo que permitió su estudio temprano y su observación directa, convirtiéndola en un pilar fundamental para la comprensión de la estructura atómica.
- La Fórmula Original de Balmer: Un Vistazo Pionero
- La Generalización de Rydberg: Un Marco Unificado
- Conexión con el Modelo Atómico de Bohr y los Niveles de Energía
- Series Espectrales del Hidrógeno: Un Espectro Completo
- Transiciones de Emisión y Absorción
- El Papel de la Serie de Balmer en la Astronomía
- Preguntas Frecuentes sobre la Serie de Balmer
- Conclusión
La Fórmula Original de Balmer: Un Vistazo Pionero
Johann Balmer, con una perspicacia asombrosa, notó que las longitudes de onda de las líneas observadas en el espectro visible del hidrógeno guardaban una relación matemática con una longitud de onda única: 364.50682 nm. Al aplicar una fórmula simple que involucraba números enteros, pudo predecir con notable precisión las longitudes de onda de las líneas existentes y, lo que es más importante, la existencia de otras que aún no habían sido observadas. Este fue un triunfo para la ciencia empírica y un indicio temprano de la naturaleza cuantizada de la energía atómica. La fórmula original de Balmer para calcular la longitud de onda (λ) de las líneas de la serie de Balmer se presentó de la siguiente manera:
λ = B (m² / (m² − n²))
Donde, para la serie de Balmer, el nivel de energía final (n) es siempre 2. Así, la fórmula se simplifica a:
λ = B (m² / (m² − 2²))
- λ representa la longitud de onda de la luz emitida o absorbida.
- B es la constante de Balmer, cuyo valor es aproximadamente 3.6450682 × 10⁻⁷ metros o 364.50682 nanómetros. Este valor también representa el límite de la serie, es decir, la longitud de onda a la que convergen las líneas a medida que 'm' tiende a infinito.
- m representa el número entero del nivel de energía inicial del electrón. Para que una transición pertenezca a la serie de Balmer, el electrón debe caer desde un nivel de energía superior (m > n), por lo que 'm' puede tomar valores enteros de 3, 4, 5, y así sucesivamente.
El genio de Balmer radicó en su capacidad para encontrar una relación matemática simple que describía un fenómeno físico complejo. Su fórmula no solo corrigió mediciones espectroscópicas que eran ligeramente imprecisas en su tiempo, sino que también predijo la existencia de líneas que fueron descubiertas posteriormente, confirmando la validez de su enfoque.
La Generalización de Rydberg: Un Marco Unificado
Años después, en 1888, el físico sueco Johannes Rydberg generalizó la fórmula de Balmer para describir todas las transiciones del átomo de hidrógeno, y de hecho, de cualquier átomo. La fórmula de Rydberg es una expresión más universal que abarca todas las series espectrales del hidrógeno (Lyman, Balmer, Paschen, Brackett, Pfund, etc.). La ecuación comúnmente utilizada para calcular las longitudes de onda en la serie de Balmer es una reordenación recíproca de la fórmula original de Balmer y se expresa de la siguiente forma:
1/λ = R_H (1/n_f² − 1/n_i²)
Para la serie de Balmer, el nivel de energía final (n_f) es siempre 2. Por lo tanto, la fórmula de Rydberg para la serie de Balmer se convierte en:
1/λ = R_H (1/2² − 1/n²) para n = 3, 4, 5, …
- λ es la longitud de onda de la luz absorbida o emitida.
- R_H es la constante de Rydberg para el hidrógeno. Esta constante es fundamental en la espectroscopia atómica y es igual a 4/B en la fórmula de Balmer. Su valor, para un núcleo infinitamente pesado, es aproximadamente 10973731.57 m⁻¹.
- n (o n_i) es el número entero del nivel de energía inicial del electrón, siempre mayor que el nivel final (n > 2).
La fórmula de Rydberg demostró la interconexión de todas las series espectrales del hidrógeno y proporcionó un marco teórico más robusto para comprender el comportamiento de los electrones en los átomos. Fue un paso crucial hacia la comprensión de los niveles de energía cuantizados dentro del átomo, un concepto que Niels Bohr desarrollaría más tarde.
Conexión con el Modelo Atómico de Bohr y los Niveles de Energía
El trabajo de Balmer y Rydberg fue puramente empírico, pero sentó las bases para la teoría atómica de Niels Bohr en 1913. Bohr postuló que los electrones solo pueden existir en órbitas o niveles de energía discretos alrededor del núcleo. Cuando un electrón salta de un nivel de energía a otro, absorbe o emite un fotón de luz con una energía y longitud de onda específicas. La energía de un fotón (ξ) está relacionada con su frecuencia (v) y longitud de onda (λ) por las ecuaciones de Planck y Einstein:
ξ = hv = hc/λ
Donde 'h' es la constante de Planck y 'c' es la velocidad de la luz. Bohr interpretó las líneas espectrales como el resultado de transiciones de electrones entre estos niveles de energía permitidos. La energía de un fotón emitido es igual a la diferencia de energía entre el estado inicial de mayor energía y el estado final de menor energía del electrón.
Para el átomo de hidrógeno, la energía de un nivel 'n' se puede expresar como:
E_n = -Rhc / n²
Donde Rhc es una constante que, para el hidrógeno, es aproximadamente 13.6 eV (la energía del estado fundamental). Así, la diferencia de energía para una transición es:
ΔE = E_final - E_inicial = Rhc (1/n_inicial² - 1/n_final²)
Y dado que ΔE = hc/λ, podemos ver la correspondencia directa con la fórmula de Rydberg:
1/λ = R_H (1/n_final² - 1/n_inicial²)
Para la serie de Balmer, el nivel de energía final es n=2. Esto significa que todas las transiciones de la serie de Balmer involucran a un electrón que cae al segundo nivel de energía. Las transiciones desde n=3, 4, 5, etc., hacia n=2, producen las líneas espectrales visibles de la serie de Balmer.
Series Espectrales del Hidrógeno: Un Espectro Completo
El espectro del hidrógeno no se limita a la serie de Balmer. Existen otras series, cada una definida por el nivel de energía final al que el electrón transita. Estas series caen en diferentes regiones del espectro electromagnético:
- Serie de Lyman: Las transiciones ocurren cuando un electrón cae al primer nivel de energía (n=1). Estas líneas se encuentran en la región ultravioleta (UV) del espectro.
- Serie de Balmer: Las transiciones ocurren cuando un electrón cae al segundo nivel de energía (n=2). Estas líneas se encuentran en la región de la luz visible.
- Serie de Paschen: Las transiciones ocurren cuando un electrón cae al tercer nivel de energía (n=3). Estas líneas se encuentran en la región del infrarrojo (IR).
- Serie de Brackett: Las transiciones ocurren cuando un electrón cae al cuarto nivel de energía (n=4). Estas líneas también se encuentran en la región del infrarrojo.
- Serie de Pfund: Las transiciones ocurren cuando un electrón cae al quinto nivel de energía (n=5). Estas líneas también se encuentran en la región del infrarrojo.
Aquí tienes una tabla comparativa de las principales series del espectro de hidrógeno:
| Serie | Nivel Final (n_f) | Niveles Iniciales (n_i) | Región Espectral |
|---|---|---|---|
| Lyman | 1 | 2, 3, 4, ... | Ultravioleta |
| Balmer | 2 | 3, 4, 5, ... | Visible |
| Paschen | 3 | 4, 5, 6, ... | Infrarrojo |
| Brackett | 4 | 5, 6, 7, ... | Infrarrojo |
| Pfund | 5 | 6, 7, 8, ... | Infrarrojo |
La existencia de estas series y la precisión con la que sus longitudes de onda podían predecirse mediante la fórmula de Rydberg fueron pruebas irrefutables de la cuantificación de la energía en los átomos y un paso gigante hacia el desarrollo de la mecánica cuántica.
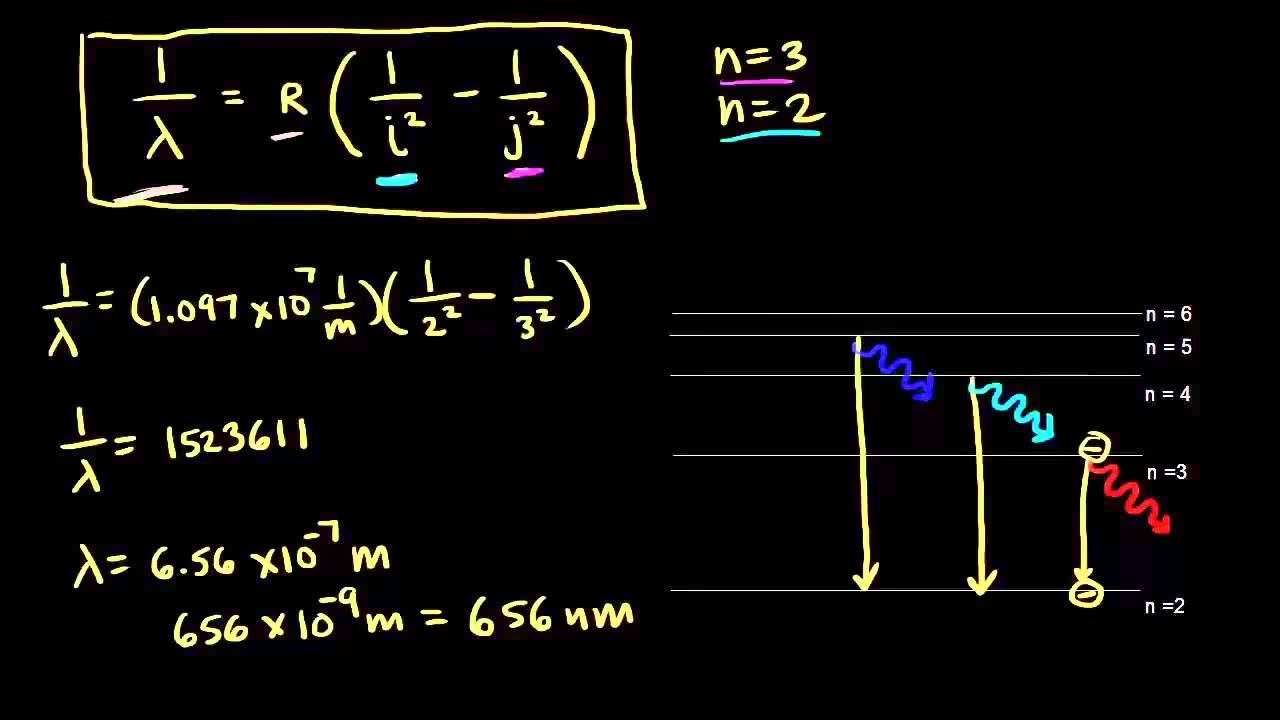
Transiciones de Emisión y Absorción
Las líneas espectrales pueden ser de emisión o de absorción. En la serie de Balmer, observamos ambos fenómenos:
- Emisión: Cuando un electrón en un átomo de hidrógeno, excitado a un nivel de energía superior (por ejemplo, n=3, 4, 5, etc.), cae espontáneamente al segundo nivel de energía (n=2), libera el exceso de energía en forma de un fotón. La longitud de onda de este fotón corresponde a una de las líneas brillantes de la serie de Balmer. Estas son las líneas que Balmer observó originalmente.
- Absorción: Si un átomo de hidrógeno en su segundo nivel de energía (n=2) es irradiado con luz que contiene fotones de la energía exacta necesaria para que un electrón salte a un nivel de energía superior (n=3, 4, 5, etc.), el átomo absorberá esos fotones. Esto crea líneas oscuras en un espectro continuo de luz de fondo. Estas líneas de absorción de Balmer son cruciales en la astronomía para identificar la presencia de hidrógeno en estrellas y galaxias.
El Papel de la Serie de Balmer en la Astronomía
La serie de Balmer juega un papel fundamental en la astrofísica. Dado que el hidrógeno es el elemento más abundante en el universo, las líneas de Balmer son omnipresentes en los espectros de estrellas, nebulosas y galaxias. Los astrónomos utilizan estas líneas para:
- Identificar hidrógeno: La presencia de las líneas de Balmer en un espectro indica la existencia de hidrógeno atómico.
- Determinar la temperatura estelar: La intensidad de las líneas de Balmer varía con la temperatura de la superficie de una estrella. Las estrellas más calientes o más frías tienen líneas de Balmer más débiles, mientras que las estrellas con temperaturas intermedias (clases espectrales A) muestran las líneas de Balmer más fuertes.
- Medir el desplazamiento Doppler: El desplazamiento de las líneas de Balmer hacia el azul o el rojo permite a los astrónomos determinar si un objeto celeste se acerca o se aleja de la Tierra, respectivamente (efecto Doppler).
- Estudiar la composición y el movimiento de las nubes de gas: En nebulosas y otras estructuras cósmicas, las líneas de Balmer pueden revelar información sobre la densidad, la temperatura y la velocidad del gas de hidrógeno.
Sin la comprensión de la serie de Balmer y su relación con la estructura del átomo de hidrógeno, gran parte de lo que sabemos sobre la composición y dinámica del universo sería un misterio.
Preguntas Frecuentes sobre la Serie de Balmer
¿Qué es la serie de Balmer?
La serie de Balmer es un conjunto de líneas espectrales en el espectro de emisión y absorción del átomo de hidrógeno, que resultan de las transiciones de un electrón desde niveles de energía superiores hacia el segundo nivel de energía (n=2). Estas líneas son particularmente importantes porque caen en la región de la luz visible del espectro electromagnético.
¿Cuál es la fórmula para la serie de Balmer?
La fórmula más comúnmente utilizada para la serie de Balmer es una derivación de la fórmula de Rydberg: 1/λ = R_H (1/2² − 1/n²), donde λ es la longitud de onda, R_H es la constante de Rydberg para el hidrógeno (aproximadamente 10973731.57 m⁻¹), y n es el número entero del nivel de energía inicial (n=3, 4, 5, ...).
¿Cuáles de las transiciones pertenecen a la serie de Lyman y Balmer?
- Serie de Lyman: Pertenecen las transiciones donde un electrón cae a o desde el primer nivel de energía (n=1). Es decir, transiciones desde n=2, 3, 4,... hacia n=1 (emisión) o desde n=1 hacia n=2, 3, 4,... (absorción).
- Serie de Balmer: Pertenecen las transiciones donde un electrón cae a o desde el segundo nivel de energía (n=2). Es decir, transiciones desde n=3, 4, 5,... hacia n=2 (emisión) o desde n=2 hacia n=3, 4, 5,... (absorción).
¿En qué transición se absorbe un fotón de la serie de Balmer?
Un fotón de la serie de Balmer se absorbe cuando un electrón en el átomo de hidrógeno salta desde el segundo nivel de energía (n=2) a un nivel de energía superior (n=3, 4, 5, etc.). Por ejemplo, la absorción de un fotón con la energía correspondiente a la transición de n=2 a n=3 produciría una línea de absorción en el espectro de Balmer.
Conclusión
La serie de Balmer es mucho más que un conjunto de líneas de luz; es un testimonio de la simplicidad y la elegancia inherentes a las leyes de la física. Desde las observaciones empíricas de Balmer hasta la generalización de Rydberg y la interpretación cuántica de Bohr, cada paso en su comprensión ha profundizado nuestro conocimiento del átomo y, por extensión, del universo. Su estudio continúa siendo una piedra angular en la física atómica y un recordatorio de cómo la curiosidad y la observación meticulosa pueden desentrañar los secretos más profundos de la naturaleza.
Si quieres conocer otros artículos parecidos a La Serie de Balmer: Desvelando el Espectro Visible puedes visitar la categoría Física.
