16/06/2025
Desde el parpadeo de una estrella distante hasta el brillo de un letrero de neón, la luz nos rodea y nos cuenta historias. Pero, ¿qué sucede cuando la luz se descompone, revelando un arcoíris de colores específicos? Es aquí donde entramos en el fascinante reino del espectro atómico, un universo de patrones luminosos que son la huella dactilar de los elementos. En particular, la Serie de Balmer es una de las series espectrales más estudiadas y significativas del átomo de hidrógeno, la cual nos ha brindado una ventana crucial para comprender los principios fundamentales de la Mecánica Cuántica.
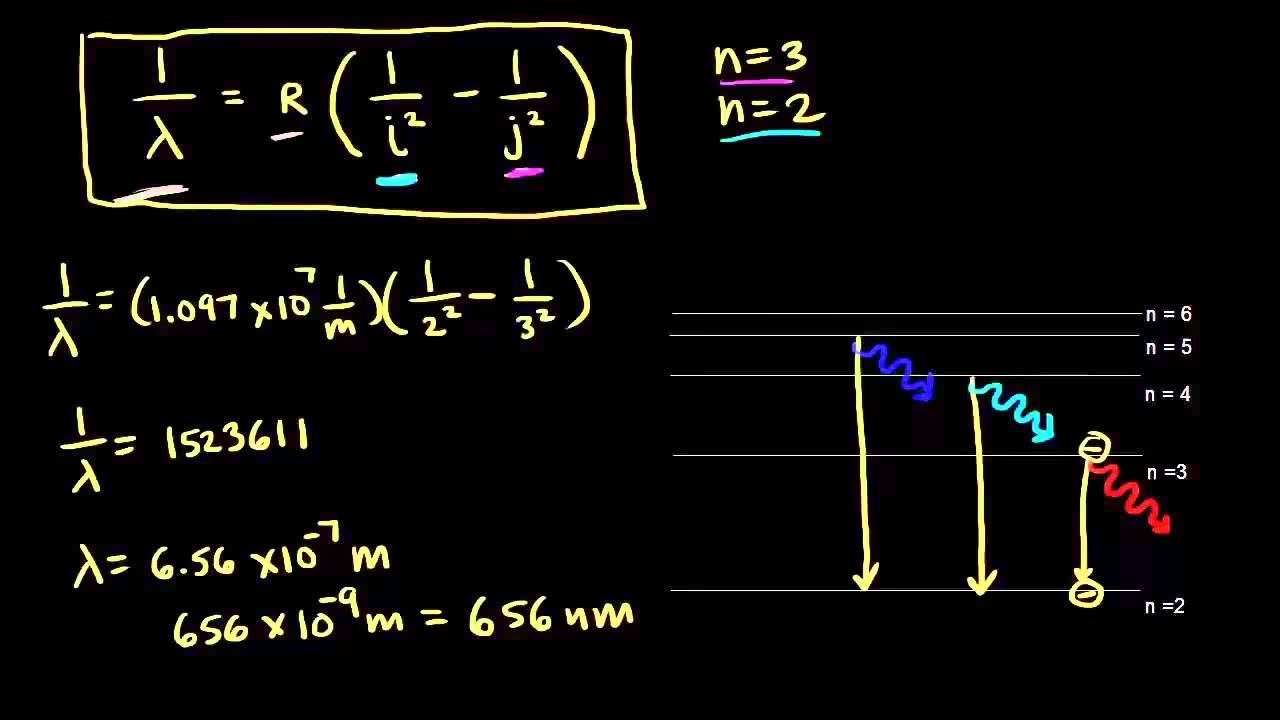
El estudio de estas líneas espectrales no es solo una curiosidad científica; es una piedra angular en la física moderna. Nos permite entender cómo los electrones se mueven dentro de los átomos, cómo emiten o absorben energía y cómo esta energía se manifiesta en forma de luz de colores muy específicos. La Serie de Balmer, al ser la única serie del hidrógeno con líneas en el espectro visible, se convirtió en una herramienta invaluable para los científicos que buscaban descifrar la estructura interna del átomo.
¿Qué es la Serie de Balmer? El Espectro Visible del Hidrógeno
La Serie de Balmer es un conjunto de líneas espectrales que resultan de las transiciones electrónicas de un electrón en el átomo de hidrógeno desde niveles de energía superiores (n > 2) hacia el segundo nivel de energía (n=2). Estas transiciones liberan energía en forma de fotones, y debido a que el segundo nivel de energía está involucrado, muchas de estas líneas caen dentro del espectro visible para el ojo humano, lo que las hace particularmente interesantes y relativamente fáciles de observar.
Johann Jakob Balmer, un físico suizo, fue el primero en descubrir una fórmula empírica en 1885 que describía las longitudes de onda de estas líneas. Su fórmula fue un triunfo, ya que predijo con precisión las posiciones de las líneas conocidas y anticipó la existencia de otras aún no observadas. Esto sentó las bases para el desarrollo de la teoría cuántica del átomo de Bohr, que más tarde proporcionaría una explicación teórica para la fórmula de Balmer.
Las Líneas de Balmer: Colores y Longitudes de Onda
Cada línea en la Serie de Balmer corresponde a una transición específica de un electrón desde un nivel de energía superior al segundo nivel. Estas líneas se designan con letras griegas, comenzando por la transición de menor energía (y por lo tanto, mayor longitud de onda) dentro de la serie:
- Hα (H-alfa): Corresponde a la transición de n=3 a n=2. Es la línea de mayor longitud de onda y se observa en el color rojo.
- Hβ (H-beta): Representa la transición de n=4 a n=2. Se manifiesta en un tono azul-verde.
- Hγ (H-gamma): Proviene de la transición de n=5 a n=2. Su color es violeta.
- Hδ (H-delta): Resulta de la transición de n=6 a n=2. También es violeta, pero con una longitud de onda más corta.
A medida que las transiciones provienen de niveles de energía cada vez más altos, las líneas se agrupan cada vez más cerca unas de otras, convergiendo hacia un límite de serie, más allá del cual el electrón se ioniza (escapa del átomo).
| Designación de la Línea | Transición (nsuperior → n2) | Color Observado | Longitud de Onda (aproximada) |
|---|---|---|---|
| Hα (H-alfa) | 3 → 2 | Rojo | 656.2 nm |
| Hβ (H-beta) | 4 → 2 | Azul-Verde | 486.1 nm |
| Hγ (H-gamma) | 5 → 2 | Violeta | 434.0 nm |
| Hδ (H-delta) | 6 → 2 | Violeta | 410.1 nm |
| Límite de la Serie | ∞ → 2 | Violeta Cercano/UV | 364.6 nm |
La Tercera Línea de la Serie de Balmer: Hγ
La información proporcionada es clara y concisa: la tercera línea de la Serie de Balmer es Hγ. Esta línea se produce cuando un electrón en un átomo de hidrógeno salta desde el nivel de energía n=5 hacia el nivel de energía n=2. La energía liberada durante esta transición se emite como un fotón de luz con una longitud de onda de 434.0 nm, lo que la ubica en la región violeta del espectro visible. Es un componente crucial en el espectro de emisión del hidrógeno y una de las líneas que Balmer pudo predecir con su fórmula.
Cálculo de la Frecuencia: La Primera Línea (Hα)
Más allá de identificar las líneas por su color y longitud de onda, la física nos permite calcular otras propiedades fundamentales, como la frecuencia de la luz emitida. La frecuencia (ν) y la longitud de onda (λ) están intrínsecamente relacionadas a través de la velocidad de la luz (c) mediante la ecuación universal: c = νλ. Para calcular la frecuencia, primero necesitamos determinar la longitud de onda con precisión, y para ello, recurrimos a la Constante de Rydberg y la fórmula de Rydberg.
La fórmula de Rydberg para el átomo de hidrógeno es una expresión matemática poderosa que relaciona las longitudes de onda de las líneas espectrales con los números cuánticos de los niveles de energía involucrados en la transición:
1/λ = R * (1/N₁² - 1/N₂²)
Donde:
- λ es la longitud de onda de la luz emitida.
- R es la Constante de Rydberg, aproximadamente 1.097 × 10⁷ m⁻¹.
- N₁ es el número cuántico principal del nivel de energía final al que desciende el electrón.
- N₂ es el número cuántico principal del nivel de energía inicial desde el que desciende el electrón (N₂ > N₁).
Paso a Paso: Determinando la Frecuencia de Hα
Vamos a aplicar esta fórmula para encontrar la frecuencia de la primera línea de la Serie de Balmer, Hα, que corresponde a una transición de N₂ = 3 a N₁ = 2.
- Paso 1: Identificar los Niveles Cuánticos
Para la primera línea de la Serie de Balmer (Hα), la transición ocurre desde un nivel de energía superior (N₂) al segundo nivel de energía (N₁ = 2). Específicamente, para Hα, el electrón transita de N₂ = 3 a N₁ = 2. - Paso 2: Aplicar la Fórmula de Rydberg
Sustituimos los valores de N₁ y N₂ en la fórmula de Rydberg:1/λ = R * (1/N₁² - 1/N₂²)1/λ = R * (1/2² - 1/3²) - Paso 3: Calcular los Cuadrados de los Niveles de Energía
Realizamos las operaciones de los cuadrados:1/λ = R * (1/4 - 1/9) - Paso 4: Encontrar un Denominador Común y Restar las Fracciones
El denominador común para 4 y 9 es 36:1/λ = R * (9/36 - 4/36)1/λ = R * (5/36) - Paso 5: Sustituir el Valor de la Constante de Rydberg
Ahora, introducimos el valor numérico de la Constante de Rydberg (R ≈ 1.097 × 10⁷ m⁻¹):1/λ = 1.097 × 10⁷ m⁻¹ * (5/36) - Paso 6: Calcular el Valor de 1/λ
Multiplicamos los valores:1/λ ≈ 1.097 × 10⁷ * 0.13888...1/λ ≈ 1.5236 × 10⁶ m⁻¹ - Paso 7: Convertir Longitud de Onda a Frecuencia
Utilizamos la relación fundamental entre frecuencia (ν), longitud de onda (λ) y la velocidad de la luz (c):c = νλ
De donde despejamos la frecuencia:ν = c / λ
También podemos escribirla como:ν = c * (1/λ)
Donde la velocidad de la luz (c) es aproximadamente 3 × 10⁸ m/s. - Paso 8: Cálculo Final de la Frecuencia
Sustituimos el valor de 1/λ y c:ν = 3 × 10⁸ m/s * 1.5236 × 10⁶ m⁻¹ν ≈ 4.57 × 10¹⁴ s⁻¹
La frecuencia de la primera línea (Hα) de la Serie de Balmer del átomo de hidrógeno es aproximadamente 4.57 × 10¹⁴ Hertz (Hz), o ciclos por segundo (s⁻¹). Este valor concuerda con la energía del fotón de luz roja que se emite durante esta transición.
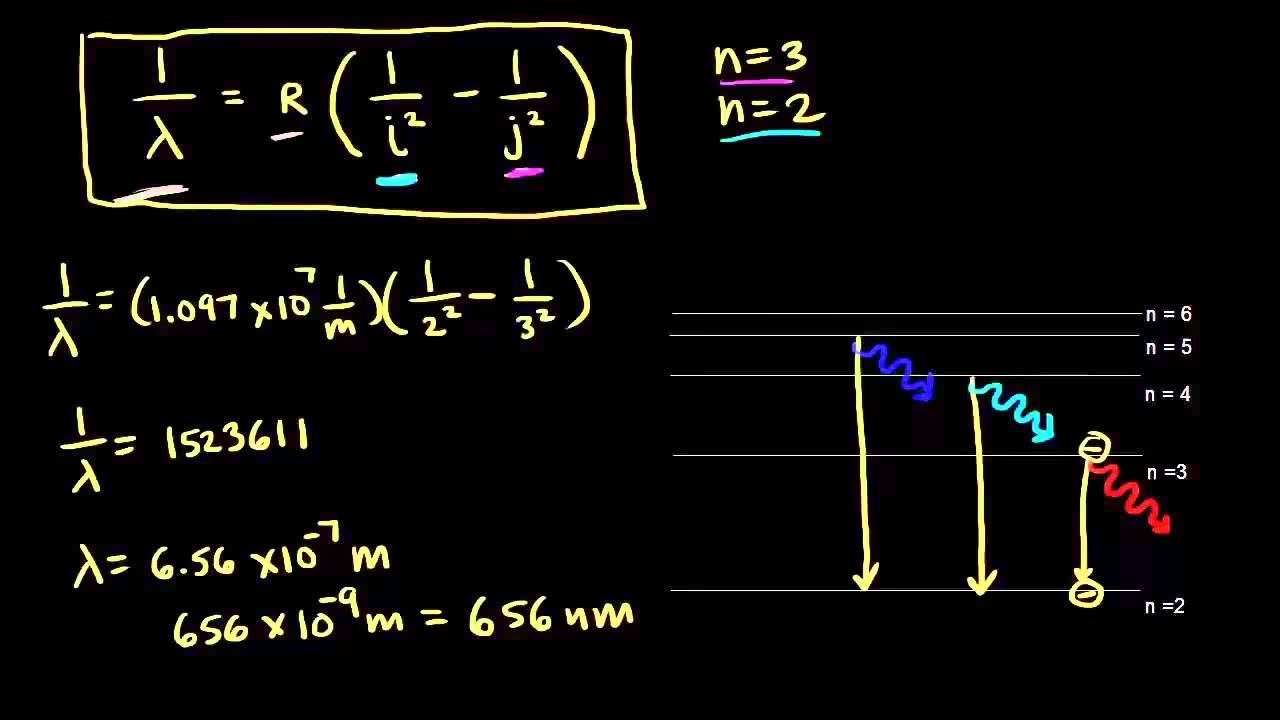
La Importancia Fundamental de la Serie de Balmer
La Serie de Balmer es mucho más que un conjunto de líneas de colores. Su descubrimiento y la posterior explicación teórica fueron hitos cruciales en el desarrollo de la física:
- Validación del Modelo de Bohr: La capacidad del modelo atómico de Bohr para predecir con precisión las líneas de Balmer (y las de otras series) fue una de las primeras y más contundentes pruebas de que los electrones ocupan niveles de energía discretos dentro del átomo, un concepto revolucionario para su época.
- Fundamento de la Mecánica Cuántica: Aunque el modelo de Bohr tenía limitaciones, sentó las bases para el desarrollo de la Mecánica Cuántica completa, que describe el comportamiento de la materia y la energía a nivel atómico y subatómico con una precisión asombrosa.
- Herramienta en Astrofísica: Las líneas de Balmer son omnipresentes en el universo. Se utilizan para clasificar estrellas, ya que la fuerza de estas líneas en el espectro estelar indica la temperatura de la atmósfera de la estrella. También son cruciales para medir el desplazamiento Doppler (corrimiento al rojo o al azul) de galaxias distantes, lo que nos permite inferir su movimiento y la expansión del universo.
Más Allá de Balmer: Otras Series Espectrales del Hidrógeno
El hidrógeno no solo emite luz en el rango visible. Dependiendo del nivel de energía final al que transita el electrón, existen otras series espectrales, cada una con sus propias características:
| Nombre de la Serie | Nivel de Energía Final (N₁) | Región del Espectro Electromagnético |
|---|---|---|
| Serie de Lyman | 1 | Ultravioleta (UV) |
| Serie de Balmer | 2 | Visible |
| Serie de Paschen | 3 | Infrarrojo Cercano (IR) |
| Serie de Brackett | 4 | Infrarrojo Medio (IR) |
| Serie de Pfund | 5 | Infrarrojo Lejano (IR) |
| Serie de Humphreys | 6 | Infrarrojo Extremo (IR) |
Cada una de estas series ofrece una visión única de las transiciones electrónicas dentro del átomo de hidrógeno, aunque la Serie de Balmer sigue siendo la más reconocida debido a su presencia en el espectro visible.
Preguntas Frecuentes (FAQ)
¿Qué es una serie espectral?
Una serie espectral es un conjunto de líneas de emisión o absorción en el espectro de un elemento, que resultan de las transiciones de electrones entre niveles de energía específicos dentro de sus átomos. Cada serie se define por el nivel de energía final al que los electrones transitan.
¿Por qué solo la Serie de Balmer es visible?
La Serie de Balmer es la única serie del átomo de hidrógeno que cae predominantemente en el espectro visible porque sus transiciones tienen como nivel de energía final el N₁=2. Las longitudes de onda asociadas a estas transiciones están dentro del rango que el ojo humano puede percibir. Otras series, como Lyman (N₁=1), emiten en el ultravioleta, y Paschen (N₁=3) en el infrarrojo.
¿Qué nos dice la Serie de Balmer sobre el átomo de hidrógeno?
La Serie de Balmer nos dice que los electrones en el átomo de hidrógeno no pueden tener cualquier energía, sino que están confinados a niveles de energía discretos o cuantizados. Las líneas específicas observadas son la prueba directa de estas transiciones de energía cuantificadas, lo que fue fundamental para el desarrollo de la teoría cuántica.
¿La Serie de Balmer existe para otros elementos?
No, la Serie de Balmer es específica del átomo de hidrógeno. Sin embargo, otros elementos tienen sus propias series espectrales únicas, que son características de su estructura electrónica particular. Cada elemento tiene un 'código de barras' espectral único que permite su identificación.
¿Cómo se mide la Serie de Balmer en la práctica?
La Serie de Balmer se mide utilizando un espectrómetro. Este instrumento descompone la luz emitida por una fuente de hidrógeno (como una lámpara de descarga de hidrógeno) en sus longitudes de onda constituyentes, revelando las distintas líneas de colores que componen la serie.
En resumen, la Serie de Balmer es un testimonio luminoso de la naturaleza cuantizada de la energía dentro de los átomos. Desde las longitudes de onda específicas que definen sus colores hasta las frecuencias calculadas que revelan la energía de sus fotones, cada aspecto de esta serie nos acerca un poco más a la comprensión de los misterios del universo a escala subatómica. Es un ejemplo perfecto de cómo la curiosidad y el cálculo pueden desvelar los secretos más profundos de la luz y la materia.
Si quieres conocer otros artículos parecidos a Desvelando la Serie de Balmer: Luz y Frecuencia puedes visitar la categoría Física.
