20/02/2022
Las enzimas, esas maravillas biológicas presentes en cada rincón de los organismos vivos, son los catalizadores por excelencia de la naturaleza. Sin ellas, innumerables reacciones químicas esenciales para la vida transcurrirían a una velocidad imperceptible, haciendo imposible la existencia tal como la conocemos. Comprender cómo funcionan y, crucialmente, cómo medir la velocidad a la que operan, es fundamental para campos que van desde la medicina hasta la biotecnología.

Este artículo explorará el concepto de la velocidad inicial de una reacción enzimática, una medida clave para caracterizar la actividad de estas proteínas. Profundizaremos en los principios que la rigen, las metodologías para su determinación y las representaciones gráficas que nos permiten descifrar su comportamiento.
- ¿Qué son las Enzimas y Cómo Funcionan?
- Medición de la Velocidad de Reacciones Enzimáticas
- ¿Qué es la Velocidad Inicial (V₀) de una Reacción Enzimática?
- Cinética de Michaelis-Menten: El Modelo Fundamental
- Gráfico de Lineweaver-Burke: La Linearización
- Factores que Afectan la Velocidad Inicial
- Conclusión
- Preguntas Frecuentes (FAQ)
¿Qué son las Enzimas y Cómo Funcionan?
Las enzimas son proteínas complejas, formadas por largas cadenas de aminoácidos que se pliegan en una estructura tridimensional precisa, conocida como estructura terciaria. Esta forma única es crucial, ya que alberga el "sitio activo", una región específica donde se une el sustrato (la molécula sobre la que actúa la enzima) para ser transformado en producto. Son catalizadores biológicos, lo que significa que aceleran drásticamente la velocidad de las reacciones químicas sin ser consumidas o alteradas permanentemente en el proceso.
La interacción entre la enzima y el sustrato se describe a menudo mediante dos modelos principales:
- Modelo de "llave y cerradura": Propone que el sitio activo de la enzima tiene una forma rígida y complementaria al sustrato, como una llave que encaja perfectamente en una cerradura.
- Modelo de "ajuste inducido": Una visión más dinámica, donde el sitio activo de la enzima puede sufrir pequeños cambios conformacionales al unirse al sustrato, adaptándose para optimizar la catálisis. Este modelo explica mejor la flexibilidad y la eficiencia de muchas enzimas.
Cualquier alteración en esta delicada estructura tridimensional, ya sea por cambios extremos de temperatura o pH, puede provocar la "desnaturalización" de la enzima. Una enzima desnaturalizada pierde su forma y, por lo tanto, su capacidad catalítica, lo que subraya la importancia de las condiciones ambientales óptimas para su función.
Medición de la Velocidad de Reacciones Enzimáticas
Dada la vasta diversidad de reacciones controladas por enzimas, no existe un método único y universal para medir sus velocidades. La técnica elegida depende directamente de la naturaleza de los reactivos y productos involucrados. El objetivo es monitorear el cambio en la concentración de un sustrato o un producto a lo largo del tiempo.
Ejemplos de Métodos de Medición:
- Producción de Gas: En el caso de la catalasa, una enzima intracelular común, descompone el peróxido de hidrógeno (un subproducto del metabolismo) en agua y oxígeno. La velocidad de la reacción puede medirse recolectando el gas oxígeno producido a lo largo del tiempo, por ejemplo, utilizando un sensor de presión o un desplazador de volumen de gas.
- Cambio de Color o Turbidez: La tripsina, una enzima extracelular, degrada la caseína de la leche, transformándola de un color blanco opaco a transparente. La velocidad de esta reacción puede cuantificarse con un colorímetro o un espectrofotómetro, que miden la absorbancia o transmitancia de la luz a través de la solución. Una disminución en la turbidez o un cambio en la absorbancia a una longitud de onda específica indica la progresión de la reacción.
- Cambio de pH: Si la reacción produce o consume iones de hidrógeno, se puede usar un medidor de pH para seguir la reacción.
- Cromatografía: Para reacciones más complejas, se pueden tomar muestras a intervalos de tiempo y analizar las concentraciones de sustratos y productos mediante cromatografía.
¿Qué es la Velocidad Inicial (V₀) de una Reacción Enzimática?
La velocidad inicial (V₀) es la velocidad de una reacción enzimática medida al comienzo de la reacción, justo después de que la enzima y el sustrato se han mezclado. Es una medida crítica en la cinética enzimática y se prefiere sobre la velocidad media o la velocidad en etapas posteriores de la reacción por varias razones fundamentales:
Condiciones de Estado Estacionario
Al inicio de una reacción enzimática, los cambios en las concentraciones del sustrato, la enzima, el complejo enzima-sustrato (ES) y el producto (P) ocurren drásticamente. Sin embargo, muy rápidamente, se establece una fase conocida como "estado estacionario".
- Al principio, las concentraciones de enzima y sustrato son altas, mientras que las del complejo ES y el producto son bajas.
- A medida que avanza la reacción, el complejo ES y el producto aumentan, mientras que la enzima libre y el sustrato disminuyen.
- El estado estacionario se alcanza cuando la velocidad de formación del complejo ES es aproximadamente igual a la velocidad de su descomposición (en enzima libre y producto, o enzima libre y sustrato). En este punto, la concentración del complejo ES permanece relativamente constante a lo largo del tiempo.
- La V₀ se mide en esta fase inicial, cuando las concentraciones de sustrato son abundantes y la concentración de producto es mínima. Esto asegura que la velocidad medida no esté limitada por la escasez de sustrato ni por la inhibición del producto (donde el producto acumulado puede ralentizar la enzima), ni por una posible reacción inversa. Hacia el final de la reacción, la disminución del sustrato y la acumulación de producto pueden llevar a una reacción inversa o a una saturación incompleta de la enzima, haciendo que la velocidad medida sea menos representativa de la actividad catalítica intrínseca de la enzima.
Las concentraciones más altas de sustrato aumentan la V₀ hasta que la reacción se aproxima a la velocidad máxima (Vmáx), un punto de saturación donde todos los sitios activos de la enzima están ocupados por el sustrato.
Cinética de Michaelis-Menten: El Modelo Fundamental
El modelo de Michaelis-Menten es la base para comprender la dependencia de la velocidad de reacción de la concentración de sustrato en muchas reacciones enzimáticas. Describe la formación de un complejo enzima-sustrato como un paso intermedio en la reacción.
La Ecuación de Michaelis-Menten:
La relación entre la velocidad inicial (V₀), la concentración de sustrato ([S]), la velocidad máxima (Vmáx) y la constante de Michaelis-Menten (KM) se expresa con la siguiente ecuación:
V₀ = (Vmáx * [S]) / (KM + [S])
Gráfico de Michaelis-Menten:
Al trazar la velocidad de reacción inicial (V₀) en el eje Y frente a la concentración de sustrato ([S]) en el eje X, se obtiene una curva hiperbólica característica. Esta curva muestra cómo la V₀ aumenta rápidamente con el incremento de [S] a bajas concentraciones, pero luego se ralentiza y se acerca asintóticamente a la Vmáx a altas concentraciones de sustrato. Esto ocurre porque la enzima se satura; todos sus sitios activos están ocupados y la enzima está trabajando a su máxima capacidad.
Parámetros Clave:
- Velocidad Máxima (Vmáx): Representa la velocidad máxima teórica de la reacción cuando la enzima está completamente saturada con sustrato. En este punto, aumentar la concentración de sustrato ya no incrementa la velocidad de la reacción, ya que todos los sitios activos están ocupados.
- Constante de Michaelis-Menten (KM): Es la concentración de sustrato a la cual la velocidad de reacción inicial es exactamente la mitad de la velocidad máxima (½ Vmáx). Se mide en el eje X cuando ½ Vmáx se mide en el eje Y. La KM es una medida inversa de la afinidad de una enzima por su sustrato.
- Un valor de KM bajo indica que la enzima tiene una fuerte afinidad por el sustrato, lo que significa que se necesita una menor concentración de sustrato para alcanzar la mitad de la Vmáx.
- Un valor de KM alto indica que la enzima tiene una menor afinidad por el sustrato, requiriendo una mayor concentración de sustrato para alcanzar la mitad de la Vmáx.
- Número de Recambio (Kcat): A menudo llamado "número de recambio", Kcat es la cantidad de producto obtenido cuando la reacción alcanza la Vmáx por unidad de tiempo por sitio activo de la enzima. Permite medir la eficiencia catalítica de la enzima, indicando cuántas moléculas de sustrato puede convertir una molécula de enzima en producto por segundo cuando está saturada.
Es importante destacar que la KM es característica de un complejo enzima-sustrato particular y es sensible a factores como la temperatura y el pH, pero es independiente de la concentración de la enzima.
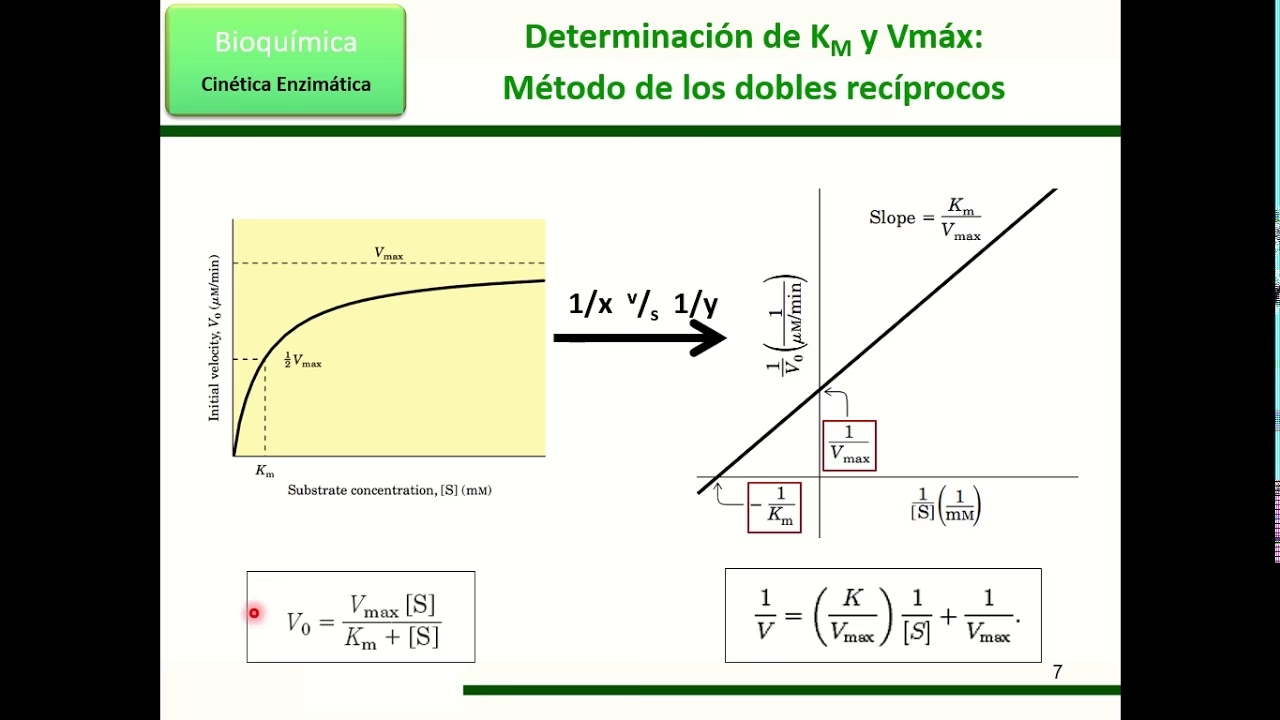
Gráfico de Lineweaver-Burke: La Linearización
Aunque el gráfico de Michaelis-Menten es intuitivo, la determinación precisa de Vmáx y KM puede ser difícil a partir de una curva hiperbólica, especialmente cuando los datos experimentales son limitados o ruidosos. Para superar esto, se utiliza el gráfico de Lineweaver-Burke, que es una doble recíproca de la ecuación de Michaelis-Menten, transformando la curva hiperbólica en una línea recta.
Construcción del Gráfico:
En un gráfico de Lineweaver-Burke:
- El eje Y representa el inverso de la velocidad inicial (1/V₀).
- El eje X representa el inverso de la concentración de sustrato (1/[S]).
El resultado es una línea recta cuya interpretación es mucho más sencilla:
- La intersección con el eje Y es igual a 1/Vmáx.
- La intersección con el eje X es igual a -1/KM.
- La pendiente de la recta es igual a KM/Vmáx.
Ventajas y Desventajas:
La principal ventaja del gráfico de Lineweaver-Burke es la facilidad para determinar Vmáx y KM de manera gráfica. Sin embargo, tiene la desventaja de magnificar los errores experimentales a bajas concentraciones de sustrato (altos valores de 1/[S]), ya que estos puntos se agrupan en un extremo del gráfico.
Comparación de Métodos Gráficos:
| Característica | Gráfico de Michaelis-Menten | Gráfico de Lineweaver-Burke |
|---|---|---|
| Ejes | V₀ vs [S] | 1/V₀ vs 1/[S] |
| Forma | Curva Hiperbólica | Línea Recta |
| Determinación Vmáx | Asintótica, menos precisa | Intersección Y (1/Vmáx) |
| Determinación KM | En ½ Vmáx, menos precisa | Intersección X (-1/KM) |
| Ventajas | Representación directa, intuitiva | Fácil determinación de parámetros |
| Desventajas | Estimación Vmáx/KM difícil | Magnifica errores a bajas [S] |
Factores que Afectan la Velocidad Inicial
Aunque la V₀ se mide bajo condiciones controladas, es crucial recordar que la actividad enzimática, y por ende la V₀, es altamente sensible a las condiciones ambientales. Factores como la temperatura y el pH pueden influir drásticamente en la estructura tridimensional de la enzima y, consecuentemente, en la eficiencia de su sitio activo. Cada enzima tiene una temperatura y un pH óptimos a los que su actividad es máxima. Desviarse de estas condiciones óptimas puede reducir la V₀ e incluso llevar a la desnaturalización.
Conclusión
La determinación de la velocidad inicial de una reacción enzimática es una herramienta indispensable en la bioquímica y la biología molecular. Proporciona una medida fiable de la actividad catalítica de una enzima en condiciones controladas, permitiendo caracterizar su eficiencia (Kcat), su afinidad por el sustrato (KM) y su capacidad máxima (Vmáx). A través de modelos como el de Michaelis-Menten y herramientas gráficas como el de Lineweaver-Burke, los científicos pueden desentrañar los mecanismos de las enzimas, lo que es vital para el desarrollo de nuevos fármacos, la optimización de procesos industriales y la comprensión fundamental de la vida misma.
Preguntas Frecuentes (FAQ)
¿Por qué es importante medir la velocidad inicial (V₀) y no la velocidad total de la reacción?
La V₀ es crucial porque se mide cuando la concentración de sustrato es abundante y la de producto es mínima. Esto asegura que la velocidad observada es una verdadera medida de la actividad intrínseca de la enzima, sin las complicaciones de la limitación del sustrato, la inhibición por el producto o las reacciones inversas que pueden ocurrir en etapas posteriores.
¿Qué significa un valor bajo de KM?
Un valor bajo de KM indica una alta afinidad de la enzima por su sustrato. Esto significa que la enzima puede alcanzar la mitad de su velocidad máxima con una concentración relativamente baja de sustrato, lo que sugiere una interacción eficiente y fuerte entre la enzima y el sustrato.
¿Cómo afectan la temperatura y el pH a la velocidad inicial de una reacción enzimática?
Tanto la temperatura como el pH influyen en la estructura tridimensional de la enzima y, por lo tanto, en la forma y función de su sitio activo. Cada enzima tiene un rango óptimo de temperatura y pH en el que su actividad es máxima. Fuera de estos rangos, la V₀ disminuirá, y a temperaturas o pH extremos, la enzima puede desnaturalizarse irreversiblemente, perdiendo toda su actividad.
¿Cuál es la diferencia entre Vmáx y Kcat?
Vmáx es la velocidad máxima a la que la reacción puede proceder cuando la enzima está completamente saturada con sustrato. Kcat (o número de recambio) es una medida de la eficiencia catalítica de una enzima individual; representa el número de moléculas de sustrato que una sola molécula de enzima puede convertir en producto por unidad de tiempo a Vmáx. Vmáx depende de la cantidad total de enzima presente, mientras que Kcat es una constante intrínseca de la enzima.
Si quieres conocer otros artículos parecidos a ¿Cómo Determinar la Velocidad Inicial Enzimática? puedes visitar la categoría Cálculos.

