12/02/2024
En el vasto universo de la química y la física, entender por qué ciertas reacciones ocurren por sí solas mientras que otras requieren un empuje constante es fundamental. Aquí es donde entra en juego un concepto crucial: la Energía Libre de Gibbs, denotada como ΔG. Esta función termodinámica no solo nos permite predecir la espontaneidad de un proceso, sino que también nos revela la cantidad máxima de trabajo útil que un sistema puede realizar. Prepárate para desentrañar los secretos de la energía que impulsa el cambio en el universo.
- ¿Qué es la Energía Libre de Gibbs (ΔG)?
- Criterios de Espontaneidad: Interpretando ΔG
- Factores que Influyen en ΔG: Entalpía vs. Entropía
- ΔG y el Trabajo Útil: La Eficiencia Energética
- Variación Estándar de Energía Libre (ΔG°)
- ΔG en Condiciones No Estándar y el Efecto de la Temperatura
- Aplicaciones de la Energía Libre de Gibbs en la Vida Real
- Preguntas Frecuentes sobre la Energía Libre de Gibbs
- Conclusión
¿Qué es la Energía Libre de Gibbs (ΔG)?
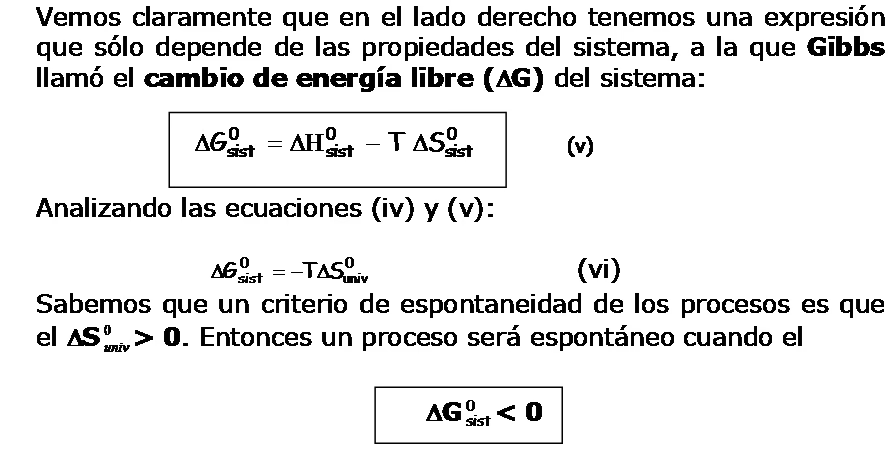
En su esencia, ΔG representa el cambio en la energía libre de un sistema cuando pasa de un estado inicial, como los reactivos, a un estado final, como los productos. Es una medida de la energía disponible en un sistema para realizar trabajo útil a temperatura y presión constantes. Si bien la segunda ley de la termodinámica establece que un proceso es espontáneo si el cambio en la entropía del universo (ΔSuniv) es positivo, calcular ΔSuniv es a menudo complejo, ya que implica considerar tanto el sistema como su entorno.
La genialidad de la Energía Libre de Gibbs radica en que nos proporciona un criterio de espontaneidad basado exclusivamente en las funciones de estado del sistema. Se define como:
Gsistema = Hsistema – T Ssistema
Donde H es la entalpía (el contenido de calor del sistema), T es la temperatura absoluta en Kelvin, y S es la entropía (el grado de desorden) del sistema. Dado que H, T y S son funciones de estado, G también lo es. Por lo tanto, para cualquier cambio de estado, el cambio en la energía libre de Gibbs se expresa como:
ΔGsistema = ΔHsistema – T ΔSsistema
Esta ecuación es el corazón de la termodinámica química y nos permite predecir la dirección de un cambio. La relación con la entropía del universo se establece al considerar que el cambio de entropía del entorno (ΔSentorno) es igual a -(ΔHsistema)/T. Al sustituir esto en la ecuación de ΔSuniv, se llega a que -TΔSuniv es igual a ΔG, confirmando que ΔG es un indicador directo de la espontaneidad.
Criterios de Espontaneidad: Interpretando ΔG
La clave para predecir si una reacción o proceso ocurrirá de forma natural reside en el signo de ΔG a temperatura y presión constantes:
- Si ΔG < 0: El proceso es espontáneo tal como está escrito. Esto significa que ocurrirá sin necesidad de un aporte externo continuo de energía.
- Si ΔG = 0: El sistema está en equilibrio. No hay un cambio neto, y las velocidades de las reacciones directa e inversa son iguales.
- Si ΔG > 0: El proceso no es espontáneo tal como está escrito. Sin embargo, el proceso inverso será espontáneo.
Consideremos un ejemplo clásico: la vaporización del agua. A 100°C (373.15 K) y 1 atm, el agua líquida y el vapor de agua están en equilibrio. En estas condiciones, ΔG para la vaporización es 0 J. Esto se debe a que la energía requerida para la vaporización (entalpía, ΔH positiva) se compensa exactamente con el aumento de la entropía del sistema (TΔS positiva). Por encima de 100°C, por ejemplo, a 110°C, el término TΔS se vuelve mayor que ΔH, lo que resulta en un ΔG negativo, indicando que la vaporización es espontánea e irreversible. Por el contrario, por debajo de 100°C, como a 90°C, el término ΔH domina, haciendo que ΔG sea positivo, lo que significa que el agua no se vaporiza espontáneamente, sino que el vapor de agua se condensaría espontáneamente a líquido.
Factores que Influyen en ΔG: Entalpía vs. Entropía
La espontaneidad de una reacción es un delicado equilibrio entre el cambio de entalpía (ΔH) y el cambio de entropía (TΔS). Estos dos términos pueden favorecer o desfavorecer la espontaneidad de diferentes maneras:
Las reacciones pueden ser:
- Impulsadas por la Entalpía: Son reacciones exotérmicas (ΔH < 0), que liberan calor y, por lo tanto, tienden a ser espontáneas.
- Impulsadas por la Entropía: Son reacciones que aumentan el desorden del sistema (ΔS > 0), lo que favorece la espontaneidad, especialmente a altas temperaturas.
La siguiente tabla resume cómo las combinaciones de ΔH y ΔS afectan la espontaneidad de una reacción:
| ΔH | ΔS | -TΔS (Contribución a ΔG) | ΔG | Espontaneidad |
|---|---|---|---|---|
| - (exotérmico) | + (productos más desordenados) | - (favorece espontaneidad) | - | Espontáneo a todas las T |
| - (exotérmico) | - (productos menos desordenados) | + (se opone a espontaneidad) | - a baja T, + a alta T | Espontáneo a baja T, No espontáneo a alta T |
| + (endotérmico) | + (productos más desordenados) | - (favorece espontaneidad) | + a baja T, - a alta T | No espontáneo a baja T, Espontáneo a alta T |
| + (endotérmico) | - (productos menos desordenados) | + (se opone a espontaneidad) | + | No espontáneo a todas las T |
ΔG y el Trabajo Útil: La Eficiencia Energética
Una de las implicaciones más fascinantes de la Energía Libre de Gibbs es su relación directa con el trabajo. El cambio en la energía de Gibbs es igual a la cantidad máxima de trabajo que un sistema puede realizar sobre su entorno durante un cambio espontáneo a temperatura y presión constantes. Esto se expresa como:
ΔG = wmax
Esta ecuación nos dice que cuando la energía se libera en un proceso exotérmico (ΔH < 0), como la combustión de un combustible, parte de esa energía puede usarse para realizar trabajo (ΔG < 0), mientras que otra parte se utiliza para aumentar la entropía del universo (TΔS > 0). Es crucial entender que, debido a que ningún sistema real es perfectamente reversible, la entropía del universo siempre aumenta durante los procesos que producen energía. Como resultado, ningún proceso que utilice energía almacenada puede ser 100% eficiente; es decir, ΔH nunca será igual a ΔG porque ΔS siempre tendrá un valor positivo en procesos reales.
La eficiencia de la conversión de energía varía enormemente entre diferentes dispositivos y procesos. Por ejemplo:
| Dispositivo/Proceso | Conversión de Energía | Eficiencia Aproximada (%) |
|---|---|---|
| Generador eléctrico grande | Mecánica → Eléctrica | 99 |
| Batería química | Química → Eléctrica | 90 |
| Horno doméstico | Química → Calor | 65 |
| Herramienta eléctrica pequeña | Eléctrica → Mecánica | 60 |
| Motor de transbordador espacial | Química → Mecánica | 50 |
| Célula hepática de mamífero | Química → Química | 30–50 |
| Motor de combustión interna | Química → Mecánica | 25–30 |
| Bombilla incandescente | Eléctrica → Luz | 5 |
Maximizar la eficiencia es uno de los mayores desafíos para los ingenieros y científicos en el diseño de nuevas tecnologías.

Variación Estándar de Energía Libre (ΔG°)
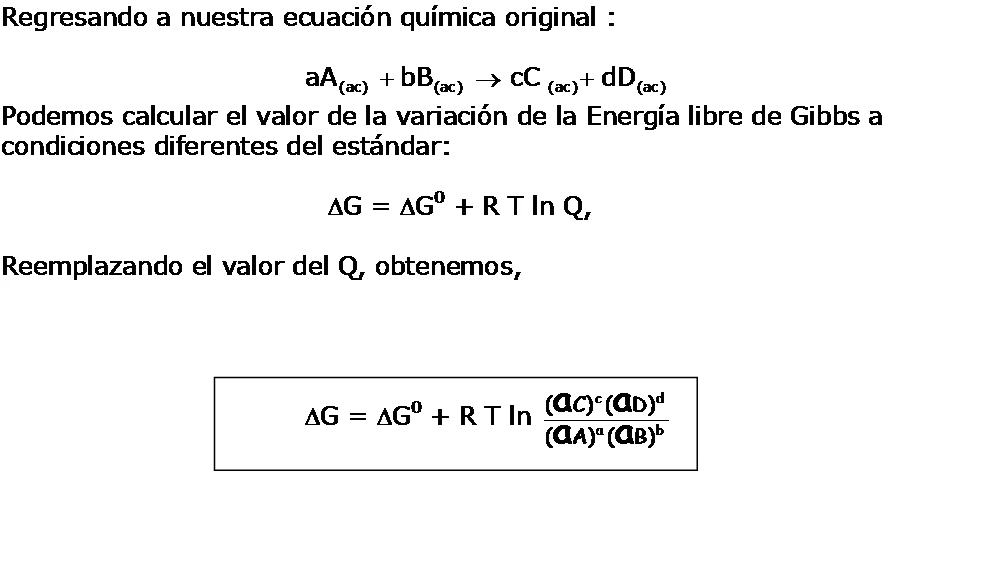
Así como no podemos medir entalpías absolutas, tampoco podemos medir energías libres absolutas, solo cambios en la energía libre. El cambio de energía libre estándar (ΔG°) es el cambio en la energía libre cuando una sustancia o un conjunto de sustancias en sus estados estándar se convierte en una o más sustancias, también en sus estados estándar. Las condiciones estándar generalmente se refieren a 25°C (298.15 K) y 1 atmósfera de presión para gases, o concentraciones de 1 M para soluciones.
ΔG° se puede calcular a partir de la entalpía estándar (ΔH°) y la entropía estándar (ΔS°) utilizando la ecuación:
ΔG° = ΔH° – TΔS°
Además, ΔG° para una reacción también se puede calcular a partir de los valores de la energía libre estándar de formación (ΔG°f) de los productos y reactivos. La ΔG°f de un compuesto es el cambio en la energía libre que ocurre cuando 1 mol de una sustancia en su estado estándar se forma a partir de sus elementos componentes en sus estados estándar. Por definición, la ΔG°f de un elemento en su estado estándar es cero. La regla es análoga a la de la entalpía de formación:
ΔG°reacción = ΣmΔG°f(productos) – ΣnΔG°f(reactivos)
Donde m y n son los coeficientes estequiométricos de cada producto y reactivo en la ecuación química balanceada. Un valor muy negativo de ΔG° indica una fuerte tendencia a que los productos se formen espontáneamente a partir de los reactivos en condiciones estándar. Sin embargo, es vital recordar que un ΔG° negativo no implica necesariamente que la reacción ocurrirá rápidamente; para eso, necesitamos evaluar la cinética de la reacción.
ΔG en Condiciones No Estándar y el Efecto de la Temperatura
Si bien ΔG° es útil para predecir la espontaneidad en condiciones estándar, muy pocas reacciones se llevan a cabo exactamente bajo estas condiciones. Lo que realmente determina si una reacción ocurrirá espontáneamente es el cambio de energía libre (ΔG) bajo las condiciones experimentales reales. Si los términos ΔH y TΔS de una reacción tienen el mismo signo, es posible revertir el signo de ΔG simplemente cambiando la temperatura. Esto puede transformar una reacción no espontánea en espontánea, o viceversa.
Por ejemplo, en la síntesis de amoníaco (N2(g) + 3H2(g) ↔ 2NH3(g)), tanto ΔH° como ΔS° son negativos. Esto significa que la reacción es espontánea a bajas temperaturas, pero se vuelve no espontánea a altas temperaturas. Esto presenta un conflicto clásico entre la termodinámica (que favorece bajas temperaturas para la espontaneidad) y la cinética (que requiere altas temperaturas para una velocidad de reacción aceptable). Los ingenieros químicos deben encontrar un equilibrio óptimo, a menudo utilizando catalizadores para acelerar la reacción a temperaturas donde la termodinámica aún es favorable.
La temperatura a la que una reacción cambia de espontánea a no espontánea (es decir, donde ΔG = 0) se puede calcular estableciendo ΔG = 0 en la ecuación y resolviendo para T:
T = ΔH° / ΔS°
Aplicaciones de la Energía Libre de Gibbs en la Vida Real
La Energía Libre de Gibbs no es solo un concepto teórico; tiene aplicaciones prácticas en muchos campos:
- Ingeniería Química: Para optimizar las condiciones de reacción en procesos industriales, como la producción de productos químicos, polímeros y fármacos.
- Materiales: Para predecir la estabilidad y la formación de nuevos materiales.
- Bioquímica y Medicina: Para comprender los procesos metabólicos y las reacciones biológicas que tienen lugar en el cuerpo humano. Por ejemplo, en la síntesis de proteínas, ΔG mide la espontaneidad de la unión de aminoácidos para formar una cadena polipeptídica. En la respiración celular, ΔG cuantifica la energía liberada cuando los nutrientes se oxidan para producir ATP, la principal fuente de energía celular.
- Ciencias Ambientales: Para analizar la viabilidad de reacciones de remediación o la formación de contaminantes.
Preguntas Frecuentes sobre la Energía Libre de Gibbs
¿Qué significa un ΔG negativo?
Un ΔG negativo significa que un proceso o reacción es espontáneo bajo las condiciones dadas. Esto implica que el proceso ocurrirá por sí mismo sin la necesidad de un aporte continuo de energía externa, liberando energía útil que puede ser convertida en trabajo.
¿Qué significa un ΔG positivo?
Un ΔG positivo indica que un proceso o reacción no es espontáneo bajo las condiciones dadas. Para que ocurra, requeriría un aporte continuo de energía externa. Sin embargo, el proceso inverso (es decir, de productos a reactivos) sería espontáneo.
¿Qué significa un ΔG igual a cero?
Cuando ΔG es igual a cero, el sistema está en equilibrio. Esto significa que no hay un cambio neto en las concentraciones de reactivos y productos, y las velocidades de las reacciones directa e inversa son iguales. Un sistema en equilibrio no realizará trabajo útil.
¿La Energía Libre de Gibbs predice la velocidad de una reacción?
No, la Energía Libre de Gibbs (ΔG) predice la espontaneidad o la viabilidad termodinámica de una reacción, es decir, si es posible que ocurra. No proporciona ninguna información sobre la velocidad a la que ocurrirá esa reacción. La velocidad de una reacción es estudiada por la cinética química, que considera factores como la energía de activación y la presencia de catalizadores.
¿Cuál es la diferencia entre ΔG y ΔG°?
ΔG (cambio de energía libre) se refiere al cambio de energía libre bajo cualquier condición de temperatura, presión y concentración. ΔG° (cambio de energía libre estándar) se refiere al cambio de energía libre bajo condiciones estándar específicas (25°C, 1 atm de presión para gases, 1 M de concentración para soluciones). ΔG° es un valor fijo para una reacción dada, mientras que ΔG puede variar dependiendo de las condiciones reales del experimento.
Conclusión
La Energía Libre de Gibbs es una herramienta indispensable en la termodinámica, proporcionando una comprensión profunda de la espontaneidad de los procesos y su capacidad para realizar trabajo. Al integrar la entalpía y la entropía, ΔG nos permite predecir la dirección de las reacciones y diseñar sistemas más eficientes, desde motores hasta procesos biológicos. Comprender ΔG es, en última instancia, comprender los principios fundamentales que rigen el flujo de energía y el cambio en nuestro universo.
Si quieres conocer otros artículos parecidos a La Energía Libre de Gibbs: Clave de la Espontaneidad puedes visitar la categoría Cálculos.
