16/02/2024
En el vasto universo de la materia, desde las moléculas más simples que componen el aire que respiramos hasta los complejos núcleos atómicos que residen en el corazón de las estrellas, existe una fuerza fundamental que mantiene todo unido: la energía de enlace. Esta energía es la manifestación de la estabilidad y la cohesión, un concepto central tanto en la química como en la física nuclear. Comprender la energía de enlace nos permite desentrañar por qué ciertas sustancias son estables, cómo ocurren las reacciones químicas y cómo se libera una inmensa cantidad de energía en los procesos nucleares. Acompáñanos en este profundo viaje para explorar qué es la energía de enlace, cómo se calcula y se mide, y su impacto en nuestro mundo.

- ¿Qué es la Energía de Enlace Química?
- ¿Cómo se Mide y Calcula la Energía de Enlace Química?
- Más Allá de los Enlaces Químicos: La Energía de Enlace Nuclear
- Diferencias Clave entre Energía de Enlace Química y Nuclear
- Preguntas Frecuentes (FAQ)
- ¿Por qué las energías de enlace químicas son valores promedio?
- ¿Qué indica una alta energía de enlace?
- ¿Cuál es la diferencia entre entalpía de enlace y energía de disociación de enlace?
- ¿La longitud de enlace afecta la energía de enlace?
- ¿Por qué la energía de enlace nuclear es tan superior a la química?
- Conclusión
¿Qué es la Energía de Enlace Química?
La energía de enlace química es una medida de la fuerza de un enlace químico particular. En términos sencillos, representa la cantidad de energía necesaria para romper un tipo específico de enlace en un mol de moléculas en estado gaseoso. Alternativamente, también puede verse como la energía liberada cuando se forma un mol de ese enlace a partir de sus átomos o fragmentos constituyentes en estado gaseoso. Cuanto mayor sea la energía de enlace, más fuerte y estable será el enlace.
Las energías de enlace se expresan comúnmente en unidades de kilojulios por mol (kJ/mol). Es crucial entender que, en la mayoría de los casos, los valores tabulados de energía de enlace son promedios. Esto se debe a que la energía requerida para romper un enlace específico (por ejemplo, un enlace O-H) puede variar ligeramente dependiendo de la molécula en la que se encuentre y de los otros enlaces presentes. Por ejemplo, en una molécula de agua (H2O), romper el primer enlace O-H requiere una cantidad de energía (energía de disociación de enlace) diferente a la requerida para romper el segundo enlace O-H en el ion hidróxido restante (OH-). La energía de enlace promedio para el O-H en agua se calcula como el promedio de estas energías de disociación sucesivas.
Existen diferentes tipos de enlaces químicos, cada uno con sus propias características de energía:
- Enlaces Covalentes: Se forman por el compartimiento de electrones entre átomos. Son los más comunes en la química orgánica e inorgánica.
- Enlaces Iónicos: Resultan de la transferencia de electrones entre átomos, formando iones con cargas opuestas que se atraen electrostáticamente.
- Enlaces Metálicos: Característicos de los metales, donde los electrones de valencia están deslocalizados en una 'nube' que mantiene unidos a los iones metálicos.
Es importante distinguir la energía de enlace de las fuerzas intermoleculares, como los puentes de hidrógeno o las fuerzas de Van der Waals (dipolo-dipolo, dispersión de London). Aunque estas últimas también implican atracción entre moléculas, son significativamente más débiles que los enlaces químicos verdaderos y requieren mucha menos energía para romperse.
¿Cómo se Mide y Calcula la Energía de Enlace Química?
La energía de enlace se mide experimentalmente determinando el calor (o entalpía) necesario para romper un mol de moléculas en sus átomos constituyentes. Este proceso se realiza típicamente en fase gaseosa para evitar complicaciones por interacciones intermoleculares. La energía de enlace es, en esencia, una medida de la estabilidad ganada cuando dos átomos se unen, en contraste con sus estados libres o no unidos.
Entalpía y Energía de Enlace
La entalpía (H) es una medida del contenido de calor de un sistema termodinámico bajo condiciones de presión constante. El cambio en la entalpía (ΔH) es una cantidad muy útil en química, ya que describe la transferencia de energía durante procesos químicos o físicos. Romper un enlace es un proceso que requiere la entrada de energía, lo que lo convierte en un proceso endotérmico (ΔH positivo). Por el contrario, la formación de un enlace libera energía, siendo un proceso exotérmico (ΔH negativo).
La energía de enlace se puede estimar a partir del cambio de entalpía (ΔH) de una reacción. Si en una reacción se rompe un enlace, la energía de enlace de ese enlace sería igual al cambio de entalpía de la reacción dividido por el número de moles de enlaces rotos. Sin embargo, como se mencionó, los valores tabulados son promedios de las energías de disociación de enlace (BDE). La energía de disociación de enlace es el cambio de entalpía estándar cuando un enlace covalente se rompe por homólisis (división simétrica del enlace) a 0 K.
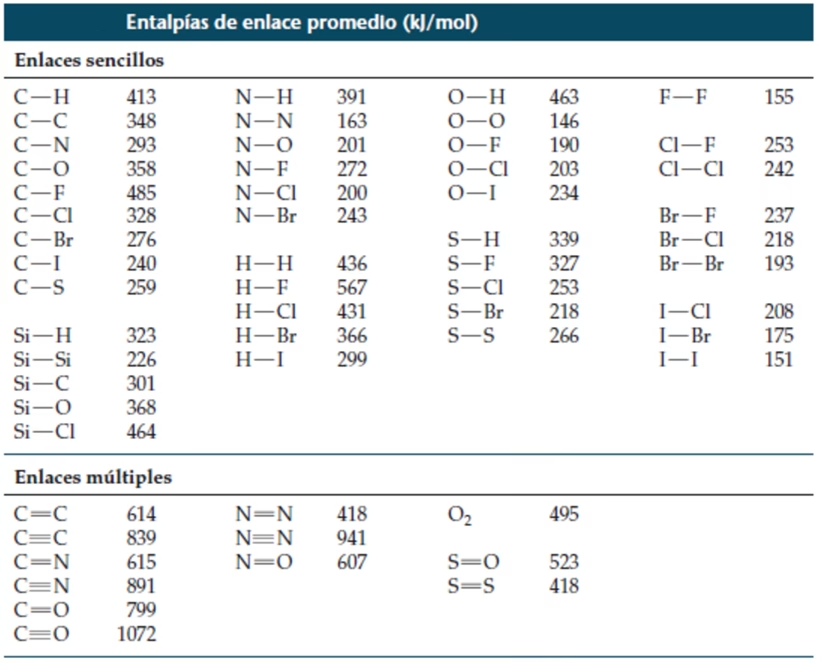
Por ejemplo, consideremos el agua (H2O):
- H-O-H(g) → H-O(g) + H(g) ΔH = 493 kJ/mol (primera disociación)
- H-O(g) → O(g) + H(g) ΔH = 424 kJ/mol (segunda disociación)
La energía de enlace promedio del enlace O-H en agua es (493 + 424) / 2 = 458.5 kJ/mol.
La Curva de Morse y la Longitud de Enlace
La relación entre la energía y la distancia internuclear entre dos átomos se representa gráficamente en una curva de Morse. Esta curva revela que:
- A grandes distancias, la energía es cero, indicando que no hay interacción entre los átomos.
- A medida que los átomos se acercan, las fuerzas atractivas dominan, y la energía disminuye hasta alcanzar un mínimo. Este punto de mínima energía corresponde a la distancia de enlace de equilibrio, también conocida como longitud de enlace.
- Si los átomos se acercan demasiado (a distancias muy pequeñas), las fuerzas repulsivas (entre núcleos y entre nubes electrónicas) se vuelven dominantes, y la energía del sistema aumenta drásticamente.
La longitud de enlace es la distancia promedio entre los núcleos de dos átomos unidos en una molécula. Se determina experimentalmente mediante técnicas como la difracción de rayos X en cristales moleculares o métodos espectroscópicos. Los enlaces no son estructuras estáticas; los átomos vibran constantemente alrededor de su posición de equilibrio debido a la energía térmica. La longitud de enlace medida es el promedio de esta distancia vibratoria.
Las longitudes de enlace suelen estar en el rango de 100-200 picómetros (pm) o 1-2 Ångstroms (Å). Existe una relación inversa general entre la fuerza del enlace (energía de enlace) y la longitud del enlace: a mayor energía de enlace, más fuerte es el enlace y, por lo general, más corta es la longitud de enlace. Esto es evidente en los enlaces múltiples: un enlace triple es más fuerte y más corto que un enlace doble, y este a su vez es más fuerte y más corto que un enlace simple.
Tabla 1: Comparación de Longitudes y Energías de Enlace (Ejemplos Típicos)
| Tipo de Enlace | Longitud Típica (pm) | Energía de Enlace Típica (kJ/mol) | Comentarios |
|---|---|---|---|
| C-C (simple) | 154 | 348 | Enlace fundamental en compuestos orgánicos |
| C=C (doble) | 133 | 614 | Más corto y fuerte que el simple C-C |
| C≡C (triple) | 120 | 839 | El más corto y fuerte de los enlaces C-C |
| O-H | 96 | 463 | Presente en agua, alcoholes, ácidos |
| C-H | 109 | 413 | Enlace muy común en hidrocarburos |
| N≡N | 110 | 945 | Muy fuerte, responsable de la inercia del N2 |
Más Allá de los Enlaces Químicos: La Energía de Enlace Nuclear
Mientras que la energía de enlace química se refiere a las fuerzas que mantienen unidos a los átomos para formar moléculas, la energía de enlace nuclear opera a una escala mucho más fundamental, dentro del núcleo atómico. Es la energía que mantiene unidos a los protones y neutrones (colectivamente llamados nucleones) dentro del núcleo, superando las potentes fuerzas de repulsión eléctrica entre los protones cargados positivamente.
¿Qué es la Energía de Enlace Nuclear?
La energía de enlace nuclear es la energía requerida para desmantelar un núcleo atómico en sus nucleones constituyentes (protones y neutrones), separándolos a una distancia tal que la fuerza nuclear fuerte ya no actúe entre ellos. Alternativamente, es la energía liberada cuando los nucleones se unen para formar un núcleo.
A diferencia de los enlaces químicos que se basan en interacciones electromagnéticas, la energía de enlace nuclear deriva de la fuerza nuclear fuerte (o interacción fuerte residual), que es la más poderosa de las cuatro fuerzas fundamentales de la naturaleza. Esta fuerza es de corto alcance, lo que explica por qué solo actúa dentro del diminuto espacio del núcleo.

El Misterio del Defecto de Masa
Uno de los conceptos más fascinantes y cruciales para entender la energía de enlace nuclear es el defecto de masa. Clásicamente, esperaríamos que la masa de un núcleo fuera simplemente la suma de las masas de sus protones y neutrones individuales. Sin embargo, las mediciones experimentales revelan que la masa de un núcleo atómico unido es siempre menor que la suma de las masas de sus nucleones libres. Esta 'pérdida' de masa se conoce como defecto de masa (ΔM).
Esta aparente contradicción se resuelve gracias a la famosa ecuación de Albert Einstein, E = mc², que establece la equivalencia entre masa y energía. La masa perdida (el defecto de masa) no desaparece, sino que se convierte en la inmensa cantidad de energía de enlace que mantiene unido al núcleo. Esta energía es liberada durante la formación del núcleo, típicamente en forma de fotones (radiación gamma) o energía cinética de otras partículas.
El defecto de masa se calcula como:
ΔM = (Suma de las masas de los protones y neutrones individuales) - (Masa medida del núcleo)
Una vez que se ha calculado el defecto de masa, la energía de enlace nuclear (Eb) se determina utilizando la ecuación de Einstein:
Eb = ΔM × c²
Donde 'c' es la velocidad de la luz en el vacío. Debido a que 'c' es un número muy grande (aproximadamente 3 x 108 m/s), incluso una pequeña cantidad de masa convertida (un defecto de masa diminuto) resulta en una cantidad gigantesca de energía liberada. Esta es la razón por la cual las reacciones nucleares (como la fisión y la fusión) liberan millones de veces más energía que las reacciones químicas.
La validez de E = mc² y su relación con la energía de enlace nuclear ha sido confirmada experimentalmente con una precisión asombrosa. Por ejemplo, en 2005, Rainville y colaboradores realizaron una prueba directa al comparar el cambio de masa en la energía de enlace de un neutrón a átomos de isótopos específicos de silicio y azufre con la energía del rayo gamma emitido durante la captura de neutrones. La concordancia fue de ±0.00004%, la prueba más precisa de E = mc² hasta la fecha.
Analogía de la Energía de Enlace Nuclear
Para entender mejor el concepto de energía de enlace, podemos usar una analogía gravitacional. Imagina dos objetos que se atraen mutuamente en el espacio debido a su campo gravitatorio. A medida que se acercan, ganan velocidad (energía cinética) a expensas de su energía potencial gravitatoria. Si nada los detiene, simplemente pasarían uno al lado del otro o rebotarían elásticamente. Para que se 'unan' y formen un objeto sólido, la energía cinética que adquirieron debe disiparse, por ejemplo, en forma de calor o luz (como ocurre en una colisión inelástica). Una vez que esta energía se ha disipado, los objetos quedan 'ligados' y vibrarán alrededor de una posición de equilibrio. La energía que fue liberada durante la unión es la energía de enlace: la energía que se necesitaría para volver a separarlos.
En el contexto nuclear, los nucleones se atraen fuertemente. Cuando se unen para formar un núcleo, liberan una cantidad de energía equivalente a su defecto de masa. Si esta energía no se libera, el sistema permanecería en un estado de mayor energía y no estaría ligado de manera estable. Una vez que la energía se irradia fuera del sistema (por ejemplo, como radiación gamma), el núcleo resultante tiene una masa menor que la suma de sus componentes individuales y es un sistema establemente ligado.
Diferencias Clave entre Energía de Enlace Química y Nuclear
Aunque ambos conceptos describen la energía que mantiene unidas a las partículas, existen diferencias fundamentales:
| Característica | Energía de Enlace Química | Energía de Enlace Nuclear |
|---|---|---|
| Partículas Involucradas | Átomos (a través de electrones de valencia) | Protones y neutrones (nucleones) |
| Fuerza Fundamental | Interacción electromagnética | Fuerza nuclear fuerte |
| Magnitud de Energía | Kilojulios por mol (kJ/mol), del orden de 100-1000 kJ/mol | Megaelectronvoltios (MeV) por nucleón, del orden de millones de kJ/mol (1 MeV ≈ 1.6 x 10-13 J) |
| Origen de la Energía | Reorganización de electrones, liberación/absorción de calor | Conversión de masa en energía (defecto de masa) según E=mc² |
| Procesos Asociados | Reacciones químicas (combustión, neutralización) | Fisión nuclear, fusión nuclear, decaimiento radiactivo |
Preguntas Frecuentes (FAQ)
¿Por qué las energías de enlace químicas son valores promedio?
Los valores de energía de enlace se presentan como promedios porque la energía necesaria para romper un enlace específico (energía de disociación de enlace) puede variar ligeramente dependiendo del entorno químico de ese enlace dentro de una molécula. Por ejemplo, el enlace C-H en el metano (CH4) no requiere exactamente la misma energía para romperse que el enlace C-H en una molécula de etano (C2H6), o incluso el segundo o tercer enlace C-H en la misma molécula de metano después de que los primeros se hayan roto. Los valores promedio ofrecen una estimación útil para cálculos termoquímicos generales.
¿Qué indica una alta energía de enlace?
Una alta energía de enlace indica un enlace químico o nuclear muy fuerte y estable. Esto significa que se requiere una gran cantidad de energía para romper ese enlace, o que se libera una gran cantidad de energía cuando se forma. En química, los enlaces con alta energía son menos reactivos y contribuyen a la estabilidad de las moléculas. En física nuclear, una alta energía de enlace por nucleón indica un núcleo muy estable.
¿Cuál es la diferencia entre entalpía de enlace y energía de disociación de enlace?
La entalpía de enlace (o simplemente energía de enlace) se refiere al valor promedio de la energía requerida para romper un tipo específico de enlace en un mol de moléculas gaseosas. Por otro lado, la energía de disociación de enlace (BDE) es la energía precisa requerida para romper un enlace particular en una molécula específica. La entalpía de enlace es una media de varias BDE para un tipo de enlace dado.
¿La longitud de enlace afecta la energía de enlace?
Sí, existe una relación directa. En general, cuanto más corta es la longitud de enlace entre dos átomos, mayor es la energía de enlace (es decir, el enlace es más fuerte). Esto se debe a que una distancia más corta permite una mayor superposición de orbitales o una atracción electrostática más intensa, lo que resulta en un enlace más estable y más difícil de romper.
¿Por qué la energía de enlace nuclear es tan superior a la química?
La energía de enlace nuclear es exponencialmente mayor que la química debido a la naturaleza de la fuerza que las rige y el principio de E=mc². Los enlaces químicos están gobernados por la fuerza electromagnética, que es relativamente débil en comparación con la fuerza nuclear fuerte que actúa dentro del núcleo. Además, la energía de enlace nuclear implica una conversión detectable de masa en energía (defecto de masa), un fenómeno que no ocurre en las reacciones químicas de manera medible con los equipos convencionales. Las reacciones nucleares liberan energía al transformar una pequeña fracción de la masa en energía pura, lo que resulta en magnitudes de energía millones de veces mayores que las liberadas en las reacciones químicas, que solo implican la reorganización de electrones.
Conclusión
La energía de enlace, ya sea en el ámbito químico que define la estructura y reactividad de las moléculas, o en el dominio nuclear que rige la estabilidad de los núcleos atómicos y las inmensas liberaciones de energía, es un concepto fundamental que subyace en la cohesión de la materia. Desde los enlaces covalentes que forman el agua hasta las fuerzas que impulsan el sol, la energía de enlace nos recuerda que la estabilidad y el cambio en el universo están intrínsecamente ligados a las interacciones energéticas a nivel más íntimo de la materia. Su comprensión no solo es vital para la ciencia básica, sino también para el desarrollo de tecnologías que van desde nuevos materiales hasta fuentes de energía sostenibles.
Si quieres conocer otros artículos parecidos a Energía de Enlace: La Fuerza que Une la Materia puedes visitar la categoría Cálculos.