13/07/2025
En el vasto universo de la química y la física, comprender por qué algunas reacciones ocurren de forma natural y otras no es fundamental. Aquí es donde entra en juego la Energía Libre de Gibbs, una de las herramientas más poderosas de la termodinámica. Esta magnitud nos permite predecir la espontaneidad de un proceso a temperatura y presión constantes, revelando si una transformación es energéticamente favorable o si requiere de un aporte externo para llevarse a cabo. La clave para desentrañar este misterio reside en una ecuación elegante que vincula la energía libre de Gibbs con otros conceptos termodinámicos vitales: la entalpía, la entropía y la temperatura.

La capacidad de predecir la dirección de un cambio es invaluable, no solo en un laboratorio, sino también en innumerables procesos naturales y aplicaciones industriales. Desde la corrosión de metales hasta la síntesis de nuevos materiales, pasando por los complejos mecanismos biológicos dentro de un ser vivo, la Energía Libre de Gibbs ofrece una perspectiva unificada sobre la viabilidad de estos fenómenos. A lo largo de este artículo, exploraremos en detalle la fórmula que define esta energía, desglosaremos cada uno de sus componentes y analizaremos cómo su valor final determina si un proceso será espontáneo o no.
- La Ecuación Fundamental de la Energía Libre de Gibbs
- Componentes Clave de la Ecuación de Gibbs
- La Espontaneidad de las Reacciones: ¿Cómo Interpretar ΔG?
- Interacción entre Entalpía, Entropía y Temperatura
- Aplicaciones Prácticas de la Energía Libre de Gibbs
- Preguntas Frecuentes sobre la Energía Libre de Gibbs
- Conclusión
La Ecuación Fundamental de la Energía Libre de Gibbs
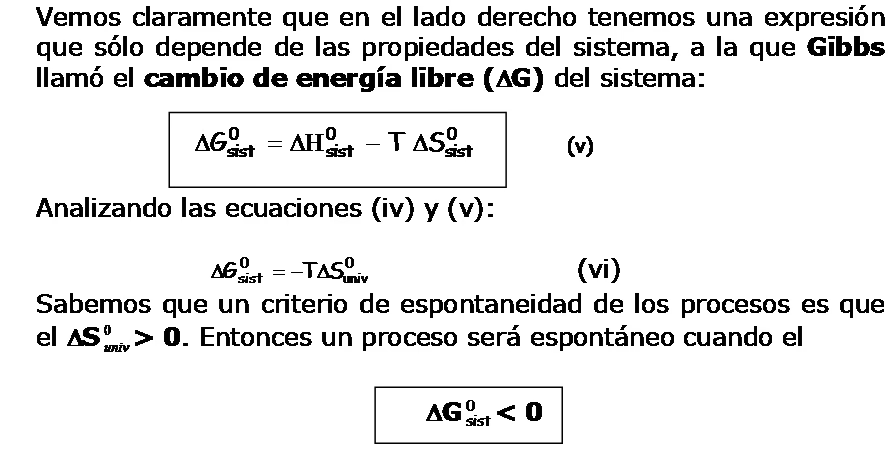
La relación que define la energía libre de Gibbs (ΔG) y que es central para nuestro entendimiento de la espontaneidad de los procesos es la siguiente:
ΔG = ΔH - TΔS
Esta ecuación, a menudo referida como la ecuación de Gibbs-Helmholtz, es una piedra angular en la termodinámica química. Nos proporciona una forma directa de calcular el cambio en la energía libre de un sistema cuando experimenta un proceso, considerando los cambios de calor y desorden, así como la temperatura a la que ocurre dicho proceso. Es crucial entender que esta ecuación se aplica específicamente a procesos que ocurren a temperatura y presión constantes, condiciones muy comunes en muchas reacciones químicas y biológicas.
Componentes Clave de la Ecuación de Gibbs
Para apreciar plenamente el significado de la Energía Libre de Gibbs, es imperativo comprender cada uno de los términos que componen su fórmula:
Cambio en la Energía Libre de Gibbs (ΔG)
El ΔG representa el cambio en la energía disponible para realizar trabajo útil en un sistema a temperatura y presión constantes. No es simplemente la energía total, sino la porción de energía de un sistema que está 'libre' para ser convertida en trabajo. Es el indicador definitivo de la espontaneidad de un proceso:
- Si ΔG es negativo (ΔG < 0), el proceso es espontáneo. Esto significa que puede ocurrir por sí mismo, sin necesidad de un aporte de energía externo.
- Si ΔG es positivo (ΔG > 0), el proceso es no espontáneo. Para que ocurra, se requiere un aporte continuo de energía del exterior.
- Si ΔG es cero (ΔG = 0), el sistema está en equilibrio. No hay una tendencia neta a que el proceso avance en una dirección u otra.
Cambio de Entalpía (ΔH)
La entalpía (H) es una medida del contenido total de calor de un sistema. El cambio de entalpía (ΔH) representa la cantidad de calor absorbido o liberado por un sistema durante un proceso a presión constante. Se mide en unidades de energía, como julios (J) o kilojulios (kJ).
- Si ΔH es negativo (ΔH < 0), la reacción es exotérmica. El sistema libera calor al entorno. Este es un factor que favorece la espontaneidad.
- Si ΔH es positivo (ΔH > 0), la reacción es endotérmica. El sistema absorbe calor del entorno. Este es un factor que desfavorece la espontaneidad, ya que requiere energía.
En términos sencillos, la entalpía nos dice si una reacción es 'caliente' o 'fría' desde el punto de vista del sistema, y cómo ese cambio de calor contribuye a la energía total del proceso.
Cambio de Entropía (ΔS)
La entropía (S) es una medida del desorden o la aleatoriedad de un sistema. El cambio de entropía (ΔS) indica cómo cambia el desorden durante un proceso. Se mide en unidades de energía por unidad de temperatura, como julios por Kelvin (J/K).
- Si ΔS es positivo (ΔS > 0), el desorden del sistema aumenta. Esto es un factor que favorece la espontaneidad, ya que los sistemas tienden naturalmente hacia un mayor desorden.
- Si ΔS es negativo (ΔS < 0), el desorden del sistema disminuye. Esto desfavorece la espontaneidad, ya que requiere un esfuerzo para organizar el sistema.
Piensa en la entropía como la tendencia de las cosas a dispersarse y mezclarse, como el gas que se expande para llenar un recipiente o un cubo de hielo que se derrite en agua líquida, aumentando su desorden.
Temperatura Absoluta (T)
La temperatura (T) en la ecuación de Gibbs es la temperatura absoluta del sistema, medida en Kelvin (K). Es crucial que la temperatura se utilice en la escala Kelvin porque esta escala no tiene valores negativos, lo que asegura que el término TΔS siempre contribuya de manera significativa y coherente al cálculo de ΔG.
La temperatura es un factor multiplicador para el término entrópico (TΔS). Esto significa que la influencia de la entropía en la espontaneidad de un proceso se vuelve más significativa a temperaturas más altas. A bajas temperaturas, el término entálpico (ΔH) tiende a dominar, mientras que a altas temperaturas, el término entrópico (TΔS) puede volverse el factor determinante.
La Espontaneidad de las Reacciones: ¿Cómo Interpretar ΔG?
La verdadera magia de la ecuación ΔG = ΔH - TΔS reside en su capacidad para predecir la espontaneidad de un proceso bajo condiciones específicas. El signo de ΔG es el criterio definitivo:
ΔG < 0 (Proceso Espontáneo): Cuando el cambio en la energía libre de Gibbs es negativo, el proceso es espontáneo y puede ocurrir sin la necesidad de un aporte de energía externo. Esto no significa que la reacción sea rápida; solo indica que es energéticamente favorable. Por ejemplo, la oxidación del hierro (formación de óxido) es espontánea, pero puede ser muy lenta.
ΔG > 0 (Proceso No Espontáneo): Si el cambio en la energía libre de Gibbs es positivo, el proceso no es espontáneo. Esto significa que para que ocurra, se debe suministrar energía continuamente desde el exterior. Un ejemplo sería la fotosíntesis en las plantas, que requiere la energía de la luz solar para convertir el dióxido de carbono y el agua en glucosa y oxígeno.
ΔG = 0 (Sistema en Equilibrio): Cuando el cambio en la energía libre de Gibbs es cero, el sistema ha alcanzado el equilibrio. En este punto, no hay una tendencia neta a que la reacción avance en la dirección de los productos ni de los reactivos. La velocidad de la reacción directa es igual a la velocidad de la reacción inversa.
Interacción entre Entalpía, Entropía y Temperatura
La belleza de la ecuación de Gibbs es que muestra cómo la entalpía y la entropía compiten o cooperan para determinar la espontaneidad, y cómo la temperatura influye en este equilibrio. A continuación, se presenta una tabla que resume las diferentes combinaciones de ΔH y ΔS y sus implicaciones para la espontaneidad a diferentes temperaturas:
| ΔH (Entalpía) | ΔS (Entropía) | Término TΔS | ΔG = ΔH - TΔS | Espontaneidad |
|---|---|---|---|---|
| Negativo (Exotérmico) | Positivo (Aumento de desorden) | Positivo | Siempre Negativo | Siempre Espontáneo |
| Positivo (Endotérmico) | Negativo (Disminución de desorden) | Negativo | Siempre Positivo | Siempre No Espontáneo |
| Negativo (Exotérmico) | Negativo (Disminución de desorden) | Negativo | Negativo a bajas T Positivo a altas T | Espontáneo a bajas T No espontáneo a altas T |
| Positivo (Endotérmico) | Positivo (Aumento de desorden) | Positivo | Positivo a bajas T Negativo a altas T | No espontáneo a bajas T Espontáneo a altas T |
Como se puede observar en la tabla, solo en dos casos extremos la espontaneidad es independiente de la temperatura: cuando la reacción es exotérmica y aumenta el desorden (siempre espontánea), o cuando es endotérmica y disminuye el desorden (siempre no espontánea). En los otros dos casos, la temperatura juega un papel crítico, determinando si el término entálpico o el entrópico domina y, por lo tanto, el signo final de ΔG.
Por ejemplo, la fusión del hielo a 0°C y 1 atm (ΔH > 0, ΔS > 0) es un proceso endotérmico que aumenta el desorden. A temperaturas por encima de 0°C, la fusión es espontánea (ΔG < 0), mientras que por debajo de 0°C es no espontánea (ΔG > 0), y a 0°C está en equilibrio (ΔG = 0).
Aplicaciones Prácticas de la Energía Libre de Gibbs
La comprensión de la Energía Libre de Gibbs no es meramente un ejercicio académico; tiene profundas implicaciones en una variedad de campos:
Química Industrial: Los ingenieros químicos utilizan ΔG para determinar las condiciones óptimas (temperatura y presión) para la síntesis de productos químicos. Permite predecir el rendimiento máximo posible de una reacción antes incluso de llevarla a cabo, ahorrando tiempo y recursos.
Biología y Bioquímica: En los sistemas biológicos, la Energía Libre de Gibbs es crucial para entender cómo las células obtienen energía de los nutrientes y cómo realizan funciones vitales. Procesos como la respiración celular, la fotosíntesis y la síntesis de proteínas son analizados en términos de sus cambios de ΔG. Las enzimas, por ejemplo, aceleran las reacciones espontáneas, pero no pueden hacer que una reacción no espontánea se vuelva espontánea.
Ciencia de Materiales: El diseño y la síntesis de nuevos materiales, desde polímeros hasta aleaciones metálicas, se basan en principios termodinámicos. ΔG ayuda a predecir la estabilidad de un material y las condiciones bajo las cuales puede formarse o degradarse.
Ciencias Ambientales: La comprensión de la espontaneidad es vital para estudiar la formación de contaminantes, la biodegradación de residuos o la viabilidad de procesos de remediación.
En esencia, la Energía Libre de Gibbs es una brújula que guía a científicos e ingenieros en la dirección de las transformaciones más eficientes y energéticamente favorables, permitiendo el desarrollo de tecnologías más sostenibles y procesos más eficaces.
Preguntas Frecuentes sobre la Energía Libre de Gibbs
¿La Energía Libre de Gibbs predice la velocidad de una reacción?
No, la Energía Libre de Gibbs (ΔG) solo predice la espontaneidad de una reacción, es decir, si es energéticamente posible que ocurra. No proporciona ninguna información sobre la velocidad a la que transcurrirá la reacción. Una reacción puede ser espontánea (ΔG < 0) pero extremadamente lenta (por ejemplo, la conversión de diamante a grafito). La velocidad de una reacción es estudiada por la cinética química, que considera factores como la energía de activación y la presencia de catalizadores.
¿Es posible que una reacción no espontánea ocurra?
Sí, una reacción no espontánea (ΔG > 0) puede ocurrir si se le suministra energía del exterior. Un ejemplo clásico es la electrólisis del agua, donde se utiliza energía eléctrica para descomponer el agua en hidrógeno y oxígeno, un proceso que no es espontáneo por sí mismo. En los sistemas biológicos, las reacciones no espontáneas a menudo se acoplan con reacciones altamente espontáneas (exergónicas) para impulsarlas.
¿Qué significa el término 'energía libre'?
El término 'energía libre' se refiere a la porción de la energía total de un sistema que está disponible para realizar trabajo útil a temperatura y presión constantes. No toda la energía de un sistema puede convertirse en trabajo; una parte siempre se pierde en forma de calor o se disipa debido al aumento del desorden (entropía). La energía libre de Gibbs es, por lo tanto, la energía máxima que puede extraerse de un sistema para realizar trabajo.
¿Por qué la temperatura debe estar en Kelvin?
La temperatura debe estar en Kelvin (escala absoluta) porque el término TΔS en la ecuación de Gibbs representa una contribución energética relacionada con la entropía. Si se usara una escala con valores negativos (como Celsius o Fahrenheit), el término TΔS podría volverse negativo a temperaturas bajas, lo que distorsionaría el significado físico de la entropía como una medida de desorden y su contribución energética. La escala Kelvin asegura que la temperatura siempre sea positiva, reflejando el hecho de que no puede haber una 'energía de desorden' negativa.
¿Cómo se relaciona la Energía Libre de Gibbs con el equilibrio químico?
Cuando ΔG = 0, el sistema está en equilibrio químico. Esto significa que las velocidades de la reacción directa e inversa son iguales, y no hay un cambio neto en las concentraciones de reactivos y productos. La Energía Libre de Gibbs también está relacionada con la constante de equilibrio (K) a través de la ecuación ΔG° = -RT ln K, donde ΔG° es el cambio de energía libre estándar, R es la constante de los gases y T es la temperatura absoluta. Esta ecuación muestra una conexión profunda entre la termodinámica y el equilibrio de las reacciones.
Conclusión
La Energía Libre de Gibbs y su fórmula fundamental, ΔG = ΔH - TΔS, es una herramienta indispensable en el estudio de las transformaciones químicas y físicas. Al integrar los conceptos de entalpía (cambio de calor), entropía (cambio de desorden) y temperatura, nos proporciona un criterio claro para determinar la espontaneidad de un proceso a presión y temperatura constantes. Comprender el signo de ΔG es crucial para predecir si una reacción ocurrirá de forma natural, requerirá energía externa o si ya ha alcanzado un estado de equilibrio.
Desde la optimización de procesos industriales hasta la comprensión de las complejidades de la vida celular, la Energía Libre de Gibbs es una demostración brillante de cómo los principios de la termodinámica nos permiten desentrañar los misterios del universo material, ofreciendo una base sólida para la innovación y el descubrimiento en diversas disciplinas científicas y de ingeniería.
Si quieres conocer otros artículos parecidos a La Fórmula de Gibbs: Entalpía, Entropía y Espontaneidad puedes visitar la categoría Cálculos.
