29/11/2024
La termodinámica, una rama fundamental de la física, nos permite desentrañar los misterios del comportamiento macroscópico de la materia. Dentro de este vasto campo, el concepto de trabajo realizado por un gas ocupa un lugar central, siendo crucial para entender desde el funcionamiento de un motor de combustión interna hasta el diseño de sistemas de refrigeración. La capacidad de cuantificar este trabajo no solo es una piedra angular en el estudio de la física, sino que también es una herramienta indispensable en diversas disciplinas de la ciencia y la ingeniería. Comprender cómo los gases transfieren y transforman energía nos brinda una perspectiva profunda sobre cómo la energía fluye y se utiliza en el universo, desde los sistemas más simples hasta las complejas máquinas que impulsan nuestra sociedad moderna.
El estudio del trabajo en un gas es una progresión lógica de los conceptos de presión y volumen, formando un trinomio inseparable que nos permite conectar leyes fundamentales como las de Boyle-Mariotte y Charles con resultados tangibles de transferencia de energía. Este conocimiento no solo es esencial para la academia, sino que sienta las bases para la comprensión de fenómenos más avanzados, como la conservación de la energía y los ciclos termodinámicos completos. Acompáñenos en este recorrido para desglosar el concepto de trabajo termodinámico, sus diferentes formas de cálculo y su representación visual.
- ¿Qué es el Trabajo Termodinámico en un Gas?
- Cálculo del Trabajo para Gases Ideales en Diferentes Procesos
- Diagramas Presión-Volumen (PV)
- Procesos Reversibles e Irreversibles
- Conceptos Clave y Leyes de la Termodinámica
- Tabla Comparativa de Fórmulas de Trabajo para Gases Ideales
- Ejemplos Prácticos de Cálculo del Trabajo
- Preguntas Frecuentes sobre el Trabajo de un Gas
- ¿Por qué el trabajo en un proceso isocórico es siempre cero?
- ¿Cuál es la diferencia entre trabajo realizado *por* el gas y trabajo realizado *sobre* el gas?
- ¿Por qué un proceso reversible produce el máximo trabajo (de expansión) o el mínimo trabajo (de compresión)?
- ¿Cómo se relaciona el trabajo con la energía interna de un gas ideal?
- ¿Qué significa el índice adiabático (γ)?
- Conclusión
¿Qué es el Trabajo Termodinámico en un Gas?
En el ámbito de la termodinámica, el trabajo es una forma de transferencia de energía que ocurre cuando una fuerza actúa sobre un sistema y provoca un desplazamiento. En el caso de un gas, esta fuerza es ejercida por la presión del gas sobre un límite móvil (como un pistón) o por el entorno sobre el gas. El trabajo termodinámico se define, de forma general, como el producto de la presión (P) y el cambio de volumen (ΔV) del gas. Si el gas se expande, realiza trabajo sobre su entorno; si se comprime, el entorno realiza trabajo sobre el gas.
Es crucial entender la convención de signos: el trabajo es positivo si se realiza sobre el gas (compresión, disminución de volumen) y negativo si es realizado por el gas (expansión, aumento de volumen). Esta convención es fundamental para la correcta aplicación de la Primera Ley de la Termodinámica, que relaciona el cambio en la energía interna de un sistema con el calor y el trabajo.
Cálculo del Trabajo para Gases Ideales en Diferentes Procesos
El cálculo del trabajo de un gas ideal varía significativamente dependiendo del tipo de proceso termodinámico que experimente. Un gas ideal es un modelo teórico que simplifica el comportamiento de los gases reales, asumiendo que sus partículas no interactúan entre sí excepto durante colisiones elásticas y que su volumen es despreciable. Aunque es una idealización, este modelo es extraordinariamente útil para comprender los principios fundamentales de la termodinámica.
Proceso Isobárico (Presión Constante)
Cuando un gas se expande o se comprime a presión constante, el cálculo del trabajo es directo. Este proceso se conoce como proceso isobárico. La fórmula es la siguiente:
W = P * ΔV = P * (Vf - Vi)
Donde:
Wes el trabajo realizado.Pes la presión constante.Vfes el volumen final.Vies el volumen inicial.
Si la expansión ocurre, Vf > Vi, y W será positivo si el trabajo se realiza sobre el gas (siguiendo la convención W = -PΔV para trabajo realizado *por* el gas), o negativo si se realiza *por* el gas. Manteniendo la convención de que W es trabajo *hecho sobre* el gas, una expansión (ΔV > 0) resultaría en W negativo. Para el trabajo *hecho por* el gas, simplemente se invierte el signo.
Proceso Isocórico (Volumen Constante)
En un proceso isocórico, el volumen del gas permanece constante (ΔV = 0). Dado que el trabajo termodinámico implica un cambio de volumen, si no hay cambio de volumen, no se realiza trabajo.
W = 0
Esto es intuitivo: si el gas no se expande ni se comprime, no hay desplazamiento contra una fuerza externa, por lo tanto, no hay trabajo.
Proceso Isotérmico (Temperatura Constante)
Cuando un gas ideal se expande o comprime a temperatura constante, el proceso se denomina isotérmico. En este caso, la presión y el volumen varían de tal manera que su producto permanece constante (P·V = constante, según la ley de Boyle-Mariotte). El cálculo del trabajo implica una integral, ya que la presión no es constante.
Para un proceso isotérmico reversible, el trabajo realizado por el gas se calcula como:
W = -nRT * ln(Vf/Vi)
O, si consideramos el trabajo realizado *sobre* el gas:
W = nRT * ln(Vi/Vf) = nRT * ln(P_f/P_i)
Donde:
nes el número de moles del gas.Res la constante de los gases ideales (8.314 J/(mol·K)).Tes la temperatura constante en Kelvin.lnes el logaritmo natural.VfyVison los volúmenes final e inicial.P_fyP_ison las presiones final e inicial.
Es importante notar que en algunos contextos, especialmente a nivel molecular, se puede encontrar la expresión W = N k_B T ln(Vf/Vi), donde N es el número de moléculas y k_B es la constante de Boltzmann (1.38 × 10^-23 J/K). Ambas fórmulas son equivalentes, ya que N k_B = n R.
Proceso Adiabático (Sin Intercambio de Calor)
En un proceso adiabático, no hay intercambio de calor entre el gas y su entorno (Q = 0). Si el gas se expande adiabáticamente, realiza trabajo y su energía interna disminuye, lo que se traduce en una caída de temperatura. Si se comprime adiabáticamente, el trabajo se realiza sobre el gas, su energía interna aumenta y su temperatura sube.
La relación entre presión y volumen en un proceso adiabático es P V^γ = constante, donde γ (gamma) es el índice adiabático (o relación de calores específicos, Cp/Cv), que es una propiedad del gas.

El trabajo realizado en un proceso adiabático para un gas ideal se puede calcular como:
W = (P2 * V2 - P1 * V1) / (1 - γ)
O, alternativamente, usando la relación P V = n R T:
W = nR (T2 - T1) / (1 - γ)
Donde:
P1, V1, T1son las condiciones iniciales.P2, V2, T2son las condiciones finales.γes el índice adiabático del gas.
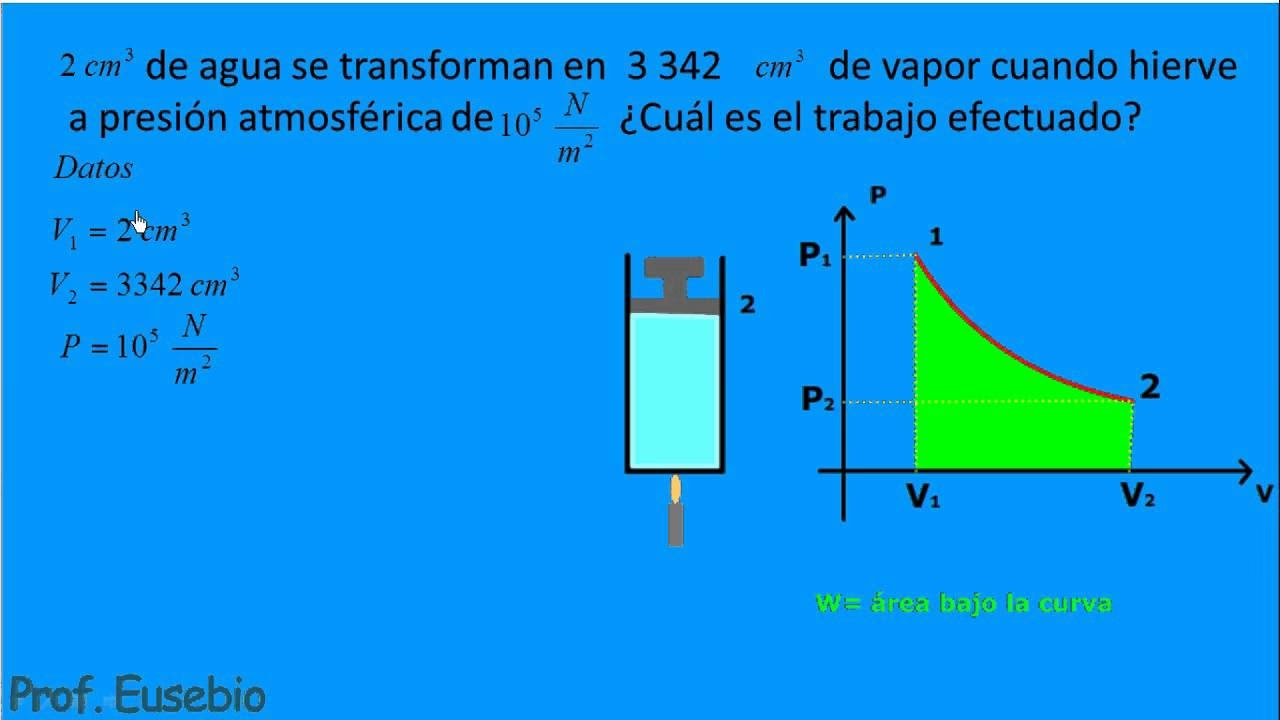
Diagramas Presión-Volumen (PV)
Los diagramas PV son herramientas gráficas extraordinariamente útiles para visualizar y analizar procesos termodinámicos en gases. En estos diagramas, la presión (P) se representa en el eje Y y el volumen (V) en el eje X. Cada punto en el diagrama corresponde a un estado termodinámico específico del gas (una combinación de P y V, y por ende, de T, según la ley de los gases ideales).
Una de las propiedades más importantes de los diagramas PV es que el trabajo realizado durante un proceso es igual al área bajo la curva del proceso. Si el proceso va de izquierda a derecha (expansión, aumento de volumen), el trabajo es realizado por el gas (W < 0). Si el proceso va de derecha a izquierda (compresión, disminución de volumen), el trabajo es realizado sobre el gas (W > 0). En un ciclo termodinámico (donde el gas regresa a su estado inicial), el trabajo neto es el área encerrada por el ciclo en el diagrama PV.
- En un proceso isobárico, la línea es horizontal. El área es un rectángulo.
- En un proceso isocórico, la línea es vertical. El área es cero, lo que confirma W=0.
- En un proceso isotérmico, la línea es una hipérbola (P = constante/V).
- En un proceso adiabático, la curva es más pronunciada que una isoterma, ya que la temperatura cambia.
Procesos Reversibles e Irreversibles
Una distinción fundamental en termodinámica es entre procesos reversibles e irreversibles. Esta clasificación es clave para entender el rendimiento máximo de los sistemas y la dirección natural de los procesos.
Proceso Reversible: Es un proceso idealizado que ocurre de manera tan lenta y gradual que el sistema y su entorno están siempre en equilibrio. Si el proceso se invierte, tanto el sistema como el entorno regresan a sus estados iniciales sin dejar ningún cambio neto en el universo. En un proceso reversible, el trabajo realizado por el gas (durante la expansión) es el máximo posible, y el trabajo realizado sobre el gas (durante la compresión) es el mínimo posible. Los cálculos de trabajo que hemos presentado (isotérmico, adiabático, etc.) generalmente se refieren a procesos reversibles.
Proceso Irreversible: La mayoría de los procesos que observamos en la naturaleza son irreversibles. Ocurren rápidamente y no permiten que el sistema y su entorno permanezcan en equilibrio. Ejemplos incluyen la expansión libre de un gas en el vacío, la transferencia de calor a través de una diferencia finita de temperatura, o la fricción. En un proceso irreversible, el trabajo realizado por el gas es siempre menor que el que se obtendría en un proceso reversible entre los mismos estados inicial y final. Esto se debe a que parte de la energía se disipa como calor o se pierde debido a factores como la fricción o la generación de entropía.
Conceptos Clave y Leyes de la Termodinámica
Para comprender plenamente el trabajo de un gas, es esencial contextualizarlo dentro de las leyes fundamentales de la termodinámica:
Primera Ley de la Termodinámica: Esta ley es una reafirmación del principio de conservación de la energía. Establece que el cambio en la energía interna (ΔU) de un sistema cerrado es igual al calor (Q) añadido al sistema más el trabajo (W) realizado sobre el sistema. Es decir:
ΔU = Q + W. Si el calor se retira del sistema o el trabajo es realizado *por* el sistema, estos valores son negativos. Es la ley más directamente relacionada con el cálculo del trabajo.Ley Cero de la Termodinámica: Establece que si dos sistemas están en equilibrio térmico con un tercero, entonces están en equilibrio térmico entre sí. Es fundamental para la definición de temperatura.
Segunda Ley de la Termodinámica: Puede enunciarse de varias maneras. Una de ellas es que el calor fluye espontáneamente de un objeto más caliente a uno más frío, y no al revés sin la intervención de trabajo. Otra formulación importante es que la entropía (o desorden) de un sistema aislado solo puede aumentar o permanecer constante, nunca disminuir. Esta ley impone límites a la eficiencia de los motores térmicos y a la dirección de los procesos naturales.
Tercera Ley de la Termodinámica: También conocida como Teorema de Nernst, establece que es imposible alcanzar el cero absoluto de temperatura (0 Kelvin o -273.15 °C) en un número finito de pasos. A medida que la temperatura se acerca al cero absoluto, la entropía de un sistema cristalino perfecto se aproxima a un valor mínimo constante.
Tabla Comparativa de Fórmulas de Trabajo para Gases Ideales
| Proceso Termodinámico | Condición Constante | Fórmula del Trabajo (W, hecho sobre el gas) | Características en Diagrama PV |
|---|---|---|---|
| Isobárico | Presión (P) | W = P * (Vf - Vi) | Línea horizontal |
| Isocórico | Volumen (V) | W = 0 | Línea vertical |
| Isotérmico (Reversible) | Temperatura (T) | W = nRT * ln(Vi/Vf) | Curva hiperbólica (isoterma) |
| Adiabático (Reversible) | Sin intercambio de calor (Q=0) | W = (P2*V2 - P1*V1) / (1 - γ) | Curva más pronunciada que la isoterma |
Ejemplos Prácticos de Cálculo del Trabajo
Ejemplo 1: Compresión Isobárica
Imagina un gas contenido en un cilindro, bajo una presión constante de 2 atmósferas. El cilindro se comprime desde un volumen inicial de 5 litros hasta un volumen final de 3 litros. Calcular el trabajo realizado sobre el gas.
Datos: P = 2 atm, Vi = 5 L, Vf = 3 L
Cálculo:W = P * (Vf - Vi)W = 2 atm * (3 L - 5 L)W = 2 atm * (-2 L)W = -4 atm·L
El signo negativo indica que el trabajo fue realizado *por* el gas (o, si se usa la convención de trabajo sobre el gas, el trabajo es -4 atm·L, lo que significa que el gas realizó trabajo negativo, es decir, el gas realizó trabajo). Si queremos el trabajo realizado *sobre* el gas, sería +4 atm·L. Para convertir a Joules, 1 atm·L = 101.325 J, entonces W = -4 * 101.325 J = -405.3 J.

Ejemplo 2: Expansión Reversible Isotérmica de un Gas Ideal
Un mol de un gas ideal a 300 K está contenido en un volumen de 4 litros. Luego se expande de manera reversible a un volumen final de 8 litros. Calcular el trabajo realizado por el gas.
Datos: n = 1 mol, T = 300 K, Vi = 4 L, Vf = 8 L, R = 8.314 J/(mol·K)
Cálculo (trabajo realizado por el gas):W_por_gas = nRT * ln(Vf/Vi)W_por_gas = (1 mol) * (8.314 J/(mol·K)) * (300 K) * ln(8 L / 4 L)W_por_gas = 2494.2 J * ln(2)W_por_gas = 2494.2 J * 0.693W_por_gas ≈ 1728.5 J
Si consideramos el trabajo realizado *sobre* el gas, sería W_sobre_gas = -1728.5 J.
Ejemplo 3: Expansión Adiabática y la Primera Ley
Un gas ideal experimenta una expansión adiabática, realizando 2000 julios de trabajo. ¿Cuánto cambia la energía interna del gas?
Datos: Q = 0 (proceso adiabático), W_por_gas = 2000 J. Si W es trabajo *sobre* el sistema, entonces W = -2000 J.
Aplicando la Primera Ley de la Termodinámica:ΔU = Q + WΔU = 0 + (-2000 J)ΔU = -2000 J
La energía interna del gas disminuye en 2000 julios, lo que es consistente con una expansión adiabática donde el gas realiza trabajo a expensas de su propia energía interna, lo que lleva a una disminución de su temperatura.
Preguntas Frecuentes sobre el Trabajo de un Gas
¿Por qué el trabajo en un proceso isocórico es siempre cero?
En un proceso isocórico, el volumen del gas permanece constante. La definición de trabajo termodinámico implica un cambio de volumen (W = PΔV). Si ΔV es cero, entonces el trabajo realizado es cero, ya que no hay desplazamiento del límite del sistema contra una fuerza externa.
¿Cuál es la diferencia entre trabajo realizado *por* el gas y trabajo realizado *sobre* el gas?
La diferencia radica en la dirección de la transferencia de energía y la convención de signos. Cuando un gas se expande, empuja contra su entorno y realiza trabajo *por* el gas. Este trabajo se considera negativo en la convención de la Primera Ley de la Termodinámica (ΔU = Q + W). Cuando el entorno comprime el gas, el trabajo se realiza *sobre* el gas, y este trabajo se considera positivo. Es vital ser consistente con la convención de signos utilizada.
¿Por qué un proceso reversible produce el máximo trabajo (de expansión) o el mínimo trabajo (de compresión)?
Un proceso reversible ocurre de manera idealmente lenta, permitiendo que el sistema esté siempre en equilibrio con su entorno. Esto significa que no hay pérdidas de energía debido a la fricción, turbulencia o gradientes de temperatura o presión finitos. Toda la energía transferida como trabajo es utilizada de la manera más eficiente posible. En contraste, en un proceso irreversible, parte de la energía se disipa (por ejemplo, como calor debido a la fricción), lo que reduce el trabajo útil que se puede obtener.
¿Cómo se relaciona el trabajo con la energía interna de un gas ideal?
Para un gas ideal, la energía interna (ΔU) depende únicamente de su temperatura. Según la Primera Ley de la Termodinámica (ΔU = Q + W), el trabajo realizado sobre o por el gas, junto con el calor transferido, determina el cambio en la energía interna. Por ejemplo, en un proceso adiabático (Q=0), todo el cambio en la energía interna se debe al trabajo (ΔU = W). Si el gas se expande (W negativo), su energía interna disminuye, y por lo tanto, su temperatura baja.
¿Qué significa el índice adiabático (γ)?
El índice adiabático (gamma) es la relación entre el calor específico molar a presión constante (Cp) y el calor específico molar a volumen constante (Cv) de un gas (γ = Cp/Cv). Es una propiedad importante de los gases que determina cómo se comportan en procesos adiabáticos. Su valor depende de la atomicidad del gas (monoatómico, diatómico, poliatómico), ya que afecta la forma en que el gas almacena energía interna.
Conclusión
El cálculo del trabajo en un gas ideal es un concepto central en la termodinámica que nos permite comprender cómo se transfiere la energía en sistemas gaseosos. Desde la sencilla relación W = PΔV para procesos isobáricos hasta las integrales complejas para procesos isotérmicos y adiabáticos, la capacidad de cuantificar el trabajo es esencial para el diseño y análisis de una vasta gama de aplicaciones tecnológicas, desde motores de combustión y refrigeradores hasta turbinas y compresores. Los diagramas PV, junto con la distinción entre procesos reversibles e irreversibles, proporcionan una comprensión visual y conceptual profunda de estos fenómenos. Dominar estos conceptos no solo enriquece nuestra comprensión del mundo físico, sino que también nos equipa con herramientas fundamentales para innovar en ingeniería y ciencia.
Si quieres conocer otros artículos parecidos a El Trabajo en Gases Ideales: Una Guía Completa puedes visitar la categoría Cálculos.
