07/11/2025
Cada célula de nuestro cuerpo es una pequeña batería, una unidad viva capaz de generar y responder a señales eléctricas. Esta capacidad es fundamental para funciones vitales como el pensamiento, el movimiento muscular y la regulación hormonal. El secreto detrás de esta actividad eléctrica reside en el 'potencial de membrana', una diferencia de voltaje a través de la delgada bicapa lipídica que envuelve cada célula. Comprender cómo se establece, se mantiene y se modifica este potencial es clave para entender la fisiología celular y las bases de muchas enfermedades. Acompáñanos en este fascinante viaje para desentrañar los mecanismos electroquímicos que rigen la vida celular.
- La Barrera Celular: Membrana Plasmática y Gradientes Iónicos
- El Potencial de Equilibrio Iónico: La Ecuación de Nernst
- El Potencial de Membrana en Reposo: Un Juego de Múltiples Iones
- El Potencial de Acción: El Impulso Eléctrico Celular
- Factores que Modifican el Potencial de Membrana: Implicaciones Prácticas
- Relevancia Clínica: Cuando el Potencial Falla
- Preguntas Frecuentes sobre el Potencial de Membrana
La Barrera Celular: Membrana Plasmática y Gradientes Iónicos
La membrana plasmática, una bicapa lipídica con proteínas incrustadas, actúa como una barrera selectiva entre el interior (citoplasma) y el exterior de la célula. Esta selectividad es crucial: la membrana es impermeable a la mayoría de las moléculas polares y a los iones, pero permite el paso controlado de algunos de ellos a través de proteínas especializadas llamadas canales iónicos y transportadores.
Gracias a esta permeabilidad diferencial y a la acción de bombas iónicas (como la bomba de sodio-potasio), existe una notable diferencia en la concentración de iones entre el medio intracelular y el extracelular. Los iones más relevantes para el potencial de membrana son el sodio (Na+), el potasio (K+), el calcio (Ca2+) y el cloro (Cl–). Observa sus concentraciones típicas en humanos:
| Ion | Concentración Intracelular (mM) | Concentración Extracelular (mM) |
|---|---|---|
| Na+ | 12 | 145 |
| K+ | 140 | 4 |
| Ca++ | 100 nM (0.0001) | 1.5 |
| Cl– | 4.2 | 123 |
Esta distribución desigual de iones crea un gradiente de concentración que impulsa a los iones a moverse a través de la membrana si esta es permeable. Sin embargo, como los iones tienen carga eléctrica, su movimiento también genera un gradiente eléctrico. El equilibrio entre estas dos fuerzas (química y eléctrica) es lo que define el potencial de membrana.
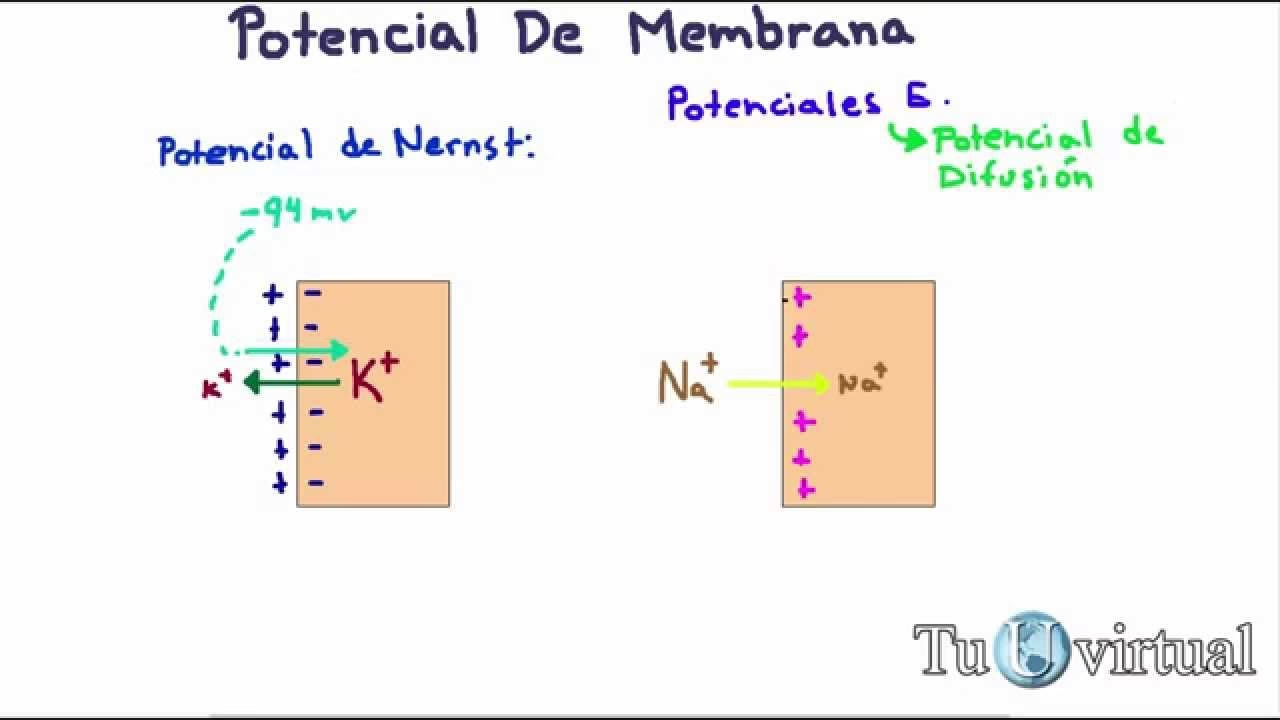
El Potencial de Equilibrio Iónico: La Ecuación de Nernst
Para comprender el potencial de membrana, primero debemos entender el 'potencial de equilibrio' para un solo ion. Imagina una membrana permeable exclusivamente a un tipo de ion, por ejemplo, el Na+. Inicialmente, el Na+ tenderá a moverse desde donde hay más (exterior) hacia donde hay menos (interior) siguiendo su gradiente de concentración. A medida que los iones Na+ cargados positivamente se mueven hacia el interior, el exterior se vuelve más negativo y el interior más positivo. Esta acumulación de cargas opuestas crea un campo eléctrico que se opone al movimiento adicional de Na+. Eventualmente, se alcanzará un punto en el que la fuerza eléctrica que impulsa al Na+ hacia afuera es exactamente igual y opuesta a la fuerza química que lo impulsa hacia adentro. En este punto, el flujo neto de Na+ a través de la membrana es cero, y la membrana ha alcanzado el potencial de equilibrio para el Na+.
Este equilibrio electroquímico para un ion específico se describe mediante la Ecuación de Nernst:
Eion = (RT / zF) * ln ([ion]e / [ion]i)
Donde:
- Eion: Potencial de equilibrio del ion (en voltios, V)
- R: Constante de los gases (8.314 J/mol·K)
- T: Temperatura absoluta (en Kelvin, K). A 37 °C (temperatura corporal), T = 310.15 K.
- z: Valencia del ion (por ejemplo, +1 para Na+, K+; -1 para Cl–; +2 para Ca++).
- F: Constante de Faraday (96485 C/mol)
- [ion]e: Concentración extracelular del ion
- [ion]i: Concentración intracelular del ion
A menudo, la ecuación se simplifica para su uso práctico a 37 °C y se expresa en milivoltios (mV):
Eion = (61.5 / z) * log10 ([ion]e / [ion]i)
Por ejemplo, calculando el potencial de equilibrio para el K+ con las concentraciones típicas (140 mM intracelular, 4 mM extracelular) y z = +1:
EK+ = (61.5 / 1) * log10 (4 / 140) ≈ 61.5 * log10 (0.02857) ≈ 61.5 * (-1.54) ≈ -94.7 mV
Esto significa que si la membrana fuera permeable solo al K+, el potencial de membrana se establecería en aproximadamente -94.7 mV. Este valor negativo indica que el interior de la célula es negativo con respecto al exterior, lo que atrae al K+ hacia el interior, oponiéndose a su gradiente de concentración que lo empuja hacia afuera.
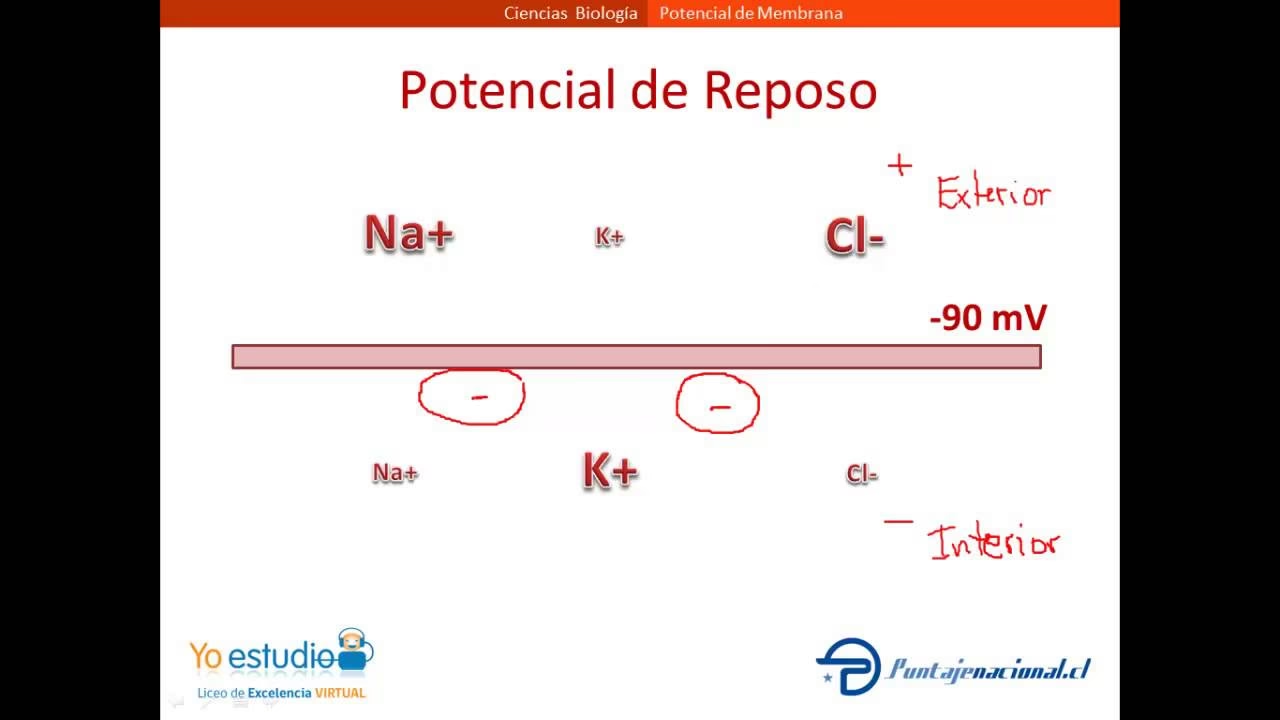
El Potencial de Membrana en Reposo: Un Juego de Múltiples Iones
Aunque la ecuación de Nernst es fundamental, la realidad celular es más compleja. Una célula en reposo no es permeable exclusivamente a un solo ion. Si bien la permeabilidad al K+ es la más alta (debido a la presencia de canales de fuga de K+), la membrana también es ligeramente permeable a otros iones como el Na+ y el Cl–. Por lo tanto, el potencial de membrana en reposo (PMR) es un promedio ponderado de los potenciales de equilibrio de todos los iones permeables, ponderado por la permeabilidad relativa de la membrana a cada uno de ellos.
Para calcular el potencial de membrana en reposo, se utiliza la Ecuación de Goldman-Hodgkin-Katz (GHK):
Em = (RT / F) * ln ((PK[K+]e + PNa[Na+]e + PCl[Cl–]i) / (PK[K+]i + PNa[Na+]i + PCl[Cl–]e))
Donde:
- Em: Potencial de membrana (en voltios, V)
- PK, PNa, PCl: Permeabilidad relativa de la membrana a K+, Na+ y Cl–, respectivamente.
- [ion]e: Concentración extracelular del ion
- [ion]i: Concentración intracelular del ion
Nótese que para los aniones (como Cl–), las concentraciones intracelular y extracelular se invierten en la ecuación para mantener la consistencia de los signos. Si usamos las permeabilidades relativas típicas (respecto a K+: PNa = 0.04, PCl = 0.45) y las concentraciones de la Tabla 1 a 37 °C, el potencial de membrana en reposo se calcula en aproximadamente -70 mV. Este valor es más positivo que el potencial de equilibrio del K+ (-94.7 mV) debido a la pequeña pero significativa entrada de Na+ a través de sus canales de fuga, lo que despolariza ligeramente la membrana.
El Potencial de Acción: El Impulso Eléctrico Celular
Mientras que el potencial de membrana en reposo describe el estado estable de una célula inactiva, el 'potencial de acción' es un cambio rápido, transitorio y regenerativo en el potencial de membrana que ocurre en células excitables como neuronas y células musculares. Es la base de la comunicación rápida a larga distancia en el sistema nervioso y de la contracción muscular.
Un potencial de acción se desencadena cuando un estímulo (eléctrico, químico o mecánico) despolariza la membrana hasta un nivel crítico llamado umbral. Una vez alcanzado el umbral, el proceso se vuelve auto-regenerativo, siguiendo la ley de "todo o nada". Un potencial de acción típico en una neurona consta de varias fases:
- Fase de Despolarización: Al alcanzar el umbral (aproximadamente -55 mV), se abren rápidamente los canales de Na+ dependientes de voltaje. El Na+ fluye masivamente hacia el interior de la célula, impulsado por su fuerte gradiente electroquímico. Esta entrada de cargas positivas hace que el potencial de membrana se vuelva rápidamente positivo, alcanzando un pico (sobretiro) de hasta +30 o +40 mV. El potencial de membrana se acerca momentáneamente al potencial de equilibrio del Na+.
- Fase de Repolarización: Poco después de la apertura, los canales de Na+ dependientes de voltaje se inactivan rápidamente, deteniendo la entrada de Na+. Casi simultáneamente, se abren los canales de K+ dependientes de voltaje, que son más lentos en activarse. El K+ fluye hacia afuera de la célula, sacando cargas positivas y haciendo que el potencial de membrana regrese a valores negativos.
- Fase de Hiperpolarización (o post-hiperpolarización): Los canales de K+ dependientes de voltaje tardan un poco en cerrarse por completo. Esto permite que una cantidad excesiva de K+ salga de la célula, llevando el potencial de membrana a valores incluso más negativos que el potencial de reposo. Este período es crucial para la regulación de la frecuencia de disparo. Finalmente, los canales de K+ se cierran y la bomba Na+/K+ restablece los gradientes iónicos originales, regresando la célula al potencial de membrana en reposo.
Durante y después de un potencial de acción, existe un 'período refractario' en el que la célula es menos excitable o completamente inexitable a un nuevo estímulo. El 'período refractario absoluto' ocurre durante la despolarización y gran parte de la repolarización, cuando los canales de Na+ están inactivos, impidiendo un nuevo potencial de acción. El 'período refractario relativo' ocurre durante la hiperpolarización, cuando se necesita un estímulo más fuerte de lo normal para alcanzar el umbral y generar un nuevo potencial de acción, debido a que la membrana está más negativa y algunos canales de K+ aún están abiertos.
Factores que Modifican el Potencial de Membrana: Implicaciones Prácticas
Los cambios en las concentraciones iónicas o en la permeabilidad de la membrana a los iones pueden tener efectos profundos en el potencial de membrana. Estos efectos son la base de muchas funciones fisiológicas y patologías.
Consideremos algunos escenarios basados en los principios de Nernst y Goldman:
- Cambios en la concentración extracelular de K+: Si la concentración extracelular de K+ disminuye (hipopotasemia), el gradiente de concentración para el K+ se vuelve más pronunciado, lo que hace que el potencial de equilibrio del K+ sea aún más negativo (por la ecuación de Nernst). Dado que la permeabilidad al K+ es alta en reposo, esto hiperpolariza la membrana (la hace más negativa), alejándola del umbral y disminuyendo la excitabilidad celular. Por el contrario, un aumento de K+ extracelular (hiperpotasemia) despolariza la membrana, acercándola al umbral e inicialmente aumentando la excitabilidad, pero una despolarización sostenida puede inactivar los canales de Na+, llevando a una falta de excitabilidad.
- Cambios en la concentración extracelular de Na+: Un aumento en la concentración extracelular de Na+ hará que el potencial de equilibrio del Na+ sea más positivo. Aunque la permeabilidad al Na+ en reposo es baja, un gran cambio en su concentración puede despolarizar ligeramente la membrana. Sin embargo, el impacto suele ser menos dramático que los cambios en K+ debido a la menor permeabilidad de la membrana en reposo al Na+.
- Cambios en la permeabilidad iónica: La apertura o cierre de canales iónicos específicos es el mecanismo principal para cambiar la permeabilidad de la membrana y, por lo tanto, modificar el potencial de membrana. Por ejemplo, la apertura de canales de Na+ (como durante la despolarización de un potencial de acción) aumenta drásticamente la permeabilidad al Na+, haciendo que el potencial de membrana se acerque rápidamente al potencial de equilibrio del Na+. De manera similar, un aumento en la permeabilidad al K+ (como durante la repolarización) acerca el potencial de membrana al potencial de equilibrio del K+.
- Cambios de temperatura: Un aumento de la temperatura aumenta la energía cinética de los iones, lo que puede afectar la velocidad de difusión y, en última instancia, la conductancia de los canales iónicos. Esto se refleja en el término RT/F de las ecuaciones de Nernst y Goldman, lo que implica que la temperatura influye directamente en la magnitud del potencial.
Relevancia Clínica: Cuando el Potencial Falla
Las alteraciones en el potencial de membrana o en los mecanismos que lo regulan son la base de muchas patologías. Aquí exploramos algunos ejemplos:
Viñeta 1: Parálisis Periódica Hipocalémica Familiar
Un paciente con debilidad generalizada tras una ingesta alta de carbohidratos y niveles séricos de potasio muy bajos (hipopotasemia). Los resultados de laboratorio, incluido el potasio sérico, representan el líquido extracelular. Estos valores de potasio tienen una relación directa con el cuadro clínico, ya que el potasio es crucial para establecer el potencial de membrana en reposo.
El potasio contribuye significativamente al potencial de equilibrio de la membrana celular porque es el ion con mayor permeabilidad en reposo. Una disminución del potasio extracelular (como en la hipopotasemia) aumenta el gradiente de concentración de potasio, haciendo que más K+ tienda a salir de la célula. Esto resulta en una hiperpolarización de la membrana celular (el interior se vuelve más negativo), alejándola del umbral de excitación. Los síntomas esperados con potasio disminuido incluyen debilidad muscular, parálisis, arritmias cardíacas e hiporreflexia, ya que las células excitables tienen dificultad para generar potenciales de acción.
En la parálisis periódica hipocalémica familiar, donde los canales de salida de potasio dependientes de voltaje están alterados, uno esperaría que, durante los episodios, la membrana se hiperpolarice anormalmente debido a una alteración en la capacidad de los canales de potasio para mantener el potencial de reposo o repolarizar correctamente. Esto llevaría a una disminución en la excitabilidad, haciendo que el umbral para desencadenar un potencial de acción sea más difícil de alcanzar, o que los potenciales de acción sean más débiles o incluso imposibles de generar, resultando en la parálisis.
Viñeta 2: Cetoacidosis Diabética e Hipopotasemia
Un paciente con cetoacidosis diabética que desarrolla debilidad muscular e hiporreflexia tras el tratamiento con insulina, con hipopotasemia grave.
Una disminución del potasio extracelular (hipopotasemia) genera una hiperpolarización del potencial de membrana. Esto se debe a que, al haber menos K+ fuera de la célula, el gradiente de concentración que impulsa al K+ hacia afuera es mayor, haciendo que el potencial de equilibrio del K+ se vuelva más negativo. Con una mayor salida de iones K+, el potencial de membrana se aleja del umbral, volviéndose más negativo y, por lo tanto, disminuyendo la excitabilidad de las células.
La insulina no solo mueve el potasio al interior de las células, sino que también puede aumentar la permeabilidad al potasio en algunas membranas. Un incremento en la permeabilidad al potasio hace que el potencial de membrana se acerque aún más al potencial de equilibrio del K+. Si el EK es más negativo (debido a la hipopotasemia), un aumento en la permeabilidad al K+ hará que el potencial de membrana se vuelva aún más negativo y se aleje del umbral, exacerbando la hiperpolarización.

Cuando se combinan una disminución del potasio extracelular y un aumento de su permeabilidad, la magnitud del cambio en el potencial de membrana es significativamente mayor que la de los factores por separado. Ambos factores conspiran para hiperpolarizar drásticamente la célula, lo que explica la debilidad muscular severa, la hiporreflexia y las anomalías cardíacas (arritmias) observadas en el paciente, ya que sus células excitables se vuelven mucho más difíciles de activar.
Viñeta 3: Síndrome de Guillain-Barré
Un paciente con imposibilidad para caminar y mover los brazos, con fuerza muscular 0/5, arreflexia e hipotonía, tras una enfermedad gastrointestinal.
El Síndrome de Guillain-Barré es una polirradiculopatía desmielinizante. La mielina es una vaina que rodea los axones de las neuronas, actuando como un aislante eléctrico y permitiendo una conducción rápida y eficiente del potencial de acción. En esta enfermedad, el sistema inmune ataca la mielina. Por lo tanto, en la conducción nerviosa de los miembros inferiores (y superiores) de este paciente, esperaríamos encontrar una disminución significativa en la velocidad de conducción nerviosa y, en casos severos, un bloqueo completo de la conducción. Los potenciales de acción no pueden propagarse eficientemente o se pierden debido a la falta de aislamiento y a la exposición de la membrana en áreas que no tienen una alta densidad de canales de sodio dependientes de voltaje.
Los miembros inferiores suelen estar más afectados que los superiores debido a la naturaleza ascendente típica de la parálisis en el Síndrome de Guillain-Barré, que progresa desde las extremidades distales hacia el tronco y las extremidades superiores.
Viñeta 4: Esclerosis Múltiple
Una paciente con episodios de visión borrosa, vértigo, disartria y afasia de expresión, con lesión de sustancia blanca en el cerebro.
La esclerosis múltiple es una enfermedad autoinmune crónica que afecta el sistema nervioso central, causando desmielinización de neuronas en el cerebro y la médula espinal. La desmielinización interrumpe la conducción normal de los potenciales de acción.
El cuadro clínico de la paciente (visión borrosa, vértigo, disartria, afasia) se explica por la interrupción de la transmisión nerviosa en las áreas desmielinizadas del cerebro. Por ejemplo, la disartria y afasia sugieren afectación de las vías motoras y del lenguaje en el cerebro.

En las neuronas de esta paciente, tanto el potencial de membrana en reposo como el potencial de acción se encontrarán alterados, pero de maneras específicas. El potencial de membrana en reposo puede no cambiar drásticamente en las regiones desmielinizadas, ya que se basa en los gradientes iónicos y la permeabilidad de fuga. Sin embargo, la generación y, crucialmente, la propagación del potencial de acción se verán gravemente comprometidas. La desmielinización hace que la conducción saltatoria (rápida) sea ineficiente o imposible. La corriente iónica "se fuga" a través de la membrana donde debería estar aislada, impidiendo que la despolarización alcance los siguientes nodos de Ranvier (donde se concentran los canales de Na+). Esto resulta en una disminución de la velocidad de conducción, un aumento del umbral de excitación o incluso el bloqueo total de la propagación del potencial de acción, lo que se manifiesta como los diversos síntomas neurológicos.
Preguntas Frecuentes sobre el Potencial de Membrana
¿Qué es la conductancia (G) en el contexto de la membrana celular?
La conductancia (G) es la propiedad de la membrana celular que representa la facilidad con la que los iones pueden pasar o atravesar un segmento de la membrana. Es el inverso de la resistencia (R) y se mide en Siemens (S). Una alta conductancia para un ion significa que la membrana es muy permeable a ese ion, permitiendo un gran flujo de corriente. Está directamente relacionada con el número y la apertura de los canales iónicos.
¿Por qué el potencial de membrana en reposo es negativo?
El potencial de membrana en reposo es negativo (típicamente entre -60 mV y -90 mV) porque la membrana celular es mucho más permeable al potasio (K+) que al sodio (Na+) en estado de reposo. Los canales de fuga de potasio permiten que el K+, que es más concentrado dentro de la célula, salga de ella. A medida que el K+ cargado positivamente sale, deja cargas negativas no difusibles (como proteínas y aniones orgánicos) en el interior, creando una diferencia de potencial eléctrico donde el interior es negativo con respecto al exterior. La bomba de sodio-potasio también contribuye al mantener los gradientes iónicos.
¿Qué es el umbral para un potencial de acción?
El umbral es el nivel crítico de despolarización que debe alcanzar el potencial de membrana para que se genere un potencial de acción. Es el punto en el que se abren un número suficiente de canales de sodio dependientes de voltaje para iniciar una respuesta regenerativa de "todo o nada". Si el estímulo no alcanza este umbral, no se producirá un potencial de acción.
¿Cuál es la diferencia entre despolarización e hiperpolarización?
La despolarización es el proceso en el que el potencial de membrana de una célula se vuelve menos negativo (o incluso positivo) en comparación con su potencial de reposo. Esto ocurre típicamente por la entrada de iones positivos (como Na+ o Ca2+). La hiperpolarización es el proceso opuesto, donde el potencial de membrana se vuelve aún más negativo que su potencial de reposo, generalmente por la salida de iones positivos (como K+) o la entrada de iones negativos (como Cl–).
¿Qué es una canalopatía?
Una canalopatía es una enfermedad causada por disfunciones en los canales iónicos, que son proteínas que forman poros en la membrana celular y controlan el paso selectivo de iones. Estas disfunciones pueden ser genéticas (mutaciones en los genes que codifican los canales) o adquiridas (por ejemplo, por autoanticuerpos). Las canalopatías pueden afectar la excitabilidad de las células nerviosas, musculares o cardíacas, llevando a una amplia gama de síntomas como parálisis, arritmias, epilepsia o dolor crónico.
En resumen, el potencial de membrana es un fenómeno electroquímico complejo pero fundamental para la vida. Desde el simple equilibrio de un solo ion hasta la compleja interacción de múltiples iones y sus permeabilidades, las ecuaciones de Nernst y Goldman-Hodgkin-Katz nos brindan las herramientas para calcular y comprender este voltaje crucial. Las alteraciones en este delicado equilibrio pueden tener profundas consecuencias clínicas, subrayando la importancia de estos principios en la fisiología y la medicina.
Si quieres conocer otros artículos parecidos a El Potencial de Membrana: Clave de la Comunicación Celular puedes visitar la categoría Cálculos.
