04/04/2022
En el fascinante mundo de la química, la farmacia, la cocina e incluso la limpieza del hogar, a menudo nos encontramos con etiquetas que indican la concentración de una sustancia en una solución. Frases como “solución al 5%” o “medicamento al 20%” son comunes, pero ¿qué significan realmente estas cifras? La concentración es un concepto fundamental que nos dice la cantidad de un soluto (la sustancia que se disuelve) presente en una cantidad determinada de disolvente (la sustancia que disuelve) o de la solución total. Entenderla es crucial para la seguridad, la precisión y la eficacia en innumerables aplicaciones.
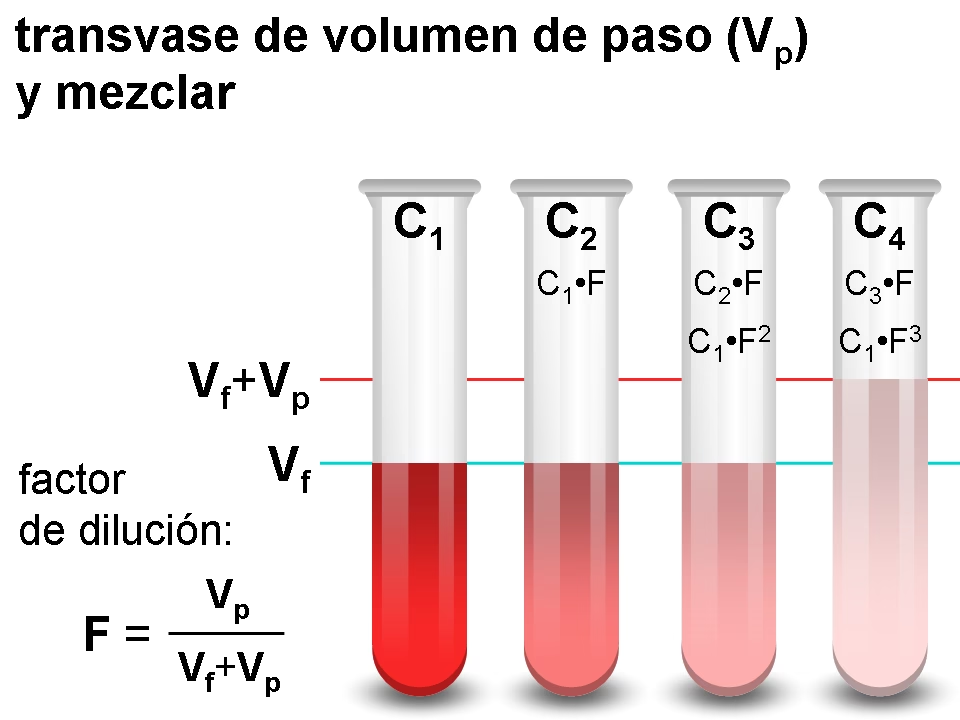
Cuando se habla de una solución al 20%, la clave para descifrar su significado preciso reside en las unidades o el tipo de porcentaje al que se refiere. La información proporcionada ya nos da una pista vital: peso/volumen (p/v). Esta es una de las formas más comunes de expresar la concentración, especialmente en campos como la farmacia y la química clínica, donde se manejan sustancias sólidas disueltas en líquidos.
- ¿Qué Significa una Concentración al 20% Peso/Volumen (p/v)?
- La Importancia de Especificar las Unidades
- Cálculos Prácticos con Concentraciones % p/v
- Preparación de una Solución al 20% p/v
- Diferencias Clave en la Expresión de Concentraciones
- Preguntas Frecuentes sobre Concentraciones
- ¿Es lo mismo una solución al 20% p/v que una al 20% p/p?
- ¿Por qué es importante la precisión en la concentración de medicamentos?
- ¿Qué es el soluto y el disolvente?
- ¿Cómo se diluye una solución concentrada para obtener una al 20%?
- ¿Se puede expresar la concentración al 20% en otras unidades, como molaridad?
- Conclusión
¿Qué Significa una Concentración al 20% Peso/Volumen (p/v)?
La concentración expresada como porcentaje peso/volumen (% p/v) es una medida directa de la cantidad de soluto en gramos que hay por cada 100 mililitros de solución. Es una forma sencilla y muy utilizada para indicar la fuerza o potencia de una solución.
Por lo tanto, si nos referimos a una solución con una concentración del 20% en peso/volumen (p/v), esto significa, de manera inequívoca, que hay 20 gramos de la sustancia activa (el soluto) en cada 100 mililitros de la solución completa. Es importante recalcar que estos 100 mililitros corresponden al volumen total de la solución, no solo al volumen del disolvente.
Este concepto es aplicable a una vasta gama de escenarios. Por ejemplo, si tienes un jarabe medicinal etiquetado como “Concentración de principio activo: 20% p/v”, significa que cada 100 ml de ese jarabe contienen 20 gramos del medicamento. Esto es vital para calcular la dosis correcta y asegurar la efectividad del tratamiento sin riesgos.
La Importancia de Especificar las Unidades
Es fundamental comprender que un simple “20%” sin unidades puede ser ambiguo. Existen otras formas de expresar la concentración porcentual, y cada una tiene un significado distinto:
- Porcentaje Peso/Peso (% p/p): Indica los gramos de soluto por cada 100 gramos de solución. Por ejemplo, una solución al 20% p/p contendría 20 gramos de soluto en 100 gramos de solución total.
- Porcentaje Volumen/Volumen (% v/v): Indica los mililitros de soluto por cada 100 mililitros de solución. Este tipo es común para soluciones donde tanto el soluto como el disolvente son líquidos, como el alcohol en agua. Una solución al 20% v/v significaría 20 ml de soluto en 100 ml de solución.
Como se puede apreciar, aunque el número “20” sea el mismo, las implicaciones son muy diferentes dependiendo de si hablamos de peso en volumen, peso en peso o volumen en volumen. La falta de especificación puede llevar a errores graves, especialmente en campos críticos como la medicina o la química analítica.
Cálculos Prácticos con Concentraciones % p/v
Una vez que entendemos lo que significa 20% p/v, podemos realizar una serie de cálculos prácticos. La base es siempre la misma: 20 g de soluto por cada 100 ml de solución.
1. Calcular la Cantidad de Soluto en un Volumen Dado de Solución:
Si sabes que tienes una solución al 20% p/v y necesitas saber cuántos gramos de soluto hay en un volumen específico, puedes usar una simple regla de tres o una fórmula directa.
Fórmula:Gramos de Soluto = (Porcentaje p/v / 100) * Volumen de Solución (ml)
Ejemplo: ¿Cuántos gramos de soluto hay en 250 ml de una solución al 20% p/v?
Gramos de Soluto = (20 / 100) * 250 ml
Gramos de Soluto = 0.20 * 250 ml
Gramos de Soluto = 50 gramos
Esto significa que en 250 ml de una solución al 20% p/v, hay 50 gramos de la sustancia activa.
2. Calcular el Volumen de Solución Necesario para una Cantidad Dada de Soluto:
Si conoces la cantidad de soluto que necesitas y quieres preparar una solución al 20% p/v, puedes calcular el volumen total de solución que obtendrás.
Fórmula:Volumen de Solución (ml) = (Gramos de Soluto / Porcentaje p/v) * 100
Ejemplo: ¿Qué volumen de una solución al 20% p/v se puede preparar con 10 gramos de soluto?
Volumen de Solución = (10 gramos / 20) * 100
Volumen de Solución = 0.5 * 100
Volumen de Solución = 50 ml
Así, con 10 gramos de soluto, se pueden preparar 50 ml de una solución al 20% p/v.
3. Calcular la Concentración (% p/v) de una Solución Dada:
Si tienes una cantidad conocida de soluto disuelta en un volumen conocido de solución, puedes calcular su concentración porcentual p/v.
Fórmula:Concentración % p/v = (Gramos de Soluto / Volumen de Solución (ml)) * 100
Ejemplo: Si disuelves 15 gramos de una sustancia en suficiente agua para hacer 300 ml de solución, ¿cuál es la concentración % p/v?
Concentración % p/v = (15 gramos / 300 ml) * 100
Concentración % p/v = 0.05 * 100
Concentración % p/v = 5% p/v
Estos cálculos son la base para preparar soluciones con la concentración deseada en laboratorios, farmacias o incluso en la preparación de productos caseros.
Preparación de una Solución al 20% p/v
El proceso de preparación de una solución con una concentración específica, como el 20% p/v, es crucial y requiere precisión.
Para preparar, por ejemplo, 100 ml de una solución al 20% p/v:
- Pesar el Soluto: Primero, se deben pesar exactamente 20 gramos del soluto (la sustancia que se va a disolver). Se utiliza una balanza de precisión para este paso.
- Disolver el Soluto: Los 20 gramos de soluto se transfieren a un recipiente adecuado, como un vaso de precipitados. Se añade una parte del disolvente (generalmente agua destilada o desionizada si no se especifica otro) y se agita hasta que el soluto se disuelva completamente. Es importante no añadir todo el volumen de disolvente al principio.
- Aforar a Volumen: Una vez disuelto el soluto, la solución se transfiere a un matraz aforado del volumen deseado (en este caso, 100 ml). Se añade más disolvente hasta que el nivel del líquido coincida exactamente con la marca de aforo del matraz. Este paso asegura que el volumen final de la solución sea el deseado, y no solo el volumen de disolvente añadido.
- Mezclar: Se tapa el matraz y se invierte varias veces para asegurar una mezcla homogénea de la solución.
La precisión en el pesaje y el aforo son vitales para asegurar que la concentración final sea exactamente del 20% p/v.
Diferencias Clave en la Expresión de Concentraciones
Para reforzar la importancia de las unidades, aquí una tabla comparativa de los tipos de porcentajes de concentración más comunes:
| Tipo de Concentración | Definición | Unidades Típicas | Ejemplo (20%) | Uso Común |
|---|---|---|---|---|
| Porcentaje Peso/Volumen (% p/v) | Gramos de soluto por cada 100 mL de solución. | g/100 mL | 20 g de soluto en 100 mL de solución. | Farmacia, química clínica, preparación de reactivos. |
| Porcentaje Peso/Peso (% p/p) | Gramos de soluto por cada 100 g de solución. | g/100 g | 20 g de soluto en 100 g de solución. | Química analítica, productos sólidos, alimentos. |
| Porcentaje Volumen/Volumen (% v/v) | Mililitros de soluto por cada 100 mL de solución. | mL/100 mL | 20 mL de soluto en 100 mL de solución. | Soluciones líquidas (alcohol, anticongelantes). |
| Partes por Millón (ppm) | Miligramos de soluto por litro de solución (para soluciones diluidas). | mg/L | 20 ppm = 20 mg de soluto en 1 L de solución. | Contaminantes en agua o aire, trazas. |
| Molaridad (M) | Moles de soluto por litro de solución. | mol/L | Una solución 20 M (muy concentrada). | Química de laboratorio, reacciones estequiométricas. |
Esta tabla subraya que, aunque la pregunta original se centra en el 20% p/v, el universo de la concentración es más amplio y requiere siempre la especificación de las unidades para evitar ambigüedades.
Preguntas Frecuentes sobre Concentraciones
¿Es lo mismo una solución al 20% p/v que una al 20% p/p?
No, no son lo mismo. Una solución al 20% p/v contiene 20 gramos de soluto por cada 100 mililitros de solución. Una solución al 20% p/p contiene 20 gramos de soluto por cada 100 gramos de solución. Para que fueran iguales, la densidad de la solución tendría que ser exactamente 1 g/ml, lo cual no siempre es el caso.
¿Por qué es importante la precisión en la concentración de medicamentos?
La precisión es vital en medicamentos para asegurar la dosis correcta. Una concentración incorrecta podría resultar en una dosis insuficiente (ineficaz) o excesiva (tóxica), poniendo en riesgo la salud del paciente. En otros campos, como la investigación o la industria, la precisión asegura la reproducibilidad de los experimentos o la calidad del producto final.
¿Qué es el soluto y el disolvente?
El soluto es la sustancia que se disuelve en otra. Generalmente es la que está en menor proporción. El disolvente es la sustancia que disuelve al soluto, y suele estar en mayor proporción. Cuando el soluto se disuelve en el disolvente, forman una solución.
¿Cómo se diluye una solución concentrada para obtener una al 20%?
La dilución es el proceso de reducir la concentración de una solución añadiendo más disolvente. Para calcular las diluciones, se suele usar la fórmula C1V1 = C2V2, donde C es la concentración y V es el volumen. Por ejemplo, si tienes una solución al 40% p/v y quieres preparar 100 ml de una solución al 20% p/v:
C1 = 40% (concentración inicial)
V1 = ? (volumen inicial que necesitas)
C2 = 20% (concentración final deseada)
V2 = 100 ml (volumen final deseado)
40% * V1 = 20% * 100 ml
V1 = (20% * 100 ml) / 40%
V1 = 50 ml
Esto significa que necesitarías tomar 50 ml de la solución al 40% y añadir suficiente disolvente hasta alcanzar un volumen final de 100 ml. Es crucial siempre añadir el disolvente hasta el volumen final deseado, no simplemente añadir 50 ml de disolvente.
¿Se puede expresar la concentración al 20% en otras unidades, como molaridad?
Sí, es posible convertir una concentración porcentual p/v a molaridad, pero se necesita información adicional: la masa molar del soluto (en g/mol) y, a veces, la densidad de la solución si la conversión es a otras unidades de concentración basadas en masa.
Para convertir 20% p/v a molaridad, primero calculamos los gramos de soluto en 1 litro (1000 ml) de solución:
20 g soluto / 100 ml solución = X g soluto / 1000 ml solución
X = 200 g soluto en 1000 ml (1 L) de solución.
Luego, se divide la cantidad de gramos por la masa molar del soluto para obtener los moles:
Moles de soluto = Gramos de soluto / Masa molar del soluto
Finalmente, la Molaridad sería Moles de soluto / 1 Litro de solución.
Conclusión
En resumen, cuando se nos pregunta sobre la concentración de una solución al 20%, la respuesta precisa y completa depende crucialmente de las unidades. En el contexto proporcionado, donde se especifica peso/volumen (p/v), la interpretación es clara: 20 gramos de soluto por cada 100 mililitros de solución. Este conocimiento no solo nos permite comprender mejor la composición de diversas sustancias, sino que también es una herramienta indispensable para realizar cálculos precisos, preparar soluciones de manera segura y garantizar la efectividad en campos tan diversos como la medicina, la investigación científica y la industria. La próxima vez que vea un porcentaje en una etiqueta, recuerde siempre buscar las unidades; ellas son la clave para desvelar la verdadera concentración.
Si quieres conocer otros artículos parecidos a Desentrañando la Concentración al 20% puedes visitar la categoría Cálculos.

