27/07/2024
En el vasto y complejo universo de la bioquímica, las enzimas son protagonistas indiscutibles. Estas proteínas especializadas actúan como catalizadores biológicos, acelerando drásticamente la velocidad de las reacciones químicas en los seres vivos sin ser consumidas en el proceso. Para comprender a fondo cómo funcionan estas maravillas moleculares, es esencial adentrarse en el campo de la cinética enzimática. Dentro de este estudio, dos parámetros destacan por su relevancia: la velocidad máxima (Vmax) y la constante de Michaelis (Km). Comprender cómo se calculan y qué representan es fundamental para cualquier persona que trabaje con enzimas, desde la investigación en un laboratorio hasta el desarrollo de nuevos fármacos.
El conocimiento de Vmax y Km nos permite caracterizar una enzima, predecir su comportamiento en diferentes condiciones y entender cómo interactúa con sus sustratos y posibles inhibidores. Estos valores no solo son teóricos; tienen aplicaciones prácticas directas en medicina, biotecnología e industria. A lo largo de este artículo, exploraremos en detalle qué son Vmax y Km, cómo se determinan experimentalmente, y cómo interpretar los resultados para obtener una visión completa de la actividad enzimática.
¿Qué son Vmax y Km en la Cinética Enzimática?
Antes de sumergirnos en los métodos de cálculo, es crucial tener una comprensión clara de lo que representan Vmax y Km. Ambos son parámetros cinéticos intrínsecos a cada enzima y su sustrato específico, determinados bajo condiciones de reacción controladas (temperatura, pH, fuerza iónica, etc.).
Vmax: La Velocidad Máxima de Reacción
La Vmax, o velocidad máxima, representa la velocidad más alta a la que una reacción catalizada por una enzima puede proceder. Se alcanza cuando la enzima está completamente saturada con el sustrato, es decir, cuando todas las moléculas de enzima tienen un sustrato unido a su sitio activo. En este punto, la adición de más sustrato no aumentará la velocidad de la reacción, ya que la enzima está trabajando a su máxima capacidad. Vmax es una medida de la capacidad catalítica intrínseca de la enzima, indicando qué tan rápido puede transformar el sustrato en producto una vez que está completamente ocupada.
Desde un punto de vista molecular, Vmax está directamente relacionada con la concentración total de enzima ([Et]) y la constante de velocidad catalítica (kcat), también conocida como el número de recambio. La relación se expresa como:
Vmax = kcat · [Et]
Donde kcat es la velocidad a la que una molécula de enzima saturada con sustrato convierte el sustrato en producto por unidad de tiempo. Un valor alto de kcat indica una enzima muy eficiente. Vmax, por lo tanto, varía de una enzima a otra, e incluso para la misma enzima con diferentes sustratos o bajo diferentes condiciones ambientales.
Km: La Constante de Michaelis
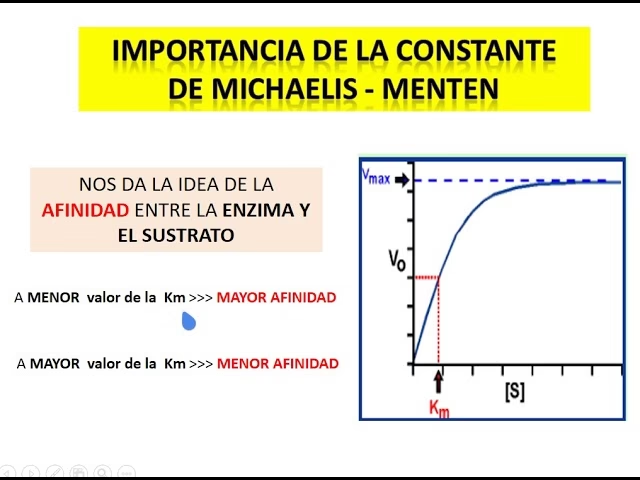
La Km, o constante de Michaelis, es un parámetro que refleja la afinidad aparente de una enzima por su sustrato. Se define como la concentración de sustrato a la cual la velocidad de la reacción es exactamente la mitad de la Vmax (V = Vmax/2). Un valor bajo de Km indica una alta afinidad de la enzima por su sustrato, lo que significa que la enzima puede alcanzar la mitad de su velocidad máxima con una concentración relativamente baja de sustrato. Por el contrario, un valor alto de Km sugiere una menor afinidad, requiriendo una mayor concentración de sustrato para alcanzar la mitad de Vmax.
Es importante destacar que Km no es una constante de disociación directa, aunque a menudo se interpreta como una medida inversa de la afinidad de la enzima por el sustrato. Su valor puede verse afectado por factores como el pH, la temperatura y la presencia de inhibidores o activadores.
Métodos para el Cálculo de Vmax y Km
La determinación experimental de Vmax y Km es un paso crucial en la caracterización enzimática. Aunque existen varios enfoques, el método más clásico y ampliamente utilizado es el análisis gráfico de Lineweaver-Burk.
El Gráfico de Lineweaver-Burk: La Doble Recíproca
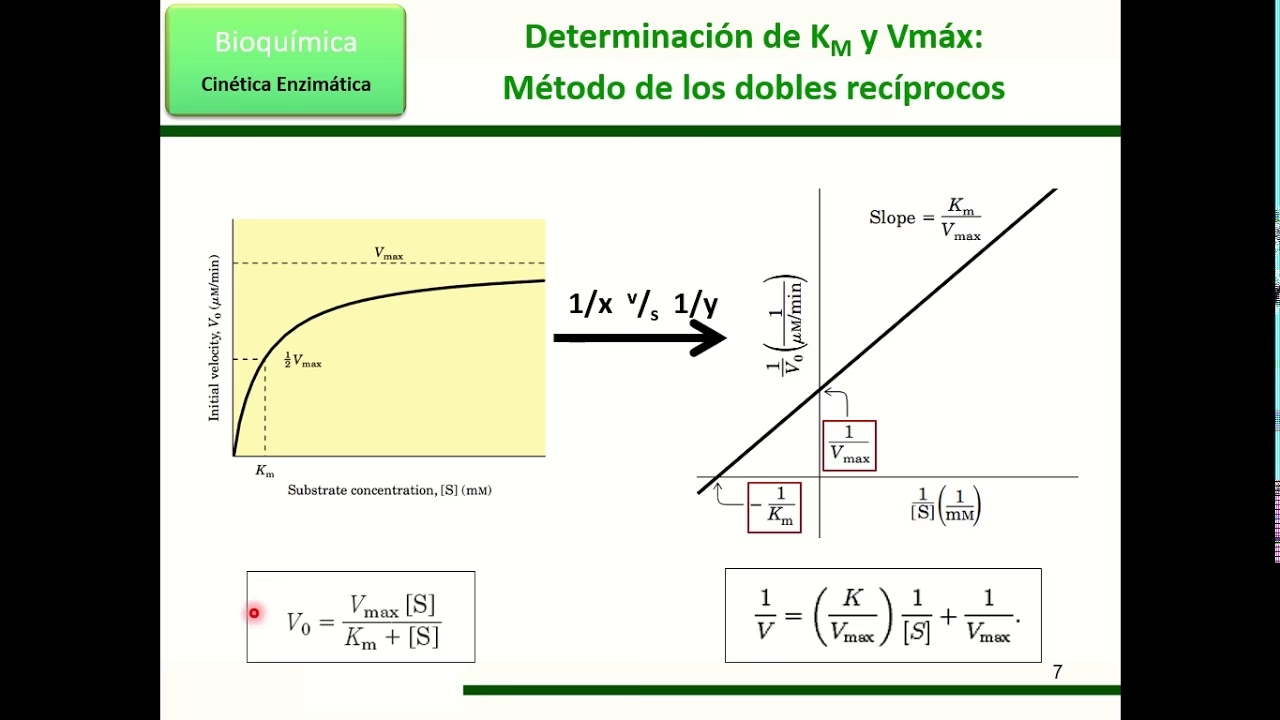
El gráfico de Lineweaver-Burk, también conocido como el gráfico de doble recíproca, es una representación lineal de la ecuación de Michaelis-Menten. La ecuación de Michaelis-Menten, que describe la relación entre la velocidad inicial de la reacción (Vo) y la concentración de sustrato ([S]), es:
Vo = (Vmax · [S]) / (Km + [S])
Al tomar el recíproco de ambos lados de esta ecuación, obtenemos la ecuación de Lineweaver-Burk:
1/Vo = (Km/Vmax) · (1/[S]) + 1/Vmax
Esta ecuación tiene la forma de una línea recta (y = mx + b), donde:
y = 1/Vo(el recíproco de la velocidad inicial)x = 1/[S](el recíproco de la concentración de sustrato)m = Km/Vmax(la pendiente de la línea)b = 1/Vmax(la intersección con el eje Y)
Para construir un gráfico de Lineweaver-Burk, se realizan experimentos midiendo la velocidad inicial de la reacción (Vo) a varias concentraciones de sustrato ([S]). Luego, se grafican los valores de 1/Vo en el eje Y contra los valores de 1/[S] en el eje X. Los puntos resultantes deben formar una línea recta, y a partir de las intersecciones y la pendiente de esta línea, se pueden calcular Vmax y Km.
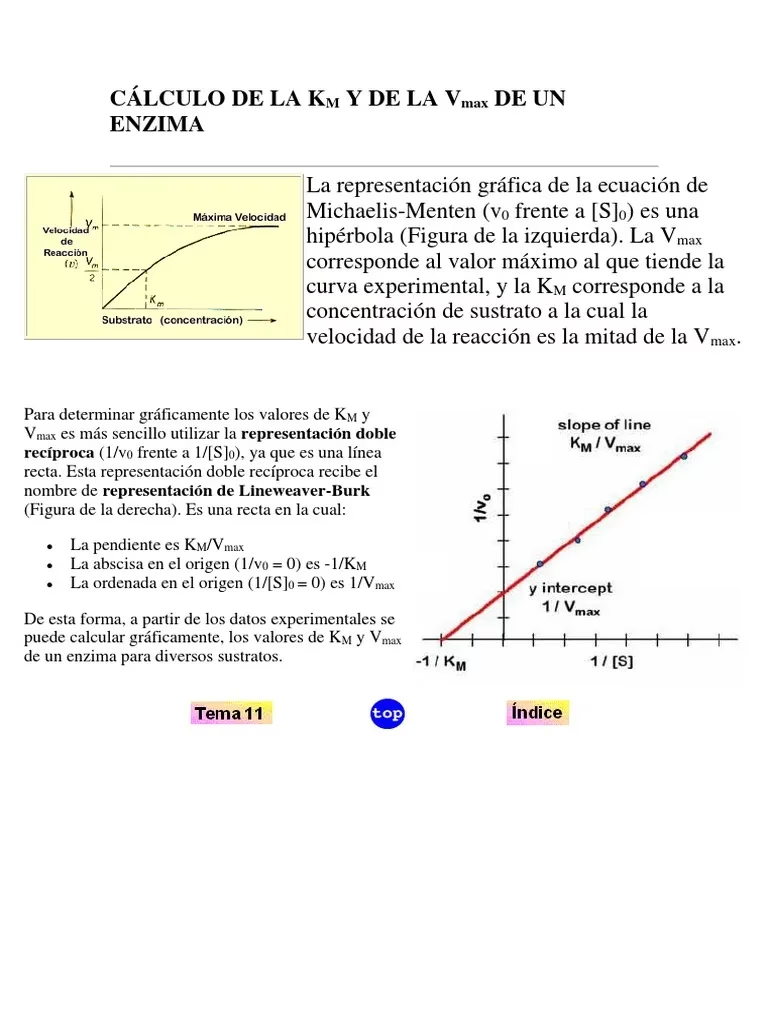
Interpretación del Gráfico de Lineweaver-Burk:
La potencia del gráfico de Lineweaver-Burk reside en su simplicidad para extraer los valores de Vmax y Km:
- Intersección con el eje Y (1/Vo): El punto donde la línea cruza el eje Y (donde 1/[S] = 0) es igual a 1/Vmax. Por lo tanto, Vmax se calcula como el recíproco de esta intersección:
Vmax = 1 / (Intersección con el eje Y). - Intersección con el eje X (1/[S]): El punto donde la línea cruza el eje X (donde 1/Vo = 0) es igual a -1/Km. Por lo tanto, Km se calcula como el recíproco negativo de esta intersección:
Km = -1 / (Intersección con el eje X). - Pendiente de la línea: La pendiente de la línea es igual a Km/Vmax. Este valor también puede usarse para verificar los cálculos o para determinar uno de los parámetros si el otro ya es conocido.
A pesar de su utilidad, el gráfico de Lineweaver-Burk tiene una desventaja: los datos tomados a bajas concentraciones de sustrato (que corresponden a valores altos de 1/[S]) tienen un peso excesivo en la determinación de la línea, y estos puntos suelen ser los que presentan mayor error experimental. Sin embargo, sigue siendo una herramienta didáctica y práctica fundamental.
Ejemplo Práctico de Cálculo
Imaginemos que hemos realizado un experimento de cinética enzimática y hemos graficado los datos en un gráfico de Lineweaver-Burk. A través de un análisis de regresión lineal, hemos determinado la ecuación de la línea recta y hemos obtenido los siguientes valores:
- Pendiente = 0.5
- Intersección con el eje Y = 0.3
Ahora, procedamos a calcular Km y Vmax a partir de estos datos:
Cálculo de Vmax:
Sabemos que la intersección con el eje Y es igual a 1/Vmax.

1/Vmax = 0.3
Para encontrar Vmax, tomamos el recíproco de la intersección con el eje Y:
Vmax = 1 / 0.3
Vmax ≈ 3.33 (unidades de concentración/tiempo, por ejemplo, mM/s)
Cálculo de Km:
Sabemos que la pendiente es igual a Km/Vmax.
Pendiente = Km / Vmax
Podemos reorganizar esta ecuación para encontrar Km:
Km = Pendiente · Vmax
Sustituimos los valores que ya tenemos:
Km = 0.5 · 3.33
Km ≈ 1.67 (unidades de concentración, por ejemplo, mM)
A partir de los datos dados, hemos calculado Km ≈ 1.67 mM y Vmax ≈ 3.33 mM/s. Este ejemplo ilustra la sencillez del cálculo una vez que se obtienen los parámetros de la línea recta del gráfico de Lineweaver-Burk.
Otros Métodos Gráficos (Breve Mención)
Aunque el gráfico de Lineweaver-Burk es el más conocido, existen otras representaciones lineales de la ecuación de Michaelis-Menten que pueden ser útiles, especialmente para mitigar las desventajas asociadas con la ponderación de errores:
- Gráfico de Eadie-Hofstee: Grafica Vo contra Vo/[S]. La pendiente es -Km y la intersección con el eje Y es Vmax.
- Gráfico de Hanes-Woolf: Grafica [S]/Vo contra [S]. La pendiente es 1/Vmax y la intersección con el eje Y es Km/Vmax.
Estos gráficos ofrecen alternativas valiosas y a menudo se utilizan en conjunto con el Lineweaver-Burk para una validación cruzada de los resultados.
Importancia y Aplicaciones de Vmax y Km
Los valores de Vmax y Km no son meros números; proporcionan información crucial sobre el comportamiento de las enzimas y tienen amplias aplicaciones en diversas áreas:
- Caracterización Enzimática: Permiten comparar la eficiencia de diferentes enzimas o la misma enzima bajo distintas condiciones (pH, temperatura, presencia de cofactores).
- Diseño de Fármacos: La comprensión de Km es vital para el desarrollo de inhibidores enzimáticos. Un inhibidor competitivo, por ejemplo, aumenta el Km aparente de la enzima, mientras que un inhibidor no competitivo disminuye Vmax.
- Bioquímica Médica: Las alteraciones en Vmax o Km pueden ser indicativas de enfermedades metabólicas o genéticas. Por ejemplo, en algunas condiciones, una mutación puede afectar la afinidad de una enzima por su sustrato (cambiando Km) o su capacidad catalítica (cambiando Vmax).
- Biotecnología e Ingeniería Enzimática: En la producción industrial o en la modificación de enzimas para mejorar su rendimiento, los parámetros cinéticos guían las estrategias de optimización.
- Regulación Metabólica: Km ayuda a entender cómo las enzimas responden a los cambios en la concentración de sustrato en las vías metabólicas y cómo se regulan estas vías.
Para ilustrar cómo estos parámetros pueden variar y qué implicaciones tienen, consideremos una tabla comparativa simplificada:
| Parámetro | Descripción | Valor Bajo Implica | Valor Alto Implica |
|---|---|---|---|
| Vmax | Velocidad máxima de reacción | Baja capacidad catalítica de la enzima | Alta capacidad catalítica de la enzima |
| Km | Concentración de sustrato a 1/2 Vmax | Alta afinidad de la enzima por el sustrato | Baja afinidad de la enzima por el sustrato |
| kcat | Número de recambio (eficiencia catalítica) | Lenta conversión de sustrato a producto | Rápida conversión de sustrato a producto |
| kcat/Km | Eficiencia catalítica general | Baja eficiencia (enzima menos 'perfecta') | Alta eficiencia (enzima más 'perfecta') |
La relación kcat/Km es particularmente importante, ya que se considera una medida de la eficiencia catalítica general de una enzima. Una enzima con un alto kcat/Km es muy eficiente, incluso a bajas concentraciones de sustrato, acercándose al límite de difusión, donde la velocidad de la reacción está limitada solo por la rapidez con la que el sustrato puede difundirse y colisionar con la enzima.
Preguntas Frecuentes sobre Vmax y Km
¿Qué significa que una enzima tenga un Km bajo?
Un Km bajo significa que la enzima tiene una alta afinidad por su sustrato. Esto indica que se necesita una concentración de sustrato relativamente baja para que la enzima alcance la mitad de su velocidad máxima. Es decir, la enzima se une eficientemente a su sustrato.

¿La Vmax de una enzima puede cambiar?
Sí, la Vmax de una enzima puede cambiar. Aunque es un parámetro intrínseco para una cantidad dada de enzima y un sustrato específico, puede variar si cambia la concentración total de la enzima ([Et]), la temperatura, el pH o si hay presencia de inhibidores no competitivos o mixtos que afectan la capacidad catalítica de la enzima.
¿Cómo afectan los inhibidores a Vmax y Km?
- Inhibidores competitivos: Aumentan el Km aparente (disminuyen la afinidad aparente del sustrato) pero no afectan la Vmax. Se puede superar su efecto aumentando la concentración de sustrato.
- Inhibidores no competitivos: Disminuyen la Vmax aparente (reducen la capacidad catalítica) pero no afectan el Km. No se puede superar su efecto con mayor sustrato.
- Inhibidores acompetitivos: Disminuyen tanto la Vmax aparente como el Km aparente.
¿Es Vmax lo mismo que la velocidad inicial de la reacción?
No, Vmax es la velocidad máxima teórica que una enzima puede alcanzar cuando está completamente saturada con sustrato. La velocidad inicial (Vo) es la velocidad de la reacción al comienzo del experimento, cuando la concentración de sustrato es conocida y la acumulación de producto es mínima. Vo es lo que se mide experimentalmente a diferentes concentraciones de sustrato para luego calcular Vmax.
¿Por qué es importante el número de recambio (kcat)?
El número de recambio (kcat) es una medida de la eficiencia catalítica de una enzima. Indica cuántas moléculas de sustrato puede convertir una sola molécula de enzima en producto por segundo cuando está saturada. Un kcat alto significa una enzima muy rápida y eficiente en su función catalítica.
Conclusión
El cálculo y la interpretación de Vmax y Km son pilares fundamentales en el estudio de la cinética enzimática. Estas constantes no solo nos permiten cuantificar la velocidad máxima de una reacción catalizada y la afinidad de una enzima por su sustrato, sino que también ofrecen una ventana invaluable a los mecanismos de regulación enzimática, el diseño de fármacos y la comprensión de enfermedades metabólicas. A través de herramientas como el gráfico de Lineweaver-Burk, los científicos pueden desentrañar el comportamiento de estas extraordinarias moléculas, abriendo caminos para avances en la medicina, la biotecnología y más allá. Dominar estos conceptos es, sin duda, un paso esencial para cualquiera que desee profundizar en el fascinante mundo de la bioquímica.
Si quieres conocer otros artículos parecidos a Cálculo de Vmax y Km: Desentrañando la Cinética Enzimática puedes visitar la categoría Cálculos.