04/01/2024
El agua, esa sustancia omnipresente y fundamental para la vida, es mucho más que un simple líquido transparente. Su fórmula química, H2O, encierra un universo de propiedades y características que la hacen única. Pero, ¿alguna vez te has preguntado cómo se determina la cantidad de masa de agua presente en una muestra o, más fascinante aún, cuánta agua se forma en una reacción química? Entender cómo calcular la masa del agua es una habilidad crucial no solo para estudiantes de química, sino para cualquiera interesado en comprender los principios fundamentales que rigen la materia y sus transformaciones.

Desde la producción industrial hasta la investigación científica y la vida cotidiana, saber cómo manejar las cantidades de sustancias es esencial. En este artículo, desglosaremos paso a paso los métodos para calcular la masa del agua, profundizando en conceptos clave como la masa molecular, el mol y la inmutable Ley de Conservación de la Masa. Prepárate para sumergirte en el fascinante mundo de la estequiometría y descubrir los secretos detrás de la cuantificación de nuestro recurso más preciado.
- Comprendiendo la Masa Molecular del Agua (H2O)
- La Ley de Conservación de la Masa: Un Principio Fundamental
- Calculando la Masa de Agua Formada en una Reacción Química
- Ejemplo Práctico: Reacción de Hidrógeno y Oxígeno para Formar Agua
- Tabla Resumen del Ejemplo de Reacción
- Factores a Considerar y Errores Comunes
- Aplicaciones Prácticas del Cálculo de la Masa de Agua
- Preguntas Frecuentes (FAQ)
- Conclusión
Comprendiendo la Masa Molecular del Agua (H2O)
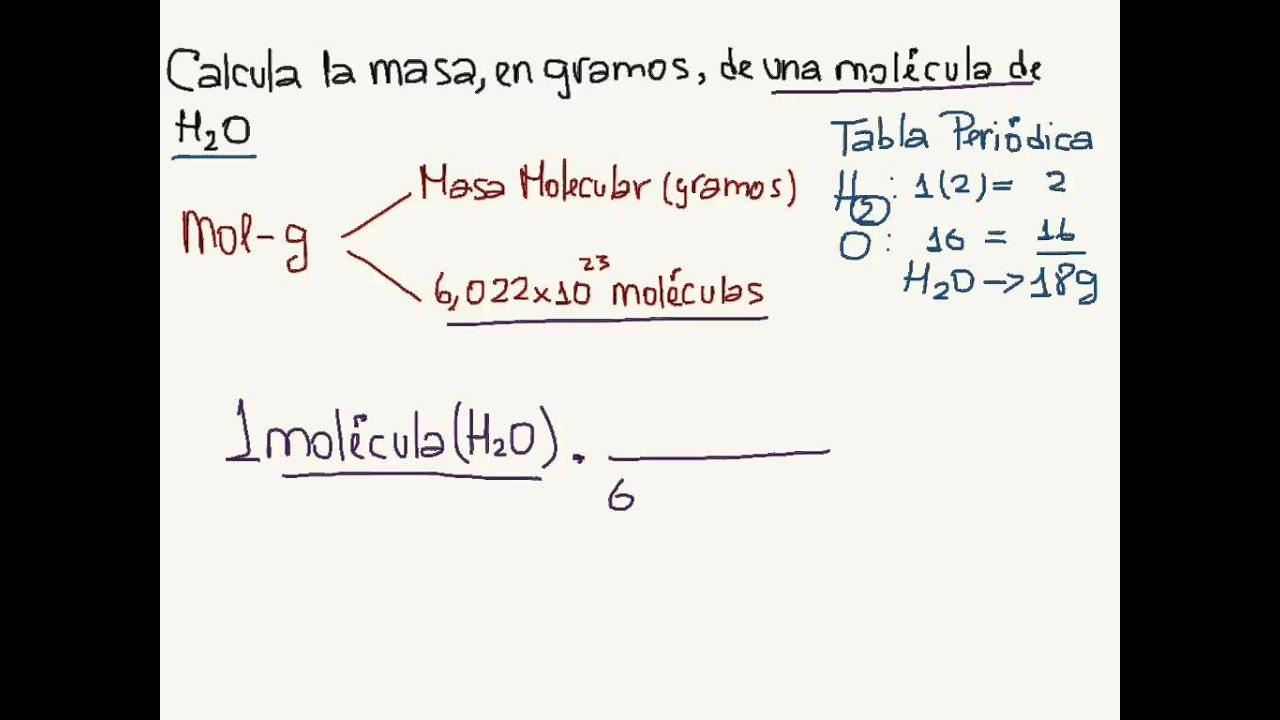
Antes de sumergirnos en cálculos complejos, es fundamental entender de qué está hecha el agua y cómo se determina su 'peso' a nivel molecular. La fórmula H2O nos indica que una molécula de agua está compuesta por dos átomos de hidrógeno (H) y un átomo de oxígeno (O). Cada uno de estos átomos tiene una masa atómica específica, que se puede encontrar en la tabla periódica.
- Hidrógeno (H): La masa atómica promedio del hidrógeno es aproximadamente 1.008 unidades de masa atómica (uma).
- Oxígeno (O): La masa atómica promedio del oxígeno es aproximadamente 15.999 uma.
Para calcular la masa molecular del agua, simplemente sumamos las masas atómicas de todos los átomos presentes en la molécula:
Masa molecular de H2O = (2 × Masa atómica de H) + (1 × Masa atómica de O)
Masa molecular de H2O = (2 × 1.008 uma) + (1 × 15.999 uma)
Masa molecular de H2O = 2.016 uma + 15.999 uma
Masa molecular de H2O = 18.015 uma
Esta es la masa de una sola molécula de agua. Sin embargo, en el mundo real, trabajamos con cantidades mucho mayores de moléculas. Aquí es donde entra en juego el concepto de mol y la masa molar.
El Concepto de Mol y la Masa Molar
Un mol es una unidad fundamental en química que representa una cantidad específica de partículas (átomos, moléculas, iones, etc.). Es similar a una docena, pero en lugar de 12, un mol contiene aproximadamente 6.022 x 10^23 partículas (el número de Avogadro). La gran ventaja del mol es que la masa molar de una sustancia (la masa de un mol de esa sustancia) en gramos es numéricamente igual a su masa molecular en uma.
Así, si la masa molecular del agua es 18.015 uma, entonces la masa molar del agua es 18.015 gramos por mol (g/mol). Esta relación es crucial para convertir entre masa y moles, una conversión constante en los cálculos químicos.
La Ley de Conservación de la Masa: Un Principio Fundamental
Uno de los pilares de la química es la Ley de Conservación de la Masa, postulada por Antoine Lavoisier. Esta ley establece que la masa no se crea ni se destruye en una reacción química ordinaria; simplemente se transforma de una forma a otra. En términos más sencillos, la masa total de los reactivos (las sustancias iniciales) en una reacción debe ser igual a la masa total de los productos (las sustancias formadas).
Este principio es vital cuando calculamos la masa de agua formada en una reacción, ya que nos asegura que la cantidad de átomos de hidrógeno y oxígeno que entran en la reacción son los mismos que salen, solo que reorganizados para formar moléculas de agua (y posiblemente otras sustancias).
Calculando la Masa de Agua Formada en una Reacción Química
El cálculo de la masa de agua producida en una reacción química es un ejercicio de estequiometría. La estequiometría es la rama de la química que estudia las relaciones cuantitativas entre los reactivos y productos en las reacciones químicas. Para realizar estos cálculos, necesitamos una ecuación química balanceada, que nos proporciona las proporciones molares entre las sustancias.

Pasos Generales para el Cálculo
- Escribir y Balancear la Ecuación Química: Asegúrate de que el número de átomos de cada elemento sea el mismo en ambos lados de la ecuación (reactivos y productos).
- Calcular las Masas Molares: Determina la masa molar de todas las sustancias involucradas en la reacción (reactivos y productos) utilizando las masas atómicas de la tabla periódica.
- Convertir la Masa Dada a Moles: Si se te da la masa de un reactivo, conviértela a moles usando su masa molar (Moles = Masa dada / Masa molar).
- Identificar el Reactivo Limitante (si aplica): En reacciones donde se dan las cantidades de más de un reactivo, uno de ellos se agotará primero y limitará la cantidad de producto que se puede formar. Este es el reactivo limitante.
- Usar las Proporciones Molares: Utiliza los coeficientes de la ecuación balanceada para determinar la relación molar entre el reactivo limitante (o el reactivo conocido) y el agua producida.
- Convertir Moles de Agua a Masa: Una vez que tengas los moles de agua formados, conviértelos a masa usando la masa molar del agua (Masa = Moles × Masa molar).
Ejemplo Práctico: Reacción de Hidrógeno y Oxígeno para Formar Agua
Consideremos el ejemplo clásico de la formación de agua a partir de hidrógeno y oxígeno gaseosos. Se nos pide calcular la masa de agua producida a partir de 8 gramos de hidrógeno y 8 gramos de oxígeno.
Vamos a aplicar los pasos descritos:
Paso 1: Escribir y Balancear la Ecuación Química
La reacción entre hidrógeno (H2) y oxígeno (O2) para formar agua (H2O) es:
2H2 (g) + O2 (g) → 2H2O (l)
Esta ecuación nos dice que 2 moles de hidrógeno reaccionan con 1 mol de oxígeno para producir 2 moles de agua.
Paso 2: Calcular las Masas Molares
- Masa molar de H2 = 2 × 1.008 g/mol = 2.016 g/mol (aproximadamente 2 g/mol)
- Masa molar de O2 = 2 × 15.999 g/mol = 31.998 g/mol (aproximadamente 32 g/mol)
- Masa molar de H2O = 18.015 g/mol (aproximadamente 18 g/mol)
Paso 3: Convertir la Masa Dada a Moles
Tenemos 8 gramos de hidrógeno y 8 gramos de oxígeno.
- Moles de H2 = Masa de H2 / Masa molar de H2 = 8 g / 2.016 g/mol ≈ 3.968 moles (o 8g / 2g/mol = 4 moles, usando la aproximación)
- Moles de O2 = Masa de O2 / Masa molar de O2 = 8 g / 31.998 g/mol ≈ 0.250 moles (o 8g / 32g/mol = 0.25 moles, usando la aproximación)
Paso 4: Identificar el Reactivo Limitante
Para determinar cuál es el reactivo limitante, comparamos la relación molar de los reactivos con la que se necesita según la ecuación balanceada.
Según la ecuación: 2 moles de H2 reaccionan con 1 mol de O2 (relación 2:1).
- Si tuviéramos 0.250 moles de O2, ¿cuántos moles de H2 necesitaríamos?
Moles de H2 necesarios = 0.250 moles O2 × (2 moles H2 / 1 mol O2) = 0.500 moles H2
Tenemos 3.968 moles de H2 disponibles, y solo necesitamos 0.500 moles de H2 para reaccionar completamente con los 0.250 moles de O2. Esto significa que tenemos un exceso de hidrógeno y que el oxígeno (O2) es el reactivo limitante.
Paso 5: Usar las Proporciones Molares para Calcular los Moles de Agua
Ahora, usamos el reactivo limitante (O2) para calcular cuántos moles de agua se formarán. Según la ecuación balanceada, 1 mol de O2 produce 2 moles de H2O.
Moles de H2O producidos = 0.250 moles O2 × (2 moles H2O / 1 mol O2) = 0.500 moles H2O
Paso 6: Convertir Moles de Agua a Masa
Finalmente, convertimos los moles de agua producidos a gramos usando la masa molar del agua:
Masa de H2O = Moles de H2O × Masa molar de H2O
Masa de H2O = 0.500 moles × 18.015 g/mol
Masa de H2O ≈ 9.0075 gramos
Por lo tanto, con 8 gramos de hidrógeno y 8 gramos de oxígeno, la masa de agua producida es aproximadamente 9 gramos.

Verificación con la Ley de Conservación de la Masa
Es importante notar que, aunque iniciamos con 16 gramos de reactivos (8g H2 + 8g O2), solo se formaron 9 gramos de agua. Esto no contradice la Ley de Conservación de la Masa. Lo que sucede es que el reactivo en exceso (hidrógeno) no se consume por completo.
- Masa de H2 inicial = 8 g
- Masa de H2 consumida = 0.500 moles H2 × 2.016 g/mol H2 ≈ 1.008 g H2
- Masa de H2 sin reaccionar = 8 g - 1.008 g = 6.992 g H2
Entonces, al final de la reacción, tenemos:
- 9.0075 gramos de H2O
- 6.992 gramos de H2 sin reaccionar
La masa total de las sustancias al final de la reacción es 9.0075 g + 6.992 g = 15.9995 g, lo cual es prácticamente igual a los 16 gramos iniciales, confirmando la Ley de Conservación de la Masa.
Tabla Resumen del Ejemplo de Reacción
Para una mejor comprensión, la siguiente tabla resume los datos y cálculos clave para la reacción de formación de agua:
| Sustancia | Fórmula | Masa Molar (g/mol) | Masa Inicial (g) | Moles Iniciales | Moles Reaccionados/Producidos | Masa Final (g) |
|---|---|---|---|---|---|---|
| Hidrógeno | H2 | 2.016 | 8 | 3.968 | 0.500 (reaccionaron) | 6.992 (sin reaccionar) |
| Oxígeno | O2 | 31.998 | 8 | 0.250 | 0.250 (reaccionaron) | 0 (limitante) |
| Agua | H2O | 18.015 | 0 | 0 | 0.500 (producidos) | 9.0075 |
Factores a Considerar y Errores Comunes
Al realizar cálculos de masa en reacciones químicas, es crucial prestar atención a ciertos detalles para evitar errores:
- Balanceo de la Ecuación: Un error en el balanceo de la ecuación llevará a proporciones molares incorrectas y, por lo tanto, a resultados erróneos. Siempre verifica que la ecuación esté correctamente balanceada.
- Identificación del Reactivo Limitante: No siempre se consumen todos los reactivos por completo. Si hay más de un reactivo y se proporcionan sus cantidades, es fundamental identificar cuál se agotará primero, ya que este determinará la cantidad máxima de producto que se puede formar.
- Uso Correcto de Unidades: Asegúrate de usar las unidades correctas (gramos para masa, g/mol para masa molar, moles para cantidad de sustancia). Las conversiones incorrectas son una fuente común de errores.
- Precisión de las Masas Atómicas: Aunque se pueden usar aproximaciones (como 1 para H y 16 para O), usar valores más precisos de la tabla periódica (como 1.008 y 15.999) proporcionará resultados más exactos.
- Pureza de los Reactivos: En la práctica real, los reactivos rara vez son 100% puros. Las impurezas no reaccionan de la misma manera y pueden afectar la masa de producto obtenida. Los cálculos estequiométricos asumen reactivos puros a menos que se especifique lo contrario.
Aplicaciones Prácticas del Cálculo de la Masa de Agua
Calcular la masa de agua, ya sea en una muestra o como producto de una reacción, tiene numerosas aplicaciones:
- Química Analítica: Determinar la cantidad de agua en una muestra es vital en análisis de humedad, control de calidad en alimentos, productos farmacéuticos y otros materiales.
- Ingeniería Química: En la producción industrial, estos cálculos son esenciales para optimizar procesos, predecir rendimientos de productos y diseñar reactores.
- Biología y Medio Ambiente: Comprender el ciclo del agua, la hidratación de organismos o la formación de agua en procesos biológicos (como la respiración celular) requiere estos conocimientos.
- Investigación Científica: En cualquier experimento que involucre agua como reactivo o producto, la cuantificación precisa de su masa es fundamental para la validez de los resultados.
Preguntas Frecuentes (FAQ)
¿Cuál es la diferencia entre masa atómica y masa molecular?
La masa atómica es la masa de un solo átomo de un elemento, expresada en unidades de masa atómica (uma). La masa molecular es la suma de las masas atómicas de todos los átomos que componen una molécula, también expresada en uma. Por ejemplo, la masa atómica del oxígeno es ~16 uma, mientras que la masa molecular del agua (H2O) es ~18 uma.
¿Por qué es importante el concepto de mol en estos cálculos?
El concepto de mol es crucial porque los átomos y las moléculas son extremadamente pequeños y no se pueden contar individualmente. El mol nos permite trabajar con cantidades macroscópicas de sustancias, relacionando el número de partículas con una masa medible en gramos (la masa molar). Es el puente entre el mundo atómico y el mundo que podemos percibir y pesar.
¿Siempre se usa la ley de conservación de la masa?
Sí, la Ley de Conservación de la Masa es un principio fundamental que se aplica a todas las reacciones químicas ordinarias. En el contexto de los cálculos de masa, significa que la masa total de los reactivos que entran en una reacción es igual a la masa total de los productos que salen, incluso si algunos reactivos no se consumen por completo.
¿Qué pasa si los reactivos no son puros?
Si los reactivos no son puros, la masa de las impurezas debe restarse de la masa total de la muestra para obtener la masa real del reactivo. Los cálculos estequiométricos solo se aplican a la parte pura de la sustancia que participa en la reacción. La presencia de impurezas reducirá la cantidad de producto que se puede formar a partir de una masa dada de muestra impura.
¿Cómo se calcula la masa de agua si tengo su volumen?
Si tienes el volumen de agua, puedes calcular su masa utilizando su densidad. La densidad es la masa por unidad de volumen (Densidad = Masa / Volumen). Para el agua líquida a 4°C, su densidad es aproximadamente 1 g/mL (o 1000 kg/m³). Así, si tienes 100 mL de agua, su masa sería 100 mL * 1 g/mL = 100 gramos. Sin embargo, este método es para una muestra de agua existente, no para la masa de agua formada en una reacción química, que es el enfoque principal de este artículo.
Conclusión
Calcular la masa del agua, ya sea su masa molecular o la cantidad formada en una reacción, es una habilidad esencial que integra varios principios químicos fundamentales. Desde la comprensión de las masas atómicas y moleculares hasta la aplicación del concepto de mol y la inquebrantable Ley de Conservación de la Masa, cada paso es crucial para obtener resultados precisos. Dominar estos cálculos no solo te permitirá resolver problemas de química, sino también apreciar la precisión y el orden inherentes a las transformaciones de la materia. El agua, en su aparente simplicidad, nos revela la complejidad y la belleza de las leyes que rigen nuestro universo.
Si quieres conocer otros artículos parecidos a Calcular la Masa del Agua (H2O): Guía Completa puedes visitar la categoría Cálculos.