15/04/2025
En el vasto universo de las matemáticas y las ciencias, existen conceptos que, aunque complejos en su esencia, resultan fundamentales para comprender cómo evolucionan y se transforman los sistemas a lo largo del tiempo. Uno de estos conceptos cruciales es la vida media, también conocida como periodo de semidesintegración. Ya sea que estemos hablando de la velocidad a la que una reacción química progresa o del ritmo al que un isótopo radiactivo se descompone, la vida media nos proporciona una medida invaluable del tiempo necesario para que una cantidad inicial se reduzca exactamente a la mitad. Este artículo se adentrará en las profundidades de este fascinante concepto, explorando su definición, sus fórmulas de cálculo y sus diversas aplicaciones, tanto en la química como en la física, y cómo las calculadoras son herramientas esenciales para su determinación.

- ¿Qué es la Vida Media? Una Definición Clara
- La Vida Media en Reacciones Químicas: El Caso del Primer Orden
- La Vida Media en la Desintegración Radiactiva
- Diferenciando Vida Media (Half-Life) y Vida Promedio (Mean Life)
- Cómo Calcular la Vida Media: Un Resumen Práctico
- Importancia y Aplicaciones de la Vida Media
- Preguntas Frecuentes sobre la Vida Media
¿Qué es la Vida Media? Una Definición Clara
La vida media (t1/2) se define como el tiempo requerido para que la concentración de un reactivo disminuya a la mitad de su valor inicial en una reacción química, o para que la cantidad de núcleos de una sustancia radiactiva se reduzca a la mitad debido a la desintegración. Es un concepto estadístico que no se refiere a la vida de un átomo individual, sino al comportamiento colectivo de una gran cantidad de ellos. Si bien la idea es sencilla, su cálculo y significado varían ligeramente dependiendo del contexto en el que se aplique, principalmente en la cinética química y la física nuclear.
Entender la vida media es fundamental porque nos permite predecir la cantidad de sustancia que quedará después de un cierto período de tiempo o, inversamente, estimar cuánto tiempo ha transcurrido basándose en la cantidad actual de una sustancia. Es un indicador directo de la velocidad de un proceso de decaimiento o de reacción. Una vida media corta implica un proceso rápido, mientras que una vida media larga indica un proceso lento y duradero.
La Vida Media en Reacciones Químicas: El Caso del Primer Orden
En el ámbito de la cinética química, la vida media es una herramienta poderosa para describir la velocidad de una reacción. Sin embargo, es vital destacar que su comportamiento no es constante para todos los órdenes de reacción. Para las reacciones de primer orden, la vida media posee una característica única y muy útil: es una constante, independiente de la concentración inicial de los reactivos. Esto significa que el tiempo que tarda la concentración en reducirse a la mitad siempre será el mismo, sin importar cuán alta o baja sea la concentración inicial.
Derivación de la Fórmula para Reacciones de Primer Orden
Para comprender cómo se calcula la vida media en una reacción de primer orden, partimos de la ley de velocidad integrada para este tipo de reacciones, que relaciona la concentración de un reactivo con el tiempo. La ecuación es:
ln([A]0 / [A]) = kt
Donde:
[A]0es la concentración inicial del reactivo.[A]es la concentración del reactivo en el tiempot.kes la constante de velocidad de la reacción.tes el tiempo transcurrido.
Por definición, en el tiempo de vida media (t1/2), la concentración del reactivo [A] se reduce a la mitad de su valor inicial, es decir, [A] = [A]0 / 2. Sustituyendo esta condición en la ecuación anterior:
ln([A]0 / ([A]0 / 2)) = k * t1/2
Simplificando la expresión dentro del logaritmo natural, obtenemos:
ln(2) = k * t1/2
Sabiendo que el logaritmo natural de 2 es aproximadamente 0.693 (a tres decimales), podemos reorganizar la ecuación para obtener la fórmula de la vida media para una reacción de primer orden:
t1/2 = 0.693 / k
Esta fórmula es extremadamente valiosa, ya que nos permite calcular la vida media si conocemos la constante de velocidad, o viceversa. Su independencia de la concentración inicial es lo que la hace tan única y predecible en este tipo de reacciones.
Comportamiento de la Concentración a lo Largo de las Vidas Medias
Una de las implicaciones más interesantes de la vida media constante para las reacciones de primer orden es cómo la concentración del reactivo disminuye en cada periodo sucesivo. Después de cada vida media, la cantidad de reactivo se reduce a la mitad de lo que quedaba al inicio de ese periodo. Esto puede ilustrarse con la siguiente tabla:
| Número de Vidas Medias (n) | Porcentaje de Reactivo Restante | Expresión Matemática |
|---|---|---|
| 1 | 50% | (1/2) * 100% |
| 2 | 25% | (1/2)2 * 100% |
| 3 | 12.5% | (1/2)3 * 100% |
| n | (100 / 2n)% | (1/2)n * 100% |
Esta tabla demuestra claramente que la cantidad de reactivo que queda después de 'n' vidas medias de una reacción de primer orden es (1/2)n veces la concentración inicial. Este patrón predecible es una de las razones por las que la vida media es tan útil en la cinética de reacciones de primer orden.

La Vida Media en la Desintegración Radiactiva
Más allá de las reacciones químicas, el concepto de vida media encuentra una aplicación quizás aún más conocida en la física nuclear, específicamente en la descripción de la desintegración de isótopos radiactivos. Al igual que las reacciones de primer orden, la desintegración radiactiva sigue una cinética de primer orden, lo que significa que la vida media de un isótopo radiactivo es una constante, característica de ese isótopo particular, e independiente de la cantidad inicial de material.
Los núcleos atómicos inestables se desintegran espontáneamente, emitiendo partículas y/o radiación electromagnética (radiación gamma) para transformarse en núcleos más estables. Este proceso es completamente aleatorio a nivel de un solo átomo, pero predecible cuando se considera una gran cantidad de átomos. La vida media de un isótopo radiactivo es el tiempo que tarda la mitad de una muestra de ese isótopo en desintegrarse.
Fórmula para la Vida Media de Isótopos Radiactivos
Para calcular la vida media de un isótopo radiactivo, se utiliza una fórmula análoga a la de las reacciones de primer orden:
t1/2 = 0.693 / λ
Donde:
t1/2es la vida media del isótopo.λ(lambda) es la constante de desintegración, que representa la probabilidad de que un núcleo individual se desintegre por unidad de tiempo. Es una propiedad intrínseca de cada isótopo radiactivo.
Por ejemplo, el plutonio-239 (Pu-239), un isótopo utilizado en armas nucleares y reactores, tiene una vida media de aproximadamente 24,200 años. Esto significa que si tuviéramos 1 kg de Pu-239, después de 24,200 años solo quedarían 500 gramos de Pu-239, mientras que los otros 500 gramos se habrían transformado en uranio-235 (U-235), que a su vez tiene una vida media de unos 700 millones de años. Otros isótopos, como el Yodo-131 (usado en medicina nuclear), tienen vidas medias de solo unos pocos días, lo que los hace ideales para aplicaciones donde se requiere que la radiactividad desaparezca rápidamente del cuerpo.
Diferenciando Vida Media (Half-Life) y Vida Promedio (Mean Life)
Es importante no confundir el concepto de vida media (traducido del inglés "half-life") con el de vida promedio (traducido del inglés "mean life"). Aunque ambos están relacionados con la duración de los núcleos radiactivos y las constantes de desintegración, representan ideas ligeramente diferentes:
- Vida Media (t1/2): Como ya se explicó, es el tiempo que tarda la mitad de los núcleos radiactivos en una muestra en desintegrarse. Es el periodo tras el cual la cantidad original de sustancia se reduce a la mitad.
- Vida Promedio (τ, tau): También conocida como tiempo de vida medio o vida media estadística. Es el tiempo promedio que un núcleo individual de una sustancia radiactiva vive antes de desintegrarse. Dado que la desintegración es un fenómeno aleatorio, es imposible predecir cuándo se desintegrará un núcleo específico, pero podemos calcular un promedio para un gran conjunto de ellos.
La relación entre la vida promedio y la constante de desintegración (λ) es bastante directa:
τ = 1 / λ
De esta relación, y de la fórmula de la vida media, podemos deducir la conexión entre ambas:
t1/2 = 0.693 / λ = 0.693 * (1 / λ) = 0.693 * τ
Así, la vida media es numéricamente igual al logaritmo natural de 2 (0.693) multiplicado por la vida promedio. Esta distinción es crucial para evitar malentendidos en cálculos y aplicaciones científicas, especialmente en campos como la datación por carbono o la medicina nuclear.
Cómo Calcular la Vida Media: Un Resumen Práctico
Calcular la vida media es un proceso directo si se dispone de la información adecuada. Aquí se resumen los pasos y las fórmulas clave:
- Identificar el Contexto: ¿Es una reacción química o la desintegración de un isótopo radiactivo?
- Determinar el Orden de la Reacción (si es química): La fórmula
t1/2 = 0.693 / ksolo es aplicable para reacciones de primer orden. Si la reacción es de orden cero o segundo, la vida media NO es constante y depende de la concentración inicial, requiriendo fórmulas integradas más complejas para cada caso. - Conocer la Constante (k o λ):
- Para reacciones de primer orden, se necesita la constante de velocidad (
k). - Para la desintegración radiactiva, se necesita la constante de desintegración (
λ).
- Para reacciones de primer orden, se necesita la constante de velocidad (
- Aplicar la Fórmula: Una vez que se tiene la constante pertinente, simplemente se divide 0.693 por ese valor.
Las calculadoras científicas son herramientas indispensables para realizar estos cálculos, especialmente cuando se trabaja con valores de constantes que pueden ser muy pequeños o muy grandes, o cuando se necesitan logaritmos naturales. Dominar el uso de estas funciones en su calculadora le permitirá determinar rápidamente las vidas medias y realizar predicciones precisas sobre la evolución de sistemas químicos y nucleares.
Importancia y Aplicaciones de la Vida Media
El concepto de vida media es mucho más que una simple fórmula matemática; es una piedra angular en diversas disciplinas científicas y tecnológicas. Sus aplicaciones son vastas y de gran impacto:
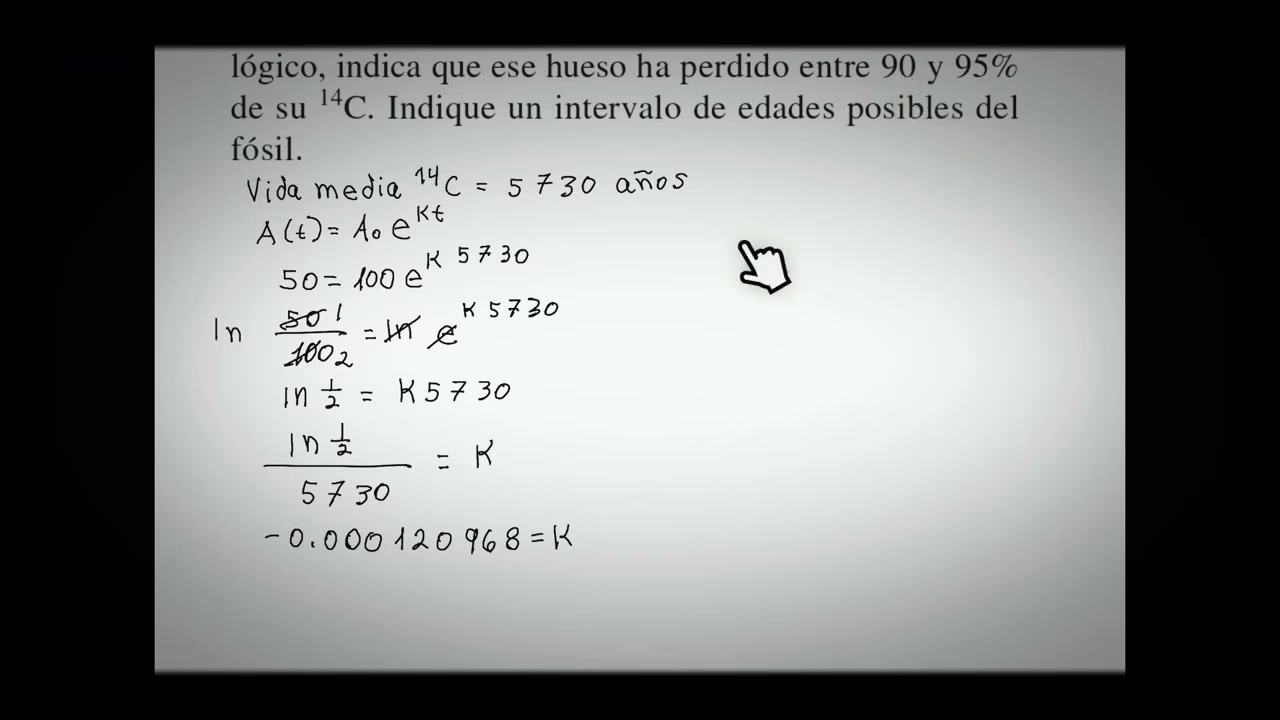
- Datación Radiométrica: Es el principio fundamental detrás de la datación por carbono-14, utilizada en arqueología y geología para determinar la edad de fósiles, artefactos y formaciones rocosas. Al medir la cantidad de un isótopo radiactivo restante y conocer su vida media, los científicos pueden estimar cuánto tiempo ha pasado desde que el organismo murió o la roca se formó.
- Medicina Nuclear: Isótopos con vidas medias cortas (como el Tecnecio-99m o el Yodo-131) se utilizan en diagnósticos por imagen (PET, SPECT) y tratamientos de cáncer. Su corta vida media asegura que la radiactividad disminuya rápidamente en el cuerpo del paciente, minimizando la exposición.
- Farmacocinética: En farmacología, la vida media de un fármaco en el cuerpo humano es crucial para determinar la dosis y la frecuencia de administración. Permite asegurar que el medicamento mantenga una concentración terapéutica efectiva sin acumularse a niveles tóxicos.
- Gestión de Residuos Radiactivos: La vida media de los materiales nucleares es un factor crítico en el diseño de instalaciones de almacenamiento de residuos nucleares. Los materiales con vidas medias muy largas requieren soluciones de almacenamiento que perduren por miles o incluso millones de años.
- Diseño de Reactores Nucleares: La vida media de los productos de fisión y los elementos combustibles influye en la seguridad y el manejo del combustible gastado en las centrales nucleares.
En resumen, la vida media es un concepto que trasciende las aulas de química y física, encontrando aplicaciones prácticas que afectan nuestra comprensión del pasado, nuestra salud y la gestión de tecnologías avanzadas.
Preguntas Frecuentes sobre la Vida Media
¿La vida media es siempre la misma para una sustancia?
Sí, para las reacciones de primer orden (como la desintegración radiactiva y muchas reacciones químicas), la vida media es una constante que solo depende de la constante de velocidad o la constante de desintegración. No depende de la concentración inicial de la sustancia. Sin embargo, para reacciones de orden cero o segundo, la vida media sí varía con la concentración inicial.
¿Qué significa una vida media corta o larga?
Una vida media corta indica que la sustancia se desintegra o reacciona muy rápidamente. Por ejemplo, algunos isótopos utilizados en medicina nuclear tienen vidas medias de minutos u horas para que su radiactividad desaparezca pronto del cuerpo. Una vida media larga significa que la sustancia decae o reacciona muy lentamente, como el uranio-238, cuya vida media es de miles de millones de años, lo que lo hace útil para la datación geológica.
¿La vida media implica que una sustancia desaparecerá por completo después de un cierto número de vidas medias?
No. Teóricamente, una sustancia nunca desaparecerá por completo, ya que la vida media significa que la cantidad se reduce a la mitad en cada período. Esto es una progresión geométrica que se acerca a cero pero nunca lo alcanza. Sin embargo, en la práctica, después de un número suficiente de vidas medias, la cantidad restante puede ser insignificante o indetectable.
¿La temperatura o la presión afectan la vida media de un isótopo radiactivo?
No, la vida media de un isótopo radiactivo es una propiedad nuclear intrínseca y no se ve afectada por factores externos como la temperatura, la presión, el estado de agregación, la combinación química (formando compuestos) o los campos magnéticos. Estos factores solo afectan las reacciones químicas, no los procesos nucleares.
La vida media es, sin duda, uno de los conceptos más poderosos y versátiles en las ciencias. Desde la datación de fósiles hasta el diseño de tratamientos médicos y la gestión de residuos nucleares, su comprensión nos permite cuantificar y predecir el comportamiento de sistemas complejos a lo largo del tiempo. Al dominar las fórmulas y los principios que la rigen, se abre una ventana a una comprensión más profunda de los procesos fundamentales que dan forma a nuestro mundo.
Si quieres conocer otros artículos parecidos a La Vida Media: Concepto, Cálculo y Aplicaciones puedes visitar la categoría Cálculos.