12/07/2024
En el vasto universo de la química, las reacciones no ocurren de forma instantánea ni lineal. Son procesos dinámicos que involucran colisiones moleculares, reordenamientos atómicos y transformaciones energéticas. En el corazón de cada reacción química se encuentra un punto crítico, un estado intermedio y altamente inestable conocido como el complejo activado. Este fugaz arreglo de átomos es el puente entre los reactivos iniciales y los productos finales, un momento de transición que determina si una colisión molecular será productiva o no. Comprender el complejo activado es fundamental para desentrañar la cinética química, predecir la velocidad de las reacciones y diseñar procesos eficientes en la industria y la investigación.
A menudo, nos preguntamos cómo es posible que las moléculas, a pesar de colisionar constantemente, no siempre den lugar a una reacción. La respuesta reside en la necesidad de alcanzar este estado de alta energía, el complejo activado, que solo se forma bajo condiciones específicas de energía y orientación. Este artículo explorará en profundidad qué es el complejo activado, cómo se 'determina' (dado que no es directamente observable), las fórmulas clave de la teoría que lo sustenta, su relación intrínseca con la energía de activación y, quizás lo más sorprendente, la increíblemente corta duración de su existencia.
- Comprendiendo el Complejo Activado: El Punto Cúlmine de una Reacción
- ¿Cómo se Determina el Complejo Activado?
- La Teoría del Complejo Activado: Una Mirada a las Fórmulas Clave
- Energía de Activación y el Complejo Activado: La Barrera a Superar
- La Efímera Vida del Complejo Activado: ¿Cuánto Dura Realmente?
- Comparación de Estados en una Reacción Química
- Preguntas Frecuentes sobre el Complejo Activado
Comprendiendo el Complejo Activado: El Punto Cúlmine de una Reacción
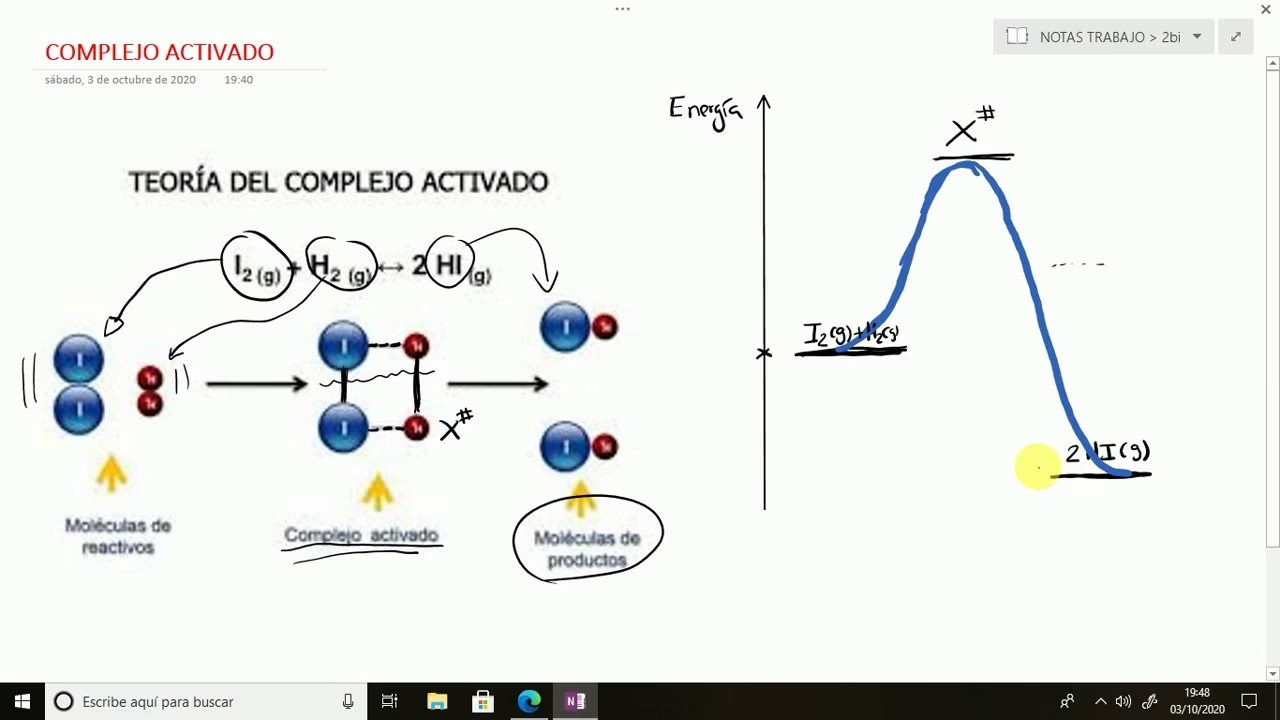
El complejo activado, también conocido como estado de transición, es una configuración molecular transitoria y de muy alta energía que se forma durante el curso de una reacción química. Imagina dos moléculas de reactivos acercándose. No todas las colisiones entre ellas resultarán en una reacción. Para que la transformación ocurra, deben chocar con suficiente energía y con la orientación espacial adecuada. Si estas condiciones se cumplen, los enlaces existentes en los reactivos comienzan a debilitarse o romperse, mientras que nuevos enlaces, que formarán parte de los productos, empiezan a establecerse. Este estado intermedio, donde los enlaces están parcialmente rotos y parcialmente formados, es precisamente el complejo activado.
Una de las características más distintivas del complejo activado es su extrema inestabilidad. Se encuentra en la cima de la barrera de energía de activación en un diagrama de energía de reacción, lo que significa que posee la mayor energía potencial de todo el proceso de reacción. Debido a esta alta energía, su existencia es increíblemente breve, apenas un parpadeo en la escala de tiempo molecular. Una vez que se forma, el complejo activado tiene dos destinos igualmente probables: puede desintegrarse y regresar a los reactivos originales, o puede continuar su camino y transformarse en los productos de la reacción. Esta dualidad es lo que lo convierte en un punto de decisión crítico en el camino de la reacción.
Su naturaleza fugaz y su alta energía hacen que el complejo activado sea extraordinariamente difícil de observar directamente. No es una especie química que pueda aislarse o detectarse con facilidad en un laboratorio. En cambio, su existencia se infiere a partir de la cinética de la reacción y de modelos teóricos que describen el camino energético que siguen las moléculas durante una transformación química. La comprensión de este estado transitorio es esencial para desentrañar los mecanismos de reacción y optimizar las condiciones para la síntesis de nuevos compuestos.
¿Cómo se Determina el Complejo Activado?
Dado que el complejo activado es una entidad teórica y transitoria, su 'determinación' no implica una observación directa o un aislamiento físico. Más bien, se 'determina' o infiere a través de un análisis profundo de la cinética de las reacciones y de la aplicación de la Teoría del Estado de Transición (TET). La TET, desarrollada por Henry Eyring y Michael Polanyi en la década de 1930, proporciona un marco conceptual y matemático para entender cómo las moléculas pasan de reactivos a productos a través de este estado intermedio.
La determinación del complejo activado se basa en:
- Análisis de la Cinética de Reacción: Midiendo la velocidad de una reacción bajo diferentes condiciones (temperatura, concentración, presión), los científicos pueden obtener datos que revelan información sobre la barrera energética y la naturaleza del estado de transición. La dependencia de la velocidad con la temperatura, por ejemplo, permite calcular la energía de activación, un parámetro directamente relacionado con la energía del complejo activado.
- Cálculos Teóricos y Computacionales: En la química computacional moderna, es posible modelar las estructuras moleculares y sus energías. Utilizando métodos de química cuántica, como la teoría del funcional de la densidad (DFT), los investigadores pueden buscar puntos de silla en la superficie de energía potencial de una reacción. Estos puntos de silla representan el complejo activado, permitiendo predecir su geometría, vibraciones y energía. Aunque son modelos, estos cálculos proporcionan una imagen detallada de cómo podría ser el complejo activado.
- Estudios Experimentales Indirectos: Aunque no se puede 'ver' el complejo activado, ciertas técnicas experimentales pueden ofrecer pistas sobre su naturaleza. Por ejemplo, estudios con isótopos (efectos isotópicos cinéticos) pueden revelar qué enlaces se están rompiendo o formando en el estado de transición. La influencia del solvente o de la presión sobre la velocidad de reacción también puede dar indicios sobre el volumen o la polaridad del complejo activado.
En resumen, la determinación del complejo activado es un proceso intelectual y computacional que nos permite construir una imagen coherente de este estado efímero, crucial para comprender la reactividad química.
La Teoría del Complejo Activado: Una Mirada a las Fórmulas Clave
La Teoría del Estado de Transición (TET) es el pilar fundamental para comprender la formación y las propiedades del complejo activado. Esta teoría postula que, en el equilibrio entre los reactivos y el complejo activado, la velocidad de la reacción está determinada por la velocidad a la que el complejo activado se descompone para formar productos. Una de las ecuaciones clave derivadas de la TET relaciona la constante de velocidad de una reacción con las propiedades termodinámicas del complejo activado.
Una expresión importante dentro de este marco es la relacionada con la energía libre de Gibbs de activación, ΔG*. Esta magnitud termodinámica representa la barrera energética que debe superarse para que los reactivos se transformen en el complejo activado. Para un caso específico, donde 'n' representa el cambio en el número de moles de gas al pasar de los reactivos al complejo activado, la energía libre de Gibbs de activación puede expresarse como:
ΔG* = Ea - ΔnRT
Donde:
- ΔG* es la energía libre de Gibbs de activación. Un valor más alto de ΔG* implica una barrera energética mayor y, por lo tanto, una reacción más lenta.
- Ea es una energía asociada con el proceso de formación del complejo activado, que en este contexto específico de la fórmula (205) mencionada en la fuente, se relaciona con una energía de activación particular dentro de esa derivación. Es importante no confundirla directamente con la energía de activación de Arrhenius de forma general, aunque ambas describen barreras energéticas.
- Δn es el cambio en el número de moles de gas al pasar de los reactivos al complejo activado. Por ejemplo, si dos moléculas de gas reaccionan para formar un complejo activado que es una única 'molécula' (aunque inestable), Δn sería -1.
- R es la constante de los gases ideales (8.314 J/mol·K).
- T es la temperatura absoluta en Kelvin.
Esta fórmula nos permite ver cómo los cambios en el número de moles de gas durante la formación del complejo activado pueden influir en la energía libre necesaria para alcanzar ese estado. Es una manifestación de cómo la entropía (a través de Δn y T) y la energía (Ea) contribuyen a la dificultad de formar el estado de transición.
Además de esta, la TET también se expresa a través de la ecuación de Eyring, que relaciona la constante de velocidad (k) directamente con las propiedades termodinámicas del complejo activado (entalpía de activación ΔH* y entropía de activación ΔS*):
k = (kBT/h) * e(-ΔG*/RT) = (kBT/h) * e(ΔS*/R) * e(-ΔH*/RT)
Donde kB es la constante de Boltzmann y h es la constante de Planck. Esta ecuación es fundamental porque conecta la velocidad macroscópica de una reacción con las propiedades microscópicas del estado de transición, proporcionando una base teórica para comprender por qué algunas reacciones son rápidas y otras lentas.
Energía de Activación y el Complejo Activado: La Barrera a Superar
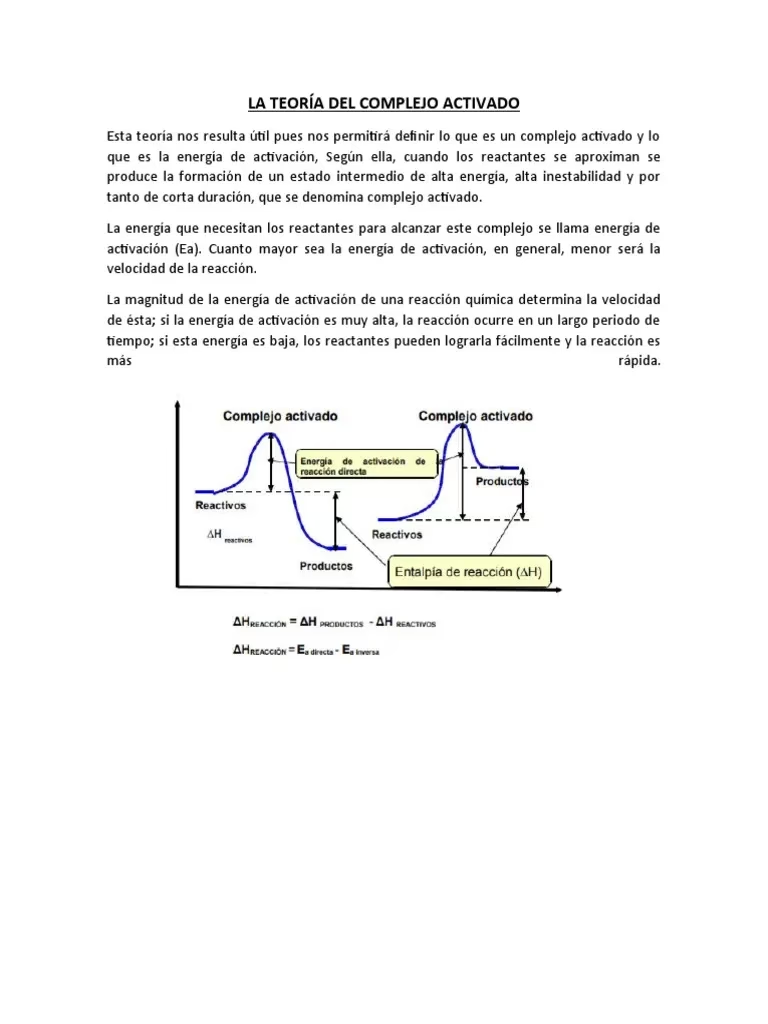
El concepto de energía de activación (Ea) está intrínsecamente ligado al complejo activado. Es la energía mínima que deben poseer las moléculas de los reactivos para que una colisión sea efectiva y conduzca a la formación del complejo activado, y posteriormente, a los productos. Imagina una colina que debes escalar para llegar al otro lado; la cima de esa colina representa la energía del complejo activado, y la altura de la colina desde el punto de partida de los reactivos es la energía de activación.
La relación entre la energía de activación y la velocidad de reacción se describe matemáticamente por la famosa ecuación de Arrhenius:
k = Ae(-Ea/RT)
Donde:
- k es la constante de velocidad de la reacción, que indica cuán rápida es la reacción.
- A es el factor pre-exponencial o factor de frecuencia. Representa la frecuencia de las colisiones entre las moléculas de los reactivos que tienen la orientación correcta para reaccionar. Es, en cierto modo, una medida de la frecuencia de los intentos de reacción.
- Ea es la energía de activación, medida en julios por mol (J/mol) o kilojulios por mol (kJ/mol). Cuanto mayor sea la Ea, más difícil será formar el complejo activado y, por lo tanto, más lenta será la reacción.
- R es la constante de los gases ideales.
- T es la temperatura absoluta en Kelvin.
El término exponencial, e(-Ea/RT), es crucial. Representa la fracción de las colisiones moleculares que poseen una energía igual o superior a la energía de activación a una temperatura dada. Solo estas colisiones 'energéticas' tienen el potencial de superar la barrera y formar el complejo activado. A medida que aumenta la temperatura (T), este término exponencial también aumenta, lo que significa que una mayor fracción de moléculas tiene suficiente energía, resultando en una constante de velocidad (k) mayor y, por ende, una reacción más rápida.
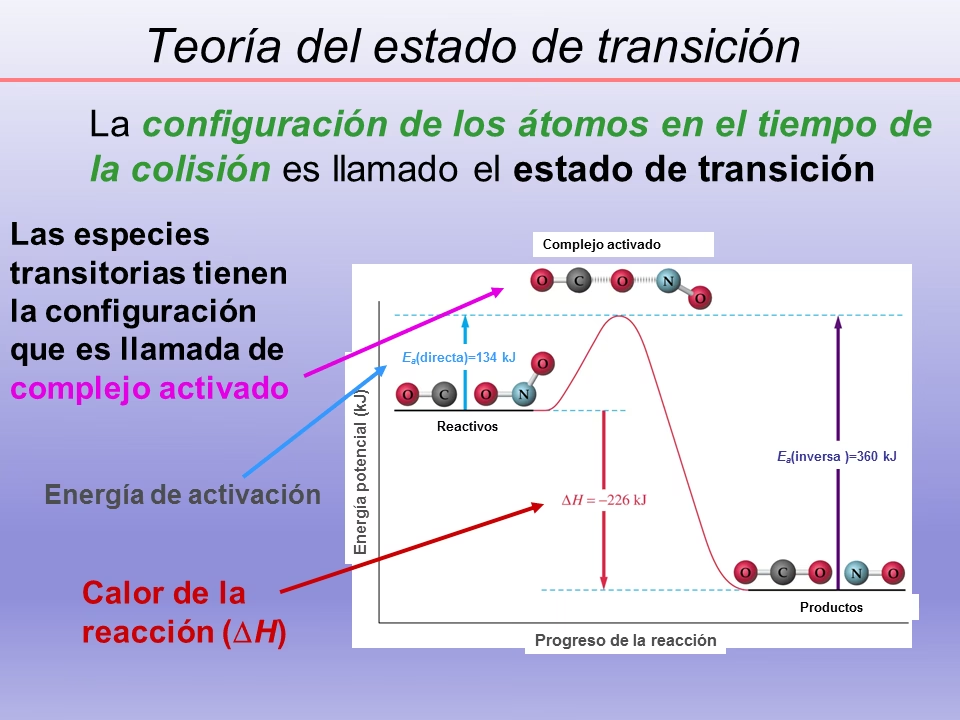
En resumen, el complejo activado se sitúa precisamente en el pico de la barrera de energía de activación. La energía de activación es la 'entrada' necesaria para llegar a ese estado de transición inestable, y la ecuación de Arrhenius nos permite cuantificar cómo esta energía influye en la velocidad global de la reacción.
La Efímera Vida del Complejo Activado: ¿Cuánto Dura Realmente?
Una de las características más asombrosas del complejo activado es su increíblemente corta duración. No es una molécula que pueda existir por un tiempo considerable ni ser aislada. Su vida útil se mide en femtosegundos (10-15 segundos), siendo el valor comúnmente citado alrededor de 10-13 segundos. Para poner esto en perspectiva, la luz tarda aproximadamente 300.000 veces más en viajar un milímetro que lo que dura un complejo activado.
Esta duración extremadamente breve se debe a su naturaleza altamente inestable y su alta energía. El complejo activado no es un mínimo de energía en la superficie de energía potencial, sino un punto de silla, lo que significa que es inestable en al menos una dirección (la dirección de la coordenada de reacción). Una vez que se forma, el sistema molecular se mueve rápidamente hacia un estado de menor energía, ya sea volviendo a los reactivos o avanzando hacia los productos.
Podemos pensar en el complejo activado como el instante en que un saltador de Velcro golpea una pared de Velcro. En ese brevísimo momento de impacto, antes de que el saltador se pegue firmemente o rebote, hay un estado de máxima interacción y tensión. En ese instante, hay una alta energía potencial. Inmediatamente después, el saltador o bien se adhiere (formando productos) o rebota (volviendo a reactivos). El complejo activado es ese punto crítico y transitorio de 'contacto' o 'transición' que define el éxito o fracaso de la reacción.
La imposibilidad de observar directamente el complejo activado se deriva precisamente de esta efímera existencia. Su estudio se basa en las consecuencias de su formación (la aparición de productos) y en modelos teóricos que nos permiten inferir sus propiedades.
Comparación de Estados en una Reacción Química
Para entender mejor el papel del complejo activado, es útil compararlo con los otros estados clave en una reacción química:
| Característica | Reactivos | Complejo Activado | Productos |
|---|---|---|---|
| Naturaleza | Moléculas estables al inicio de la reacción. | Arreglo inestable de átomos, transitorio. | Moléculas estables al final de la reacción. |
| Energía | Relativamente baja (punto de partida). | Muy alta (pico de la barrera de energía). | Baja (para reacciones exotérmicas) o alta (para endotérmicas) en relación a los reactivos, pero estable. |
| Estabilidad | Estable, existen por tiempo indefinido si no reaccionan. | Extremadamente inestable, existencia fugaz. | Estable, se acumulan al final de la reacción. |
| Duración | Indefinida (hasta que reaccionan). | Aproximadamente 10-13 segundos. | Indefinida. |
| Observabilidad | Directamente observables y aislables. | No observable directamente, inferido teóricamente. | Directamente observables y aislables. |
| Rol | Sustratos iniciales que se transforman. | Estado intermedio crucial que determina el éxito de la reacción. | Resultados finales de la reacción. |
Preguntas Frecuentes sobre el Complejo Activado
¿Qué es exactamente el complejo activado?
El complejo activado es un arreglo transitorio y altamente inestable de átomos que se forma en el pico de la barrera de energía de activación durante una reacción química. Es el estado intermedio entre los reactivos y los productos, donde los enlaces antiguos se están rompiendo y los nuevos se están formando.
¿Se puede observar el complejo activado directamente?
No, el complejo activado no puede observarse directamente debido a su extrema inestabilidad y su increíblemente corta duración (aproximadamente 10-13 segundos). Su existencia se infiere a partir de estudios cinéticos y cálculos teóricos de la superficie de energía potencial de las reacciones.
¿Cuál es la relación entre la energía de activación y el complejo activado?
La energía de activación (Ea) es la energía mínima necesaria para que los reactivos alcancen el estado del complejo activado. El complejo activado se encuentra en el punto más alto de la trayectoria energética de la reacción, que corresponde a la cima de la barrera de energía de activación.
¿Por qué es tan inestable el complejo activado?
Es inestable porque posee una energía muy alta en comparación con los reactivos y los productos. Se encuentra en un punto de silla en la superficie de energía potencial, lo que significa que cualquier pequeña desviación lo empujará rápidamente hacia los reactivos o hacia los productos, estados de menor energía y mayor estabilidad.
¿Qué factores influyen en la formación del complejo activado?
Los factores clave que influyen en la formación del complejo activado son la energía de las colisiones entre los reactivos (deben tener energía igual o mayor a la Ea) y la orientación espacial de las moléculas durante la colisión. Una orientación inadecuada, incluso con suficiente energía, puede impedir la formación del complejo activado.
El complejo activado es un concepto fundamental en la cinética química que nos permite comprender por qué y cómo ocurren las reacciones. Aunque su existencia es efímera y su naturaleza evasiva, su estudio teórico y sus implicaciones prácticas son inmensas, brindando una visión profunda de los mecanismos moleculares que rigen las transformaciones en nuestro mundo.
Si quieres conocer otros artículos parecidos a El Misterio del Complejo Activado: Desvelando su Naturaleza y Cálculo puedes visitar la categoría Cálculos.