23/04/2024
Desde los albores de la Revolución Industrial, la humanidad ha buscado incansablemente mejorar la eficiencia de las máquinas que transforman el calor en trabajo. Fue en este contexto, a principios de la década de 1820, cuando el ingeniero francés Sadi Carnot se propuso desentrañar los límites fundamentales de estas máquinas. Sus estudios culminaron en la propuesta de un ciclo de trabajo hipotético, conocido hoy como el ciclo de Carnot, que representa el máximo rendimiento posible entre dos reservorios de temperatura dados. Este ciclo ideal no solo sirve como modelo para centrales eléctricas y refrigeradores, sino que también es crucial para comprender la segunda ley de la termodinámica y establecer una escala de temperatura absoluta.
El concepto de rendimiento de Carnot es fundamental en la termodinámica, ya que establece un límite superior teórico para la eficiencia de cualquier máquina térmica. Ningún motor real puede superar este rendimiento, lo que lo convierte en una referencia esencial para ingenieros y científicos. Comprender cómo se calcula y qué factores lo afectan es clave para optimizar los sistemas energéticos y avanzar en el diseño de tecnologías más eficientes.
- ¿Qué es el Ciclo de Carnot?
- Cálculo del Rendimiento de Carnot
- El Principio de Carnot y la Segunda Ley de la Termodinámica
- Aplicaciones del Ciclo de Carnot: Refrigeradores y Bombas de Calor
- Ejemplos Prácticos de Cálculo
- Limitaciones y Realidad Práctica
- Tabla Comparativa: Máquina de Carnot vs. Máquina Real
- Preguntas Frecuentes (FAQ)
- ¿Por qué el rendimiento de Carnot es el máximo posible?
- ¿Las temperaturas deben estar en Kelvin para el cálculo del rendimiento de Carnot?
- ¿Puede una máquina real alcanzar el rendimiento de Carnot?
- ¿Cómo se puede aumentar la eficiencia de una máquina térmica real?
- ¿Es el ciclo de Carnot útil si no se puede construir en la práctica?
¿Qué es el Ciclo de Carnot?
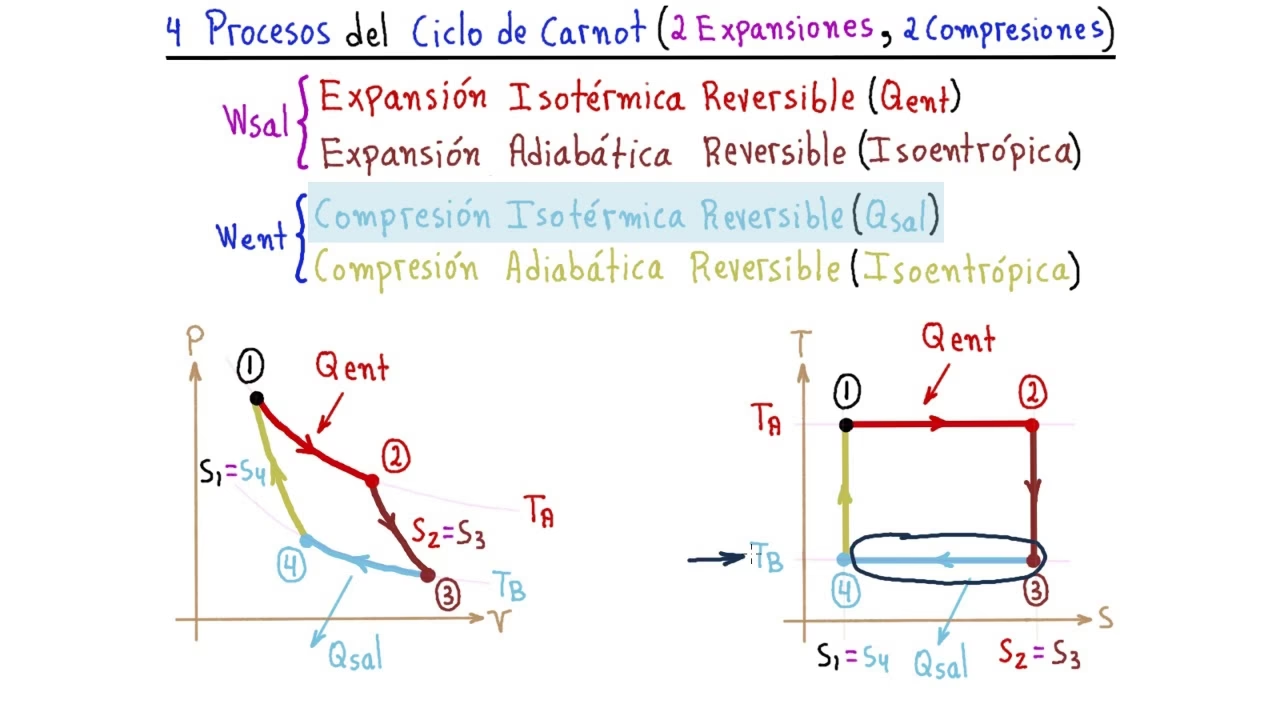
El ciclo de Carnot es un ciclo termodinámico ideal y reversible que describe el funcionamiento de una máquina térmica teórica. Se compone de cuatro procesos reversibles que una sustancia de trabajo (comúnmente un gas ideal) experimenta entre un reservorio caliente a una temperatura Th y un reservorio frío a una temperatura Tc. Estos procesos son los siguientes:
Expansión Isotérmica (M a N)
En esta primera etapa, el gas entra en contacto térmico con el reservorio caliente a una temperatura constante Th. El gas absorbe una cantidad de calor Qh del reservorio y se expande, realizando trabajo (W1) sobre el entorno. Dado que la temperatura es constante, la energía interna del gas ideal no cambia (ΔEint = 0). Según la primera ley de la termodinámica (ΔEint = Q - W), el calor absorbido es igual al trabajo realizado: Qh = W1.
Expansión Adiabática (N a O)
Una vez completada la expansión isotérmica, el gas se aísla térmicamente del entorno, lo que significa que no hay intercambio de calor (Q = 0). El gas continúa expandiéndose, realizando trabajo (W2), lo que provoca una disminución de su temperatura de Th a Tc. Este proceso es clave para la transición entre los reservorios de calor.
Compresión Isotérmica (O a P)
En esta fase, el gas se pone en contacto térmico con el reservorio frío a una temperatura constante Tc. El entorno realiza trabajo (W3) sobre el gas, comprimiéndolo. Durante esta compresión, el gas cede una cantidad de calor Qc al reservorio frío. Al igual que en la expansión isotérmica, la energía interna del gas ideal permanece constante, y el calor cedido es igual al trabajo realizado sobre el gas.
Compresión Adiabática (P a M)
Finalmente, el gas se aísla térmicamente de nuevo y se comprime adicionalmente, lo que eleva su temperatura de vuelta a Th. El trabajo (W4) se realiza sobre el gas, completando el ciclo y devolviendo la sustancia de trabajo a su estado inicial. Al ser adiabático, no hay intercambio de calor con el entorno.
El trabajo neto realizado por el gas en un ciclo completo de Carnot es la suma algebraica de los trabajos realizados en cada etapa (W = W1 + W2 - W3 - W4). Debido a que el estado inicial y final del sistema son idénticos, el cambio total en la energía interna del gas durante un ciclo completo es cero (ΔEint = 0). Por lo tanto, aplicando la primera ley de la termodinámica, el trabajo neto realizado es igual a la diferencia entre el calor absorbido del reservorio caliente y el calor cedido al reservorio frío: W = Qh - Qc.
Cálculo del Rendimiento de Carnot
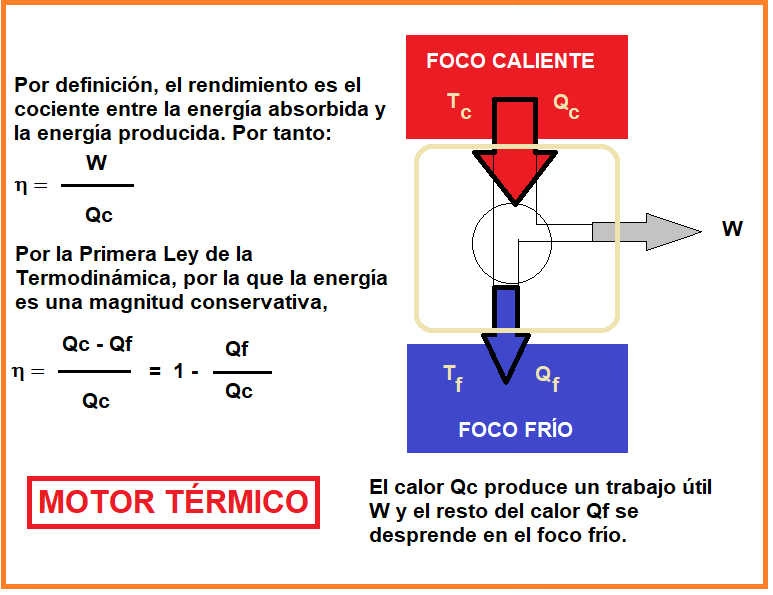
El rendimiento térmico (e o η) de una máquina térmica se define como la relación entre el trabajo neto realizado (W) y el calor absorbido del reservorio caliente (Qh). Para el ciclo de Carnot, esta relación adquiere una forma sorprendentemente simple y elegante, que depende únicamente de las temperaturas de los reservorios.
La eficiencia de una máquina de Carnot se expresa mediante la siguiente fórmula fundamental:
e = 1 - (Tc / Th)
Donde:
ees el rendimiento o eficiencia de Carnot.Tces la temperatura absoluta del reservorio frío (en Kelvin).Thes la temperatura absoluta del reservorio caliente (en Kelvin).
Es crucial que las temperaturas se expresen en una escala de temperatura absoluta, como la escala Kelvin, ya que un valor de cero en Kelvin representa el cero absoluto, donde no hay energía térmica. El uso de grados Celsius o Fahrenheit daría resultados incorrectos.
Derivación Simplificada de la Fórmula
Aunque la derivación completa implica consideraciones sobre las relaciones de volumen en los procesos adiabáticos e isotérmicos, el resultado clave es que la relación entre el calor cedido al reservorio frío (Qc) y el calor absorbido del reservorio caliente (Qh) es directamente proporcional a la relación de sus temperaturas absolutas:
Qc / Qh = Tc / Th
Sustituyendo esta relación en la definición general de rendimiento (e = W / Qh) y recordando que W = Qh - Qc, obtenemos:
e = (Qh - Qc) / Qh = 1 - (Qc / Qh)
Y finalmente, al sustituir la relación de temperaturas:
e = 1 - (Tc / Th)
Esta ecuación demuestra que la eficiencia de Carnot solo depende de las temperaturas de los reservorios, lo que la hace una medida universal del límite de eficiencia.
El Principio de Carnot y la Segunda Ley de la Termodinámica
El estudio de Carnot culminó en un principio fundamental, conocido como el Principio de Carnot: "Ninguna máquina que trabaje entre dos reservorios a temperatura constante puede tener un rendimiento mayor que una máquina reversible."
Este principio es, en esencia, otra formulación de la segunda ley de la termodinámica, y se ha demostrado que es equivalente a los enunciados de Kelvin-Planck y Clausius. Implica varias consecuencias importantes:
- Todas las máquinas térmicas reversibles que operan entre los mismos dos reservorios de temperatura tienen exactamente el mismo rendimiento.
- Ninguna máquina térmica real (irreversible) puede tener un rendimiento mayor que una máquina de Carnot que opere entre los mismos dos reservorios. De hecho, todas las máquinas reales son menos eficientes.
Esto subraya la importancia de la reversibilidad en los procesos termodinámicos para alcanzar la máxima eficiencia. Sin embargo, en la práctica, la reversibilidad perfecta es inalcanzable debido a factores como la fricción, la transferencia de calor a velocidad finita y otros efectos disipativos.
Aplicaciones del Ciclo de Carnot: Refrigeradores y Bombas de Calor
El ciclo de Carnot no solo describe el funcionamiento ideal de un motor térmico, sino que también puede operarse a la inversa, actuando como un refrigerador o una bomba de calor. En estos casos, en lugar de producir trabajo a partir de un flujo de calor, se utiliza trabajo para transferir calor de una región fría a una caliente.
Refrigerador de Carnot
Un refrigerador de Carnot extrae calor Qc de un reservorio frío a temperatura Tc y lo cede a un reservorio caliente a temperatura Th, requiriendo un aporte de trabajo W. El coeficiente de rendimiento (KR) de un refrigerador se define como la relación entre el calor extraído del reservorio frío y el trabajo realizado:
KR = Qc / W
Para un refrigerador de Carnot, esta relación se simplifica a:
KR = Tc / (Th - Tc)
Bomba de Calor de Carnot
Una bomba de calor de Carnot funciona de manera similar a un refrigerador, pero su objetivo es transferir calor Qh a un reservorio caliente (por ejemplo, el interior de una casa) desde un reservorio frío (el exterior). El coeficiente de rendimiento (KP) de una bomba de calor se define como la relación entre el calor entregado al reservorio caliente y el trabajo realizado:
KP = Qh / W
Para una bomba de calor de Carnot, la fórmula es:
KP = Th / (Th - Tc)
Estas ecuaciones para el coeficiente de rendimiento, al igual que la del rendimiento del motor, son válidas independientemente de la sustancia de trabajo, siempre y cuando el ciclo sea reversible.
Ejemplos Prácticos de Cálculo
Veamos cómo aplicar las fórmulas del rendimiento y los coeficientes de rendimiento en situaciones concretas.
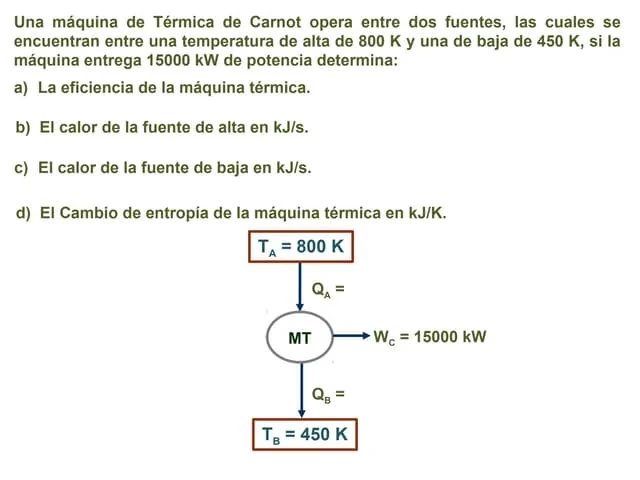
Ejemplo 1: Rendimiento de una Máquina de Carnot
Una máquina de Carnot tiene un rendimiento del 60% (0.60) y la temperatura de su reservorio frío es de 300 K.
(a) ¿Cuál es la temperatura del reservorio caliente?
Usamos la fórmula del rendimiento: e = 1 - (Tc / Th)
0.60 = 1 - (300 K / Th)
300 K / Th = 1 - 0.60
300 K / Th = 0.40
Th = 300 K / 0.40 = 750 K
La temperatura del reservorio caliente es de 750 K.
(b) Si la máquina realiza 300 J de trabajo por ciclo, ¿cuánto calor se extrae del reservorio de alta temperatura por ciclo?
El rendimiento también se define como e = W / Qh
0.60 = 300 J / Qh
Qh = 300 J / 0.60 = 500 J
Se extraen 500 J de calor del reservorio caliente por ciclo.
(c) ¿Cuánto calor se cede al reservorio de baja temperatura por ciclo?
Por la primera ley de la termodinámica, W = Qh - Qc, entonces Qc = Qh - W
Qc = 500 J - 300 J = 200 J
Se ceden 200 J de calor al reservorio frío por ciclo.
Ejemplo 2: Coeficiente de Rendimiento de una Bomba de Calor de Carnot
Imaginemos que una bomba de calor de Carnot funciona entre una temperatura exterior de 0 °C y una temperatura interior de 20.0 °C. ¿Cuál es el trabajo necesario si el calor suministrado al interior de la casa es de 30.0 kJ?
Primero, convertimos las temperaturas a Kelvin:
- Tc = 0 °C + 273.15 = 273.15 K
- Th = 20.0 °C + 273.15 = 293.15 K
Calculamos el coeficiente de rendimiento de la bomba de calor:
KP = Th / (Th - Tc)
KP = 293.15 K / (293.15 K - 273.15 K)
KP = 293.15 K / 20 K ≈ 14.66
Ahora, usamos la definición de KP: KP = Qh / W
Necesitamos encontrar el trabajo (W): W = Qh / KP
W = 30.0 kJ / 14.66 ≈ 2.046 kJ
El trabajo necesario para suministrar 30.0 kJ de calor al interior es de aproximadamente 2.046 kJ.
Estos ejemplos ilustran cómo el rendimiento de Carnot y los coeficientes de rendimiento están intrínsecamente ligados a las temperaturas de los reservorios, destacando que una mayor diferencia de temperatura entre el reservorio caliente y el frío generalmente conduce a una mayor eficiencia para los motores y un menor coeficiente de rendimiento para refrigeradores/bombas de calor.
Limitaciones y Realidad Práctica
Aunque el ciclo de Carnot es un ideal fundamental, es importante reconocer sus limitaciones en el mundo real. Una máquina de Carnot es teóricamente perfecta y opera con procesos "reversibles", lo que implica que no hay pérdidas de energía por fricción, turbulencia o transferencia de calor a través de diferencias de temperatura finitas. En la práctica, esto es imposible de lograr.
Las condiciones para un motor de Carnot incluyen:
- Interacciones mecánicas sin fricción: No se pierde energía en forma de calor debido al rozamiento. Esto implica procesos adiabáticos perfectos.
- Interacciones térmicas infinitamente lentas (cuasiestáticas): La transferencia de calor ocurre de manera tan lenta que la diferencia de temperatura entre el sistema y el reservorio es casi nula. Esto asegura procesos isotérmicos perfectos.
Debido a estas idealizaciones, una máquina de Carnot real sería terriblemente impráctica. Si bien maximizaría la eficiencia, su velocidad de operación sería extremadamente lenta, lo que resultaría en una producción de trabajo insignificante por unidad de tiempo. Como se ha dicho, "no te molestes en instalar un motor de Carnot en tu coche; si bien aumentaría tu consumo de gasolina, los peatones te adelantarían".
A pesar de su impracticabilidad, el rendimiento de Carnot es una referencia invaluable. Permite a los ingenieros y diseñadores entender el máximo potencial de sus sistemas y sirve como un objetivo al que aspirar. Las máquinas reales siempre tendrán un rendimiento menor que el de Carnot, pero la comprensión de este límite ayuda a identificar áreas de mejora y a evaluar cuán cerca están los diseños actuales del ideal termodinámico.
En el caso de las bombas de calor, aunque son muy eficientes energéticamente en climas templados (como se vio en el ejemplo, con un bajo consumo de trabajo para una gran cantidad de calor transferido), su eficiencia disminuye drásticamente a medida que la temperatura exterior baja. Por debajo de ciertos umbrales (aproximadamente -10 °C), el calor que proporcionan puede ser menor que la energía eléctrica utilizada para su funcionamiento, volviéndolas menos prácticas en climas muy fríos.
Tabla Comparativa: Máquina de Carnot vs. Máquina Real
| Característica | Máquina de Carnot (Ideal) | Máquina Térmica Real |
|---|---|---|
| Eficiencia | Máxima posible (e = 1 - Tc/Th) | Siempre menor que la de Carnot |
| Procesos | Reversibles (isotérmicos, adiabáticos) | Irreversibles (fricción, transferencia de calor finita) |
| Pérdidas de Energía | Nulas (sin fricción, sin disipación) | Siempre presentes (fricción, calor disipado) |
| Velocidad de Operación | Infinitamente lenta (cuasiestática) | Finita y práctica |
| Objetivo | Límite teórico de eficiencia | Conversión práctica de calor en trabajo |
| Existencia | Hipotética | Real y funcional |
Preguntas Frecuentes (FAQ)
¿Por qué el rendimiento de Carnot es el máximo posible?
El rendimiento de Carnot es el máximo posible porque se basa en un ciclo reversible. La reversibilidad implica que no hay pérdidas de energía por irreversibilidades como la fricción o la transferencia de calor a través de diferencias de temperatura finitas. La segunda ley de la termodinámica establece que ninguna máquina real puede ser más eficiente que una máquina reversible que opere entre las mismas temperaturas.
¿Las temperaturas deben estar en Kelvin para el cálculo del rendimiento de Carnot?
Sí, es absolutamente esencial que las temperaturas (Tc y Th) se expresen en una escala de temperatura absoluta, como la escala Kelvin. Esto se debe a que la fórmula se deriva de principios termodinámicos que dependen de la relación de temperaturas absolutas, donde cero Kelvin representa la ausencia total de energía térmica. Usar grados Celsius o Fahrenheit daría resultados incorrectos.
¿Puede una máquina real alcanzar el rendimiento de Carnot?
No, una máquina real nunca puede alcanzar el rendimiento de Carnot. Las máquinas reales siempre experimentan irreversibilidades (como fricción, turbulencia, transferencia de calor irreversible) que disipan energía y reducen su eficiencia por debajo del límite teórico de Carnot. Sin embargo, el rendimiento de Carnot sirve como un objetivo ideal y una referencia para evaluar cuán eficientes son los motores reales.
¿Cómo se puede aumentar la eficiencia de una máquina térmica real?
Para aumentar la eficiencia de una máquina térmica real, se pueden buscar dos caminos principales, inspirados en la fórmula de Carnot: aumentar la temperatura del reservorio caliente (Th) o disminuir la temperatura del reservorio frío (Tc). Además, es fundamental reducir las irreversibilidades del sistema, minimizando la fricción, optimizando la transferencia de calor y mejorando el diseño de los componentes para acercarse lo más posible a un comportamiento reversible.
¿Es el ciclo de Carnot útil si no se puede construir en la práctica?
Aunque una máquina de Carnot perfecta no puede construirse, su ciclo es extremadamente útil. Sirve como un estándar de comparación para todas las máquinas térmicas reales, permitiendo a los ingenieros evaluar su eficiencia y buscar mejoras. Además, el ciclo de Carnot es fundamental para el desarrollo de la termodinámica, la comprensión de la segunda ley y la definición de la escala de temperatura absoluta. Es una herramienta conceptual indispensable en la física y la ingeniería.
Si quieres conocer otros artículos parecidos a ¿Cómo Calcular el Rendimiento de Carnot? puedes visitar la categoría Cálculos.