16/07/2025
La interacción de la luz con la materia es un fenómeno fundamental en la ciencia, con aplicaciones que van desde el análisis químico en laboratorios hasta la comprensión de cómo la radiación solar afecta nuestra atmósfera. Dos conceptos clave que nos permiten cuantificar esta interacción son la absortividad molar y la absortividad de radiación. Aunque ambos describen la capacidad de una sustancia para absorber luz, se aplican en contextos ligeramente diferentes y se calculan con consideraciones específicas. Este artículo explorará en detalle cómo determinar y calcular estas magnitudes, proporcionando una guía completa sobre sus fundamentos, fórmulas, factores que las afectan y las fuentes de error que pueden influir en su precisión.
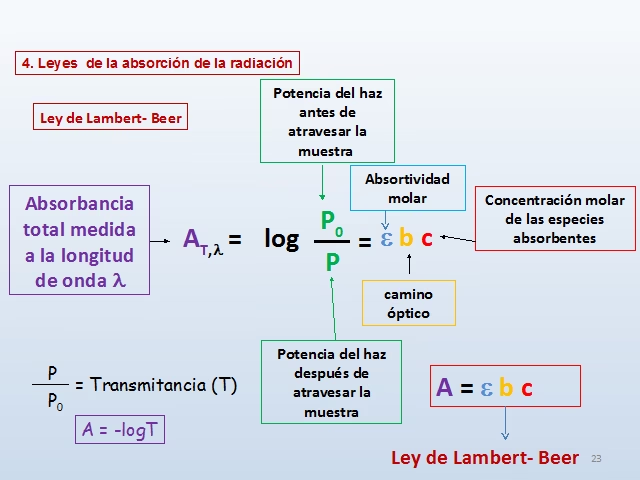
La Ley de Beer-Lambert: El Fundamento Común
En el corazón de la comprensión de la absorción de luz se encuentra la Ley de Beer-Lambert, una relación empírica que describe cómo la luz es atenuada al pasar a través de un medio absorbente. Esta ley establece que la absorbancia de una solución es directamente proporcional a la concentración de la especie absorbente y a la longitud del camino que la luz recorre a través de la solución.
En su forma más general, la Ley de Beer-Lambert se expresa como:
A = εbc
Donde:
Aes la absorbancia (adimensional).ε(épsilon) es el coeficiente de absortividad molar (o absortividad molar).bes la longitud del camino óptico (generalmente en centímetros).ces la concentración de la sustancia absorbente.
Si bien esta es la forma más conocida en química, la ley tiene equivalentes y aplicaciones en otros campos, como la física atmosférica, donde la absorción de radiación es crucial.
Absortividad Molar: Explorando la Eficiencia en Soluciones
La absortividad molar (ε), también conocida como coeficiente de extinción molar, es una medida de cuán fuertemente una sustancia química absorbe la luz a una longitud de onda particular. Es una propiedad intrínseca de la sustancia en un disolvente y condiciones específicas (como pH y temperatura). Cuanto mayor sea la absortividad molar, más eficientemente absorberá la luz una sustancia.
Cálculo de la Absortividad Molar
Para determinar la absortividad molar, se utiliza una forma reorganizada de la Ley de Beer-Lambert. La información proporcionada sugiere una definición específica para la concentración en gramos por litro:
ε = (A * M) / (b * c)
Donde:
Aes la absorbancia medida experimentalmente.Mes el peso molecular del soluto (en g/mol).bes la longitud del camino óptico de la celda (en cm).ces la concentración de la solución (en gramos por litro, g/L).
Las unidades de ε, bajo esta definición, son L · mol⁻¹ · cm⁻¹. Es importante destacar que, más comúnmente, la concentración c en la Ley de Beer-Lambert se expresa directamente en moles por litro (molaridad, M), en cuyo caso la fórmula se simplifica a ε = A / (b * c), donde c ya está en mol/L.
Factores que Influyen en la Absortividad Molar
La absortividad molar no es una constante universal para una molécula, sino que puede variar significativamente debido a varios factores:
- Longitud de Onda: La absortividad molar es altamente dependiente de la longitud de onda de la luz. Cada sustancia tiene un espectro de absorción único con picos de máxima absorción en longitudes de onda específicas.
- pH del Disolvente: Cambios en el pH pueden alterar la forma ionizada de una molécula, lo que a su vez afecta su capacidad para absorber luz.
- Naturaleza del Disolvente: El disolvente puede influir en el entorno electrónico de la molécula, lo que modifica sus niveles de energía y, por lo tanto, su espectro de absorción.
- Temperatura: Aunque menos pronunciado que el pH o el disolvente, la temperatura puede afectar el equilibrio químico y las propiedades físicas de la solución, alterando ligeramente la absorción.
- Interacciones Moleculares: La presencia de otras moléculas en la solución puede formar complejos o causar agregación, lo que también afecta la absortividad.
Fuentes de Error en la Medición de la Absortividad Molar
La determinación precisa de la absortividad molar es crucial, especialmente en campos como la química clínica. Sin embargo, diversas fuentes de error, tanto sistemáticas como aleatorias, pueden afectar la exactitud de las mediciones.
Errores Sistemáticos
Los errores sistemáticos son aquellos que son predecibles y consistentes, afectando las mediciones de una manera particular. Pueden ser corregidos si se conocen su magnitud y dirección.
Errores Gravimétricos y Volumétricos: La preparación de soluciones con concentraciones exactas es fundamental. Esto incluye la calibración de balanzas analíticas con pesas certificadas, el conocimiento preciso de la temperatura de la solución (que afecta la densidad del disolvente y el volumen) y la aplicación de correcciones por flotabilidad del aire en las pesadas, especialmente para sustancias de alta masa molecular o baja absortividad molar.

Para la materia que absorbe y no dispersa, la absortividad es a = 1 \u2013 t . Nótese que, en este caso, la emisividad es \u03b5 = a = 1 \u2013 t. Generalmente, aunque no siempre, \u03c3 es función de la altitud, ya que a menudo es función de la presión y la temperatura, que varían a diferentes altitudes. Errores en la Longitud del Camino Óptico (Celda): Asumir el valor nominal de la longitud de la celda (por ejemplo, 1 cm) puede introducir errores significativos. Celdas de alta precisión deben ser medidas con dispositivos especializados (como calibres electrónicos) para determinar su longitud exacta, idealmente con una precisión de ±0.0001 cm. La falta de paralelismo en las ventanas de la celda también puede ser una fuente de error.
Errores de Alineación del Haz: Si la radiación incidente no es perfectamente paralela a la normal de las ventanas de la celda, o si la celda no está correctamente orientada, la longitud efectiva del camino óptico se incrementa, lo que lleva a una absorbancia observada mayor que la real. Desviaciones de más de 1° pueden ser significativas.
Errores por Reflexión: Cuando la luz pasa de un medio a otro (por ejemplo, aire a vidrio), una fracción se refleja. Aunque se puede compensar parcialmente restando la absorbancia del disolvente puro, las reflexiones múltiples dentro de la celda (donde la luz rebota varias veces antes de llegar al detector) pueden inflar la absorbancia aparente, especialmente a altas transmitancias.
Efecto del Ancho de Hendidura Finito: La Ley de Beer-Lambert es estrictamente válida solo para luz monocromática. Los espectrofotómetros utilizan un haz de luz con un ancho de banda finito (rango de longitudes de onda), lo que puede causar que la absorbancia observada sea menor que la verdadera, a menos que el espectro de absorción sea muy plano en la región de interés. El error es una función de la relación entre el ancho de banda espectral y el ancho de banda natural de la banda de absorción.
Radiación Dispersa (Stray Radiation): Se refiere a la luz que llega al detector con longitudes de onda fuera del rango deseado. Esta radiación puede o no ser absorbida por la muestra. Si no es absorbida, la absorbancia observada será menor que la verdadera. La cantidad de radiación dispersa es mayor en regiones donde la intensidad de la fuente o la sensibilidad del detector son bajas, o cuando se trabaja con absorbancias muy altas.
Precisión de la Longitud de Onda y la Absorbancia: Los espectrofotómetros deben ser calibrados regularmente para asegurar la exactitud de la longitud de onda y las lecturas de absorbancia. Un sesgo sistemático en la configuración de la longitud de onda puede llevar a errores en la absorbancia medida, especialmente si se está en una parte empinada de la curva de absorción.
A continuación, se resume el rango típico de error que pueden introducir estas fuentes sistemáticas:
| Fuente de Error Sistemático | Rango de Error (partes por mil) |
|---|---|
| Temperatura de la solución | -2 a +2 |
| Volumen específico aparente del soluto | 0 a -1 |
| Corrección por flotabilidad | +0.2 a +1 |
| Longitud del camino de la celda | -10 a +10 |
| Orientación de la celda | 0 a +1 |
| Reflexiones múltiples | +0.5 a +3 |
| Ancho de hendidura finito | 0 a -1 |
| Radiación dispersa | 0 a -1 |
| Desplazamiento de longitud de onda | 0 a -1 |
Errores Aleatorios
Los errores aleatorios son impredecibles y varían de una medición a otra. Se asocian con la incertidumbre inherente en cualquier proceso de medición. En la determinación de la absortividad molar, los errores aleatorios significativos pueden surgir del pesado del soluto y del disolvente, y de la lectura de la absorbancia de la solución. Se minimizan utilizando equipos de alta sensibilidad y realizando múltiples mediciones para promediar los resultados.

Propagación de Errores
Cuando se combinan las mediciones (absorbancia, longitud del camino, concentración) para calcular la absortividad molar, los errores individuales se propagan. La incertidumbre relativa total en la absortividad molar es aproximadamente la suma de las incertidumbres relativas de la absorbancia, la longitud del camino y la concentración:
Δε/ε ≈ ΔA/A + Δb/b + Δc/c
Donde Δ representa la incertidumbre absoluta de cada variable. Es importante recordar que las mediciones repetitivas pueden reducir el componente de error aleatorio, pero los errores sistemáticos no se ven afectados y siempre contribuirán con una cantidad constante a la incertidumbre final.
Importancia en la Química Clínica
En la química clínica, la absortividad molar precisa es un requisito previo para la exactitud de muchos análisis. Por ejemplo, en la enzimología clínica, las actividades enzimáticas en el suero sanguíneo se miden espectrofotométricamente, y la exactitud de los resultados depende directamente de la exactitud de las mediciones de absorbancia y del valor asumido para la absortividad molar del sustrato o producto. Un ejemplo destacado es el NADH, un coenzima clave en muchas reacciones; un valor exacto de su absortividad molar a 340 nm es crítico para la cuantificación precisa de la actividad enzimática.
Absortividad de Radiación: Un Viaje a Través de la Atmósfera
En el contexto de la radiación atmosférica, la absortividad se refiere a la fracción de radiación que es absorbida a medida que pasa a través de un medio, como una capa de gas. Aquí, la Ley de Beer-Lambert se adapta para describir la atenuación de la irradiancia (intensidad de la luz) a través de una trayectoria.
Cálculo de la Absorción de Radiación
Supongamos que un haz de radiación con una radiancia I(λ) (W m⁻² esterad⁻¹ nm⁻¹) pasa a través de una capa infinitesimal de un medio absorbente. La disminución de la radiancia (dI) debido a la absorción se describe por:
dI(λ) = -I(λ) σ(λ) n ds
Donde:
I(λ)es la radiancia a una longitud de ondaλ.σ(λ)es la sección transversal de absorción de una sola molécula o partícula (en m²), que cuantifica la eficiencia de absorción a esa longitud de onda.nes la densidad numérica de los absorbedores (número de moléculas por m³).dses la longitud del camino de la luz a través de la capa infinitesimal (en m).
Integrando esta expresión sobre el espesor total del volumen (s), obtenemos la forma de la Ley de Beer-Lambert aplicable a la radiación:
I(λ) = Io(λ) exp[-σ(λ)ns]
Donde Io(λ) es la radiancia en el borde frontal del camino y I(λ) es la radiancia a una distancia s a lo largo del camino.
Términos Clave en la Absorción de Radiación
Coeficiente de Absorción (κa): A menudo, el producto
σnse sustituye por un único términoκa, el coeficiente de absorción (en m⁻¹). Así, la ecuación se convierte enI(λ) = Io(λ) exp[-κa s].Profundidad Óptica (τ): Para un gas uniforme, el producto
σnsse conoce como profundidad óptica y se denota con el símboloτ(tau). Si la profundidad óptica es grande, muy poca radiación logra atravesar el medio. Así,I(λ) = Io(λ) exp[-τ].Transmitancia (t): La fracción de radiación que atraviesa el medio se llama transmitancia (
t), y es igual aexp[-τ]. Es decir,t = I(λ) / Io(λ).
La espectrofotometría es el método más común y sencillo para determinar el coeficiente de extinción . Mediante un espectrofotómetro, los investigadores pueden medir la absorbancia de una solución a diferentes longitudes de onda y, posteriormente, calcular el coeficiente de extinción. Absortividad (a): Para la materia que absorbe pero no dispersa la radiación, la absortividad (
a) se define comoa = 1 - t. En este caso ideal, la emisividad (ε) es igual a la absortividad (ε = a).
Influencia del Ángulo Cenital Solar (SZA)
El ángulo cenital solar (SZA) es el ángulo entre el cenit (directamente sobre la cabeza) y la posición del Sol. Afecta la longitud total del camino que la radiación solar debe atravesar a través de los absorbedores en la atmósfera. Si la atmósfera se considera una capa paralela, la longitud diferencial del camino (ds) se relaciona con la altura diferencial (dz) por:
ds = sec(SZA) dz
Incorporando esto en la forma diferencial de la Ley de Beer:
dI(λ) / I(λ) = -σ(λ) n sec(SZA) dz
Integrando esta expresión a lo largo de la altura z, obtenemos:
I(λ, z) = Io(λ) exp[-sec(SZA) ∫ σ(λ)n(z) dz]
El integral ∫ σ(λ)n(z) dz se conoce como el espesor óptico o camino óptico. La transmitancia, en este caso, es exp[-sec(SZA) τ], donde τ es la profundidad óptica.
Ejemplo Práctico: Capa de Ozono
Un ejemplo clásico de la aplicación de la absortividad de radiación es la absorción de la radiación ultravioleta (UV) por la capa de ozono. La sección transversal de absorción del ozono varía drásticamente con la longitud de onda. A 310 nm, el ozono absorbe menos, permitiendo que una fracción significativa de UV solar llegue a la superficie terrestre. Sin embargo, a longitudes de onda más cortas, como 290 nm, la sección transversal de absorción del ozono es mucho mayor, lo que resulta en una absorción casi completa de la radiación UV, protegiendo así la vida en la Tierra. Este es un testimonio de la importancia de la absortividad en la protección de nuestro planeta.
Diferencias Clave y Aplicaciones Prácticas
Aunque ambos conceptos se basan en el principio de la Ley de Beer-Lambert, sus aplicaciones y la forma en que se manejan los parámetros difieren:
Absortividad Molar (ε): Se usa principalmente en química analítica y bioquímica para caracterizar sustancias en solución. Es una propiedad de la molécula que depende de las condiciones del disolvente y la longitud de onda. Su cálculo se centra en la concentración de una especie específica en una solución.
Absortividad de Radiación (a, o a través de σ y n): Se aplica en física atmosférica, teledetección y ciencia de materiales para describir la atenuación de la radiación a través de medios gaseosos, líquidos o sólidos. Aquí, el enfoque está en cómo la radiación se atenúa a lo largo de una trayectoria, considerando la densidad de los absorbedores y su sección transversal de absorción. El ángulo de incidencia de la radiación (como el SZA) es una consideración importante.
Preguntas Frecuentes
- ¿Cuál es la diferencia entre absortividad molar y coeficiente de absorción?
- El término "coeficiente de absorción" puede ser genérico y referirse a diferentes magnitudes. En el contexto de la absortividad molar (ε), se refiere específicamente a la eficiencia de absorción de una sustancia a una concentración molar dada. En la física de la radiación, el "coeficiente de absorción" (κa = σn) es el producto de la sección transversal de absorción de una molécula y la densidad numérica de esas moléculas, y tiene unidades de longitud inversa (por ejemplo, m⁻¹).
- ¿Por qué es importante la precisión en la absortividad molar?
- La precisión es fundamental para obtener resultados analíticos confiables. En química clínica, por ejemplo, los valores exactos de absortividad molar son esenciales para determinar con precisión la concentración de analitos o la actividad de enzimas, lo que impacta directamente en diagnósticos y tratamientos.
- ¿Cómo afecta la longitud de onda a la absorción?
- La absorción es altamente dependiente de la longitud de onda. Las moléculas solo absorben fotones cuya energía coincide con las transiciones de energía dentro de la molécula (electrónica, vibracional, rotacional). Por lo tanto, cada sustancia tiene un espectro de absorción único, con picos de máxima absorción en longitudes de onda específicas.
- ¿Qué es la profundidad óptica?
- La profundidad óptica (τ) es una medida adimensional de la opacidad de un medio a la radiación. Representa cuántas "longitudes de absorción" tiene el medio. Una profundidad óptica grande significa que muy poca radiación puede pasar a través del medio, indicando una fuerte absorción.
- ¿Cómo influye el ángulo cenital solar en la absorción de radiación atmosférica?
- El ángulo cenital solar (SZA) afecta la longitud efectiva del camino que la luz solar debe recorrer a través de la atmósfera. Cuando el sol está directamente sobre la cabeza (SZA=0°), el camino es el más corto. A medida que el sol se acerca al horizonte (SZA cercano a 90°), el camino se alarga significativamente, lo que resulta en una mayor absorción de radiación y, por lo tanto, en una menor cantidad de luz que llega a la superficie.
En resumen, la determinación y comprensión de la absortividad molar y la absortividad de radiación son pilares para cuantificar cómo la luz interactúa con la materia. Ya sea en un laboratorio químico midiendo la concentración de un analito o modelando la penetración de la radiación solar en la atmósfera, la aplicación rigurosa de los principios de la Ley de Beer-Lambert y la consideración cuidadosa de las fuentes de error son esenciales para obtener resultados precisos y significativos.
Si quieres conocer otros artículos parecidos a Calculando la Absorción: Absortividad Molar y de Radiación puedes visitar la categoría Física.

