08/06/2025
En el vasto universo de la electroquímica y la fisiología, pocas herramientas son tan fundamentales y reveladoras como la Ecuación de Nernst. Esta fórmula matemática, aparentemente simple, desentraña la compleja relación entre la concentración de especies químicas y el potencial eléctrico que pueden generar. Desde el funcionamiento intrincado de nuestras células nerviosas hasta la predicción del voltaje en una batería, la Ecuación de Nernst es un pilar que nos permite comprender y cuantificar fenómenos eléctricos impulsados por gradientes de concentración. Prepárese para sumergirse en los principios que rigen la electricidad en la materia viva y en los sistemas electroquímicos.

La ecuación de Nernst es una de las dos ecuaciones centrales en electroquímica, diseñada para describir la dependencia del potencial de un electrodo de su entorno químico. En términos más precisos, nos indica cuál es el potencial de un electrodo cuando está rodeado por una solución que contiene una especie redox-activa con una actividad de sus especies oxidadas y reducidas. Es una herramienta poderosa que conecta la termodinámica con la electroquímica, permitiendo predecir y entender los voltajes generados por reacciones químicas.
- ¿Qué Calcula la Ecuación de Nernst?
- Aplicaciones Típicas de la Ecuación de Nernst
- El Potencial de Nernst en Sistemas Biológicos: Un Vistazo Celular
- El Potencial de Nernst del Potasio
- Derivación de la Ecuación de Nernst para Iones Biológicos
- Validación Experimental y Desviaciones del Potencial de Reposo
- Concentraciones Iónicas Típicas en Células de Mamíferos y Potenciales de Equilibrio
- Preguntas Frecuentes sobre la Ecuación y el Potencial de Nernst
- ¿Qué es el potencial de Nernst o potencial de equilibrio?
- ¿Por qué es tan importante la ecuación de Nernst en biología?
- ¿Cuáles son las limitaciones de la ecuación de Nernst?
- ¿Cómo influye la temperatura en el potencial de Nernst?
- ¿Es el potencial de Nernst lo mismo que el potencial de reposo de una célula?
¿Qué Calcula la Ecuación de Nernst?
La Ecuación de Nernst es crucial para determinar el potencial de un electrodo bajo condiciones no estándar. La forma completa de la ecuación es la siguiente:
E = E° - (RT/zF)lnQ
Donde cada parámetro tiene un significado específico:
E: Es el potencial actual del electrodo en voltios (V).E°: Es el potencial estándar del electrodo en voltios (V), medido bajo condiciones estándar (1 M de concentración para soluciones, 1 atm de presión para gases, 298 K o 25 °C).R: Es la constante universal de los gases, con un valor de 8.314 J/(mol·K).T: Es la temperatura absoluta en Kelvin (K).z: Es el número de electrones transferidos por molécula en la reacción redox.F: Es la constante de Faraday, que representa la carga de un mol de electrones, aproximadamente 96,487 culombios/mol.Q: Es el cociente de reacción, que expresa la relación de las actividades (o concentraciones, en soluciones diluidas) de los productos y los reactivos en equilibrio. Específicamente,Q = [aOx] / [aRed], dondeaOxes la actividad de la especie oxidada yaRedes la actividad de la especie reducida.
Es más común utilizar una versión simplificada de la ecuación de Nernst para cálculos rápidos a una temperatura específica, comúnmente 298 K (25 °C):
E = E° - (0.0592 V/z)logQ
En esta versión simplificada, se introduce un nuevo parámetro, el potencial formal E°', que incluye la influencia de los coeficientes de actividad, facilitando los cálculos en condiciones experimentales específicas.
Es esencial para cualquier electroquímico comprender que esta ecuación funciona en dos direcciones. Si se cambia el potencial del electrodo, la solución en contacto con él debe alcanzar la relación de concentración de especies activas indicada por la ecuación de Nernst. Para lograr esto, una reacción electroquímica debe tener lugar en el electrodo. Inversamente, si las concentraciones de las especies cambian, el potencial del electrodo se ajustará según lo dictado por la ecuación.
Aplicaciones Típicas de la Ecuación de Nernst
Una aplicación común de la ecuación de Nernst es calcular los potenciales de dos elementos diferentes y luego determinar la diferencia entre estos potenciales para predecir el potencial a través de una celda electroquímica. Por ejemplo, si se va a construir una batería, la ecuación de Nernst puede utilizarse para predecir el voltaje entre sus dos semiceldas.
Consideremos un ejemplo práctico. Si deseamos predecir el voltaje de una batería improvisada, podemos utilizar la ecuación de Nernst. Supongamos que tenemos una solución de 1 M de CuSO₄ y un alambre de cobre. Además, en un armario, encontramos una solución con 0.5 M de FeCl₃ y 0.5 M de FeCl₂. Para calcular el voltaje de esta celda, necesitaríamos los potenciales estándar (E°) de las reacciones de reducción del cobre y del hierro. Con estos valores y las concentraciones dadas, la ecuación de Nernst nos permitiría determinar el potencial de cada semicelda y, por ende, el voltaje total de la batería.
Además de las baterías, la ecuación de Nernst es fundamental en:
- Sensores electroquímicos: Para diseñar y calibrar sensores que miden la concentración de iones específicos en una solución, como los medidores de pH.
- Corrosión: Para entender y predecir la tendencia de los metales a corroerse en diferentes entornos.
- Biología: Como veremos a continuación, para comprender los potenciales de membrana en células vivas.
El Potencial de Nernst en Sistemas Biológicos: Un Vistazo Celular
El soma de una célula nerviosa típica tiene dimensiones microscópicas, generalmente entre 10 y 30 µm de diámetro. Sin embargo, el poder de la "batería" generada a través de su membrana externa es sorprendentemente grande, alcanzando unos 100 mV, lo cual es casi una décima parte del voltaje de una pila AA ordinaria. Esta capacidad en un elemento tan diminuto genera la pregunta crucial: ¿de dónde proviene la energía para generar tal potencial?
Para responder a esta pregunta, debemos buscar dentro y fuera de la célula elementos relacionados con cargas eléctricas, ya que para producir una señal eléctrica debe haber un flujo de partículas cargadas, como los iones. Dado que los electrones no se encuentran libres en las células biológicas, debemos analizar la distribución de iones dentro y fuera. Varios de ellos, como los iones de potasio (K+), sodio (Na+), calcio (Ca2+) y cloro (Cl-), contribuyen al establecimiento de esta batería eléctrica.
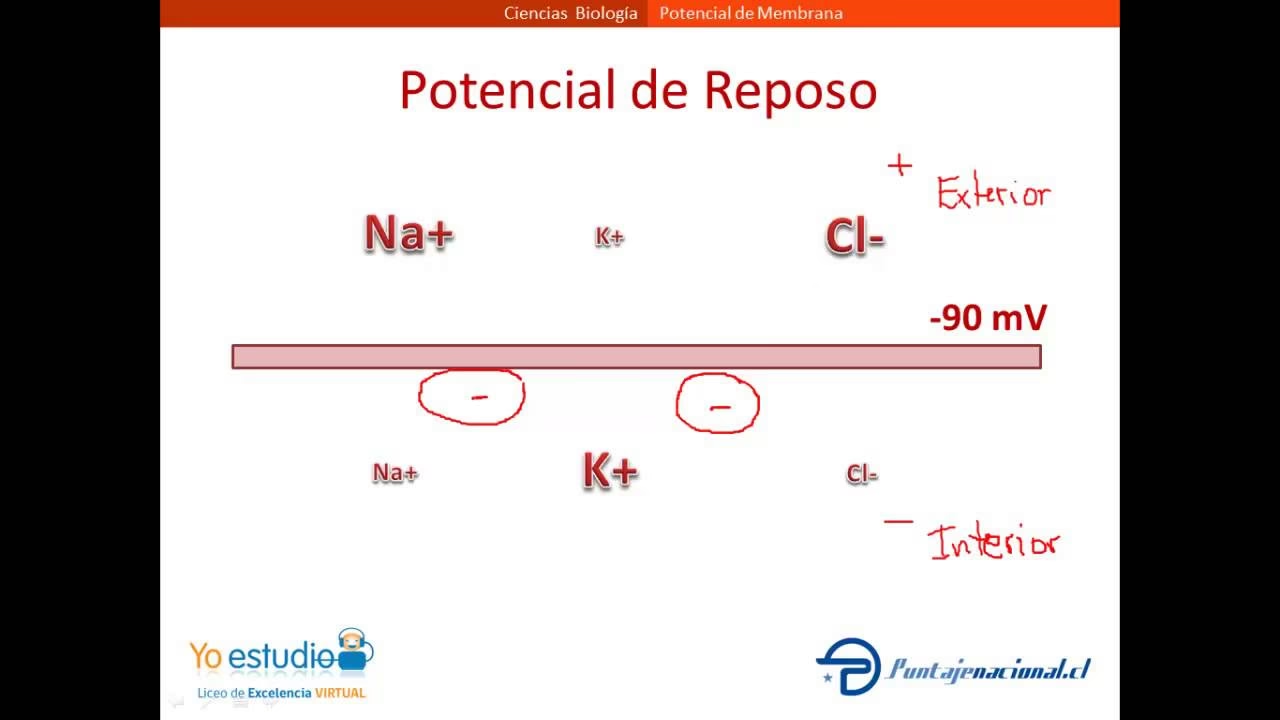
Al medir las concentraciones de estos iones en el interior y el exterior de una célula, se observan patrones interesantes:
- En el exterior de la célula, la concentración de iones positivos (cationes) es igual a la de iones negativos (aniones), manteniendo la electroneutralidad en el líquido extracelular.
- Dentro de la célula, el número de cationes y aniones es también igual, lo que significa que hay electroneutralidad intracelular.
- La concentración de iones Na+ en el exterior de la célula es considerablemente mayor que en el interior.
- La concentración de iones K+ dentro de la célula es mucho mayor que en el exterior.
- La concentración de iones Cl- fuera de la célula es mayor que en el interior.
Estas diferencias en la concentración iónica a través de la membrana celular son fundamentales y se deben a la presencia de la membrana, que actúa como una barrera semipermeable. Si la membrana no existiera, los iones se moverían libremente para igualar sus concentraciones a ambos lados. Este gradiente iónico a través de la membrana es una forma de energía, comparable a tener un tanque de agua a cierta altura: al abrir una válvula, el agua fluye con una fuerza proporcional a la altura. Sin embargo, a diferencia de las moléculas de agua, los iones son partículas cargadas, lo que introduce dos fuerzas concurrentes: una fuerza química (debida al gradiente de concentración) y una fuerza eléctrica (debida a la carga de los iones).

El Experimento del Huevo: Una Analogía Simple
Para comprender mejor el comportamiento de los iones, podemos imaginar un experimento con un huevo de gallina. Hacemos pequeños orificios en los extremos del cascarón, dejando intacta la membrana en el compartimento de aire y abriéndola en el otro. Después de vaciar y lavar el huevo, lo colocamos en un soporte dentro de un vaso. En el compartimento exterior (e) añadimos una sal simple (KCl) a 100 mM, y en el interior (i) una sal diferente con proteína (P-) y Na+ también a 100 mM. Suponemos que la membrana es semipermeable, permitiendo el paso de iones K+ y Cl-, pero no de las grandes moléculas de P-.
Inicialmente, hay electroneutralidad a ambos lados y no hay diferencia en las concentraciones de iones positivos. Pero al permitir el paso a través de la membrana:
- Los iones Cl- (más concentrados fuera) entrarán al huevo, llevando consigo su carga negativa. Esto hará que el interior se vuelva negativo con respecto al exterior.
- Esta negatividad interior atraerá a los iones K+ del exterior, que comenzarán a moverse hacia el interior.
- A medida que los K+ entran, neutralizan parte de la negatividad del Cl-, lo que a su vez permite que más Cl- entren. Este proceso continúa hasta que se establece un estado de equilibrio, donde no hay movimiento neto de iones K+ ni Cl-.
En este estado de equilibrio, se observará que hay más iones K+ en el interior del huevo que en el exterior, el interior del huevo será ligeramente más negativo que el exterior, y la mayoría de los iones Cl- permanecerán en el exterior, con una concentración ligeramente menor en el interior. Las P- permanecerán confinadas en el interior.
Este modelo del huevo es notablemente similar a las condiciones en las células biológicas, donde la concentración de K+ es mayor intracelularmente y la de Cl- es mayor extracelularmente, y el interior celular es más negativo que el exterior. Las diferencias cuantitativas son mínimas y se deben principalmente a las concentraciones iónicas específicas y los valores de potencial, pero el principio subyacente es el mismo.
Para mantener este estado estacionario de forma continua en las células vivas, existe un mecanismo adicional: la bomba Na+/K+. Esta bomba, que consume energía (ATP), expulsa iones sodio que entran continuamente a la célula y simultáneamente introduce iones potasio que hayan salido. Esta acción de bombeo asegura que los gradientes iónicos se mantengan estables mientras la célula esté viva.
Así, el potencial eléctrico a través de la membrana de las células vivas tiene las siguientes características clave:
- Está directamente relacionado con el gradiente de concentración de los iones que pueden permear la membrana a través de canales específicos, gracias a la permeabilidad selectiva de la membrana.
- Es mantenido activamente por la bomba Na+/K+, que requiere energía metabólica.
- Cambia en respuesta a las variaciones en los gradientes de concentración o la disponibilidad de canales iónicos.
- Es un proceso que sigue las reglas de la difusión y las fuerzas electroquímicas.
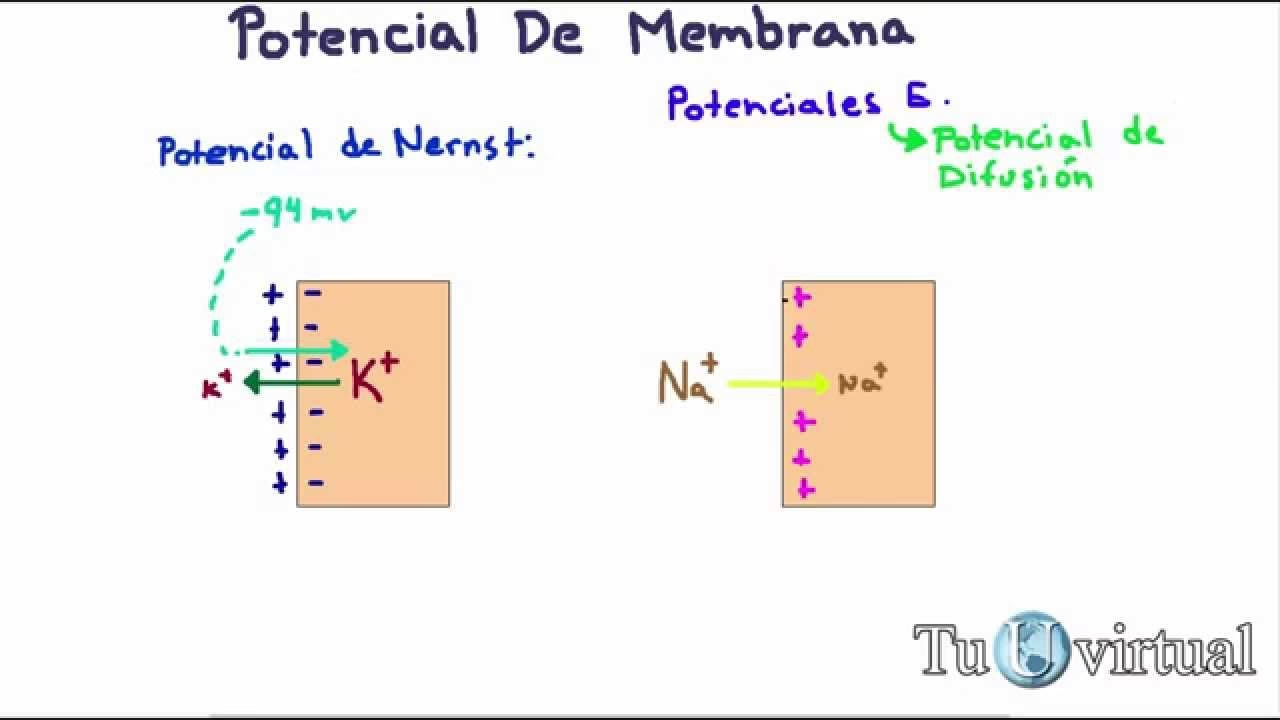
El Potencial de Nernst del Potasio
Para el potasio, el punto exacto en el que el potasio que sale de la célula debido al gradiente de concentración es igual al potasio que vuelve a entrar en la célula debido al gradiente electrostático se denomina potencial de equilibrio o potencial de Nernst para el potasio. Este valor es de aproximadamente -92 mV. Este potencial representa el voltaje teórico al cual el flujo neto de iones potasio a través de la membrana sería cero, incluso si los canales de potasio estuvieran abiertos.
Derivación de la Ecuación de Nernst para Iones Biológicos
La ecuación de Nernst nos proporciona el voltaje al cual se alcanza un potencial de membrana específico, conocido como "potencial de equilibrio", donde por cada ión que entra a la célula, uno sale, y por lo tanto, el potencial de membrana permanece constante. Este concepto es fundamental para entender la electrofisiología.
La derivación de la ecuación comienza definiendo la diferencia de energía potencial eléctrica para un mol de un ión (por ejemplo, K+). Este es el trabajo requerido para mover un mol de K+ a través de la membrana contra una diferencia de potencial eléctrico (V1 - V2):
WE = zF(V1 - V2)
Donde WE es el trabajo eléctrico, z es la valencia del ión (por ejemplo, +1 para K+), F es la constante de Faraday, y (V1 - V2) es la diferencia de potencial.
De manera similar, el trabajo requerido para mover un mol de K+ contra su gradiente de concentración (la diferencia de potencial químico) se describe como:
WC = RT ln([K+]i / [K+]o)
Donde WC es el trabajo químico, R es la constante de los gases, T es la temperatura, y [K+]i y [K+]o son las concentraciones de potasio en el interior y exterior de la célula, respectivamente.
El trabajo total realizado para mover los iones K+ contra sus gradientes eléctrico y de concentración es la suma de ambos trabajos:
WTotal = WE + WC = zF(V1 - V2) + RT ln([K+]i / [K+]o)
Cuando los iones K+ alcanzan el equilibrio a través de la membrana, el flujo neto es cero, lo que significa que el trabajo total es cero (WTotal = 0). En este punto, (V1 - V2) se convierte en el potencial de membrana de equilibrio para ese ión, denotado como EK (o Vm en la derivación original). Despejando Vm (o EK) de la ecuación, obtenemos:
0 = zF EK + RT ln([K+]i / [K+]o)
EK = -(RT/zF) ln([K+]i / [K+]o)
O, invirtiendo el logaritmo para tener la concentración externa sobre la interna:
EK = (RT/zF) ln([K+]o / [K+]i)
Esta es la ecuación de Nernst aplicada a un ión en sistemas biológicos, y proporciona el valor del potencial al cual los iones se encuentran en equilibrio a través de la membrana. Este potencial de membrana es también llamado el 'potencial de equilibrio del ion potasio (EK)'. Cuando un ión se encuentra a su potencial de equilibrio, se dice que está distribuido pasivamente.
Validación Experimental y Desviaciones del Potencial de Reposo
La hipótesis de que la ecuación de Nernst describe el potencial de membrana dado por el potasio cuando la neurona está en reposo fue validada mediante la medición del potencial de reposo del axón gigante del calamar. Los experimentos pioneros realizados por Hodgkin y Horowicz, utilizando microelectrodos insertados en el interior del axón, encontraron que su valor (el potencial transmembrana, Vm) era de -65 a -70 mV. Este valor era cercano, pero no exactamente igual, al potencial de equilibrio (EK+) calculado para los iones K+.
Para investigar más a fondo, Hodgkin y Horowicz decidieron estudiar la influencia de la concentración externa de potasio sobre el potencial de reposo. Aumentaron la concentración de [K+] extracelular y observaron que los resultados se ajustaban a una línea con una pendiente de -58 mV por cada aumento de diez veces en la concentración de potasio. Este resultado experimental es una fuerte evidencia de que el potasio es el ión dominante en la determinación del potencial de reposo, ya que la ecuación de Nernst predice un cambio de aproximadamente 58 mV (a 25 °C) por cada factor de 10 en la relación de concentraciones para un ión monovalente.
Sin embargo, también notaron desviaciones significativas a concentraciones externas bajas de K+. Esto indicó que, si bien el potasio es el principal contribuyente al potencial de reposo, hay otros iones que influyen en el potencial de membrana. La membrana también es permeable a los iones Na+ y Cl-, aunque la permeabilidad al Na+ es mucho más baja que la de los iones K+. La influencia del Cl- sobre el potencial de membrana de reposo suele ser menor en muchas células, ya que su potencial de equilibrio a menudo está cerca del potencial de reposo, o porque las bombas de Cl- mantienen un gradiente diferente.
Estas observaciones llevaron a la comprensión de que el potencial de reposo de una célula viva no es puramente el potencial de Nernst de un solo ión, sino una combinación ponderada de los potenciales de equilibrio de todos los iones permeables, influenciados por sus respectivas permeabilidades, lo que se describe más precisamente por la ecuación de Goldman-Hodgkin-Katz.
Concentraciones Iónicas Típicas en Células de Mamíferos y Potenciales de Equilibrio
Para ilustrar las bases del potencial de Nernst en biología, es útil observar las concentraciones típicas de los principales iones en el interior y exterior de una célula de mamífero, así como sus potenciales de equilibrio calculados usando la ecuación de Nernst (asumiendo 37°C y z=1 para iones monovalentes, o z=2 para iones divalentes como Ca2+).

| Ión | Concentración Intracelular (mM) | Concentración Extracelular (mM) | Potencial de Equilibrio (Eion) a 37°C |
|---|---|---|---|
| K+ | ~140 | ~5 | ~-92 mV |
| Na+ | ~15 | ~145 | ~+66 mV |
| Cl- | ~7-10 | ~110 | ~-65 a -70 mV |
| Ca2+ | ~0.0001 | ~1-2 | ~+120 a +130 mV |
Como se puede apreciar, el potencial de equilibrio del K+ es el más cercano al potencial de reposo de muchas neuronas, lo que subraya su papel fundamental en el mantenimiento de este estado.
Preguntas Frecuentes sobre la Ecuación y el Potencial de Nernst
¿Qué es el potencial de Nernst o potencial de equilibrio?
El potencial de Nernst, también conocido como potencial de equilibrio para un ión específico, es el potencial eléctrico a través de una membrana que equilibra el gradiente de concentración de ese ión, de modo que no hay flujo neto de iones a través de la membrana. Es el voltaje teórico donde las fuerzas químicas (debido a la diferencia de concentración) y las fuerzas eléctricas (debido a la carga del ión) se anulan mutuamente para ese ión en particular.
¿Por qué es tan importante la ecuación de Nernst en biología?
Es fundamental en biología porque permite calcular el potencial de equilibrio para cada tipo de ión permeable a través de la membrana celular. Esto es crucial para comprender cómo se generan y mantienen los potenciales de membrana, que son la base de la excitabilidad celular en neuronas y células musculares, la transmisión de señales y numerosos procesos fisiológicos.
¿Cuáles son las limitaciones de la ecuación de Nernst?
La ecuación de Nernst asume que la membrana es permeable solo a un tipo de ión y que ese ión está en equilibrio. En la realidad, las membranas celulares son semipermeables a múltiples iones y el potencial de reposo es un equilibrio dinámico, no estático. Por lo tanto, la ecuación de Nernst solo da el potencial de equilibrio para un ión individual. Para una descripción más precisa del potencial de membrana en células vivas, especialmente cuando hay múltiples iones permeables, se utiliza la ecuación de Goldman-Hodgkin-Katz, que considera las permeabilidades relativas de cada ión.
¿Cómo influye la temperatura en el potencial de Nernst?
La temperatura (T) es un factor directo en la ecuación de Nernst. A medida que la temperatura aumenta, el término RT/zF (o 0.0592/z en la forma simplificada a 25°C) también aumenta, lo que significa que un gradiente de concentración dado generará un potencial de equilibrio ligeramente mayor (en magnitud) a temperaturas más altas. Esto se debe a que el movimiento de los iones por difusión es más vigoroso a temperaturas elevadas.
¿Es el potencial de Nernst lo mismo que el potencial de reposo de una célula?
No son exactamente lo mismo, aunque están estrechamente relacionados. El potencial de Nernst es el potencial de equilibrio teórico para un ión específico, calculando el voltaje donde el flujo neto de ese ión es cero. El potencial de reposo de una célula, sin embargo, es el potencial de membrana real de la célula cuando no está activamente señalizando. Es un potencial transmembrana estable que surge de la permeabilidad diferencial de la membrana a varios iones (principalmente K+, Na+, Cl-) y la acción de bombas iónicas (como la bomba Na+/K+). El potencial de reposo es una combinación ponderada de los potenciales de Nernst de los iones permeables, siendo el potencial de Nernst del K+ el que más se aproxima al potencial de reposo en muchas células debido a la alta permeabilidad de la membrana al K+ en reposo.
En conclusión, la ecuación de Nernst es una herramienta indispensable en la electroquímica y la biología, proporcionando una comprensión profunda de cómo los gradientes de concentración pueden traducirse en potenciales eléctricos. Desde la predicción del voltaje en una batería hasta el complejo funcionamiento de nuestras células, esta ecuación nos permite desentrañar el delicado equilibrio de fuerzas que rigen el mundo microscópico y más allá.
Si quieres conocer otros artículos parecidos a La Ecuación de Nernst: Clave de Potenciales puedes visitar la categoría Cálculos.